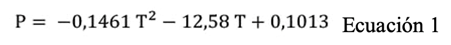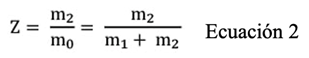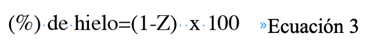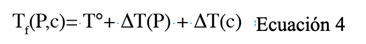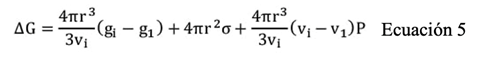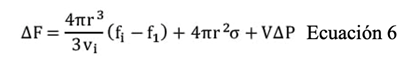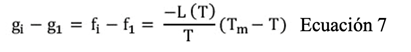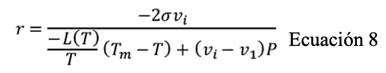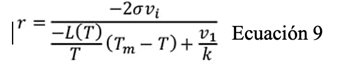Introducción
La congelación de alimentos es una técnica de preservación utilizada, tanto a nivel doméstico como industrial. Dicha técnica consiste en disminuir la temperatura del alimento cerca de los -18 ºC, lo cual provoca un cambio de estado en el agua y una disminución de la actividad del agua (Aw). La finalidad de esta operación es inhibir tanto las reacciones de deterioro (químicas y enzimáticas) como el crecimiento microbiológico. Durante el almacenamiento de los alimentos en congelación, el crecimiento microbiano se detiene a temperaturas menores a los -18 ºC, mientras que cambios enzimáticos y no enzimáticos se producen a tasas muy bajas (Nida et al., 2021; Rahman & Velez-Ruiz, 2007).
El cambio de estado en el agua provoca la formación de cristales de hielo durante las etapas de congelación y almacenamiento a bajas temperaturas. Lo cual genera cambios físicos en la estructura de los alimentos y en la mayoría de los casos reduce la calidad de estos (James et al., 2015). Múltiples matrices alimentarias, como arándanos, fresas y uvas, han sido evaluadas, y se evidencia efectos sobre color, textura, capacidad de retención de agua, degradación de compuestos químicos, entre otros (Cao et al., 2018; Šamec & Piljac-Žegarac, 2015).
Los cambios fisicoquímicos asociados a la calidad provocados por la congelación, en general son menores a los que ocurren cuando el alimento se somete a otras técnicas de conservación. Esto ocurre siempre que el método de congelación se aplique de manera que se puedan retener compuestos propios de los alimentos. Lo que resulta a su vez en un producto de mayor valor nutricional comparado a otras tecnologías donde se aplica calor como método de preservación (Van der Sman, 2020).
La congelación como tecnología de preservación busca, entre otras cosas, disminuir el desperdicio de alimentos a nivel mundial. Este desperdicio ha alcanzado cifras muy altas en los últimos años y se prevén aumentos si no se toman acciones al respecto. En el año 2019 se estimó un desperdicio en alimentos de 931 millones de toneladas, 61 % proveniente de los hogares, 26 % de los servicios de alimentación y 13 % de supermercados. Lo anterior sugiere que un 17 % de la producción global de alimentos no se aprovecha (United Nations Environment Programme (UNEP), 2021).
En Costa Rica, el desperdicio de alimentos en hogares se estima que es de 70 kg / cápita / año. Lo cual equivale a 365 609 toneladas de alimentos no aprovechados por año. Estados Unidos de América genera alrededor de 19 359 951 toneladas / año de desperdicio de alimentos proveniente de los hogares (UNEP, 2021). Dichas cifras podrían reducirse al utilizar de forma eficiente los métodos de conservación de alimentos, como lo es la congelación.
La congelación isocórica es una tecnología novel en la cual, la congelación se da a volumen constante. Esta condición permite disminuir efectos negativos de la congelación sobre la calidad del alimento (Nida et al., 2021). Los resultados promisorios hacen ver a la congelación isocórica como una tecnología capaz de generar un impacto positivo en la seguridad alimentaria y sostenibilidad ambiental (Zhao, Powell-Palm et al., 2021).
La presente revisión bibliográfica aborda el mercado de alimentos congelados, las tecnologías de congelación utilizadas, así como las emergentes, y estudiar a profundidad los fundamentos teóricos de la congelación isocórica y las ventajas en la industria alimentaria con respecto a los sistemas tradicionales de congelación y evidenciar los posibles campos de investigación relacionados con dicha tecnología.
Mercado de alimentos congelados
El mercado de alimentos congelados al finalizar el año 2020 tuvo un valor de 231,38 miles de millones de dólares. Se espera que para el año 2028 crezca a 385,04 miles de millones de dólares (Fortune Business Insights, 2022). El mercado en estudio abarca alimentos variados, desde productos cárnicos, de panadería y lácteos, comidas preparadas, hasta frutas y verduras, por lo tanto, el aumento de la vida útil del producto es la principal razón para someter los alimentos a dicho proceso.
Costa Rica es un país de alta producción agrícola, las exportaciones se enfocan en piña y banano (frescos y procesados). Según datos de la Promotora de Comercio Exterior de Costa Rica (Promotora de Comercio Exterior (PROCOMER), 2022), la pandemia provocada por el SARS-CoV-2 (COVID 19) ha provocado un aumento en el consumo de frutas y vegetales. Por ende, ha incentivado el consumo de esos productos en cualquier forma de procesamiento. El aumento se debe a la tendencia que existe a nivel mundial por mejorar el sistema inmunológico a través de la alimentación y el ejercicio (Reyes Ramos & Meza Jiménez, 2021). Como consecuencia, las frutas y vegetales congeladas son parte importante en el mercado de alimentos congelados. Debido al aumento en la vida útil de los alimentos se logra que diferentes frutas y verduras se puedan comercializar en cadenas comerciales más largas sin afectarse la calidad, además, las mismas se podrían consumir en regiones que por condiciones climáticas no se pueden desarrollar o se producen solo en cierta época del año (Xin, et al., 2015).
En el año 2020 se reportaron ventas de frutas congeladas de 19 392 toneladas mientras que, en el año 2021, fueron de 26 703 toneladas (Central America Data, 2022). Además, en el año 2021, según datos de PROCOMER (2022), las exportaciones en Costa Rica de frutas congeladas aumentaron en un 35 %. El resultado coloca a este producto como el que posee mayor crecimiento en el sector agrícola, junto con la exportación de plantas ornamentales.
Tecnologías de congelación tradicionales en la industria alimentaria
Existen diferentes tecnologías utilizadas en la industria de alimentos para la congelación. Las mismas han evolucionado con el tiempo con la finalidad de realizar dicha operación de la forma más eficiente posible. Esto mediante la reducción del tiempo de congelamiento. Algunas de las tecnologías más comunes se describen a continuación.
Congelación rápida individual
La congelación rápida individual es una de las tecnologías más aplicadas en la industria de alimentos. Los productos preservados mediante esta técnica tienen por lo general mejores características de calidad en comparación con los sometidos a una congelación lenta. La tecnología individual quick freezing (IQF, por sus siglas en inglés) consiste en disminuir la temperatura del alimento, el cual se encuentra en pequeñas porciones, mediante diferentes sistemas de enfriamiento que se encuentran a muy bajas temperaturas (Plotean, 2017).
Los sistemas empleados en la congelación IQF tienen asociados coeficientes de transferencia térmica elevados y por ende, favorecen una congelación en un corto tiempo, en algunos dicha congelación podría ocurrir en segundos (Plotean, 2017). El proceso por su eficiencia, permite la formación de cristales de hielo de menor tamaño. El daño celular en los tejidos del alimento y en compuestos específicos se ve reducido debido a la alta velocidad de congelación, lo que evita que la calidad del alimento se afecte (Ojha et al., 2021).
Diversos equipos han sido diseñados con la finalidad de aumentar la eficiencia y eficacia de los procesos de congelación rápida individual. La finalidad de estos equipos es generar alimentos con mejores características para el consumidor, para ello, se modifican parámetros críticos dentro del proceso de congelación o incluso el medio de enfriamiento (Plotean, 2017).
Congelación mediante fluidos criogénicos
Los fluidos criogénicos son sustancias que tienen su punto de ebullición a temperaturas por debajo de los -90 ºC a una presión estándar de 1 atmósfera. Entre ellos se encuentran el nitrógeno, oxígeno y helio líquidos. Estos han sido utilizados como medio de congelación rápida, con base en el fundamento de la congelación IQF. El objetivo final, es la congelación rápida, que desemboca en la minimización de la pérdida de calidad del alimento y en la formación de cristales de hielo pequeños (Scurlock, 2015).
La congelación mediante contacto directo con fluidos criogénicos se utiliza en alimentos de tamaño pequeño como filetes de pescado, camarones y frutas como las bayas y vegetales. Este método es bastante adecuado para procesos continuos, ya que las pérdidas por enfriamiento son menores (7 %) que los métodos más comunes, donde el aire es el medio de enfriamiento (alrededor de 30 %) (Horbaniuc et al., 2012). Además, los métodos clásicos de congelación con aire o por salmuera involucran el uso de otros refrigerantes que han sido reconocidos por tener un mayor impacto ambiental en función de los potenciales ODP (Ozone Depletion Potential) y GWO (Global Warming Potential), los cuales podrían tener efectos ambientales adversos (Horbaniuc et al., 2012).
Congelación por salmuera
La congelación por salmuera consiste en sumergir un producto en un fluido que se compone de una solución salina o hecha a base de un agente que disminuya el punto de congelación del agua. De manera que, se alcancen temperaturas de hasta -21 ºC. La congelación de alimentos sólidos mediante esta técnica de inmersión en salmuera genera elevados coeficientes de transferencia de calor entre el sólido, en este caso el alimento, y el líquido a menor temperatura. La salmuera es un líquido refrigerante secundario no tóxico de manera que los alimentos pueden entrar en contacto directo con el mismo sin que se afecte su inocuidad (López Toro, 2020). Los productos marinos han sido congelados con el empleo de esta tecnología durante años. Esto se debe a que, al ser otro método de congelación rápida, permite mantener buenas propiedades del alimento durante la congelación y en el proceso de descongelación. Además, se utiliza en muchos casos por las embarcaciones pesqueras para mantener los alimentos en buen estado hasta el momento de desembarque (Aubourg & Gallardo, 2005).
Tecnologías de congelación emergentes en la industria alimentaria
La búsqueda de tecnologías más eficientes y con el menor efecto posible sobre el alimento, ha llevado al desarrollo de diferentes formas de congelación. A continuación, se describen algunas de las tecnologías emergentes en la industria de alimentos.
Congelación mediante película de vacío
La congelación por película de vacío (VFC, por sus siglas en inglés), se basa en la relación entre la presión de la cámara y la presión de saturación. Al inicio del proceso, la presión de la cámara es mayor a la presión de saturación, lo que genera una temperatura del alimento constante. A medida que la presión en la cámara desciende, la temperatura del alimento disminuye de manera rápida lo que genera fuerte burbujeo y líquidos de vaporización. Una vez que el equilibrio vuelve (presión de la cámara mayor a la presión de saturación) se da una etapa de evaporación leve o ebullición (presiones igualadas) (Zhu et al., 2020). Los estudios sobre el efecto de la congelación en vacío en alimentos aún son limitados, por lo que futuros experimentos deben ser desarrollados para generar conclusiones sobre la aplicabilidad en la industria de alimentos (Zhu et al., 2020).
Congelación por aspersión de vacío
La congelación por aspersión de vacío (VSC, por sus siglas en inglés), tiene como principio la evaporación rápida debido a los cambios de presión (de forma similar a la tecnología VFC). Las gotas generadas por el aspersor pasan de condiciones ambientales al vacío, y producen una caída rápida de temperatura que a su vez enfría el medio líquido. Debido a la complejidad para realizar experimentos donde se determine la temperatura de las gotas, los estudios han sido direccionados a resultados mediante modelos numéricos (Zhu et al., 2020). La rapidez con que ocurre la congelación por medio de la aspersión de vacío, presenta una forma eficaz y eficiente para la industria alimentaria. Sin embargo, es necesario generar más información respecto a los efectos tanto negativos como positivos de la tecnología sobre diferentes alimentos.
Congelación por cambio de presión
La congelación por cambio de presión (PFS, por sus siglas en inglés), permite generar cristales de tamaño pequeño, lo que disminuye el efecto de la operación sobre la matriz a congelar. Los cambios de presión pueden darse en un ámbito entre 0,1 MPa a 210 MPa, lo que reduce el punto de fusión del agua cerca de los -21 ºC (Zhu et al., 2020). El diferencial de presión y temperatura generado genera tasas de congelación eficientes, lo que resulta en cristales pequeños y mayor homogeneidad (Sanz & Otero, 2014). Algunos alimentos como pescado y carne de cerdo han sido evaluados con la congelación PFS, con lo que se obtiene una reducción en la degradación de lípidos y una mayor suavidad de la carne (Choi et al., 2016; Sequeira-Muñoz et al., 2005).
Congelación isocórica
El estudio de la tecnología de la congelación isocórica empezó a inicios de los años 2000, cuando Rubinsky et al. (2005) profundizaron en el estudio de aspectos termodinámicos relacionados con dicha tecnología. El motivo de estudio nace de la necesidad de preservar material biológico por periodos extensos, para conservar sus características tal como si fuera tejido sin ningún tipo de procesamiento. Esta tecnología generó gran interés para la industria médica, agrícola, veterinaria, biotecnológica y alimentaria (Rubinsky et al., 2005).
Durante la congelación isocórica, el volumen del sistema se mantiene constante mientras que la presión y la temperatura son factores variables. Al mantener el volumen constante, el proceso isocórico sigue la línea entre el agua líquida y el hielo I, tal como se describe en la Figura 1, la cual a su vez es representada por la ecuación 1 (Nida et al., 2021). Los datos teóricos y experimentales demuestran que un 45 % del volumen permanece sin congelar en el punto triple en un proceso de congelación a volumen constante (Lyu et al., 2017; Rubinsky et al., 2005).
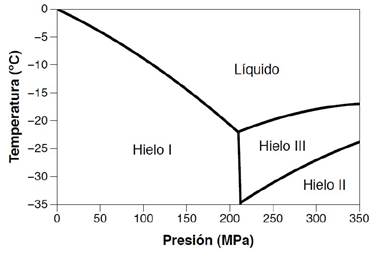
Figure 1 Water phase diagram in the region between water, ice I and ice III (Bridgman, 1912; Schlüter, 2003).
Donde, T es la temperatura (ºC) y P la presión (MPa) (Rubinsky et al., 2005).
El hielo I es el hielo formado a presión atmosférica y es estable hasta alcanzar una presión cercana a los 210 MPa. Por encima de esta presión ocurre la formación de hielo II e hielo III. Estos son estables a nivel termodinámico en función de la temperatura y la presión. Para el hielo I, el punto de congelación del agua decrece al aumentar la presión, caso contrario ocurre para el hielo II y III, donde al aumentar la presión, el punto de fusión también aumenta (Sanz & Otero, 2014).
Una vez que la temperatura del sistema desciende a menos 0 ºC, el principio de Le Chatelier explica que a medida que el agua se expande al congelarse, la alta presión dificultará la creación adicional de hielo. Dicho efecto también ejercerá presión hidrostática sobre el material biológico en proceso. Por este motivo, se debe procurar que las condiciones de operación, de presión y temperatura, minimicen la presión hidrostática generada. El daño en los alimentos sería mayor si el sistema alcanza una temperatura de -21,985 ºC y una presión de 209,9 MPa (punto triple). En este punto, el equilibrio (hielo-agua) que evita la cristalización del agua dentro del alimento no se podría mantener debido a la presencia de otros tipos de hielo (Preciado & Rubinsky, 2010; Rubinsky et al., 2005). Además de la presión y la temperatura, es importante conocer el porcentaje de masa de agua con respecto a la masa total de la mezcla de hielo I y agua en un sistema isocórico. Dicho parámetro se identifica como Z en la ecuación 2 y es conocido como el parámetro de calidad. Se define que los subíndices 0, 1 y 2 representan el estado inicial de la masa, la masa de hielo y la masa de agua líquida, respectivamente (Preciado, 2007; Rubinsky et al., 2005).
A partir de la ecuación 2 es posible calcular el porcentaje de hielo presente en la mezcla hielo-agua. El mismo está definido por la ecuación 3, en la cual z es el parámetro de calidad antes descrito (Rubinsky et al., 2005).
En las ecuaciones 1 a 3 se representa el comportamiento del agua pura bajo condiciones de congelación isocórica. Sin embargo, la congelación de alimentos que emplea esta tecnología requiere de una solución isotónica, por lo que el comportamiento no sería descrito de forma exacta por dichas ecuaciones. La ecuación 4 fue propuesta por Rubinsky et al. (2005) como una aproximación de primer orden de la temperatura de congelación de una solución acuosa bajo condiciones de congelación isocórica. Donde, se asume que el efecto de la presión y de la concentración del soluto sobre la temperatura de congelación del agua son independientes uno del otro.
Donde Tf es la temperatura de cambio de fase, Tº es la temperatura de congelación del agua pura a una presión de referencia de 1 atm, (T(P) es el cambio de temperatura debido al incremento en la presión y el (T(c) es el cambio de temperatura de la solución como función de la concentración del soluto. Para que la congelación del agua ocurra, las moléculas deben ensamblarse mediante su movimiento aleatorio en una estructura similar al hielo y mayor al tamaño crítico de nucleación. Dicho tamaño crítico corresponde a una barrera energética. Una vez superada la barrera, las moléculas de agua tienen energía favorable para unirse a la estructura de hielo, lo que conduce así a un crecimiento de este. Es de relevancia indicar que existe una diferencia en el volumen específico entre el agua y el hielo. Esto provoca en un sistema isobárico la formación de cristales de hielo y por consecuencia, un incremento en el volumen, mientras que en el proceso isocórico provocará un aumento en la presión del sistema (Szobota & Rubinsky, 2006).
Existen tres componentes que determinan el efecto de la energía libre sobre la formación de cristales de hielo en un proceso isobárico: el cambio en la energía libre de Gibbs entre el hielo y el agua líquida, la energía asociada a la formación de la interfase entre el hielo y el agua, y el incremento en el volumen del sistema debido a la presión. Lo anterior está representado en la Ecuación 5. Esto para cristales de hielo con radio r y volumen 4(r3 / 3vi (Szobota & Rubinsky, 2006).
Donde (G es el cambio en la energía de Gibbs, 4(r3 / 3 el volumen, g i y g 1 son la energía de Gibbs específica del hielo y agua por unidad de masa, σ es la tensión superficial entre hielo y agua, v i y v 1 son los volúmenes específicos de hielo y agua, y P la presión.
Para un sistema isocórico los tres componentes que determinan el efecto de la energía libre sobre la formación de cristales son el cambio en la energía libre de Helmholtz entre el hielo y el agua, la energía asociada a la formación en la interfase entre hielo y líquido y la energía asociada con el incremento en la presión dentro del volumen definido. Estos parámetros se representan en la ecuación 6 (Szobota & Rubinsky, 2006).
Donde (F es el cambio en la energía libre de Helmholtz, fi y f1 son la energía específica de Helmholtz para hielo y agua por unidad de masa, 4(r3 / 3 el volumen, y (P el cambio de presión.
El cambio en la energía libre sobre la trasformación está en función de la temperatura, esto tanto para un proceso isocórico como para uno isobárico y se muestra en la ecuación 7 (Szobota & Rubinsky, 2006).
Donde, g i y g 1 son la energía de Gibbs para hielo y agua por unidad de masa, f i y f 1 son la energía específica de Helmholtz para hielo y agua por unidad de masa, L es el calor latente de fusión por unidad de masa, T la temperatura y T m es la temperatura de fusión a una presión dada.
El tamaño crítico para la propagación de cristales de hielo corresponde al valor máximo del diferencial de la energía de Gibbs ((G) y la energía de Helmholtz ((F) para un proceso isobárico y uno isocórico, respectivamente. El radio crítico de agrupamiento es obtenido al diferenciar el valor ((G) y ((F) respecto al radio e igualar el resultado a cero. Tal como se muestra en la ecuación 8 y ecuación 9 para un proceso isobárico y uno isocórico respectivamente (Szobota & Rubinsky, 2006).
Donde, tanto para la ecuación 8 como la ecuación 9, σ es la tensión superficial entre hielo y agua, vi el volumen específico del hielo, L es el calor latente de fusión, T la temperatura, T m la temperatura de fusión a una presión dada, v1 el volumen específico del agua, P la presión y k la pendiente en cualquier sección de la curva.
Mediante las ecuaciones 8 y 9 es posible también demostrar que en un proceso isocórico se disminuye la probable formación de un núcleo crítico de hielo a temperaturas menores que en un sistema isobárico. Además, el estudio termodinámico desarrollado permite concluir que el sistema isocórico no depende de tasas de transferencia térmica para prevenir la formación de cristales de hielo de gran tamaño. Esto a diferencia de las otras tecnologías de congelación utilizadas en la industria de alimentos (Rubinsky et al., 2005; Szobota & Rubinsky, 2006).
Con el fin de poner en práctica todos los conceptos teóricos antes descritos se han desarrollado equipos piloto para procesos isocóricos. Estos equipos consisten en un recipiente rígido capaz de resistir altas presiones. En dichos recipientes el alimento es inmerso en una solución isotónica y se introduce un punto de nucleación para evitar la formación de hielo en forma aleatoria. Lo anterior se representa en la Figura 2 (Rubinsky et al., 2005).
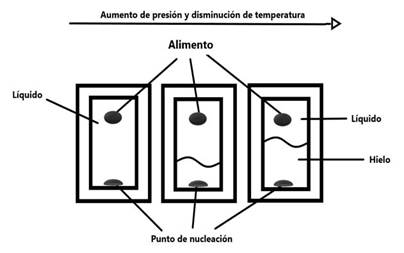
Figure 2 Schematic of an isochoric freezing system and its variation according to temperature and pressure changes (Lyu et al., 2017).
Las condiciones seleccionadas para cada proceso deben ser estudiadas con la finalidad de evitar la pérdida de calidad en el alimento, así como asegurar la estabilidad de este durante el almacenamiento a bajas temperaturas (Nida et al., 2021).
Ventajas de la congelación isocórica
Debido a las diferencias que ya se han evidenciado de la congelación isocórica en relación con las demás tecnologías de congelación, existen múltiples beneficios que se pueden obtener al aplicar la tecnología de congelación isocórica en diferentes alimentos. Los efectos se muestran en diferentes parámetros de calidad, los cuales van desde aspectos fisicoquímicos hasta microbiológicos. A continuación, se detallan el efecto de la tecnología sobre diferentes parámetros de calidad en varias matrices estudiadas.
Efectos fisicoquímicos
Se han realizado diferentes estudios en matrices alimentarias con la finalidad de evaluar los efectos de la congelación isocórica sobre el objeto en estudio. Los parámetros de calidad más relevantes se detallan a continuación.
Cambio de masa
Los cambios en la masa en los alimentos ocurren durante la descongelación de estos. Dichos cambios ocurren y se deben a la pérdida de agua a consecuencia de la ruptura celular de los tejidos del alimento (Zhao, Bilbao-Sainz et al., 2021). Los datos obtenidos de diferentes estudios sobre el efecto del cambio de masa según la tecnología utilizada para la congelación se resumen en el Cuadro 1.
Cuadro 1 Efectos de diferentes tecnologías de congelación en el cambio de masa en varios alimentos.
| Producto | Tecnología de congelación | Condiciones de proceso | Cambio de masa (%) | Referencia |
| Papa | Cuarto frío | -5 ºC | - 13,1 | Lyu et al. (2017) |
| Isocórico | -5 ºC | 0 | ||
| Isocórico | -3 ºC / 37 MPa TC 0,16 MPa /s | 13,6 | ||
| Isocórico | -9 ºC / 101 MPa TC 0,16 MPa /s | 9,2 | Zhao, Bilbao-Sainz et al. (2021) | |
| Isocórico | -15 ºC / 156 MPa /TC 0,16 MPa /s | - 10,9 | ||
| Isocórico | -3 ºC / 4 Sem | -10,2 | Bilbao-Sainz, Zhao et al. (2020) | |
| Isobárico | - 3 ºC / 4 Sem | -21,4 | ||
| IQF | - 90 ºC / -3 ºC 4 Sem | -12,4 | ||
| Tomate | Isocórico | -2,5 ºC / 25 MPa / 4 Sem | 0,2 | Bilbao-Sainz et al. (2021) |
| Cuarto frío | 10 ºC / 85 % HR / 4 Sem | -8,6 | ||
| Isobárico | -2,5 ºC / 4 Sem | -16,3 | ||
| IQF | -90 ºC/ 4 Sem a 20 ºC | -16,7 | ||
| Espinaca | Isocórico | -4 ºC / 29,7 MPa / 1 día | 41,2 | Bilbao-Sainz, Sinrod, Dao et al. (2020) |
| Isocórico | -4 ºC / 29,7 MPa / 7 días | 27,2 | ||
| Isobárico | -4 ºC / 1 día | 3,8 | ||
| Isobárico | -4 ºC / 7 días | -7,9 | ||
| Cereza | Isocórico | -4 ºC / 1 día / 29,5 MPa | 2,99 | Bilbao-Sainz et al. (2019) |
| Isocórico | -7 ºC / día 62,1 MPa | 2,27 | ||
| Isobárico | -4 ºC / 1 día | 0,02 | ||
| Isobárico | -7 ºC / 1 día | -0,45 | ||
| IQF | -90 ºC / 1 día a -20 ºC | -0,36 |
TC: tasa de compresión. HR: humedad relativa. Sem: cantidad de semanas almacenados hasta el análisis. / TC: compression rate. HR: relative humidity. Sem: number of weeks stored until analysis.
Los datos presentados en el Cuadro 1 muestran que la congelación isocórica disminuyó la pérdida de masa. Este fenómeno se debe a la inhibición de la formación de hielo y por ende de cristales capaces de dañar la estructura celular de la matriz alimentaria (Preciado & Rubinsky, 2010).
Las soluciones en las cuales se sumerge el alimento deben ser isotónicas, con la finalidad de no producir un aumento en la masa del alimento. Este efecto sería consecuencia de la diferencia de la concentración de solutos entre el alimento y la solución de inmersión, y que a su vez podría cambiar aspectos sensoriales del alimento (Zhao, Bilbao-Sainz et al., 2021). La concentración y el tipo de solutos para utilizar dependen del alimento que se desee analizar. En una investigación con pescado se utilizararon soluciones salinas (Năstase et al., 2017), mientras que en diferentes estudios se han utilizado soluciones de sacarosa (Bilbao-Sainz et al., 2019; Bilbao-Sainz, Sinrod, Dao et al., 2020; Bilbao Sainz, Zhao et al., 2020; Bilbao-Sainz et al., 2021; Zhao, Bilbao-Sainz et al., 2021).
El control de la temperatura y la presión durante el proceso isocórico es fundamental. A una mayor presión y menor temperatura se aumenta la presión hidrostática generada dentro del contenedor, produce un mayor daño al alimento y genera pérdidas de masa (Bilbao-Sainz, Sinrod, Williams et al., 2020). Otras técnicas de congelación como las mostradas en el Cuadro 1 producen un mayor daño celular. Esto resulta en mayores pérdidas de masa y de calidad en el alimento (Bilbao-Sainz et al., 2021).
El aumento de masa observado en los procesos isocóricos, debidos a las soluciones hipertónicas, podría generar un campo amplio de investigación. En el cual, el uso de la tecnología no solo sería como técnica de preservación sino también como método para mejorar la nutrición de los alimentos sometidos a este proceso (Rubinsky, 2021).
Color
El color es una de las principales cualidades de calidad en un alimento. En muchos casos determina si el producto será aceptado o rechazado por el consumidor (Pathare et al., 2013). Durante el almacenamiento en congelación puede ocurrir degradación enzimática y no enzimática de compuestos generadores de color. De esta manera se afecta la calidad del alimento (Lyu et al., 2017). En el Cuadro 2 se muestran diferentes efectos de procesos isocóricos e isobáricos de congelación sobre el color de dos alimentos.
Cuadro 2 Efectos de diferentes tecnologías de congelación en el cambio de color en dos alimentos.
| Producto | Tecnología de congelación | Parámetros de color | Referencia | ||
| L* | a* | b* | |||
| Tomate | Fresco | 31,4 ± 0,8 | 8,8 ± 1,8 | 11,1 ± 0,9 | Bilbao-Sainz et al. (2021) |
| Isocórico 4 Sem | 30,1 ± 0,7 | 7,7 ± 1,3 | 11,2 ± 1,1 | ||
| Cuarto frío 4 Sem | 30,2 ± 0,6 | 7,2 ± 1,7 | 3,1 ± 1,0 | ||
| Isobárico 4 Sem | 31,3 ± 1,2 | 7,3 ± 1,5 | 4,9 ± 0,8 | ||
| IQF 4 Sem | 32,6 ± 0,6 | 8,2 ± 1,9 | 15,5 ± 2,5 | ||
| Espinaca | Fresca | 43,91 ± 2,92 | -7,96 ± 0,86 | 20,69 ± 2,38 | Bilbao-Sainz, Sinrod, Dao et al. (2020) |
| Isocórico 1 día | 33,73 ± 3,89 | -7,78 ± 1,41 | 18,51 ± 4,74 | ||
| Isobárico 7 días | 32,08 ± 3,87 | -7,73 ± 1,84 | 16,43 ± 4,79 | ||
| Isobárico 1 día | 37,16 ± 1,54 | -8,57 ± 0,90 | 19,19 ± 2,84 | ||
| Isobárico 7 días | 30,48 ± 3,13 | -6,64 ± 1,25 | 13,70 ± 3,48 | ||
| Comercial | 35,09 ± 2,61 | -7,55 ± 1,81 | 20,90 ± 2,73 | ||
Sem: cantidad de semanas almacenados hasta el análisis. / Sem: number of weeks stored until analysis.
Se logró observar efectos leves en los parámetros L*, a* y b*, en las muestras sometidas a procesos isocóricos respecto a la muestra control (Bilbao-Sainz, Sinrod, Dao et al., 2020). El parámetro L* se relaciona a la luminosidad, el a* a las coordenadas entre rojo y verde y el parámetro b* a las coordenadas entre amarrillo y azul (Mathias-Retting & Ah-Hen, 2014). En el caso de la espinaca se mostraron diferencias significativas en el parámetro L* para todos los procesos en comparación con la muestra fresca. Lo anterior indica un oscurecimiento en el producto consecuencia de las diferentes tecnologías de congelación aplicadas. Además, los valores de a* se mantuvieron muy constantes en el tiempo, mientras que el valor b* en procesos isobáricos e isocóricos tuvieron una notable disminución después de 7 días de almacenamiento. Lo anterior indica una disminución en la cantidad de clorofila presente en la muestra (Bilbao-Sainz, Sinrod, Dao et al., 2020).
En el tomate no se encontraron diferencias entre la muestra fresca y las muestras sometidas a la congelación isocórica, lo cual difiere de las muestras en donde se empleó otra técnica de congelación. El parámetro b* incrementó para las tecnologías a presión contante evaluadas, lo que indica un aumento en el color amarillo de los tomates en comparación con la muestra fresca. Dicho aumento podría ser debido a la oxidación de los carotenoides. Este efecto fue mayor en la congelación IQF debido a las corrientes de aire utilizadas para enfriar el producto (Bilbao-Sainz et al., 2021).
Otro alimento evaluado han sido las cerezas, en donde se ha estudiado el efecto del procesamiento isocórico, isobárico e IQF sobre el color de estas (Bilbao-Sainz et al., 2019). En el proceso isocórico se dio una disminución en el parámetro L* y un leve aumento en los parámetros b* y a*. Es probable que estos efectos son dados por la solución isotónica utilizada durante el proceso (Bilbao-Sainz et al., 2019).
No se detectaron diferencias entre las muestras procesadas a -4 ºC y -7 ºC en sistema isocórico. Lo anterior indica que la presión hidrostática no tiene efecto sobre la degradación del β-caroteno. Este es el principal compuesto asociado al color amarillo de las cerezas. Por otro lado, las muestras sometidas al proceso isobárico e IQF mostraron disminuciones significativas en los valores L* y b*. Además, el valor a* incrementó en comparación con la muestra fresca. La pérdida de color amarillo y el oscurecimiento fueron provocados por la degradación del β-caroteno y la actividad enzimática, respectivamente. Dichas reacciones son aceleradas por el daño celular causado durante la congelación. Este daño no se identificó en el proceso isocórico (Bilbao-Sainz et al., 2019). El comportamiento enzimático antes descrito también ha sido investigado en diferentes estudios en papa. Se ha demostrado que la congelación isocórica reduce el pardeamiento enzimático sin eliminarlo en su totalidad. Lo anterior se explica ya que existe un menor daño celular debido a la ausencia de cristales de hielo. Este efecto a su vez, disminuye las interacciones entre el sustrato polifenólico y la enzima polifenoloxidasa (Bilbao-Sainz, Zhao et al., 2020; Lyu et al., 2017; Zhao, Bilbao-Sainz, et al., 2021).
Textura
La congelación produce un daño estructural en los tejidos de los alimentos. Múltiples matrices han sido evaluadas para determinar si los procesos isocóricos permiten obtener alimentos con texturas similares al mismo alimento fresco.
En una investigación donde se aplicaron diferentes tratamientos a hojas de espinaca, se evaluaron los parámetros de la distancia de rotura (mm), fuerza máxima (g) y módulo de elasticidad (Pa) (Bilbao-Sainz, Sinrod, Dao et al., 2020). Los tratamientos evaluados fueron: isocórico con 1 y 7 días de almacenamiento, isobárico con 1 y 7 días de almacenamiento, empacada isobárica, empacada isocórica, comercial y la muestra control representada como la muestra fresca. Los datos evidencian que las muestras con mejores propiedades mecánicas fueron las sometidas a procesos isocóricos.
Las muestras evaluadas además presentaron solo una leve disminución en la rigidez con el tiempo, pero mantiene el grado de crujido. Este efecto se muestra en una corta distancia de rotura y valores de fuerza máxima similares a los de la muestra control: 125,35 g y 106,02 g para los procesos isocóricos a 1 y 7 días, respectivamente y 117,9 g para la muestra fresca (Bilbao-Sainz, Sinrod, Dao et al., 2020). Por otro lado, las muestras evaluadas bajo condiciones isobáricas presentaron una mayor diminución en el módulo de elasticidad (ya que perdieron su grado de crujido) y una mayor distancia a la rotura, lo cual generó mayores diferencias con el control (Bilbao-Sainz, Sinrod, Dao et al., 2020).
Los parámetros de fuerza de fractura y elasticidad fueron determinados en tomates frescos. Se obtuvieron valores de 26,3 N y 0,16 MPa, respectivamente. Estos datos se compararon con datos obtenidos de muestras tratadas bajo congelación isocórica, isobárica, IQF y congelación en cuarto frío. En las muestras sometidas al proceso isocórico, después de una semana la fuerza de fractura disminuyó en un 20 %. Sin embargo, este valor se mantuvo constante durante el tiempo restante en almacenamiento de cuatro semanas en total. Además, no hubo diferencia significativa en el parámetro de elasticidad entre las muestras isocóricas y las frescas después de cuatro semanas de almacenamiento (Bilbao-Sainz et al., 2021).
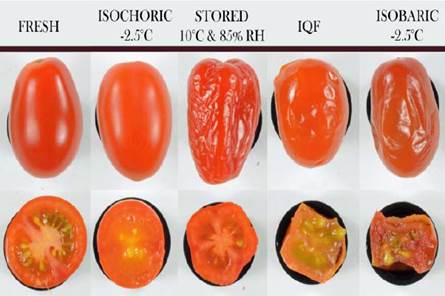
Los cambios mayores en las propiedades de textura de los tomates fueron relacionados con los procesos isobáricos e IQF. En los cuales se obtuvieron tomates con escasa fuerza de fractura y una gran pérdida de elasticidad. Estos efectos son causados por la desintegración de las membranas, daños en los tejidos, actividad enzimática, recristalización y probables ciclos de descongelación-congelación. Lo anterior se representa de forma visual en la Figura 3 (Bilbao-Sainz et al., 2021).
Las cerezas sometidas a una congelación isocórica a -4 ºC no mostraron diferencias significativas en los parámetros de fuerza máxima, elasticidad y fuerza de rotura respecto a cerezas frescas. Al realizar el mismo proceso a -7 ºC se obtuvo una ligera disminución en firmeza y rigidez de las cerezas debido a un aumento en la presión hidrostática. Lo que ocasionó daño celular durante la congelación, y confirma así la importancia de la selección de condiciones de proceso específicas para cada alimento. Los procesos isobáricos e IQF también analizados, mostraron grandes cambios en las propiedades de textura. Además, no se encontró diferencia significativa entre dichas tecnologías de congelación, lo cual evidencia la ventaja del proceso isocórico sobre el proceso isobárico (Bilbao-Sainz et al., 2019).
Al comparar el efecto de cuatro diferentes procesos isocóricos en papa: 1) 37 MPa a -3 ºC, 2) 71 MPa a -6 ºC, 3) 101 MPa a -9 ºC y 4) 156 MPa a -15 ºC, cada una a dos tasas de compresibilidad (0,02 MPa/s y 0,16 MPa/s), en diferentes empaques y disoluciones, respecto a una muestra control, se obtuvieron diferencias en los parámetros de estrés máximo y elasticidad. Para la muestra fresca se obtuvo un valor de máximo estrés de 1,18 MPa y 2,83 MPa en el módulo de elasticidad. Mientras que en las muestras procesadas se determinó un rango entre -20 % y 68 % de incremento en el estrés máximo y de 5 % de aumento a 89 % disminución en la elasticidad, lo que depende de las condiciones en los procesos isocóricos (Bilbao-Sainz et al., 2019). Además, las muestras inmersas en agua procesadas a -15 ºC tuvieron una mayor pérdida de textura debido a la mayor presión generada en el sistema. Esto provocó la ruptura celular de las membranas y produjo pérdidas de agua y daños permanentes en la textura del alimento. Similar efecto ocurrió en las muestras empacadas al vacío, ya que mostraron pérdida de textura respecto a la muestra fresca (Bilbao-Sainz et al., 2019).
Las muestras empacadas e inmersas en ácido ascórbico tuvieron valores comparables a las muestras frescas. Lo anterior a pesar de que las muestras a temperaturas de -9 ºC y -15 ºC tuvieron valores de dureza mayores a las muestras de referencia. Esto podría ser debido a una inactivación parcial de la enzima pectinmetilestearasa, la cual es liberada por las altas presiones y es causante de la desesterificación de la pectina metilada lo que genera un gel con iones divalentes de calcio y magnesio, y aumenta de esta manera el valor de dureza (Vega-Gálvez et al., 2014; Zhao, Bilbao-Sainz et al., 2021).
Efecto en compuestos químicos
Durante el almacenamiento en congelación, los alimentos sufren pérdidas de diferentes compuestos como vitaminas, carotenoides, antioxidantes, entre otros. Estos efectos generan, en la mayoría de los casos, pérdidas de calidad por efectos adversos en el alimento o pérdidas nutricionales. El efecto de las tecnologías de congelación estudiadas sobre los compuestos fenólicos y carotenoides presentes en diferentes alimentos se muestra en el Cuadro 3. Los resultados de la aplicación de diferentes tecnologías en varias matrices alimentarias sobre el ácido ascórbico se muestran en el Cuadro 4. Los datos obtenidos del estudio en tomates muestran una mayor retención de los compuestos estudiados en las muestras isocóricas. En el caso del licopeno, la disminución es debido a la reducción en la actividad enzimática. Esta actividad es intensificada por el daño celular ocurrido en las otras tres tecnologías.
Cuadro 3 Efecto de diferentes tecnologías de congelación sobre los compuestos fenólicos y carotenoides presentes en varios alimentos.
| Alimento | Compuesto | Tecnología de congelación | Condiciones de proceso | Retención (%) | Referencia |
| Tomate | Licopeno | Isocórico | -2,5 ºC / 25 MPa / 4 Sem | 90 | Bilbao-Sainz et al. (2021) |
| Cuarto frío | 10 ºC / 85 % HR / 4 Sem | 75 | |||
| Isobárico | -2,5 ºC / 4 Sem | 48 | |||
| IQF | -90 ºC/ 4 Sem a -20 ºC | 33 | |||
| Compuestos fenólicos solubles | Isocórico | -2,5 ºC / 25 MPa / 4 Sem | 88 | ||
| Cuarto frío | 10 ºC / 85 % HR / 4 Sem | 52 | |||
| Isobárico | -2,5 ºC / 4 Sem | 18 | |||
| IQF | -90 ºC/ 4 Sem a -20 ºC | 40 | |||
| Cereza | Compuestos fenólicos solubles | Isocórico | -4 ºC / 1 día / 29,5 MPa | +100 | Bilbao-Sainz et al. (2019) |
| Isocórico | -7 ºC / día 62,1 MPa | +100 | |||
| Isobárico | -4 ºC / 1 día | 29 | |||
| Isobárico | -7 ºC / 1 día | 82 | |||
| IQF | -90 ºC / 1 día a -20 ºC | 90 | |||
| Espinaca | Clorofila | Isocórico | -4 ºC / 29,7 MPa / 1 día | 31 | Bilbao-Sainz, Sinrod, Dao et al. (2020) |
| Isocórico | -4 ºC / 29,7 MPa / 7 días | 23 | |||
| Isobárico | -4 ºC / 1 día | 16 | |||
| Isobárico | -4 ºC / 7 días | 15 | |||
| Papa | Compuestos fenólicos | Isocórico | -3 ºC / 4 Sem | +100 | Bilbao-Sainz, Zhao et al. (2020) |
| Isobárico | -3 ºC / 4 Sem | +100 | |||
| IQF | -90 ºC / 4 Sem a -3 ºC | +100 |
Sem: cantidad de semanas almacenados hasta el análisis. +100: hubo mayor cantidad de dicho compuesto respecto al control. / Sem: number of weeks stored until analysis. +100: there was a greater amount of the compound compared to the control.
Cuadro 4 Efecto de diferentes tecnologías de congelación sobre la cantidad de ácido ascórbico presente en diferentes alimentos.
| Alimento | Compuesto | Tecnología de congelación | Condiciones de proceso | Retención (%) | Referencia |
| Tomate | Ácido ascórbico | Isocórico | -2,5 ºC/25 MPa/ 4 Sem | 100 | Bilbao-Sainz et al. (2021) |
| Cuarto frío | 10 ºC/ 85 % HR/ 4 Sem | +100 | |||
| Isobárico | -2,5 ºC / 4 Sem | 10 | |||
| IQF | -90 ºC / 4 Sem a -20 ºC | 83 | |||
| Cereza | Ácido ascórbico | Isocórico | -4 ºC / 1día / 29,5 MPa | 100 | Bilbao-Sainz et al. (2019) |
| Isocórico | -7 ºC/ 1 día / 62,1 MPa | 100 | |||
| Isobárico | -4 ºC / 1 día | 37 | |||
| Isobárico | -7 ºC / día | 49 | |||
| IQF | -90 ºC / 1 día a -20 ºC | 28 | |||
| Espinaca | Ácido ascórbico | Isocórico | -4 ºC / 29,7 MPa / 1 día | 32 | Bilbao-Sainz, Sinrod, Dao et al. (2020) |
| Isocórico | -4 ºC / 29,7 MPa / 7 días | 10 | |||
| Isobárico | -4 ºC / 1 día | 15 | |||
| Isobárico | -4 ºC / 7 días | 15 | |||
| Papa | Ácido ascórbico | Isocórico | -3 ºC / 4 Sem | 10,4 | Bilbao-Sainz, Zhao et al. (2020) |
| Isobárico | -3 ºC / 4 Sem | 6,6 | |||
| IQF | -90 ºC / 4 Sem a - 3 ºC | 1,2 |
El efecto se evidencia de igual manera en la retención del ácido ascórbico (Cuadro 4), donde hay una total retención en las muestras congeladas de manera isocórica y una disminución en las congeladas por el proceso isobárico e IQF. El aumento en el contenido del ácido en las muestras procesadas en cuarto frío podría estar relacionado a un efecto de la maduración como lo han reportado otros autores (Gürbüz et al., 2020; Katirci et al., 2020). Los compuestos fenólicos son afectados de la misma manera mediante la actividad enzimática. Dicha actividad es menor durante la congelación isocórica debido a la ausencia de formación de cristales de hielo (Bilbao-Sainz et al., 2021).
En el estudio realizado en cerezas por Bilbao-Sainz et al. (2019), las muestras procesadas a volumen constante retuvieron en su totalidad el contenido de ácido ascórbico comparado con una muestra fresca. Lo anterior es debido al leve daño celular ocurrido en las cerezas a diferencia de los otros métodos, donde la retención fue menor debido a la actividad enzimática derivada del efecto negativo sobre las células del alimento.
En una investigación se demostró que no existió un efecto negativo de la presión hidrostática (presente en un sistema isocórico) sobre compuestos con enlaces covalentes, como lo son algunas vitaminas (Patras et al., 2009). Por su parte, el aumento en los compuestos fenólicos en las muestras sometidas a congelación isocórica podría estar relacionado a dos efectos: la extracción de dichos compuestos por el leve daño celular ocurrido o la síntesis de ácidos fenólicos debido al estrés sufrido por el alimento durante las condiciones de proceso (Bilbao-Sainz et al., 2019).
En el estudio también se observó la disminución de los compuestos fenólicos en las muestras procesadas bajo la tecnología isobárica e IQF. Esta reducción se relaciona de forma directa al incremento de la actividad de la polifenoloxidasa. Este efecto es derivado de la formación de cristales de hielo causantes del daño celular severo durante la congelación (Bilbao-Sainz et al., 2019).
Los datos para espinaca muestran una mayor retención del ácido ascórbico y la clorofila en las muestras sometidas a condiciones isocóricas. La pérdida de estos compuestos se debe a disminución de la actividad enzimática tanto de la ascorbato peroxidasa como de la clorofilasa, efecto que es incrementado con el daño celular ocurrido durante las operaciones de congelación (Bilbao-Sainz, Sinrod, Dao et al., 2020; Cocetta et at., 2014; Lin & Charng, 2021).
En el caso de la papa, el contenido de ácido ascórbico fue mayor en el proceso isocórico, sin embargo, todas las tecnologías presentaron pérdidas considerables. Lo anterior podría ser debido a la liberación del ascorbato oxidasa de las células dañadas durante la congelación, corte y pelado, esto genera como consecuencia una mayor interacción entre la enzima y el ácido correspondiente. Contrario al efecto en el ácido ascórbico, los compuestos fenólicos aumentaron después de cuatro semanas de almacenamiento, con valores de 81 %, 45 % y 82 % para los procesos isocórico, isobárico e IQF, respectivamente (Bilbao-Sainz, Zhao et al., 2020).
En las muestras sometidas a condiciones isocóricas, los resultados podrían ser explicados por el incremento en la actividad de la enzima fenilalanina amonio liasa debido al daño celular por el incremento en la presión durante la congelación (Formica de Oliveira, 2017). Mientras que los datos obtenidos del proceso IQF e isobárico podrían deberse a dos efectos contrarios: un incremento en el contenido de compuestos fenólicos por el daño celular ocurrido y una disminución por la actividad de la polifenoloxidasa al entrar en contacto con los compuestos fenólicos en estudio (Bilbao-Sainz, Sinrod, Dao et al., 2020).
Efecto en bacterias
Diferentes bacterias han sido estudiadas bajo condiciones isocóricas con la finalidad de evaluar si la tecnología de congelación en estudio tiene un efecto sobre ellas. Escherichia coli no patogénica fue evaluada por Salinas-Almaguer et al. (2015), a tres diferentes temperaturas: - 15 ºC, - 20 ºC y -30 ºC. Los resultados muestran que en las temperaturas más bajas hay una inhibición parcial de la población de bacterias, mientras que a -15 ºC hay una reducción total de la carga bacteriana. Lo anterior es explicado debido a que a -20 ºC y -30 ºC existe formación de hielo III y hielo I (Figura 1) donde E. coli utiliza los cristales formados como refugio para replicarse después del proceso de congelación (Nida et al., 2021; Salinas-Almaguer et al., 2015).
Entre los resultados de un estudio realizado, se obtuvo una disminución de 2,5 logaritmos de una población de E. coli no patogénica a -15 ºC / 145 MPa y -20 ºC / 186 MPa después de 12 h de proceso (Powell-Palm et al., 2018). Además, se reportó una disminución del 75 % de la población después de 24 h a -20 ºC. Los estudios mencionados concluyen que hay un mayor efecto sobre la muerte celular debido las altas presiones hidrostáticas generadas dentro de una cámara isocórica, que debido al daño por temperatura, deshidratación celular y formación de cristales de hielo en procesos isobáricos (Power-Palm et al., 2018; Salinas-Almaguer et al., 2015).
Otras bacterias patógenas también han sido foco de estudio bajo condiciones de congelación isocórica. Los resultados muestran que la operación isocórica a temperatura de -15 ºC durante 24 h reduce la población de Listeria monocytogenes y Salmonella Typhimurium a niveles no recobrables. La mayor eficiencia de este efecto ocurrió después de 6 y 12 h para L. monocytogenes y Salmonella Typhimurium, respectivamente (Bridges et al., 2020). Además, se evidenció la presencia de células desfiguradas con separaciones de regiones del citosol y las paredes celulares. Lo cual demuestra que las condiciones isocóricas son capaces de lograr una reducción considerable de estas bacterias patógenas (Bridges et al., 2020).
Al comparar el efecto entre una congelación isocórica y una isobárica se demostró que a las temperaturas de -4 ºC y -7 ºC, la reducción en las poblaciones de las bacterias Listeria monocytogenes y Salmonella enterica serovar Typhimurium fue de menos de 1 logaritmo. Caso contrario ocurrió a las muestras sometidas a -15 ºC. Los resultados indican que la operación isocórica redujo casi en su totalidad a la población bacteriana y la operación isobárica obtuvo reducciones de 2,1 logaritmos para L. monocytogenes y 1,3 para S. entérica serovar Typhimurium (Bridges et al., 2020). Un efecto similar obtuvieron Powell-Palm et al. (2018), ya que a temperaturas de -15 ºC y -20 ºC bajo condiciones isocóricas la población de E. coli se redujo en 2,5 logaritmos. Mientras en condiciones isobáricas solo se obtuvo 1 logaritmo de reducción. Los resultados anteriores muestran una efectividad del proceso isocórico. Aun así, el efecto en otros tipos de microorganismos, así como el efecto de la tecnología sobre los microorganismos en una matriz alimentaria deben ser estudiados a profundidad.
Efectos energéticos, ambientales y económicos
La congelación de alimentos es una técnica de gran demanda energética. Se estima que solo el almacenamiento a bajas temperaturas doméstico representa un 4 % de la energía global consumida por año (Dupont et al., 2019). Mientras que las emisiones de carbono relacionadas a este proceso rondan las 6,54 x 108 toneladas anuales (Zhao, Powell-Palm et al., 2021). Debido a esto, se han desarrollado estudios para evaluar los efectos energéticos y ambientales relacionados a la congelación isocórica.
Los resultados obtenidos del análisis termodinámico desarrollado por Powell-Palm & Rubinsky (2019), muestran que la congelación isocórica podría reducir un 70 % del consumo energético respecto a los procesos isobáricos. Además, bajo un modelo teórico desarrollado, se estima un ahorro energético de 6,49 miles de millones de kWh acompañado de una reducción de 4,56 miles de millones de kg en las emisiones de carbono (Zhao, Powell-Palm et al., 2021). La reducción en emisiones de carbono y en gasto energético están dados por la ausente formación de hielo durante el proceso a volumen constante. Lo antes descrito permite tanto beneficios de calidad en el alimento como económicos (Nida et al., 2021).
Al comparar entre un proceso de congelación isocórica a -5 ºC y uno isobárico a -18 ºC (temperaturas ideales para cada tipo de congelación), los resultados muestran que, bajo dichas condiciones, sería posible una disminución de consumo de 148 millones de KWh de electricidad. Esto es equivalente a un ahorro de 19,28 millones de dólares. De igual manera, se estima un ahorro aproximado de 849,33 millones de dólares anuales. Esto al considerar un cambio en el tipo de congelación aplicado, es decir pasar de la congelación isobárica a -18 ºC a una congelación isocórica a -5 ºC (Zhao, Powell-Palm et al., 2021).
La implementación de una cadena global de congelación isocórica no requiere de cambios importantes en la estructura mundial de los sistemas de congelación. Esto se explica debido a que es un modo de almacenamiento de alimentos dentro de un sistema de congelación ya existente. Lo antes descrito evita el impacto logístico y económico que representaría reemplazar las miles de unidades de congeladores domésticos e industriales ya existentes (Powell-Palm & Rubisnky, 2019).
Oportunidades de estudio en la congelación isocórica
Los resultados obtenidos de las diferentes investigaciones realizadas muestran un gran potencial de la tecnología de congelación isocórica. Sin embargo, es necesario estudiar a profundidad ciertos efectos adversos evidenciados.
La primera oportunidad de mejora en los procesos isocóricos deriva de que existe un daño en los alimentos cuando se empieza a disminuir la temperatura y aumentar la presión. Dicho fenómeno es evidenciado en las diferentes matrices vegetales estudiadas, y se relaciona con el aumento en la presión hidrostática y el efecto negativo de este fenómeno sobre los tejidos de los alimentos (Bilbao-Sainz et al., 2019; Bilbao-Sainz, Sinrod, Dao et al., 2020; Bilbao-Sainz, Zhao et al., 2020; Bilbao-Sainz et al., 2021; Zhao, Bilbao-Sainz et al., 2021). Por lo tanto, es necesario optimizar las combinaciones de temperatura y presión para realizar el proceso que afecte en menor medida a la calidad del alimento. Además, las condiciones determinadas deben ser específicas para cada alimento y en una segunda etapa ser sujetas al escalamiento industrial.
Como segundo campo de estudio, la sobrevivencia del nemátodo Caernorhabditis elegans durante un proceso de congelación isocórica (Mikus et al., 2016), permite plantear la hipótesis de si otros parásitos pudieran también sobrevivir a dicho proceso, lo cual supondría un problema de inocuidad en alimentos congelados bajo esta tecnología. La congelación tradicional por su parte, genera un efecto más letal sobre los parásitos (Podolska et al., 2019). Lo anterior también difiere del efecto positivo evidenciado en las investigaciones realizadas con bacterias donde se demostró una reducción considerable de la carga (Bridges et al., 2020; Nida et al., 2021; Powell-Palm et al., 2018; Salinas-Almaguer et al., 2015). Además, es necesario realizar estudios microbiológicos, tanto de bacterias como parásitos. Estos estudios deben ser en matrices alimentarias para así evidenciar si el alimento tiene algún efecto, sea positivo o negativo, sobre la sobrevivencia del microorganismo en estudio. Las investigaciones planteadas permitirían tener un mejor panorama del efecto de la tecnología sobre la sobrevivencia microbiana y tener un mejor entendimiento de la calidad e inocuidad de los alimentos que se deseen preservar bajo esta tecnología.
Otro campo de estudio es el uso de soluciones hipertónicas. Se ha evidenciado que es posible un aumento en la masa del alimento, posterior a ser sometidos a la congelación isocórica (Bilbao-Sainz, Sinrod, Dao et al., 2020; Bilbao-Sainz et al., 2019; Zhao, Bilbao-Sainz et al., 2021). Por lo tanto, el utilizar soluciones hipertónicas en los procesos isocóricos permitiría una nueva forma de fortificación de alimentos (Rubinsky, 2021). Esto mejora la calidad y a su vez, reduce las pérdidas nutricionales provocadas por el efecto de la operación (presión y temperatura). También es importante considerar que la mayoría de los estudios realizados sobre el efecto de la congelación isocórica en alimentos fueron desarrollados en frutas y vegetales, lo cual representa solo una parte del mercado mundial de alimentos congelados. Cuando se evaluó el efecto de la congelación isocórica sobre el músculo de pescado, los resultados mostraron que a -5 ºC en condiciones isocóricas el músculo mantuvo sus características morfológicas en relación con el músculo fresco y no presentó deshidratación celular (Năstase et al., 2017). También se identificó un menor daño de muestras de tilapia sometidas a congelación isocórica respecto a la congelación tradicional (Bilbao-Sainz, Sinrod, Williams et al., 2020).
En un estudio en donde se investigó el efecto de la congelación isocórica sobre la preservación de corazones de rata, dio una aproximación al comportamiento esperado para tejido animal que no provenga de pescados. De dicho estudio es posible concluir que a temperaturas de - 4 ºC o mayores el tejido animal se preserva. Lo contrario ocurre cuando se utilizan temperaturas menores, ya que el aumento en la presión hidrostática empieza a ejercer un efecto negativo en la matriz (Wan et al., 2018).
Los resultados obtenidos, tienen implicaciones en el ámbito alimentario debido a que permitiría obtener carnes congeladas con mejores características de calidad. Por lo tanto, es vital desarrollar más investigaciones en diferentes categorías de alimentos para así evidenciar el efecto del proceso sobre los productos que abarcan todo el mercado de alimentos congelados. Es necesario el diseño de los equipos que permitan escalar las investigaciones realizadas a nivel industrial. El uso de una cámara rígida capaz de soportar altas presiones supone un reto para lograr trasladar dicho sistema a la industria alimentaria, lo cual abre otro campo importante de desarrollo e investigación.
Conclusiones
La congelación isocórica produce mejoras en la calidad de los productos congelados estudiados. Los parámetros de proceso, diseño de equipos y futuros estudios en diferentes campos deben ser optimizados y realizados con la finalidad de respaldar las investigaciones hasta ahora desarrolladas. De manera que, se ponga en práctica la tecnología en la industria alimentaria y en los hogares de las personas. Además, los efectos ambientales y económicos de la congelación isocórica beneficiarían al mercado de alimentos congelados. Esto, mediante un sistema de congelación más eficiente y con productos de mayor calidad para toda la población.