Introducción
La hipertensión arterial (HTA) es una enfermedad crónica en la que los vasos sanguíneos tienen una tensión permanentemente elevada. (OMS, 2019) En su fisiopatología son centrales los cambios en la resistencia vascular periférica. La pulpa dental es un tejido altamente vascularizado, inervado y colagenizado (Cárdenas, 2011) Vale la pena analizar si los cambios en la resistencia periférica que afectan de manera sistémica al paciente ante una crisis antihipertensiva tienen manifestaciones en la resistencia periférica de los vasos pulpares.
La HTA se describe principalmente por presentar:
Disfunción endotelial
Ruptura del equilibrio entre los factores relajantes del vaso sanguíneo, como el óxido nítrico (NO), el factor hiperpolarizante del endotelio (EDHF) y los factores vasoconstrictores, en especial la endotelina o el factor de necrosis tisular beta (TGF-β ). (Wagner, 2010)
Todo ello produce vasoconstricción y favorece el remodelado vascular, causando hipertrofia e hiperplasia del músculo liso de la capa media de las arteriolas de resistencia, dificultando el paso de la sangre, ocasionando que el corazón trabaje más de lo que suele hacerlo. (Gomes et al., 2014). Es conocido el decremento a nivel del endotelio de la prostaciclina PGI2 vasodepresora y el incremento relativo del tromboxano TXA2 intracelular vasoconstrictor. (Wagner, 2010)
Por otro lado, hay un aumento en la resistencia vascular periférica a nivel precapilar, incluyendo las arteriolas y las pequeñas arterias debido a alteraciones estructurales y funcionales. La remodelación vascular de estos vasos contribuye al desarrollo de la hipertensión y su asociado daño en los órganos blanco. La resistencia periférica incrementada está relacionada con un descenso en el número de vasos y una disminución de su luz, sin aumentar el grosor de la pared. (Mulvany et al., 1993; Gamboa, 2006)
Además, múltiples factores que controlan la presión arterial contribuyen también al desarrollo de la hipertensión. Los mecanismos hormonales (hormona natriurética, renina angiotensina-aldosterona) o trastornos en los electrolitos (sodio, cloruro, potasio). La hormona natriurética causa un aumento de las concentraciones de sodio en las células, lo que lleva a un aumento de la presión arterial. El sistema renina angiotensina aldosterona regula el volumen de sodio, potasio y sangre, que finalmente regulará la presión arterial en las arterias. (Bell, 2015) Igual mente de sus acciones propiamente vasculares, causa estrés oxidativo a nivel del tejido, el que ocasiona tanto modificaciones estructurales como funcionales, principalmente disfunción endotelial, que establecen la patología hipertensiva. (Wagner, 2010) La angiotensina II provoca el estrechamiento de los vasos sanguíneos, aumenta la liberación de sustancias químicas que elevan la presión arterial y aumenta la producción de aldosterona. La constricción de los vasos sanguíneos aumenta la presión arterial. La aldosterona hace que el sodio y el agua permanezcan en la sangre. Como resultado, hay un mayor volumen sanguíneo, lo que aumentará la presión sobre el corazón, ocasionando HTA. (Bell, 2015)
El remodelamiento vascular, dado por el SRAA (Sistema renina-angiotensina-aldosterona), es diferente en las arterias grandes y en las pequeñas. Se habla de una remodelación hipertrófica; y de una remodelación eutrófica, respectivamente. (Wagner, 2010)
En cuanto al sistema nervioso simpático, el incremento en la actividad de este aumenta la presión sanguínea y permite el desarrollo y mantenimiento de la hipertensión por medio de la estimulación del corazón, de la vasculatura periférica y de los riñones, generando un incremento en el gasto cardiaco, en la resistencia vascular y en la retención de líquidos. Los mecanismos del aumento de la actividad simpática son complejos e involucran alteraciones en los barorreceptores y quimiorreceptores. (Gamboa, 2006) Los barorreceptores los cuales se encuentran situados en las paredes de diversos vasos sanguíneos son capaces de detectar irregularidades en la presión arterial normal (Estañol, 2009) por lo que son reajustados a nivel más alto en los pacientes hipertensos, principalmente por acción de la angiotensina II y por el efecto de radicales libres y la endotelina. (Gamboa, 2006)
La pulpa dental es un tejido especializado y vascularizado. Se localiza encerrado dentro de un medio sólido y rígido, sin la posibilidad de distenderse para aumentar su volumen durante la vasodilatación y la presión tisular incrementada, que se da ante cualquier tipo de noxa que sufra el diente. (Cárdenas, 2014) La integridad de las funciones pulpares es regulada por su microcirculación pulpar, (Kim et al.,1989) se le conoce de esta forma por la ausencia de venas o arterias, ya que los vasos más grandes que se encuentran son las vénulas y las arteriolas. Con respecto a las últimas, presentan un diámetro de 50 nm, las cuales son el sitio principal de resistencia al flujo sanguíneo, y los pequeños cambios en su calibre causan grandes diferencias en la resistencia periférica total.
Por otra parte, las vénulas son las encargadas de la recolección, pues son las primeras en recibir el flujo sanguíneo proveniente del lecho capilar. Están caracterizadas por presentar músculo liso. Dentro de sus funciones se puede mencionar que participan en la regulación de la presión hidrostática postcapilar. Además, las derivaciones de las anastomosis arteriovenosas, permiten el control regional del flujo sanguíneo de la pulpa a través de la derivación directa de la sangre desde las arteriolas a las vénulas. Por otro lado, los capilares presentan una pared de espesor de 0,5 µm, la cual está formada por una única capa de endotelio, rodeada por una membrana basal y un grupo de fibras reticulares y colágenas, sirviendo como una membrana semipermeable. (Harold, 2002)
Los vasos sanguíneos presentes en la pulpa dental poseen receptores α- adrenérgicos y β- adrenérgicos y otros receptores putativos en sus paredes. (Kim, 1989)
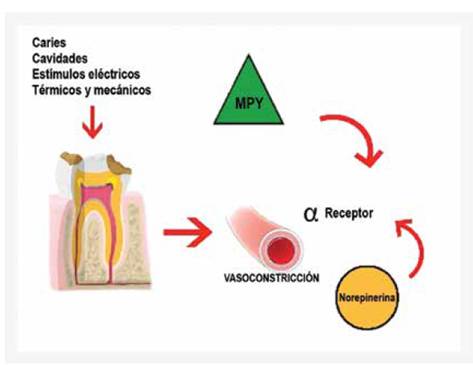
La activación del sistema nervioso, ante diferentes situaciones de estrés, estimula el neuropéptido Y (NPY), el cual se libera junto con la noradrenalina. En el tejido pulpar, los diferentes tipos de estímulos, activan las fibras nerviosas simpáticas provocando la constricción de los vasos sanguíneos pulpares y disminuye la presión del líquido del tejido. Estos efectos pueden atribuirse a los efectos de NPY y norepinefrina. (Figura 1) (Caviedes-Bucheli et al., 2004) Se ha demostrado que la vasoconstricción simpática es dirigida por receptores adrenérgicos ubicados en las células del músculo liso vascular y en las vénulas y arteriolas. (Abdulmesih, 2011)
El sistema de microcirculación regula el flujo sanguíneo en respuesta a diferentes tipos de estímulos, como por ejemplo los inflamatorios, causando cambios en las propiedades circulatorias y en la expresión endotelial. (Harold, 2002)
En los últimos años, se ha vuelto cada vez más evidente que la hipertensión es un proceso inflamatorio (McMaster, 2015; Pastelin, et al., 2007) que implica la transmigración y la acumulación tanto de las células inmunitarias innatas y las adaptativas en el intersticio de los tejidos afectados donde liberan citoquinas y promueven el estrés oxidativo. (McMaster, 2015) Con la medición de los diversos marcadores de inflamación sistémica en la HTA, se pretende profundizar en el conocimiento de la fisiopatología de la hipertensión arterial. (Pastelin et al., 2007)
La hipertensión está asociada con células T y la acumulación de monocitos y macrófagos tanto en los vasos sanguíneos como en el riñón, las cuales producen citoquinas que afectan la función de ambas estructuras. (McMaster, 2015) Diversas citoquinas como la interleucina-6 (IL-6) y algunos reactivos de fase aguda de inflamación como la proteína C reactiva (PCR), son considerados como mediado- res los principales sistémicos. La PCR favorece el desarrollo de la disfunción endotelial al reducir la producción de NO. Asimismo, se consideran al fibrinógeno, al amiloide sérico A, al factor de necrosis tisular (TNF-α ), al factor nuclear de transcripción inflamatoria kB (NFkB), y a las moléculas de adhesión intercelular (ICAM-1) y vascular (VCAM-1) como marcadores dentro del proceso inflamatorio de esta patología. (Pastelin et al., 2007)
Por otra parte, cuando se presenta alguna noxa a nivel dental, también hay un aumento de las concentraciones de citoquinas y mediadores inflamatorios en los tejidos periapicales de los dientes afectados endodónticamente. (Barkhordar et al., 1999)
Las citoquinas proinflamatorias, tales como la interleucina-1 β (IL- 1 β), IL-6, interleucina-11 (IL-11), interleucina- 17 (IL-17) y factor de TNF-α, son secretadas por los leucocitos principalmente, los cuales se encuentran relacionadas con la respuesta periapical inmune. Estas células y los mediadores inflamatorios juegan un rol importante en la patogénesis de la periodontitis apical crónica. (Ajuz et al., 2014). A medida que avanza el proceso de resorción ósea, el área donde se está produciendo la enferme- dad se convierte en un reservorio para marcadores inflamatorios como las citoquinas mencionadas anteriormente, anticuerpos y PCR. (Gomes et al., 2014)
En cuanto a la IL-6 es un mediador importante de la respuesta del huésped ante una lesión e infección tisular. En un estudio realizado por Barkhordar y col. se examinó el nivel de IL-6 en seis pulpas inflamadas y seis lesiones periapicales en humanos de origen endodóntico mediante la técnica de ELISA, se demostraron niveles significativos de IL-6 en comparación con pulpas sanas indicando que la IL-6 es producida y liberada local- mente en la pulpa inflamada y en lesiones periapicales. (Barkhordar et al., 1999)
Al mismo tiempo, las dos acciones principales de los mediadores de la inflamación son las alteraciones en el flujo sanguíneo de la pulpa y el aumento de la permeabilidad capilar, que conducen a la extravasación de plasma. El aumento de la permeabilidad de los vasos permite el escape de proteínas plasmáticas y leucocitos de los capilares hacia el área inflamada para llevar a cabo la neutralización, dilución y fagocitosis del agente irritante. En la pulpa inflamada, los loops vasculares, las anastomosis, el aumento del flujo sanguíneo y del linfático pueden representar cambios protectores contra la inflamación. (Harold, 2002)
Dentro de las similitudes, cabe mencionar que en la HTA se afectan vasos sanguíneos que en común se encuentran en el tejido pulpar, y en ambos se liberan ciertos mediadores durante el proceso de inflamación. A pesar de esto, la microcirculación pulpar no logra presentar grandes cambios, debido a los diferentes procesos de defensa que presenta, como se pueden mencionar:
Los puntos de ramificación de las arteriolas terminales y los capilares están caracterizados por la presencia de grupos de músculo liso que sirven como esfínteres precapilares. Estos esfínteres están bajo el control neuronal y celular y actúan regulando el flujo sanguíneo local por medio de un lecho capilar. Estas unidades funcionales permiten detectar cambios en el flujo sanguíneo y filtración capilar. Por lo tanto, la inflamación de la pulpa puede provocar una respuesta circulatoria localizada restringida al área de la inflamación y no necesariamente produce cambios circulatorios en toda la pulpa. (Harold, 2002)
Además, las anastomosis arteriovenosas en los procesos inflamatorios que incrementan la resistencia de la sangre, tienen la capacidad de redirigir la entrada de sangre, y se aumenta el flujo sanguíneo, por acción de fibras nerviosas a las células pulpares para ofrecerles más nutrientes y dar paso a las células inmunitarias. También, los vasos linfáticos existentes en la pulpa funcionan como vía a los ganglios linfáticos para las células dendríticas que capturan y exhiben los antígenos a los linfocitos, iniciando la respuesta del sistema inmunológico, es decir, la migración de los leucocitos. (Bergenholtz, 2011)
También, debido a que mediadores químicos como la histamina, serotonina, bradiquinina, prostaglandinas y otros vasoactivadores serán liberados durante el proceso inflamatorio de las células dañadas, para iniciar un proceso de reacción donde el tejido va a combatir la injuria. (Kim, 1985) Por lo que, la respuesta circulatoria de la pulpa dental ante un estímulo inflamatorio es la causa de que la HTA no afecte dicho tejido en los pacientes que padezcan de dicha enfermedad.