Introducción
Las enfermedades crónicas no transmisibles (ECNT) son una de las grandes epidemias del siglo XXI. Estas, matan a 41 millones de personas por año, el 71% de todas las muertes que se producen alrededor del mundo; dentro de estas se encuentran las enfermedades cardiovasculares, el cáncer, las enfermedades respiratorias crónicas y la diabetes1.
Por otro lado, las enfermedades cardiovasculares (ECV) son la primera causa de deceso a nivel global. En el año 2015 fallecieron 17,5 millones de personas, el equivalente al 31% de todas las defunciones registradas a nivel mundial; 7,4 millones se debieron a cardiopatía coronaria. Más de tres cuartas partes de las defunciones por ECV ocurren en los países de bajos ingresos2. El creciente aumento en la tasa de mortalidad a nivel mundial por alteraciones cardiovasculares responde a factores como el envejecimiento, sobrepeso y obesidad, hipertensión arterial (HTA), sedentarismo, entre otros; hasta el 30% de los pacientes fallecen en el primer año tras el primer episodio (Agra Bermejo et al., 2018)3,4.
La insuficiencia cardiaca (IC) se define como un síndrome clínico que puede diferenciarse por diversos síntomas, principalmente edema en tobillos, disnea y fatiga5. Además, puede presentar signos causados por una alteración miocárdica estructural o funcional, como crépitos pulmonares, edema periférico e hipertensión venosa yugular6. La IC puede llevar a una disminución del gasto cardiaco o aumento de la presión sanguínea en las cavidades cardiacas al someterse a estrés o en reposo, Lo que conduce al miocardio a una progresiva desadaptación7.
En el desarrollo de la insuficiencia cardiaca intervienen varios procesos fisiopatológicos que desencadenan un desequilibrio circulatorio como el estrés oxidativo, la activación neurohormonal, y la reacción inflamatoria8. El estrés oxidativo se vincula a un exceso de moléculas de oxígeno que reaccionan con el óxido nítrico, alterando la señalización fisiológica produciendo moléculas tóxicas y reactivas (aminotioles, pe- roxinitrito, isoprostano). Estas moléculas aumentan el catabolismo de las purinas, (Uno de los compuestos químicos que las células usan para elaborar los elementos fundamentales del ADN y el ARN)9.
Tras la destrucción de las purinas se incrementa la actividad de la xantina oxidasa (enzima que cataboliza las purinas), las concentraciones séricas de ácido úrico y aumenta la liberación de mieloperoxidasa (enzima responsable de la actividad microbicida) por los neutrófilos y monocitos, favoreciendo la necrosis y remodelado miocárdico10.
La activación neurohormonal implica la respuesta de varios sistemas compensatorios, el aumento del sistema nervioso simpático, la acción de los sistemas renina-angiotensi- na-aldosterona reteniendo líquidos y sodio11. Además, existe una activación de la arginina-vasopresina (también conocida como hormona antidiurética), quien controla la reabsorción de moléculas de agua en el cuerpo, y el sistema de péptidos natriuréticos opositores del sistema renina-angiotensina aldosterona12. La reacción inflamatoria incluye la activación de la respuesta del sistema inmune, aumento de mediadores proinflamatorios (factor de necrosis tumoral, interleucina-1, interleucina-6 y ST2) y producción de anticuerpos13-15.
Dentro del tratamiento de la IC hay aspectos a tomar en cuenta que podrían ser focos de atención, dado que existen usuarios que presentan sintomatología o cuadros clínicos distintos. Estas manifestaciones específicas requieren de una mayor atención pudiendo complicar el estado de la insuficiencia cardiaca presentando restricciones conductuales, de- presión, estrés, valvulopatías, infecciones, endocrinopatías y miocardiopatías16.
Los aspectos esenciales del tratamiento no farmacológico en la IC son el autocuidado y un buen seguimiento del tratamiento. El autocuidado debe contemplar diferentes aspectos como la promoción del ejercicio, prevención de situaciones que puedan acelerar la sintomatología de la enfermedad, limitación del consumo de sustancias nocivas (tabaco, alcohol, sustancias psicoactivas, otras), el autocuidado, y una dieta baja en sodio.
Una dieta hiposódica en personas con IC reduce el acumulo anormal de líquidos corporales, el edema periférico y central, el estrés en la pared ventricular y mejora la percepción sobre el patrón respiratorio17. Por otro lado, el ejercicio físico realizado de manera frecuente, aun cuando se realicen sesiones cortas, de ejercicio (15 minutos) contribuye a controlar factores asociados a las ECV, como la HTA, la obesidad, el sedentarismo, entre otros18.
El ejercicio físico en la IC provoca un acondicionamiento significativo de las estructuras periféricas, como cambios hemodinámicos que contribuyen a parar o revertir el progreso establecido de la IC19. Otras de las modificaciones del ejercicio en la IC es el aumento del gasto cardiaco máximo, volumen de eyección pico y velocidad llenado diastólico, además de retrasar el remodelado del ventrículo izquierdo, mejorando así la tolerancia al ejercicio que por ende repercutirá en la calidad de vida de los pacientes20.
El ejercicio ha demostrado ser una modalidad terapéutica segura y efectiva para la insuficiencia cardíaca. El High Intensity Interval Training (HIIT) consiste en la alternancia de periodos de ejercicio aeróbico intenso con periodos de recuperación pasiva o activa a intensidad media/moderada21. El principal interés recae en que este tipo de entrenamiento ofrece la posibilidad de mantener la intensidad alta del ejercicio durante periodos más largos que con el ejercicio continuo; es un método de entrenamiento conveniente para mejorar la capacidad aeróbica máxima22.
El HIIT es una de las herramientas terapéuticas actuales con mayor tendencia por su utilidad23. En esta intervención se aplican estímulos de ejercicio más altos en los músculos esqueléticos a través de una mayor intensidad de ejercicio24. De hecho, el HIIT está siendo cada vez más usado por los beneficios que aporta en términos de capacidad aeróbica y la posibilidad de revertir la remodelación del ventrículo izquierdo25. Así, este estudio pretende revisar cuáles son los efectos del entrenamiento interválico de alta intensidad en pacientes adultos con falla cardiaca.
Materiales y métodos
Diseño
Se realizó una revisión sistemática con análisis descriptivo y cronología retrospectiva, de artículos científicos publicados en bases de datos indexadas entre Enero del año 2015 a Enero del año 2019. Todos los estudios donde se realizaron intervenciones con seres humanos contaron con un consentimiento informado y la aprobación para que los datos fuesen usados con fines de divulgación científica.
Estrategia de búsqueda
Se realizó una revisión sistemática bajo las consideraciones de la Colaboración Cochrane para la elaboración de estudios de revisión y meta-análisis. Por otro lado, se accedió a los criterios de la Declaración de PRISMA26 (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) para la inclusión de ensayos clínicos y otros tipos de estudios en revisiones sistemáticas.
Se usaron descriptores asociados a las variables descritas en el título del estudio: HIIT & heart failure; y los operadores booleanos: AND & OR. Así, la estrategia de búsqueda fue la siguiente: (high intensity intervalic training OR cardio- vascular rehabilitation OR physical therapy OR physical activity OR exercise) AND (heart failure OR cardiac failure OR congestive heart failure OR cardiovascular disease).
Con base a lo anterior, se evaluó de la calidad metodológica de los estudios incluidos en la revisión sistemática bajo los 11 criterios para filtrar los estudios de investigación que no cumplen con una calidad metodológica con una alta validez y confiabilidad. Estos criterios permiten determinar si, sobre los ensayos clínicos, los sujetos fueron asignados al azar a los grupos, a asignación fue oculta, los grupos fueron similares al inicio en relación a los indicadores de pronóstico más importantes y los sujetos, terapeutas y los evaluadores que midieron los resultados fueron cegados.
De la misma manera, la escala de evaluación metodológica de ensayos clínicos de PEDro27 permite valorar si las medidas de los resultados fueron obtenidas de más del 85% de los sujetos inicialmente asignados a los grupos, si se presentaron resultados de todos los sujetos que recibieron tratamiento o fueron asignados al grupo control, o cuando esto no pudo ser, los datos fueron analizados por “intención de tratar”, los resultados de comparaciones estadísticas entre grupos fueron informados y si los estudios proporcionan medidas puntuales y de variabilidad de resultados. En tanto, se desarrolló la búsqueda de documentos en las bases de datos Redalyc, EMBASE, Medscape y MEDLINE, DOAJ.
Criterios de elegibilidad
Se tomaron en cuenta ensayos clínicos con asignación aleatoria en pacientes con insuficiencia cardiaca de mediana edad ≥50 años que hayan sido intervenidos en un programa de rehabilitación con ejercicios interválicos. Así mismo, estudios con fecha de publicación no mayor a 4 años en español o inglés.
Se excluyeron estudios no indexados en bases de datos científicas, como literatura gris (libros, tesis, trabajos de grado, otros) y estudios elaborados en animales. Artículos con pacientes que no presentan algún tipo de alteración de índole cardiaco y pacientes menores de edad. Así mismo, se eliminaron aquellos estudios que tras la evaluación del título, resumen y palabras clave se consideraron que no cumplían los criterios de aceptabilidad y estudios no concluyentes o que tras la evaluación de texto completo no respondían al objetivo de esta revisión.
Selección de estudios
La búsqueda y extracción de los diferentes documentos fue efectuado por un autor (CQ), revisados y examinados por un segundo colaborador (DP-JP) y consensuado por todos los colaboradores de la investigación. Por otro lado, la evaluación del cumplimiento de los criterios de selección fue desarrollada por un tercer participante (JC); la evaluación a texto completo se realizó por un cuarto miembro (JP) y la descripción de los datos por otros (AM-DG) de manera independiente.
Evaluación de la calidad
La calidad metodológica de las investigaciones se evaluó a través de los criterios de riesgo de sesgo de la Colaboración Cochrane y los criterios de la Escala de PEDro para la evaluación de la calidad metodológica por el autor principal (JP). Así, se definió el sesgo en la selección de estudios frente a los criterios de selección de los estudios y pérdidas de documentos.
Estrategia de búsqueda
Los estudios incluidos en esta revisión fueron evaluados de forma discriminada por dos revisores. De esta manera, se eliminaron los estudios duplicados que se obtuvieron en la búsqueda y luego se hizo una selección de los estudios de acuerdo con título y resumen. Los estudios filtrados luego de la evaluación anterior, fueron evaluados en su totalidad nuevamente de manera independiente por cada uno de los revisores, verificando los estudios que cumplían con los criterios de elegibilidad para su revisión completa.
Recolección de datos
Se extrajeron datos sobre la población, grupos de intervención y control, tipología de la patología, intervención, período y frecuencia de intervención y resultados. Dada la heterogeneidad en el análisis de datos, se efectuó una síntesis narrativa de los resultados de los estudios analizados.
Resultados
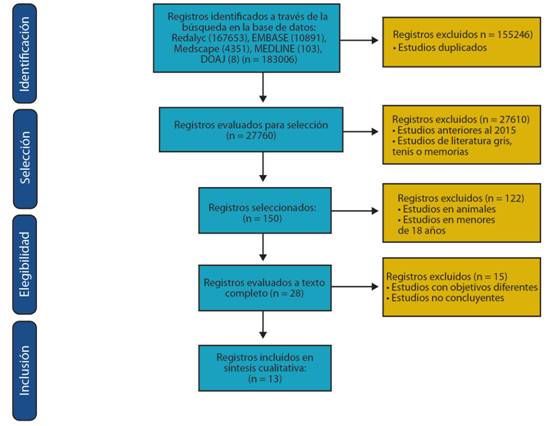
En tanto, se desarrolló la búsqueda de documentos en las bases de datos Redalyc (167653), EMBASE (10891), Medscape (4351), MEDLINE (103) y DOAJ (8). Por otro lado, también se realizó la búsqueda de ensayos clínicos en la base de datos de la Colaboración Cochrane (102) para evitar el sesgo de publicación de resultados.
En concordancia con los criterios de inclusión, se evaluaron 27760 estudios para filtrar literatura gris, estudios desarrollados en animales y estudios de tipo documental. Por otro lado, 150 estudios fueron incluidos para la revisión a título y finalmente se evaluaron 28 ensayos clínicos a texto completo (figura 1). A partir de la revisión completa de texto y de sus conclusiones se seleccionaron 13 ensayos clínicos para ser incluidos en la revisión.
En concordancia con los criterios de inclusión, se evaluaron 27760 estudios para filtrar literatura gris, estudios desarrollados en animales y estudios de tipo documental. Por otro lado, 150 estudios fueron incluidos para la revisión a título y finalmente se evaluaron 28 ensayos clínicos a texto completo (figura 1). A partir de la revisión completa de texto y de sus conclusiones se seleccionaron 13 ensayos clínicos para ser incluidos en la revisión.
Así, se sometieron a evaluación de calidad de evidencia los estudios incluido en la revisión; esta evaluación de la calidad metodológica se basó en las consideraciones metodológicas para ensayos clínicos de la Escala de PEDro para revisiones sistemáticas y meta-análisis (Tabla 1). De esta manera los estudios seleccionados se muestran en la Tabla 2, donde se describe el diagnóstico, la intervención, frecuencia y consideraciones tras la intervención.
Así, se sometieron a evaluación de calidad de evidencia los estudios incluido en la revisión; esta evaluación de la calidad metodológica se basó en las consideraciones metodológicas para ensayos clínicos de la Escala de PEDro para revisiones sistemáticas y meta-análisis (Tabla 1). De esta manera los estudios seleccionados se muestran en la Tabla 2, donde se describe el diagnóstico, la intervención, frecuencia y consideraciones tras la intervención.
A partir de lo anterior, se identificaron 554 sujetos con falla cardiaca, con una fracción de eyección reducida entre 27±9% y 65±5%. De otra manera, se intervinieron 275 pacientes con insuficiencia cardiaca a través de ejercicio interválico de alta intensidad (HIIT), y se controlaron 279 sujetos que fueron intervenidos con entrenamiento moderado continuo (MTC), ejercicio regular o que recibieron recomendaciones para realizar ejercicio desde el hogar con supervisión28-40.
Tabla 1 Escala de PEDro para la evaluación de la calidad metodológica de los estudios incluidos en la revisión (n = 13).
| Reference | P1 | P2 | P3 | P4 | P5 | P6 | P7 | P8 | P9 | P10 | P11 | Total |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Angadi, S., et al.28 | + | + | - | + | - | + | - | + | + | + | + | 8 |
| Benda, N., et al.29 | + | + | - | + | - | - | - | + | + | + | + | 7 |
| Benda, N., et al.30 | + | - | + | + | - | - | + | + | + | + | + | 8 |
| Cheng-Hsien, C., et al.31 | + | + | - | + | - | + | + | + | + | + | + | 9 |
| Chrysohoou, C., et al.32 | + | + | - | + | - | - | - | + | + | + | + | 7 |
| Ellingsen, Ø., et al.33 | + | + | + | + | - | - | + | + | + | + | + | 9 |
| Isaksen, K., et al.34 | + | - | + | + | - | - | - | + | + | + | + | 7 |
| Lima, B.E., et al.35 | + | - | - | + | - | - | - | + | + | + | + | 6 |
| Gayda, M., et al.36 | + | + | - | + | - | - | - | + | + | + | + | 7 |
| Safiyari-Hafizi, H., et al.37 | + | + | - | + | - | + | + | + | + | + | + | 9 |
| Spee, R., et al.38 | + | + | + | + | - | + | + | + | + | + | + | 10 |
| Tzanis, G., et al.39 | + | + | - | + | - | + | + | + | + | + | + | 9 |
| Zampier, A., et al.40 | + | + | + | + | + | + | + | + | + | + | + | 11 |
PEDro (Physiotherapy Evidence Data+base): + Sí; - No.
P1: Criterios de elección; P2: Asignación aleatoria; P3: Ocultamiento de la asignación; P4: Grupos similares en línea de base; P5: Cegamiento de los participan- tes; P6: Cegamiento de los terapeutas; P7: Cegamiento del evaluador; P8: Abandonos < 15%; P9: Análisis por intención a tratar; P10: Diferencias reportadas entre grupos; P11: Punto estimado y variabilidad reportada.
Sobre el protocolo de entrenamiento, los sujetos de los grupos de intervención fueron entrenados a partir de las di- rectrices basado en el trabajo desarrollado por Wisloff, et al.27 En 11 de los estudios identificados se intervino a los pacientes con falla cardiaca por 12 semanas con una frecuencia de 3 sesiones por semana30-40. Por otro lado, en los estudios restantes esta relación fue de 10 semanas (3días*semana), 4 semanas (3días*semana) y 2 sesiones28-29. El protocolo de entrenamiento consistió en tres fases: calentamiento, entrenamiento interválico de alta intensidad y relajación. El calentamiento duró entre 3 a 10 minutos a través de cicloergómetro, cinta rodante o bicicleta estática a una intensidad entre el 30% al 70% de la frecuencia cardiaca máxima.
El entrenamiento de alta intensidad fue desarrollado mediante bloques con intervalos entre 30 segundos y 4 minutos con ciclos de trabajo hasta del 100% y hasta alcanzar una FCM entre 75% y 95%. Por otro lado, el enfriamiento duró en promedio 5 minutos a partir de una intensidad moderada; algunos estudios incluyeron ejercicios de resistencia y fuerza. A pesar de un mayor estrés miocárdico en pacientes con insuficiencia cardíaca, ni el ejercicio de resistencia ni el HIT conducen a una liberación excesiva de biomarcadores cardíacos indicativos de daño cardíaco agudo27. Algunos estudios no consideran que exista diferencia entre un programa de in- tensidad moderada o alta. También se considera que, si bien existen mejoras significativas en los parámetros de la aptitud física, no se observan mejoras en la función cardiovascular en reposo o en la calidad de vida; sin embargo, en ningún caso estas conducen al deterioro de la función cardíaca28,28,30,33.
El HIIT durante 12 semanas podría elevar la tasa de consumo de O2 mitocondrial plaquetario a través del aumento de las actividades del Complejo I y II en pacientes con fracción de eyección reducida por falla cardiaca31. Además, promueve un aumento en el diámetro de la arteria braquial y una reducción en la presión arterial sistólica, pero no cambia la dilatación mediada por el flujo y la presión arterial diastólica35.
Otro de los efectos descritos a partir de la intervención en estos pacientes con el entrenamiento aeróbico de alta intensidad es el aumento en la oxidación de carbohidratos y lípidos en pacientes36. En caso de anomalías metabólicas musculares se recomienda los períodos de recuperación pasiva. En la misma medida, los protocolos de HIIT con recuperación activa se asociaron con un mayor gasto de energía, CHO y una menor oxidación de los lípidos. Además, se sugiere que El HIIT podría revertir la miopatía esquelética de los pacientes con insuficiencia cardíaca con las respuestas adaptativas del sistema de biorregulación IGF-1 y con esto disminuir la tasa de morbilidad asociada a la caquexia cardiaca39
Tabla 2 Características generales de los estudios incluidos (n = 13)
| Autor | n | Diagnóstico | Grupos | Intervención | Duración | Conclusiones |
|---|---|---|---|---|---|---|
| Angadi, S., et al.28 | 15 sujetos | IC NYHA clase II-III. Fracción de eyección del 65±5%. | I: 9 pacientes con IC. C: 6 pacientes con IC. | Los pacientes comenzaron con intervalos de 2 min de duración a 80-85% de FCM, separados por 2 min de recuperación a 50% de FCM para lograr un total de 16 min de ejercicio de alta intensidad. En la segunda semana de entrenamiento realizaron cuatro intervalos de 4 minutos a un 85-90% de FCM, separados por 3 minutos a un 50% de FCM. Cada sesión de entrenamiento comenzó con un calentamiento de 10 minutos al 50% de FCM y terminó con un enfriamiento de 5 minutos a la misma intensidad. | 4 semanas (3días*semana) | No se ha establecido la dosis óptima de HIIT, aunque la intensidad (~ 85-90% de FC máxima), la duración del intervalo (4 min) y el número (4), y la intensidad de recuperación entre intervalos (50% de FC máxima) y la duración (3 min), son consistentes con las recomendaciones recientes y pueden ser la prescripción óptima de ejercicio para pacientes con IC. El HIIT parece ser seguro y bien tolerado en pacientes con HFrEF y se ha informado que es preferible al MI-ACT en pacientes con HFrEF. |
| Benda, N., et al.29 | 27 sujetos | IC NYHA clase I-III. Fracción de eyección 35±8%. | I: 13 pacientes con IC. C: 14 pacientes sanos. | Ejercicios de resistencia isocalórica (30 minutos a 65% VO2max). HIT (10 * 1 minuto a 90% VO2max, alternados por 2,5 minutos a 40% VO2max) en orden aleatorio. Ambas sesiones de ejercicio incluyeron un calentamiento (10 minutos al 40% del pico de VO2) y un enfriamiento (5 minutos al 30% del pico de VO2). | 2 sesiones | A pesar de un mayor estrés miocárdico en pacientes con insuficiencia cardíaca, ni el ejercicio de resistencia ni el HIT conducen a una liberación excesiva de biomarcadores cardíacos indicativos de daño cardíaco agudo. |
| Benda, N., et al.30 | 20 sujetos | IC NYHA clase I-III. Fracción de eyección 38±6%. | I: 10 pacientes con IC. C: 10 pacientes con IC. | Períodos de ejercicio de 3,5 minutos, que consistían en intervalos de 1 minuto al 90% de la carga de trabajo máxima y de 2,5 minutos al 30% de la carga de trabajo máxima. | 12 semanas (3días*semana) | El HIIT durante 12 semanas en pacientes con IC se asocia con mejoras en los parámetros de la aptitud física, mientras que no se observan mejoras en la función cardiovascular en reposo o en la calidad de vida. |
| Cheng-Hsien, C., et al.31 | 34 sujetos | IC NYHA clase I-III. Fracción de eyección ≤ 40%. | I: 17 pacientes con IC. C: 17 pacientes con IC. | Ejercicios de calentamiento durante 3 minutos a 30% de VO2max y ejercicios de cinco intervalos de 3 minutos a 80% de VO2max. Cada intervalo fue seguido por un ejercicio de 3 minutos al 40% de VO2max. La sesión de ejercicios finalizó con un enfriamiento de 3 minutos al 30% de VO2peak. | 12 semanas (3días*semana) | El HIIT durante 12 semanas eleva la tasa de consumo de O2 mitocondrial plaquetario a través del aumento de las actividades del Complejo I y II. Además, la capacidad aeróbica sistémica se asocia positivamente con la tasa de consumo de O2 mitocondrial plaquetaria en pacientes con insuficiencia cardíaca. |
| Chrysohoou, C., et al.32 | 72 sujetos | IC NYHA clase II-IV. Fracción de eyección ≤50%. | I: 33 pacientes con IC. C: 39 pacientes con IC. | Ejercicio a una intensidad equivalente a un pico de trabajo del 80% y progresivamente a un pico de trabajo del 100% durante 30s, alternados con 30s de descanso. El entrenamiento de resistencia se desarrolló a una intensidad del 30% de la repetición máxima durante las primeras 2 semanas, seguidas de 3 semanas de entrenamiento con una intensidad de 50% y al 90% durante las semanas restantes. | 12 semanas (3días*semana) | El HIIT combinado con el ejercicio de fuerza, parece beneficiar la capacidad de dilatación aórtica y la presión sistólica aumentada en paralelo con la mejora de la función diastólica del ventrículo izquierdo y la calidad de vida. |
| Ellingsen, Ø., et al.33 | 215 sujetos | IC NYHA clase II-IV. Fracción de eyección <35%. | I: (MTC=73) (HIIT=82) pacientes con IC. C: 76 pacientes con IC. | HIIT realizó cuatro intervalos de 4 minutos con de 90-95% de la FCM separados por períodos de recuperación activa de 3 minutos de intensidad moderada. Las sesiones HIIT duraron 38 minutos, incluyendo calentamiento y enfriamiento a intensidad moderada. Las sesiones de MCT apuntaron al 60-70% de FCM y duraron 47 minutos. | 12 semanas (3días*semana) | No se confirma la hipótesis de que un programa de 12 semanas de entrenamiento supervisado con HIIT es superior al MCT para reducir la remodelación del ventrículo izquierdo en pacientes con IC. Ninguna de las intervenciones condujo al deterioro de la función cardíaca, y ambos programas de ejercicio aumentaron la capacidad aeróbica, |
| Isaksen, K., et al.34 | 38 sujetos | IC NYHA clase I- III. Fracción de eyección de 37.6±10.9%. | I: 26 pacientes con IC. C: 12 pacientes con IC. | El programa de entrenamiento incluyó 15 minutos de calentamiento a 60-70% de la frecuencia cardíaca máxima. Después del calentamiento, los pacientes realizaron cuatro intervalos de 4 minutos al 85% de FC máxima. Los intervalos se interrumpieron por 3 minutos de recuperación activa al 60-70% de la FC máxima. Un enfriamiento de 5 minutos. Cada sesión terminó con 15 minutos de ejercicios de fuerza, estiramiento y relajación. | 12 semanas (3días*semana) | Un programa de entrenamiento aeróbico interválico es factible y parece seguro en una población con IC estable y bien tratada. Además, este protocolo durante 3 meses produce un aumento significativo de la capacidad aeróbica y la función endotelial en esta población. |
| Lima, B.E., et al.35 | 16 sujetos | IC NYHA clase I- III. Fracción de eyección de >50%. | I: 16 pacientes con IC. | La sesión de HIIT comenzó con un calentamiento de 8 minutos a intensidad moderada seguido de cuatro bloques de 4 minutos cada uno a una frecuencia cardíaca máxima de 85-95%, alternados con 3 minutos a 60- 70% de frecuencia cardíaca máxima. La sesión terminó con 3 minutos de enfriamiento a intensidad moderada, totalizando 36 minutos. | 12 semanas (3días*semana) | Una sesión de HIIT promueve un aumento en el diámetro de la arteria braquial y una reducción en la presión arterial sistólica, pero no cambia la dilatación mediada por el flujo y la presión arterial diastólica. |
| Ribeiro, P.A., et al.42 | 18 sujetos | IC NYHA clase I- III. Fracción de eyección de 27±9%. | I: 18 pacientes con IC. | Los protocolos HIIT difirieron en la duración del intervalo (30 y 90 segundos) y el tipo de recuperación (recuperación activa al 50% frente a la recuperación pasiva 0%. Cada paciente hizo ejercicio durante un tiempo máximo de 30 minutos o hasta agotamiento debido a fatiga. | 1 semana (3días*semana) | El HIIT puede aumentar favorablemente la oxidación de carbohidratos y lípidos en pacientes con IC. Los episodios más cortos en HIIT con recuperación pasiva podrían ser beneficiosos en pacientes con IC con anomalías metabólicas musculares al comenzar un nuevo programa de ejercicios. Por otro lado, los protocolos HIIT con recuperación activa se asociaron con mayor gasto de energía y menor oxidación de lípidos. |
| Safiyari- Hafizi, H., et al.37 | 29 sujetos | IC NYHA clase I- III. Fracción de eyección de 27±9%. | I: 14 pacientes con IC. C: 15 pacientes con IC. | Los participantes se ejercitaron utilizando series de trabajo de alta intensidad (80- 85% VO2max) seguidas de períodos de recuperación activa (40-50% VO2max). La duración de cada intervalo varió y se individualizó cuidadosamente para cada paciente en función de su capacidad funcional. | 12 semanas (3días*semana) | La rehabilitación cardíaca supervisada en el hogar, combinada con ejercicios interválicos de alta intensidad y entrenamiento de resistencia, mejoran significativamente la capacidad de física, la calidad de vida y el consumo de oxígeno en el umbral ventilatorio. |
| Spee, R., et al.38 | 26 sujetos | IC NYHA clase II- III. Fracción de eyección ≤40%. | I: 12 pacientes con IC. C: 14 pacientes con IC. | Período de calentamiento de 5 min. y cuatro intervalos de 4 minutos con una carga de trabajo correspondiente al 85-95% del pico de VO2máx. Los intervalos se separaron mediante pausas activas de 3 min.. Después de completar las sesiones de intervalo, hubo un enfriamiento de 5 min. | 12 semanas (3días*semana) | El HIT mejoró en la capacidad máxima de ejercicio. Los efectos del HIT en la capacidad del ejercicio submáximo está mediado por una mejor compatibilidad entre el suministro de oxígeno microvascular y su utilización. |
| Tzanis, G., et al.39 | 26 sujetos | IC NYHA clase <III. Fracción de eyección 37±9 %. | I: 13 pacientes con IC. C: 13 pacientes con IC. | Seis pacientes se ejercitaron con HIIT durante 3 minutos al 50% de consumo de oxígeno máximo seguidos de 4 ciclos, alternando 4 minutos de ejercicio al 80% con 3 minutos al 50% de VO2max, para un total Duración de 31 min. Siete pacientes se ejercitaron con HIIT y entrenamiento de fuerza durante 3 minutos al 50% de VO2max seguidos de 2 ciclos, alternando 4 minutos de ejercicio al 80% de VO2max con 3 minutos al 50% de VO2max, para una duración total de 17 minutos, seguidos de 14 minutos de entrenamiento de fuerza. | 12 semanas (3días*semana) | El HIIT revierte la miopatía esquelética de los pacientes con insuficiencia cardíaca con las respuestas adaptativas del sistema de biorregulación IGF-1 que posiblemente contribuya a estos efectos. |
| Ulbrich, A., et al.40 | 18 sujetos | IC NYHA clase II- III. Fracción de eyección 40%. | I: 12 pacientes con IC. C: 10 pacientes con IC. | Período de calentamiento de 7 a 10 min. a una intensidad correspondiente al 70% de la frecuencia cardíaca máxima. Los pacientes caminaron con intervalos de 3 minutos a una intensidad equivalente a ~ 95% de la frecuencia cardíaca máxima. En promedio, los pacientes asignados al azar a HIIT realizarían 4-6 intervalos. Todas las sesiones de entrenamiento para MCT y HIIT finalizaron con un período de enfriamiento de 5 minutos al 50% del pico de VO2, con un total de 60 minutos por sesión. | 12 semanas (3días*semana) | Independientemente de la intensidad del ejercicio en pacientes con ICC, se obtiene una mejora significativa en la calidad de vida. La alta intensidad del ejercicio puede ser un factor importante para mejorar la capacidad aeróbica en pacientes con ICC. |
IC: insuficiencia cardiaca; NYHA: escala de la New York Heart Association; VO2: consumo máximo de oxígeno; FCM: frecuencia cardiaca máxima; HIIT: high intensity interval training; MCT: moderate continuous training; HFrEF: fracción de eyección reducida en falla cardiaca: HFpEF: heart failure with reduced ejection fraction.
Por otro lado, se ha descrito que el entrenamiento interválico de alta intensidad combinado con entrenamiento de resistencia mejora significativamente la capacidad de física, la calidad de vida y el consumo de oxígeno en el umbral ventilatorio37. Del mismo modo, el HIIT asistido por ejercicio de fuerza aumentan la capacidad de dilatación aórtica y la presión sistólica aumentada en paralelo con la mejora de la función diastólica del ventrículo izquierdo y la calidad de vida32; de esta manera, ejercicio aeróbico interválico de alta intensidad es seguro y bien tolerado en pacientes con fracción de eyección reducida en falla cardiaca.
A pesar de lo anterior, no se ha establecido la dosis óptima, no obstante, se recomienda intensidades entre 85-90% de FC máxima, duración de intervalo de 4 min e intensidad de recuperación entre intervalos al 50% de FC máxima por 3 min28,35,38. Así, el entrenamiento interválico de alta intensidad (HIIT) en pacientes con falla cardiaca en intervalos entre 30 segundos y 4 minutos con ciclos de trabajo hasta del 100% y FCM entre 75% y 95% no conllevaría a una liberación excesiva de biomarcadores cardíacos indicativos de daño cardíaco agudo y es seguro32.
El HIIT mejora la capacidad aeróbica en insuficiencia cardiaca y se sugiere que existe un aumento en el consumo máximo de oxígeno, reduce la presión arterial sistólica y mejora la función endotelial31,34,38,40. Por otro lado, se considera que en presencia de trastornos metabólicos es mejor los períodos de recuperación36,39. Además, se considera que no existe diferencia significativa entre el HIIT y el MCT.
Algunos de los estudios sugieren que el HIIT, aunque no aumenta el riesgo de mortalidad en pacientes con falla cardiaca, tampoco mejora significativamente el pronóstico, sin embargo, combinado con ejercicios de resistencia y fuerza tiene mayor impacto sobre el sistema cardiovascular, metabólico y musculo-esquelético32,37,39.
Lo anterior, aunque se ha descrito en algunos estudios, no puede aseverarse pues no existe evidencia actual que confirme este pre-dicho. Además de esto, solo se han descrito los efectos reportados actualmente del HIIT para el caso de pacientes con IC, sin embargo, otros estudios han descrito diferentes efectos en pacientes con enfermedad coronaria, revascularización miocárdica e implante cardiaco, entre otros41-44.
En un estudio de revisión desarrollado por Pinkstaff, et al.45 donde se describen y discuten los efectos del entrena- miento de alta intensidad en pacientes con insuficiencia cardiaca, se establece que, aunque el entrenamiento continuo de intensidad moderada (MITC) ha sido el estándar clínico para los pacientes con insuficiencia cardíaca, la evidencia de la eficacia del HIIT en estos pacientes es cada vez mayor. Este estudio sugiere que, en el caso del MITC, aunque no se haya asociado su práctica en pacientes IC con eventos adversos, los estudios realizados hasta la fecha son pocos y desactualizados, lo que sucede aún con el HIIT. De esta manera, se sugiere que se desarrollen investigaciones actualizadas que permitan definir un protocolo de intervención antes de considerarse en el estándar clínico para pacientes con insuficiencia cardíaca.
Por otro lado, Gomes, et al.46 en un meta-análisis incluyeron 13 ensayos clínicos con una población total de 411 pacientes con ICC. Este estudio comparó los efectos del MITC con el HIIT y demostró que, si bien el entrenamiento interválico de alta intensidad mejora el pico del VO2máx en pacientes con falla cardiaca y fracción de eyección reducida, no existe diferencia significativa con respecto al MICT en el entrenamiento de la capacidad aeróbica.
De la misma manera, Ballesta, et al.47 desarrollaron una revisión sistemática y meta-análisis con 19 ensayos clínicos para demostrar los efectos del HIIT en pacientes con falla cardiaca y en enfermedad coronaria (EC). Así este estudio demostró que el entrenamiento interválico de alta intensidad mejora significativamente el pico de VO2 en pacientes con IC y EC. No obstante, cuando el programa tenía una duración menor a 12 semanas no existieron diferencias significativas para los pacientes con falla cardiaca, pero sí en enfermedad coronaria. Además, no hubo cambios mejorías cuando la intensidad del HIIT fue del 40% del VO2max o menos.
De esta manera, estos datos sugieren que un es necesario que se desarrollen más ensayos clínicos con una muestra significativa que demuestren los efectos del entrenamiento interválico de alta intensidad en pacientes con insuficiencia cardiaca antes de establecerse como guía de intervención en pacientes con falla cardiaca. Es necesario que aún se aborde a los pacientes con enfermedad cardiaca a través del método individualizado de prescripción de entrenamiento de ejercicio de acuerdo a las necesidades y preferencias de los pacientes.
Conclusiones
El entrenamiento interválico de alta intensidad durante 12 semanas podría elevar el consumo de oxígeno pico en pacientes con fracción de eyección reducida por falla cardiaca. Sin embargo, tiene mayores efectos si se acompaña de ejercicios de fuerza o resistencia. Se sugiere que se realicen nuevos ensayos clínicos con una muestra más representativa para poder considerar el HIIT como guía estándar en la intervención del paciente con falla cardiaca.