Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.6 n.1 San José Jan. 2004
* Asistente de Cirugía Cardiovascular, Hospital México, C.C.S.S., San José, Costa Rica.
** Médico General.
*** Residente de Circulación Extracorpórea, Hospital México, C.C.S.S., San José, Costa Rica.
Resumen
Introducción: El drenaje venoso pulmonar anómalo es una cardiopatía congénita en la que las venas pulmonares drenan en el atrio derecho o la circulación venosa sistémica. Puede tener anomalías cardíacas asociadas. El tratamiento quirúrgico varía de acuerdo a las características anatómicas de cada caso. El objetivo de nuestro trabajo es exponer una técnica quirúrgica innovadora que no requirió de circulación extracorpórea, ni arresto circulatorio, con excelentes resultados, en una paciente sin hipertensión pulmonar ni comunicación interauricular.
Abstract
Anomalous pulmonary venous connection is when the pulmonary veins drain into the right atrium or into the systemic venous circulation. It can be associated with other cardiac anomalies. The surgical approach varies according to the anatomic features of each case. Th e aim of this review is to present an alternative approach that obviates the need of cardiopulmonary bypass in a patient without pulmonary hypertension nor atrial septal defects.
Femenina, enfermera de profesión, vecina de San José. Antecedentes de Cardiopatías congénitas no especifi cadas en familia paterna.
Conocida en Pediatría por falla para progresar y cardiopatía congénita tipo situs inversus completo con dextrocardia. Cursa la infancia y adolescencia con episodios de disnea de esfuerzos y cianosis distal. A los 27 años de edad inicia embarazo que cursa con disnea aún en reposo, cianosis distal, edemas podálicos hasta las rodillas y ortopnea franca. Se maneja aparentemente como insuficiencia cardíaca y se decide interrumpir gestación mejorando parcialmente su condición general.
Posteriormente reincide súbitamente sintomatología incapacitante y progresiva caracterizada por palpitaciones, dolor torácico en hemitórax derecho y disnea de pequeños esfuerzos por lo que a sus 35 años se interna para estabilización y estudios hemodinámicos.
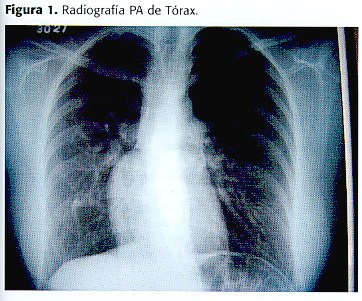
Estudios de gabinete y electrocardiográficos se reportan dentro de límites normales (figura 2). Radiología de tórax muestra imagen tubular en borde derecho de silueta cardíaca que hace cuerpo con la misma (figura 1) . Se corrobora con Tomografía, la cual ubica la estructura tubular a nivel del lóbulo inferior derecho pulmonar, que toma el medio de contraste y parece originarse de arteria pulmonar derecha.
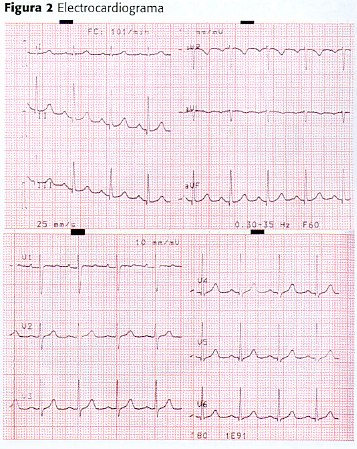
Se realiza Ecocardiograma transesofágico que describe una única vena pulmonar drenando al atrio y una estructura vascular que cursa por cara dorsal del atrio derecho, drenando a la vena cava inferior. Se descartan defectos septales y valvulopatías.
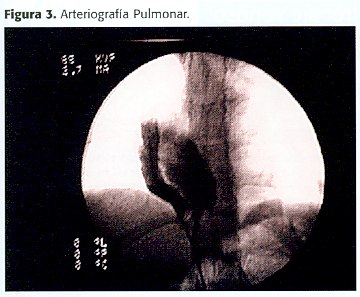
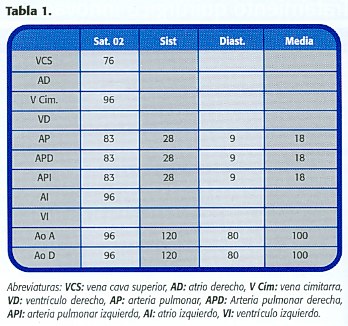
El Cateterismo cardíaco a sus 35 años muestra un drenaje anómalo de venas pulmonares derechas al tercio superior de la vena cava inferior, a través de un conducto colector recogiendo todo el flujo pulmonar derecho. Venas pulmonares izquierdas drenando a través de un conducto común al atrio izquierdo, sin estenosis (figura 3 y 4) (Tabla 1). Arteriografía pulmonar no sugiere hipoplasia significativa. Índices de presión y resistencia pulmonares normales.
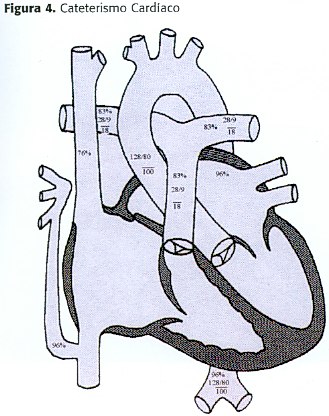
Cálculos
ASC = 1,54 m2
Qp = 9,50 l/min (6,17 l/min/m2)
Qs 6,18 l/min (4,01 l/min/m2)
Qp / Qs = 1,54 : 1
Paciente recobra mejoría de su sintomatología. Cinco meses después inicia súbitamente dolor pélvico importante. Se realiza Ultrasonografía que muestra la presencia de un quiste en ovario izquierdo de 56 x 38 mm. , el que se reseca, con mala evolución. Un Ultrasonido Doppler Duplex demuestra trombosis venosa profunda a nivel ilio femoral izquierdo y se anticoagula con heparina. Posteriormente presentó cuadro súbito con sudoración, taquicardia y dolor torácico derecho, que cedió en 30 minutos, dejando en duda la posibilidad de un tromboembolismo pulmonar. En el quinto día postoperatorio requiere reintervención quirúrgica por hemoperitoneo, drenándose aproximadamente 1 litro de sangre en cavidad. Progresivamente mejora condición general y se egresa un mes después con anticoagulación oral. Un año más tarde se suspende anticoagulación al descartarse trombosis, mediante flebografía diagnóstica y ultrasonidos doppler control.
Se maneja su cardiopatía conservadoramente, aunque persisten episodios sintomáticos de disnea con moderados esfuerzos y eventos de palpitaciones.
A los 40 años reaparece súbitamente sintomatología caracterizada de nuevo por palpitaciones, dolor torácico disnea incapacitante, asociando además ortopnea franca y edemas lo que obliga a iniciar tratamiento con Digoxina, Nifedipina y diuréticos. Revalorando su condición mediante nuevos estudios se encuentra ligera dilatación del ventrículo y atrio derecho, con presiones sistólicas de arteria pulmonar entre 30 y 35 mmHg. Las pruebas de función respiratoria mostraron importante restricción de su capacidad vital. Una peltismografía encontró datos de tromboembolismo pulmonar.
Dado estos hallazgos hemodinámicos correlacionados con la sintomatología de la paciente, se presenta el caso para decidir tratamiento definitivo.
Drenaje V enoso Anómalo Pulmonar
Un Drenaje Venoso Pulmonar Anómalo Parcial (DVPAP) ocurre cuando una o más (pero no todas) las venas pulmonares drenan en el atrio derecho o a la circulación venosa sistémica. Ambos sexos se afectan por igual. El defecto embriológico se debe a la obliteración temprana de la vena pulmonar común y la persistencia de uno de los todavía presentes canales venosos pulmonar-sistémicos como una ruta para el drenaje venoso pulmonar.
Existen varios tipos de DVPAP descritos. Entre ellos el Síndrome de la Cimitarra, descrito por primera vez por en 1836 por Cooper y Chassinat. Sin embargo el signo radiológico de la cimitarra fue descrito por Halasz y col. en 1956.
Una Vena pulmonar derecha anómala (vena cimitarra), generalmente drena la totalidad del pulmón derecho pero ocasionalmente drena sólo los lóbulos medio e inferior (figura 5). Esta vena desciende a través del diafragma más o menos paralela al borde pericárdico, mostrando un curso vertical hacia el ángulo cardiofrénico y ensanchándose distalmente encorvándose a la izquierda justo por debajo de la unión VCI-AD, adquiriendo la forma de una cimitarra (tipo de espada turca) (Figura 6).
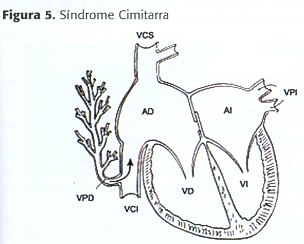
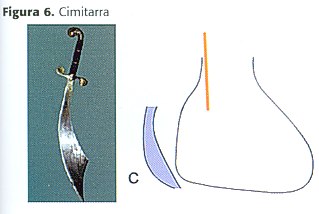
El drenaje venoso pulmonar anómalo usualmente pasa anterior al hilio pulmonar derecho, pero ocasionalmente es posterior. Su entrada a la VCI es justo por encima de los orificios de las venas hepáticas.
Como en éste caso el septo atrial puede estar intacto aunque un DSA puede estar presente.
Ocasionalmente la vena anómala también puede conectarse con el AI y muy excepcionalmente el síndrome de la cimitarra puede verse con la conexión de la vena anómala al AI; teniendo en este caso un drenaje venoso pulmonar normal.
El síndrome de la cimitarra ocurre como un fenómeno aislado en una minoría de casos o acompañarse de anomalías pulmonares derechas. La más común de estas anomalías es la hipoplasia pulmonar derecha, que cuando es severa se acompaña de un marcado desplazamiento mediastinal y dextrocardia.
La irrigación del pulmón derecho hipoplásico proviene principalmente de una rama de la Aorta abdominal en la región celíaca que asciende a través del ligamento pulmonar inferior para suplir un lóbulo inferior, o más frecuentemente a la totalidad del pulmón.
Una pequeña arteria pulmonar puede estar presente, pero frecuentemente las porciones central e hiliar de la arteria pulmonar derecha están ausentes.
Ocasionalmente podría existir un verdadero secuestro broncopulmonar del lóbulo inferior derecho, con la formación secundaria de un quiste intrapulmonar.
También se observan diafragmáticas con herniación pulmonar, o anormalidades cardíacas, en aproximadamente un 20% de los casos, las que incluyen CIA (más común), PCA, coartación de Aorta o tetralogía de Fallot.
En pacientes sintomáticos el tratamiento es agresivo con cirugía temprana. Algunos pacientes con datos de hipertensión pulmonar en el ecocardiograma y en el cateterismo cardíaco terminan en un transplante pulmonar por hipertensión pulmonar persistente o estenosis de la anastomosis.
Fisiología
La alteración fisiológica fundamental del DVPAP es similar a la de un defecto del septo Interventricular o atrial, o de una persistencia del conducto arterioso. Existe un flujo sanguíneo pulmonar aumentado como consecuencia de la recirculación de sangre oxigenada a través de los pulmones. El hiperflujo a la circulación menor conlleva insidiosamente a disminución del retorno venoso. En ausencia cardiopatías congénitas complejas asociadas, la alteración fisiopatológica y la sintomatología depende del número de venas anómalas y su sitio de conexión, la presencia y tamaño de una comunicación interauricular y el estado del lecho vascular pulmonar.
Manifestaciones clínicas
La conexión anómala de una sola vena pulmonar no es aparente desde el punto de vista clínico.
Los síntomas son infrecuentes en la infancia, pero podría existir alguna disnea al ejercicio.
La cianosis también es infrecuente en la infancia aunque un pequeño cortocircuito izquierda-derecha pueda estar presente.
La frecuencia de pacientes que se presentan con cianosis se incrementa durante la tercera y cuarta décadas debido a cambios en el lecho pulmonar, hipertensión pulmonar e incremento del cortocircuito.
El aumento de volumen circulatorio durante el embarazo es un evento desencadenante, que torna intolerante la sintomatología y atenta con la vida de la paciente.
También las infecciones respiratorias son frecuentes en éstos pacientes y se dan como consecuencia de las anormalidades asociadas en el parénquima pulmonar.
Éstos pacientes frecuentemente tienen evidencia de un hemitórax derecho pequeño y dextrocardia.
Cuando el septo atrial está intacto, la separación del segundo ruido no es marcada.
Un soplo de flujo de salida pulmonar está usualmente presente y un soplo de flujo diastólico tricuspídeo puede también estar presente cuando el septo atrial está intacto.
Manifestaciones electrocardiográficas
Ondas P picudas e hipertrofia ventricular derecha con el patrón de sobrecarga sistólica se observan en pacientes que tienen hipertensión pulmonar.
El electrocardiograma es comunmente normal en el paciente con el septo atrial intacto (figura 1).
Manifestaciones ecocardiográficas
Los hallazgos en el DVPAP son dependientes de la magnitud del flujo sanguíneo pulmonar (cortocircuito izquierda-derecha).
Cuando sólo una vena pulmonar se conecta anómalamente, el cortocircuito es pequeño y el ecocardiograma es normal.
Cuando todas las venas de un pulmón se conectan anómalamente el cortocircuito es equivalente al observado en un gran DSA simple y el ecocardiograma es similar.
Manifestaciones radiológicas
La radiografía de rutina demuestra el flujo pulmonar aumentado y la dilatación ventricular derecha (figura 2).
El paciente con drenaje anómalo de las VPD a la VCI presenta una típica sombra creciente en el campo pulmonar inferior medial derecho, y debido a ésta imagen es que se le conoce como síndrome de cimitarra.
Hipoplasia del hemitórax derecho, dextrocardia y anormalidades del parénquima pulmonar pueden observarse cuando el drenaje venoso de las VPD se da a la VCI.
Discusión
Como ya hace más de un siglo señaló Rudolf Virchow, la estasis venosa es uno de los tres principales factores predisponentes de la trombosis venosa . El "corto circuito izquierda a derecha", propio de esta cardiopatía congénita, produce gran hiperflujo pulmonar que predispone a congestión pulmonar. Esto lleva inicialmente a estasis venosa, precipitando crisis de trombosis venosa profunda (y eventualmente tromboembolismos pulmonares).
Finalmente, perpetuar dicho hiperflujo pulmonar, llevará a la paciente a aumento de las resistencias vasculares pulmonares e Hipertensión pulmonar, complicando el cuadro con Core pulmonare e Insuficiencia Cardíaca Congestiva irreversible.
Estos hallazgos fisiopatológicos marcarían la pauta para un tratamiento quirúrgico definitivo en esta paciente, que corrija el corto circuito y elimine definitivamente el hiperflujo pulmonar.
Tomando en cuenta que se encontraba en muy mala condición general, el resultado de una cirugía cardíaca con circulación extracorpórea (CE), sería probablemente de mucho riesgo.
Tratamiento quirúrgico innovador
El abordaje quirúrgico del síndrome de la cimitarra varía de acuerdo a las características anatómicas y patológicas de cada caso.
Muchos métodos con circulación extracorpórea se han propuesto para la corrección de este defecto, la mayoría de los cuales utilizan un conducto intracardíaco entre la vena cimitarra y el AI a través de un DSA o un parche intra artrial que conduzca el flujo pulmonar al AI. Éstas técnicas son efectivas pero conllevan el riesgo de la circulación extracorpórea y no evitan la potencial oclusión de la luz del conducto o estenosis en la anastomosis con la vena cimitarra.
En nuestro reporte describiremos una técnica simple para pacientes sin DSA asociado, en la que la vena colectora es anastomosada directamente al atrio izquierdo, evitando la CE y un conducto intracardíaco.
Técnica Quirúrgica
Mediante anestesia general y colocación en decúbito lateral izquierdo se realiza una toracotomía antero-lateral derecha entre el quinto y sexto espacio intercostal.
El pulmón derecho se libera de adherencias y el ligamento pulmonar inferior se secciona. Por debajo del diafragma se identifica la vena colectora anómala unida a la vena cava inferior. (figura 7 y 8) . Se coloca una pinza que ocluye parcialmente la VCI en la entrada de la vena cimitarra, y se secciona. Luego se cierra la VCI mediante sutura continua.
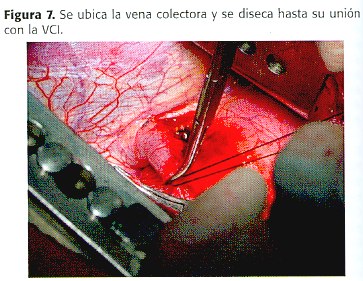
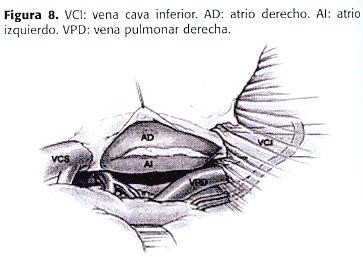
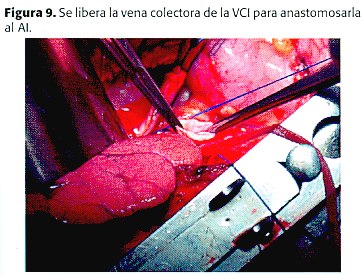
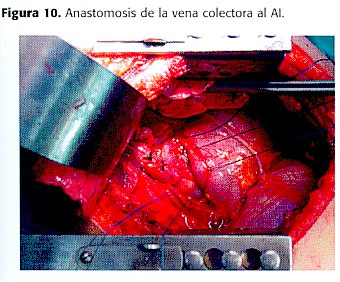
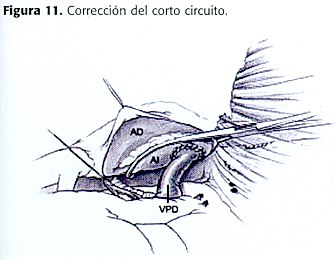
Se realiza una ventana pericárdica exponiendo el AI. Este se pinza parcialmente para anastomosarle la vena colectora anómala, mediante sutura continua 5-0 monofilamento (figura 9) , previa infusión de Heparina y colocación de la paciente en Trendelenburg para remover aire (figura 10 y 11). Para evitar hernias, se cierra el pericardio.
En este caso, transoperatoriamente se identificó un secuestro pulmonar inferior derecho, procediendo a ligar las arterias sistémicas anómalas.
Resultados
La excelente evolución postoperatoria es alentadora. El rápido alivio de la sintomatología producida por la estasis venosa fue evidente. Además las probabilidades de trombosis venosa y embolismo pulmonar se redujeron al evitarse el hiperflujo pulmonar asociado al cierre del corto circuito.
Estudios ecocardiográficos control mostraron significativa reducción en la dilatación de cavidades derechas y en cifras de presión en Arteria Pulmonar.
A pesar de no contar con una amplia experiencia con ésta técnica quirúrgica, vaticinamos una probable reducción en la morbimortalidad asociado al hecho de no requerir de CE y arresto circulatorio, así como disminución en el tiempo operatorio.
Es importante enfatizar que no todos los casos son candidatos a este tipo de cirugía, dado que si existen malformaciones cardíacas asociadas, hipertensión pulmonar severa o hipoplasias pulmonares importantes la técnica variaría. El transplante de pulmón se reserva para este subgrupo de pacientes de alto riesgo.
Se concluye que éste abordaje quirúrgico del Síndrome de Cimitarra es simple, seguro y efectivo en relación a las técnicas usualmente utilizadas para tratar éste grupo de pacientes.
Bibliografía
1. Dupuis C. The adult from of the Scimitar Syndrome. Am J. Cardiol. 1992, 70(4):502-7. [ Links ]
2. Brown J. Surgical Managnent of Scimitar Syndrome. J. Toracic and Cardiovascular Surg. 2003, 125(2):238-45. [ Links ]
3. Royce F. A novel operative aproach to scimitar syndrome. Ann Thorac Surg 2003, 76:301-3 [ Links ]
4. Shin-ichi Takeda. Two Cases of Scimitar Variant. Chest 1994, 105:292-93. [ Links ]
5. Adnan Cobanoglu. J Thorac Cardiovasc Surg 1984, 88:141-9. [ Links ]
6. Ho Chistopher. Scimitar Syndrome. J Emergency Medicine. 2001, 21(3):279-81. [ Links ]
7. Ioana Bratu. The multiple facets of Pulmonary Sequestration. J Pediatric Surg. 2001, 35(5):784-90. [ Links ]
8. Puig-Massana M. A new technique in the correction of partial annomalus pulmonary venous drenaige. J Thorac Surg. 1972:64 108-113. [ Links ]
9. Zubiate P. Surgical correction of anomalous pulmonary venous conection. Ann Surg. 1962, 156: 234-50. [ Links ]
10. Shumacker HB. Parcial anomalous pulmonary venous return with reference to drainage in to the inferior vena cava and to an intact atrial septum. J.Cardiovasc Surg. 1962. 156:134-50. [ Links ]
11. Tornvall SS. Anomalous drainage of the pulmonary veins into the inferior vena cava. J. Thorac Cardiovasc. Surg. 1961. 42:413-7. [ Links ]
12. Kirklin JW. Treatment of anoumalus pulmonary venous conection in association with interatrial comunication. Surgery. 1956. 39:389-98. [ Links ]
13. Honey M. Anomalous pulmonary venous dranaige of right lung to inferior vena cava. Q.J. Med. 1977;46:463-83. [ Links ]
14. Murphy JW. Intracardiac repair for anomalous pulmonary venous connection of rigth lung to inferior vena cava. Ann Thorac Surg. 1971; 11:38-42. [ Links ]
15. Woody JN. Hypoplasic right lung with systemic blood supply and anomalous pulmonary venous drainage: reversal of pulmonary hypertension with surgical management in infancy. Am Heart J. 1972;83:82-8. [ Links ]














