Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.4 n.1 San José Apr. 2002
Caso clínico
Introducción
Es conocida la relación entre la prolongación de la repolarización ventricular y la aparición de taquicardia ventricular polimorfa helicoidal o torsión de puntas, que eventualmente puede degenerar en fibrilación ventricular y muerte. Aunque esta arritmia en particular se relaciona típicamente al síndrome de QT largo congénito, es más frecuentemente observada en adultos, siendo la causa más común el efecto farmacológico de un sin número de drogas, en especial, antiarrítmicos.
Se presenta un caso en una paciente portadora de una miocardiopatía valvular, QT largo y torsión de puntas que fue tratada con estimulación cardíaca permanente.
La taquicardia ventricular (TV) polimorfa helicoidal o llamada también torsión de puntas, puede degenerar en fibrilación ventricular (FV) y muerte por lo que es indiscutible su importancia pronóstica y explica alrededor del 20% de todas las muertes súbitas (1).
Los casos congénitos de QT largo se deben a diversas mutaciones de los genes responsables de codificar los canales de potasio o de sodio "voltaje dependientes" del miocardio, hasta hoy descritos en número de seis (2). Los sujetos afectados son individuos jóvenes y los síntomas de presentación son síncope (que frecuentemente es confundido con síndrome convulsivo) y muerte súbita. Tradicionalmente se ha postulado que las crisis de torsión de puntas son desencadenadas por estímulos adrenérgicos (taquicardias "adrenérgico-dependientes"), pero en estos pacientes también se ha comprobado que aparecen precedidos por ciclos corto-largo de los intervalos RR (3) (ver el siguiente párrafo), hecho que tiene importancia terapéutica.
En los casos adquiridos se postula que los individuos afectados son portadores de alguna de estas mutaciones pero que fenotípicamente sólo se expresan ante ciertos estímulos como por ejemplo, el efecto de algunas drogas antiarrítmicas (2). También ocurre en otras circunstancias como en bradicardia severa, hipokalemia, trastornos del sistema nervioso central (como hemorragia subaracnoidea), en miocardiopatías (como la hipertrófica o dilatada) y por un gran número de fármacos no cardioactivos como antihistamínicos y antifúngicos (2, 4). Típicamente las crisis de torsión de puntas están precedidas por ciclos RR corto-largo, por lo que se han denominado "bradicardico-dependientes" o "pausa-dependientes". Esto es, bradicardia importante o bien, la presencia de extrasístoles ventriculares frecuentes que generan ciclos RR cortos (el latido de base y el prematuro) y largo (la pausa postextrasistólica), fenómeno que dispersa la repolarización notoriamente (5).
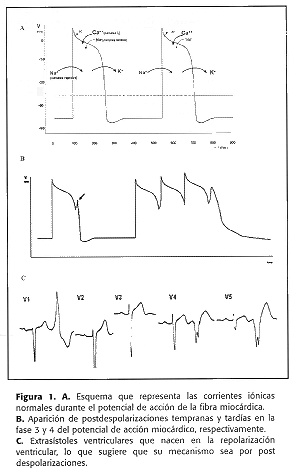
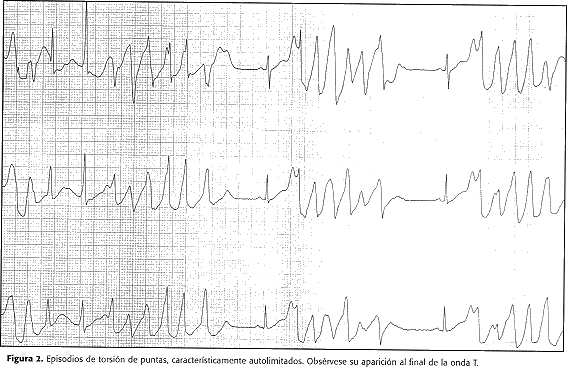
El mecanismo por el cual la prolongación de la repolarización da lugar a torsión de puntas es controversial. La mayor evidencia experimental y clínica apoya la presencia de postdespolarizaciones tempranas como mecanismo iniciador, de ahí el nombre de "actividad disparada". Las postdespolarizaciones aparecen como consecuencia de corrientes ionicas anormales las que de alcanzar el umbral, generan potenciales de acción en la fase 3 en cada uno de los latidos (figura 1), apareciendo el ritmo ventricular repetitivo; también se ha postulado que las crisis pueden perpetuarse por mecanismo de reentrada. Dado que el impulso recorre un circuito que presenta marcada anisotropía, en parte por la presencia de un desbalance autonómico, el eje electrocardiográfico cambia rotacionalmente y de ahí su morfología característica (figura 2). Las postdespolarizaciones van reduciendo su amplitud gradualmente hasta que no se alcanza el umbral, por lo que típicamente esta taquicardia se presenta como paroxismos autolimitados.
Quizás lo más importante del tratamiento de la torsión de puntas por QT largo adquirido sea un diagnóstico correcto de la causa subyacente. Frecuentemente, pacientes que toman diuréticos y que presentan arritmias ventriculares son medicados con, por ejemplo, quinidina, lo que obviamente empeora la situación. Además de la suspensión del agente responsable y de un diagnóstico adecuado, las crisis agudas pueden prevenirse con isoproterenol o estimulación cardíaca temporal para contrarrestar la bradicardia, hasta revertirse la causa. Los episodios de torsión de puntas pueden surpimirse con sulfato de magnesio en una dosis inicial de 2 g por vía intravenosa y dosis de mantenimiento de 2 a 18 mg/minuto.
Si el factor causal no es claro o el paciente presenta recurrencias o es portador de una miocardiopatía que conllevan mayor riesgo de muerte súbita, existen otros métodos de prevención de las crisis, los que se discutirán más adelante.
Caso clínico
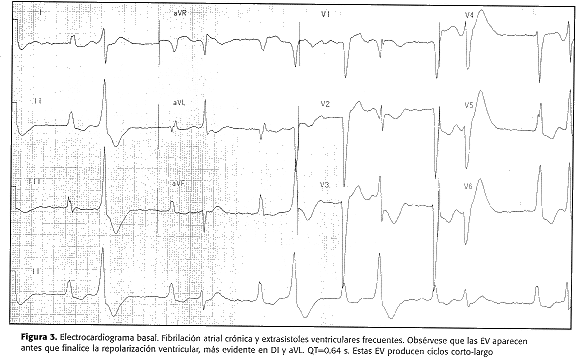
Paciente, de sexo femenino, 46 años, quien es portadora de una prótesis mitral mecánica implantada en 1998 por insuficiencia mitral severa por secuela de fiebre reumática en la infancia. La función ventricular está disminuida moderadamente (fracción de eyección=0.4) y presenta además fibrilación atrial crónica e hipertensión pulmonar moderada, como secuela de su valvulopatía. La paciente ha tenido tres internaciones en los últimos años por insuficiencia cardíaca sistólica y fue medicada con enalapril, digoxina, amiodarona, diuréticos y warfarina. En la figura 3 se muestra un electrocardiograma basal de la paciente.
Aproximadamente un mes antes de la última internación por insuficiencia cardíaca, la paciente presenta además episodios breves de pérdida de conocimiento no precedidos de pródromos que revierten espontáneamente así como "sacudidas" nocturnas, que despiertan al esposo.
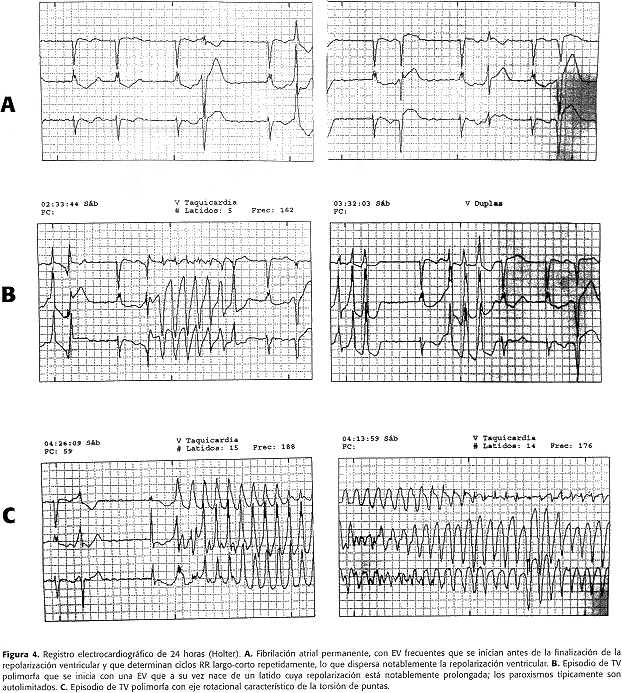
Durante su estancia hospitalaria se constatan estos episodios de aparición predominantemente nocturna, que se tratan de crisis sincopales con convulsiones tónico clónicas que se resuelven espontáneamente en pocos minutos. Se realizó un electrocardiograma de 24 horas (Holter), documentándose frecuentes episodios autolimitados de taquicardia ventricular polimorfa (torsión de puntas) disparados por EV precedidas de ciclos largo-corto (figura 4).
Considerando el potencial mal pronóstico que conlleva este tipo de taquicardia ventricular en presencia de insuficiencia cardíaca, se decidió implantar un marcapasos definitivo VVI con el fin de uniformizar la repolarización ventricular y por tanto suprimir las crisis (véase la discusión). Además se constató nivel sérico de potasio de 3.4 mEq/L iniciándose aporte por vía oral de cloruro de potasio y se suspendió la amiodarona, ambos factores coadyuvantes que pudieran prolongar también el QT.
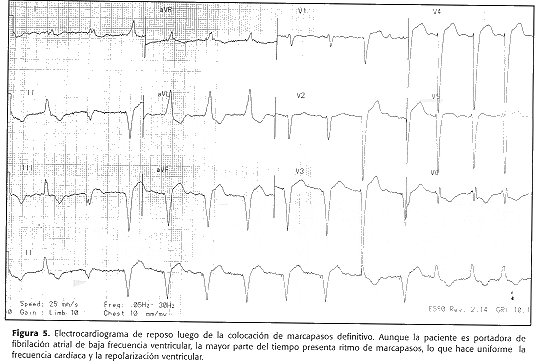
Dos meses después se comprobaron umbrales de captura y sensado adecuados del marcapasos y ausencia total de síntomas y de episodios de torsión de puntas en Holter de control. En la figura 5 se muestra un electrocardiograma a los 6 meses de seguimiento, la paciente ha permanecido asintomática.
Discusión
Este caso deja varias enseñanzas. En primer lugar, la presencia de extrasístoles ventriculares frecuentes por sí sola no amerita administrar un antiarrítmico, más aún cuando la mayoría de los casos son asintomáticos, ya que estos agentes podrían prolongar aún más la repolarización y eventualmente provocar TV polimorfa (efecto proarrítmico), empeorando aún más el pronóstico por iatrogenia. Este concepto fue establecido en forma contundente en pacientes con cardiopatía isquémica en el estudio CAST (6) y otros y está bien documentado con los antiarrítmicos de la clase I de Vaugham Williams como quinidina, disopiramida o flecainida.
Quizás la excepción a esta regla la constituya la amiodarona, cuando se trata de pacientes con insuficiencia cardíaca. El estudio GESICA (7), demostró un efecto favorable en la sobrevida de los pacientes con insuficiencia cardíaca, probablemente más notorio en insuficiencia cardíaca no isquémica. Sin embargo, en este estudio la presencia de arritmia ventricular no fue un criterio de inclusión sino solamente la mera presencia de insuficiencia cardíaca sistólica grave. Este fármaco prolonga notablemente la repolarización ventricular aunque también debe anotarse que sus efectos proarrítmicos por este motivo son infrecuentes, quizás porque lo hace en forma homogénea y por ende menor dispersión de la refractariedad. En cardiopatía isquémica, especialmente el paciente postinfarto de miocardio, este fármaco también ha demostrado beneficio (8) pero aún es controversial por lo que no se recomienda para uso habitual en todos estos enfermos.
Otro concepto importante es el relacionado al pronóstico del síncope. En ausencia de cardiopatía, la causa más común es el síncope neuralmente mediado o llamado también neurocardiogénico, cuya causa es una disautonomía funcional y reversible (a diferencia de otros trastornos orgánicos del sistema nervioso autónomo) y de pronóstico excelente (9). Por el contrario, siempre debe considerarse potencialmente grave el síncope que aparece en presencia de cardiopatía, ya que en la mayoría subyace una bradiarritmia o una taquiarritmia ventricular potencialmente letal. Este concepto tiene aún mayor validez en presencia de insuficiencia cardíaca ya que como es sabido, esta población tiene elevada mortalidad (7), como es el caso de la paciente discutida.
Existen varias formas de tratar las arritmias ventriculares. Sea mediante procedimientos que buscan suprimir la aparición de las mismas o bien, los que una vez aparecidas, administran terapias que las interrumpan, evitando así en muchos casos la muerte del sujeto.
Entre los primeros están los fármacos antiarrítmicos, la ablación quirúrgica y la ablación por catéter. El uso de fármacos antiarrítmicos como única terapia ha declinado por su menor eficacia que los desfibriladores (11, 13) (respecto a mortalidad total), sus efectos colaterales (incluyendo muertes) y la población relativamente limitada a la que pueden administrarse: la mayoría tiene efecto inotrópico negativo importante que no permite su uso en pacientes con insuficiencia cardíaca y como se mencionó, este es el grupo de mayor riesgo y en la mayoría no se encuentra una droga que suprima la aparición de TV/FV mediante pruebas electrofisiológicas. La ablación quirúrgica es efectiva pero requiere experiencia del equipo quirúrgico en procedimientos como la resección subendocárdica con mapeo electrofisiológico intraoperatorio y sólo se beneficia de ella un grupo muy limitado de pacientes. La ablación por catéter tiene una tasa de éxito menor que con las taquiarritmias supraventriculares en pacientes con cardiopatías, en especial isquémica, pero es muy efectiva y curativa en ciertos tipos específicos de arritmia ventricular como la taquicardia ventricular por reentrada entre ramas del haz de His o en los pacientes con TV y corazón estructuralmente normal (13).
Por estas razones, se ha popularizado el uso de cardiodesfibrilador implantable como método abortivo, una vez aparecida una arritmia ventricular potencialmente letal (10,11,12,13). Aunque estos dispositivos no evitan la recurrencia de la arritmia sino que aplican terapias una vez aparecidas, en estudios aleatorizados han demostrado reducir mejor la mortalidad en comparación a los fármacos antiarrítmicos administrados empíricamente o según los resultados del estudio electrofisiológico.
La estimulación cardíaca permanente pertenece al primer grupo de terapias: es un método de prevención de la recurrencia y es aplicable a aquellos casos en los que se documente que la arritmia ventricular está precedida de ciclos RR cambiantes (largo-corto), típicamente EV frecuentes. En este caso, la variación tan amplia y aguda de la duración del ciclo RR condiciona similares cambios en la repolarización ventricular. Esta repolarización cambiante ocasiona a su vez que diferentes áreas de tejido miocárdico presenten diferentes períodos refractarios (dispersión de la refractariedad), condiciones ideales para la generación de reentrada, mecanismo de la mayoría de las TV o bien de postdespolarizaciones que disparan la TV.
La estimulación con marcapasos homogeniza los períodos refractarios en el ventrículo (reduciendo su dispersión) (3,14), lográndose que la mayor parte del miocardio tenga similares propiedades electrofisiológicas evitando así la aparición de reentrada y/o postdespolarizaciones. Este tratamiento ha demostrado ser efectivo en varias situaciones en las que la TV polimorfa se relaciona a ciclos largo-corto, tanto en casos congénitos como adquiridos de prolongación del intervalo QT.
En algunos modelos de marcapasos existe un algoritmo matemático que detecta cambios agudos en la duración del RR según el promedio de los intervalos RR previos (15). Por lo general, estos cambios agudos se deben a extrasístoles. Si se detecta una diferencia RR mayor de un valor programado, el marcapasos inicia estimulación cardíaca inmediatamente (evitando la pausa postextrasistólica) a un RR igual al último RR promedio y lo va disminuyendo a una tasa constante, por ejemplo en un 15% de la duración del ciclo hasta reiniciarse ritmo propio o la frecuencia mínima programada. Esta función se denomina "uniformización de la frecuencia cardíaca" o "algoritmo de estimulación preventivo de pausas" (14) o en inglés "rate smoothing" y ha demostrado efectividad en el tratamiento de estos pacientes (15).
A los pacientes que tienen recurrencias pese a la estimulación cardíaca permanente, debe colocárseles un cardiodesfibrilador automático implantable (13). Durante las crisis agudas la cardioversión eléctrica externa puede ser necesaria repetidas veces hasta que el factor desencadenante sea revertido o incluso puede no ser efectiva. Como terapia crónica, en casos seleccionados la desfibrilación endocárdica puede ser la única terapia que prevenga los síntomas o la muerte.
Conclusión
La estimulación cardíaca con marcapasos es una forma efectiva de prevención de los episodios de torsión de puntas en el síndrome de QT largo adquirido, en especial en pacientes con alto riesgo de recurrencia como en las miocardiopatías.
1. Jimenez RA.,Myerburg RJ.: Sudden Cardiac Death: Magnitude of the problem, Substrate/Trigger Interaction, and Populations at Risk. In: Crawford MH, ed. Cardiology Clinics. Cardiac Arrhythmias and related Sindromes: Current Diagnosis and Management. Philadelphia WB Saunders; 1993; 11: 1-10 [ Links ]
2. Vincent GM. Sindrome de QT largo. En: Miller JD, ed. Clínicas Cardiológicas de Norteamérica. McGraw-Hill-Interamericana de España, S.A.U., 2000;2:343-361 [ Links ]
3. Viskin S, Fish R, Zelster D, Laniado S, Belhassen B, Lesh M, Dorostkar P, Scheinmann M. Pause-dependent vs. Non pause-dependent initiation of torsade de pointes in the congenital long QT síndrome. PACE 1998; 21: 851 (Abstract) [ Links ]
4. Grogin HR, Scheinman: Evaluation and Management of Patients with Polymorphic Ventricular Tachycardia. In: Crawford MH, ed. Cardiology Clinics. Cardiac Arrhythmias and related Sindromes: Current Diagnosis and Management. Philadelphia WB Saunders; 1993; 11: 39-44 [ Links ]
5. Gutiérrez O. El electrocardiograma de alta resolución. Rev Costarr Cardiol 2001; 3: 48-53 [ Links ]
6. The Cardiac Arrhythmia Supression Trial (CAST) Investigators: Preliminary Report: Effect of Encainide and Flecainide on Mortality in a Randomized Trial of Arrhythmia Supression after Moyocardial Infarction. N Engl J Med 1989;321: 406-412 [ Links ]
7. Doval HC, Nul DR, Grancelli HO, Perrone SV, Bortman GR, Curiel R: Randomised Trial of Low-dose Amiodarone in Severe Congestive Heart Failure. Lancet 1994; 344: 493-498 [ Links ]
8. Amiodarone Trials Meta-Analysis Investigators. Effect of prophylactic amiodarone on mortality after acute myocardial infarction and in congestive heart failure: meta-analysis of individual data from 6500 patients in randomised trials. Lancet, 1997; 350(9089): 1417-24 [ Links ]
9. Gutiérrez O. Síncope neurocardiogénico: diagnóstico y tratamiento. Boletín de la Sociedad Peruana de Medicina interna 1998; 11: 151-156 [ Links ]
10. Moss AJ, Hall WJ, Cannom DS, Daubert JP, Higgins SL, Klein H, Levine JH, Saksena S, Waldo AL, Wilber D, Brown MW and Heo M for the MADIT Investigators. Improved Survival with Implanted Defibrillator in Patients with Coronary Disease at High Risk of Ventricular Arrhythmias. N Engl J Med 1996; 335: 1933-1940 [ Links ]
11. The Antiarrhythmic Versus Implantable Defibrilllator (AVID) investigators: A comparision of Antiarrhythmic-drug Therapy with Implantable Defibrillators in patients Resuscitated from Near-fatal Ventricular Arrhythmias. N Engl J Med 1997; 337: 1576 [ Links ]
12. Buxton AE, Lee KL, Fisher JD et al: A randomized, controlled study of the primary prevention of sudden death in patients with coronary artery disease. N Engl J Med 1999; 341: 1882
[ Links ]13. Marchlinski Fe, Zado ES, Callans DJ, Patel V, Ashar MS, Russo AM. Tratamiento híbrido de las arritmias ventriculares. En: Miller JD ed. Clínicas Cardiológicas de Norteamérica. McGraw-Hill-Interamericana de España, S.A.U., 2000;2:435-451
[ Links ]14. Viskin S, Glikson M, Fish R, Glik A, Cooperman Y, Saxon L. Rate Smoothing with cardiac pacing for preventing Torsade de pointes. Am J Cardiol 2000; 86 (suppl): 111k-115K
[ Links ]15. Viskin S, Fish R, Bros D, Laniado S, Belhassen B, Cooperman Y, Lesh M, Scheinmann M, Saxon L. Prevention of pause-dependent torsade de pointes and malignant ventricular arrhythmias with a pause-preventing pacing algorithm. PACE 1998; 21: 826 (Abstract)
[ Links ]*Cardiólogo-electrofisiólogo
Clínica de Arritmias, San José, Costa Rica
Servicio de Cardiología, Hospital México
Cátedra de Medicina, Universidad de Costa Rica
Ap. Postal 471-1300 San José, Costa Rica
Telefax (506) 255-0505 oswcr@hotmail.com














