Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.4 n.1 San José Apr. 2002
Revisión
Resumen
Las estatinas son un grupo de fármacos que se utilizan en el tratamiento de las dislipidemias porque inhiben la HMG-CoA reductasa, enzima clave en la síntesis de colesterol. Además, se han postulado muchas otras acciones, directas o indirectas, que pueden modificar de manera beneficiosa el proceso que conduce a la aterosclerosis.
Existen importantes diferencias farmacocinéticas y farmacodinámicas entre los distintos miembros de esta clase de drogas, que pueden constituirse en elementos fundamentales a la hora de escoger determinada estatina en la práctica clínica. Las diferencias más notables se encuentran en la magnitud de los cambios que producen sobre el perfil de los lípidos sanguíneos, en las vías metabólicas que utilizan para ser eliminadas del organismo, y en el potencial para sufrir interacciones medicamentosas.
A pesar de que en general son bien toleradas, es necesario tener algunos cuidados básicos que permitan utilizar estas drogas de una manera eficaz y segura, porque algunos efectos adversos, aunque infrecuentes, pueden ser muy serios y eventualmente fatales.
Introducción
Las estatinas han revolucionado la terapia de las dislipidemias, debido a que tienen un mejor perfil de eficacia y tolerabilidad que los restantes tipos de fármacos anteriormente usados para tal fin. En la actualidad, se usan varios tipos de estatinas en la práctica clínica: lovastatina, pravastatina y simvastatina son derivados del metabolismo fúngico; fluvastatina y atorvastatina, considerados de segunda generación, son sintéticos y estructuralmente distintos, mientras que cerivastatina fue recientemente retirada del mercado por la compañía productora. Es probable que otros compuestos, como rosuvastatina, estén disponibles a corto plazo.
Debido al extenso empleo de estas drogas en la práctica clínica contemporánea, y a los temores recientes en cuanto a su seguridad, es necesario conocer los aspectos fundamentales de la farmacología de esta clase de medicamentos. El objetivo de este artículo es que, a través de una revisión de sus características básicas, se pueda aspirar a comprender mejor las evidencias clínicas actuales y a utilizar de manera racional y segura este importante recurso terapéutico.
Mecanismo de acción
La HMG-CoA reductasa es la enzima que regula la velocidad de síntesis de colesterol en el hígado y en otros tejidos. Su estructura es un tetrámero; los cuatro monómeros que la componen son idénticos, y todos contribuyen al sitio activo de la enzima. El colesterol, y otros productos intermediarios, llamados isoprenoides, ejercen un retrocontrol negativo sobre la expresión del gen que codifica la producción de reductasa (figura 1) (1).
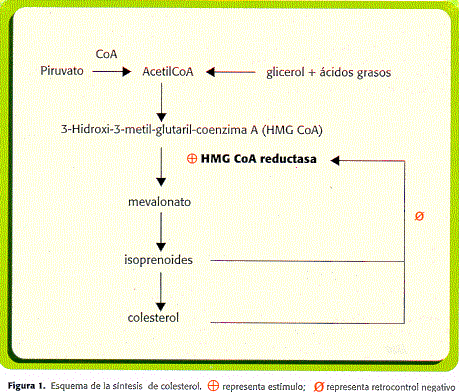

Las estatinas se unen de manera covalente al sitio activo de la reductasa, con mayor afinidad que la HMG-CoA y, por lo tanto, funcionan como inhibidores competitivos, por lo cual disminuyen la síntesis y el contenido intracelular de colesterol (2,3). La estructura química de cada una de estas drogas determina la avidez para unirse al sitio activo, y puede tener relación directa sobre la potencia de cada compuesto.
Recientemente, se ha descrito que las estatinas no solo compiten con el sustrato natural por el sitio activo de la enzima, sino que, además, alteran la conformación de esta última y limitan su actividad funcional, lo que aumenta su eficacia y su especificidad (4).
A consecuencia de la disminución intracelular de colesterol, se activa una proteasa (SREBP) que libera proteínas reguladoras del retículo endoplásmico; a nivel nuclear, esas proteínas facilitan la expresión del gen que codifica al receptor B/E (5). La mayor disponibilidad de receptores B/E en la membrana celular provoca un aumento en la captura, mediante endocitosis, de LDL y otros tipos de lipoproteínas, principalmente en el hígado, la glándula suprarrenal y el tejido graso (figura 2) (6).
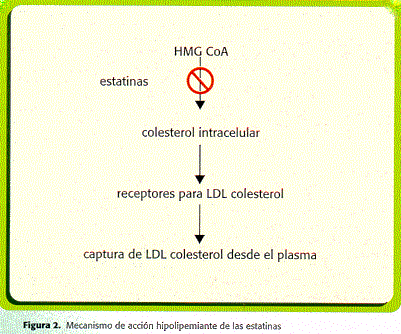

Como resultado final, se obtienen cambios en los niveles sanguíneos de lípidos: disminución significativa del colesterol LDL (17 a 54%), aumento discreto del colesterol HDL (5 a 10%) y, en el caso de algunas estatinas, descenso de los triglicéridos. La magnitud de esos cambios en el perfil de lípidos dependerá del fármaco específico y de la dosis utilizada (cuadro1)(7). El máximo efecto sobre los niveles sanguíneos de lipoproteínas se consigue después de 4 a 6 semanas de uso del medicamento, independientemente de las características cinéticas de cada droga (8,9).
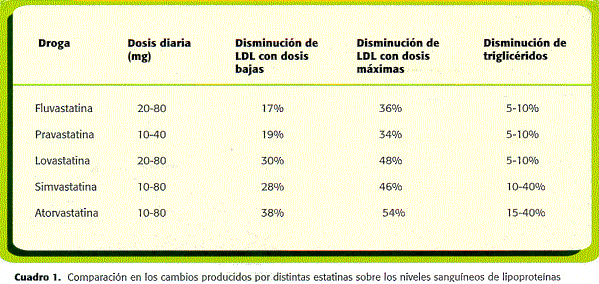

Se han detectado y analizado experimentalmente muchas otras acciones de las estatinas (cuadro 2) (10-33); esas propiedades no lipídicas pueden diferir entre las distintas drogas de la clase. Aunque es difícil establecerlo con certeza, pues algunos datos indican que la función endotelial puede mejorar con solo un agresivo descenso del colestero¦ LDL por medios no farmacológicos (34), hay evidencias de que al menos algunos de esos otros mecanismos son independientes, y no solo la consecuencia de los efectos metabólicos de esta clase de drogas (35,36). Es muy importante señalar que varios de esos procesos están estrechamente relacionados entre sí, de manera que la mejoría de alguno de ellos puede influir positivamente al resto. La conclusión es que todas esas otras propiedades de las estatinas combaten, directa o indirectamente, la disfunción endotelial, y modifican la estructura y la composición de las placas de ateroma, que se vuelven más estables a la erosión y a la ruptura (37-41). Algunos de esos cambios aparecen poco tiempo después del inicio de la administración de las drogas (42), y transforman las características protrombóticas y vasoespásticas que tiene el endotelio en los estados de hipercolesterolemia (43).


A nivel molecular, uno de los mecanismos que está cobrando mayor vigencia en la actualidad para explicar estos hallazgos es que las estatinas aumentan la producción de óxido nítrico en el endotelio vascular, que suele estar inhibida por acción de radicales de oxígeno libres producidos a partir de las moléculas oxidadas de LDL (44).
Aunque todavía no se ha definido con certeza el impacto clínico que estas acciones dinámicas puedan tener, se cree que son responsables de algunos de los beneficios obtenidos a corto plazo en el tratamiento de los pacientes con enfermedad coronaria (36, 45-47).
Farmacocinética
Existen muchas diferencias cinéticas entre las estatinas, con posibles implicaciones prácticas (cuadro 3). Fluvastatina es la que se absorbe mejor; la escasa absorción de lovastatina aumenta de manera notable cuando se administra con los alimentos (9, 48). La biodisponibilidad oral de lovastatina y simvastatina es muy baja, lo cual no trae grandes repercusiones porque se administran como prodrogas y, por lo tanto, la actividad farmacológica depende de sus metabolitos (48, 49).
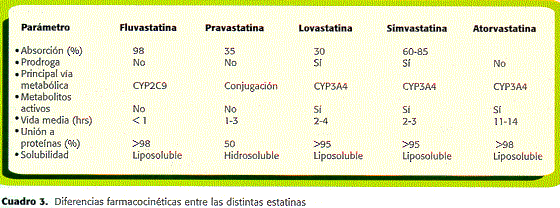
Con la excepción de pravastatina, que se metaboliza por medio de reacciones de fase II, todas las otras sufren un extenso metabolismo hepático de primer paso por el sistema enzimático microsomal del citocromo P450 (50). Algunas tienen metabolitos activos.
Atorvastatina es la más selectiva para actuar a nivel hepático y, además, produce la inhibición más prolongada sobre la HMG-CoA reductasa (51); se cree que esta propiedad es responsable de su mayor efecto sobre los niveles sanguíneos de colesterol LDL y de triglicéridos (8, 52).
A diferencia de pravastatina, las restantes estatinas se ligan extensamente a la albúmina y a otras proteínas del plasma (50, 53).
La excreción urinaria es relevante solo en el caso de pravastina y, en menor grado, de simvastatina y lovastatina (49,53), por lo que es preciso realizar ajustes de sus dosis en presencia de insuficiencia renal (cuadro 4).


Interacciones medicamentosas
Los compuestos liposolubles deben metabolizarse a sustancias más hidrofílicas para poder ser excretados, mientras que una porción mayor de las drogas hidrosolubles puede excretarse, sin cambios, por la orina; esta característica incide en que el último tipo de fármacos, como pravastatina, tenga un menor potencial de interacciones medicamentosas (54).
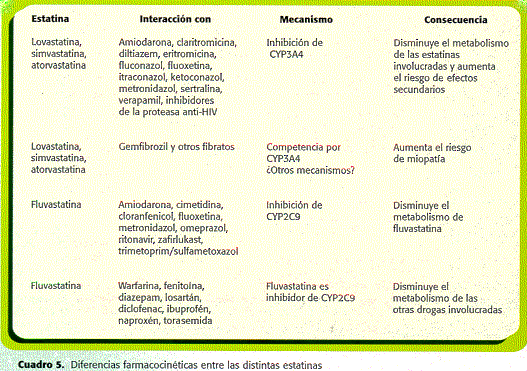
Debido a que está involucrada en la mayoría de las reacciones metabólicas relacionadas con los fármacos y las sustancias endógenas, la isoforma CYP3A4 es la enzima más importante del citocromo P450. Se ha observado que la utilización simultánea, en un mismo paciente, de un fármaco inhibidor de la isoforma CYP3A4, disminuye el metabolismo y aumenta notablemente las concentraciones sanguíneas de lovastatina, simvastatina y atorvastatina, pero no las de pravastatina (55, 56) (cuadro 5); esta información, que es congruente con las distintas vías metabólicas utilizadas por cada una de esas drogas, adquiere gran importancia práctica porque muchos de los efectos adversos de los fármacos están directamente relacionados con su concentración sanguínea. La inhibición de la isoforma CYP2C9 también puede ocasionar muchas interacciones (cuadro 5).

Este aspecto adquiere una especial relevancia en los sujetos que genéticamente tienen una isoforma de CYP450 con actividad baja o nula, pues ellos son más sensibles a sufrir interacciones medicamentosas y efectos adversos serios por el acúmulo de los fármacos que, en condiciones normales, deberían haber utilizado esa vía metabólica para su eliminación (57).
El ligado extenso a las proteínas del plasma puede ser otro mecanismo productor de interacciones medicamentosas, pues, al desplazar a otros compuestos de su sitio de unión, se produce una mayor concentración de droga libre activa; sin embargo, todavía se desconoce el impacto clínico que este tipo de interacciones pueda tener en el caso de las estatinas.
Efectos adversos
Los efectos adversos reportados con mayor frecuencia han sido estreñimiento, náusea, dolor abdominal, diarrea, flatulencia, insomnio y cefalea, que suelen ser leves y transitorios(58).
Se ha descrito una elevación de las transaminasas hepáticas aproximadamente en el 1-2% de los pacientes tratados (7), pero la hepatitis sintomática es rara. La alteración en las transaminasas ha sido mencionada con todas las estatinas, en especial cuando se usan a dosis altas. Se recomienda realizar esa prueba de laboratorio antes de administrar el medicamento, y luego cada 4-6 semanas durante los primeros meses de terapia; no debe iniciarse, o debe suspenderse el fármaco, si se detectan niveles de transaminasas tres veces por encima del valor normal. La prueba usualmente retorna al valor normal en los tres meses siguientes a la suspensión de la droga (59).
La toxicidad sobre el músculo estriado es un efecto adverso poco frecuente de las estatinas. Cuando se utilizan como monoterapia, este efecto adverso se ha presentado en cerca de un caso por cada mil pacientes tratados (7). Su intensidad puede variar desde mialgias no específicas hasta miositis, que en raras ocasiones progresa a rabdomiolisis, potencialmente mortal por insuficiencia renal aguda. Se cree que una deficiencia enzimática está involucrada en la predisposición de determinados individuos a sufrir ese serio inconveniente (60). La muerte de más de 50 pacientes reportada a nivel mundial por ese síndrome, fue la causa de que la compañía productora de cerivastatina retirara ese producto del mercado hace varios meses.
Aunque no se ha aclarado el mecanismo preciso, algunos datos sugieren que estos efectos sobre el músculo esquelético pueden ser causados por la depleción intracelular de metabolitos intermediarios esenciales derivados del mevalonato (61). Se ha postulado, entonces, que las estatinas liposolubles, por tener una mayor penetración en los miocitos, serían más propensas a desencadenar lesiones a ese nivel. Sin embargo, esa hipótesis no se ha corroborado; la miotoxicidad ha ocurrido con todas las estatinas disponibles, y no existen aún estudios comparativos directos de seguridad entre ellas (62).
Dado que la miotoxicidad es un efecto secundario dosis-dependiente, adquieren relevancia las interacciones medicamentosas que impliquen una disminución del metabolismo de las estatinas por inhibición del sistema enzimático del citocromo P-450 (cuadro 5). Por ejemplo, es bien conocido el hecho de que la combinación con gemfibrozil, otro fármaco hipolipemiante, aumenta el riesgo de rabdomiolisis (63); se piensa que el problema podría ser menos frecuente si se usara un fibrato con vida media más corta y una estatina cuyo metabolismo no dependa exclusivamente de CYP 3A4 (64).
Otros factores de riesgo para miopatía inducida por estatinas son insuficiencia hepática o renal, hipotiroidismo, infección aguda y edad avanzada (50).
Debido a la potencial severidad del problema, es indispensable que todo paciente que empieza a recibir terapia con una estatina sea informado sobre la importancia de reportar la aparición de mialgias o de debilidad muscular; el diagnóstico de miositis, que se confirma con determinaciones séricas de creatinfosfoquinasa (CPK) diez veces por encima del valor normal, obliga a suspender el fármaco.
En estudios de cohorte, se ha observado un mayor riesgo de accidente vascular cerebral hemorrágico en hombres con colesterol LDL inferior a 160 mg/dL (64, 65); obviamente, esos datos epidemiológicos pueden estar influidos por otras condiciones concomitantes, pues no se han repetido en los ensayos clínicos con estatinas.
A pesar de algunos temores iniciales derivados de estudios en animales de laboratorio, no se ha demostrado que exista un riesgo aumentado de cáncer en los pacientes tratados con estatinas (66, 67).
No deben usarse estos fármacos durante el embarazo, pues el colesterol es necesario para el adecuado desarrollo del producto de la gestación, y el uso de estas drogas podría ocasionarle serios problemas.
Aunque no se cuente con evidencias de seguridad a muy largo plazo, los datos existentes después de siete años de uso son alentadores (68). Sin embargo, es necesario mencionar un hallazgo muy interesante del estudio AFCAPS/TexCAPS (69), en lo que se refiere a eventos adversos serios. Por definición, los eventos adversos serios incluyen cualquier suceso no deseado, que ocasione la muerte, amenace la vida, requiera hospitalización, prolongue la estancia hospitalaria, o resulte en una discapacidad persistente o significativa (70), y deben incluirse en todos los reportes de ensayos clínicos, aunque en ese momento no pueda establecerse con certeza si el hecho se relaciona o no con el procedimiento en estudio. AFCAPS/TexCAPS es un ensayo clínico controlado, que evaluó el uso de lovastatina en comparación con placebo, en la prevención primaria de la enfermedad coronaria en más de 6.000 pacientes con niveles de colesterol LDL dentro del rango normal (69). A pesar de que se detectó una disminución significativa en el riesgo de sufrir infarto de miocardio o mortalidad cardiovascular con el fármaco, la tasa de eventos adversos serios fue similar en ambos grupos; ese hallazgo plantea la interrogante de si existe un aumento en el riesgo absoluto de otros eventos serios con el uso del medicamento, pero no se brinda información al respecto. A la luz del problema reciente con cerivastatina, es vital que este aspecto sea aclarado, en especial cuando se refiere al uso de estatinas en pacientes con un riesgo cardiovascular global bajo, y tomando en cuenta que, recientemente, se documentó que los datos de seguridad no son reportados de manera precisa en muchos ensayos clínicos (71).
Conclusión
Indudablemente las estatinas han provocado un cambio rotundo en el manejo médico de las dislipidemias. A pesar de toda la información disponible, es indispensable contar con nuevas evidencias que permitan definir con exactitud el papel de estas drogas en la terapéutica.
Se debe aclarar los otros mecanismos de acción propuestos, independientes de su acción sobre el metabolismo del colesterol, ya que podrían convertirse en nuevos sitios importantes para la manipulación farmacológica, de manera que el proceso de aterosclerosis pueda atacarse a diferentes niveles.
Es indispensable que se identifique el proceso responsable de los efectos adversos serios, que se evite el uso simultáneo de drogas que puedan interactuar con las estatinas, que se determine la relación riesgo/beneficio para cada caso en particular, y que, a través de un adecuado sistema de farmacovigilancia, se establezca un reporte eficiente de los efectos adversos.
A pesar de sus similitudes, existen también diferencias entre las distintas drogas de esta clase: simvastatina y atorvastatina son las que producen cambios cuantitativamente mayores en los niveles de lipoproteínas plasmáticas, mientras que pravastatina es la menos problemática en cuanto a interacciones medicamentosas.
La importancia de estas discrepancias en la farmacología básica de las distintas estatinas es que esos factores pueden traducirse en diferencias en la eficacia, en la seguridad y en el riesgo de efectos adversos; sin embargo, toda esa información debe analizarse bajo la luz de los hallazgos de los ensayos clínicos controlados, y debe enfatizar, además, la necesidad de estudios comparativos a largo plazo entre las distintas drogas de esta clase.
Bibliografía
1- Brown MS, Goldstein JL. Multivalent feedback of HMG CoA reductase, a control mechanism coordinating isoprenoid synthesis and cell growth. J Lip Res 1980;21:505-517.
3- Corsini A, Bellosta S, Baetta R, et al. New insights into the pharmacodynamic and pharmacokinetic properties of statins. Pharmacol Ther 1999;84:413-428.
4- Istvan ES, Deisenhofer J. Structural mechanism for statin inhibition of HMG-CoA reductase. Science 2001;292:1160-1164.
5- Vaughan CJ, Gotto AM, Basson CT. The evolving role of statins in the management of atherosclerosis. J Am Coll Cardiol 2000;35:1-10.
6- Brown MS, Goldstein JL. A receptor-mediated pathway for cholesterol hemostasis. Science 1986;232:34-47.
7- Maron DJ, Fazio S, Linton MF, et al. Current perspectives on statins. Circulation 2000;101:207-213.
8- Jones P, Kofonek S, Laurora I, et al. Comparative dose efficacy study of atorvastatin versus simvastatin, pravastatin, lovastatin and fluvastatin in patients with hypercholesterolemia (the CURVES Study). Am J Cardiol 1998;81:582-587.
9- Chong PH, Seeger JD, Franklin C. Clinically relevant differences between the statins: implications for therapeutic selection. Am J Med 2001;111:390-400.
10- Egashira K, Hirooka Y, Kai H, et al. Reduction in serum cholesterol with pravastatin improves endothelium-dependent coronary vasomotion in patients with hypercholesterolemia. Circulation 1994;89:2519-2524.
11- Eichstadt HW, Eskotter H, Hoffman I, et al. Improvement of myocardial perfusion by short-term fluvastattin therapy in coronary artery disease. Am J Cardio 1995;76:122-125A.
12- Aviram M, Dankner G, Cogan U, et al. Lovastatin inhibits LDL oxidation and alters its fluidity and uptake by macrophages: in vitro and in vivo studies.Metabolism 1992;41:229-235.
13- Kleinveld HA, Demacker PN, de Haan AF, et al. Decreased in-vitro oxidizability of low-density lipoprotein in hypercholesterolaemic patients treated with 3-hydroxy-3-methylglutaryl-CoA reductase inhibitors. Eur J Clin Invest 1993;23:289-295.
14- Lehr HA, Seemuller J, Hubner C, et al. Oxidized LDL-induced leukocyte/endothelium interaction in vivo inolves the receptor for platelet activating factor. Arterioscler Throm 1993;13:1013-1018.
15- Webwe C, Erl W, Weber KSC, et al. HMG-CoA reductase inhibitors decrease CD11b expresión and CD11b-dependent adhesión of monocytes to endothelium and reduce increased adhesiveness of monocytes isolated from patients with hipercolesterolemia. J Am Coll Cardiol 1997;30:1212-1217.
16- Colli S, Eligini S, Lalli M, et al. Vastatins inhibit tissue factor in cultured human macrophages: a novel mechanism of protection against Atherosclerosis. Arterioscler Thromb Vasc Biol 1997;17:265-272.
17- Toschi V, Gallo R, Lettino M, et al. Tisue factor modulates the thrombogenicity of human atherosclerotic plaque. Circulation 1997;95:594-599.
18- Negre-Aminou P, van Vliet AK, van Erck M, et al. Inhibition of proliferation of human smooth muscle cells by various HMG-CoA reductase inhibitors: comparison with other cell types. Biochim Byophys Acta 1997;1345:259-268.
19- Bellosta S, Bernini F, Ferri N, et al. Direct vascular effects of HMG-CoA reductase inhibitors. Atherosclerosis 1998;1337:S101-S109.
20- Corsini A, Pazzucconi F, Arnaboldi L, et al. Direct effects of statins on the vascular wall. J Cardiovasc Pharmacol 1997;31:773-778.
21- Laufs U, La Fata V, Plutzky J, et al. Upregulation of endotelial nitric oxide synthase by HMG-CoA reductase inhibitors. Circulation 1998;97:1129-1135.
22- John S, Schlacih M, Langenfeld M, et al. Increased bioavailability of nitric oxide after lipid-lowering therapy in hypercholesterolemic patients: a randomized, placebo-controlled, double-blind study. Circulation 1998;98:211-216.
23- Kaesemeyer WH, Caldwell RB, Huang JZ, et al. Pravastatin sodium activates endothelial nitric oxide synthase independent of its cholesterol-lowering actions. J Am Coll Cardiol 1999;33:234-241.
24- Hernández-Perera O, Pérez-Sala D, Navarro-Antolín J, et al. Effects of the 3-hydroxy-3-methylglutaryl-CoA reductase inhibitors,
atorvastatin and simvastatin, on the expresión of endothelin-1 and endotelial nitric oxide synthase in vacular endotelial cells. J Clin Invest 1998;101:2711-2719.
25- Lacoste L, Lam JY, Hung J, et al. Hyperlipidemia and coronary disease: correction of the increased thrombogen potential with cholesterol reduction. Circulation 1995;92:3172-3177.
26- Mitropoulos K, Armitage J, Collins R. Randomized placebo-controlled study of the effects of simvastatin on haemostatic variables, lipoproteins and free fatty acids. Eur Heart J 1997;18:235-241.
27- Rosenson RS, Lowe GDO. Effects of lipids and lipoproteins on thrombosis and rheology. Atherosclerosis 1998;140:271-280.
29- Jialal I, Stein D, Balis D, et al.. Effect of hydroxymethyl glutaryl coenzyme A reductase inhibitor therapy on high sensitive C-Reactive protein levels. Circulation 2001;103:1933-1935.
30- Ridker PM, Rifai N, Pfeffer MA, et al. Long-term effects of pravastatin on plasma convçcentration of C-reactive protein. Circulation 1999;100:230-235.
31- Kwak B, Mulhaupt F, Mach F. Statins as a newly recognized type of immunomodulator. Nat Med 2000;6:1399-1402.
32- Weitz-Schmidt G, Welzenbach K, Brinkman V, et al.. Statins selectively inhibit leukocyte function antigen-1 by binding to a novel regulatory integrin site. Nat Med 2001;7:687-692.
33- Kobashigawa JA, Katznelson S, Laks H, et al. Effect of pravastatin on outcomes after cardiac transplantation. N Eng J Med 1995;333:621-627.
34- Tamai O, Matsuoka H, Itabe H, et al. Single LDL apheresis improves endothelium-dependent vasodilation in hypercholesterolemic humans. Circulation 1997;95:76-82.
35- Davignon J, Laaksonen R. Low-density lypoprotein independent effects of statins. Curr Opin Lipidol 1999;10:543-559.
36- Jukema J, Bruschke A, van Boven A, et al.. Effects of lipid lowering by pravastatin on progression and regression of coronary artery disease in symptomatic men with normal to moderately elevated cholesterol levels: the Regression Growth Evaluation Statin Study (REGRESS). Circulation 1995;91:2528-2540.
37- Davies MJ. Going from immutable to mutable atherosclerotic plaques. Am J Cardiol 2001;88(suppl):2F-9F.
38- Davies M. Stability and instability: two faces of coronary atherosclerosis. Circulation 1996;94:2013-2020.
39- Libby P. What have we learned about the biology of atherosclerosis? The role of inflammation. Am J Cardiol 2001;88(suppl):3J-6J.
40- Weissberg PL. Atherosclerosis involves more than just lipids: plaque dynamics. Eur Heart J 1999;1(suppl):T13-T18.
42- O’Driscoll GO, Green D, Taylor RR. Simvastatin, an HMG-coenzyme A reductase inhibitor, improves endothelial function within 1 month. Circulation 1997;95:1126-1131.
43- Rosenson RS, Tangney CC. Antiatherothrombotic properties of statins: implications for cardiovascular event reduction. JAMA 1998;279:1643-1650.
44- Liao JK, Shin WS, Lee WY, et al. Oxidized low-density lipoprotein decreases the expresión of endotelial nitric oxide synthase. J Biol Chem 1995;270:319-324.
45- Dupuis J, Tardiff JC, Cernacek P, et al. Cholesterol reduction rapidly improves endotelial function after acute coronary syndromes: the RECIFE (Reduction of Cholesterol in Ischemia and Function of the Endothelium) trial. Circulation 1999;99:3227-3232.
46- Pitt B, Mancini JGB, Ellis SG, et al., for the PLAC-I Investigators. Pravastatin limitation of Atherosclerosis in the coronary arteries (PLAC-I): reduction in atherosclerosis progression and clinical events. J Am Coll Cardiol 1995;26:1133-1139.
47- Waters D, Higginson L, Gladstone P, et al. Effects of monotherapy with an HMG-CoA reductase inhibition on the progression of coronary atherosclerosis as assessed by serial quantitative atherography: the Canadian Coronary Atherosclerosis Intervention trial.
Circulation 1994;89:959-968.
48- Lennernas H, Fager F. Pharmacodynamics and pharmacokinetics of the HMG-CoA reductase inhibitors. Clin Pharmacokinet 1997;32:403-425.
49- Mauro VF. Clinical pharmacokinetics and practical applications of simvastatin. Clin Pharmacokinet 1993; 24:195-202.
50- Horsmans Y. Different metabolism of statins: importance in drug-drug interactions. Eur Heart J 1999;1(suppl T):T7-T12.
51- Cilla Jr DD, Whitfield LR, Gibson DM, et al. Multiple-dose pharmacokinetics, pharmacodynamics and safety of atorvastatin, an inhibitor of HMG-CoA reductase, in healthy subjects. Clin Pharmacol Ther 1996; 60:687-95.
52- Brown AS, Bakker-Arkema RG, Yellen L,e t al. Treating patients with documented atherosclerosis of National Cholesterol Education Program recommended low-density-lipoprotein cholesterol goals with atorvastatin, fluvastatin, lovastatin, ans simvastatin. J Am Coll Cardiol 1998;32:665-672.
53- Quion JAV, Jones PH. Clinical pharmacokinetics of pravastatin. Clin Pharmacokinet 1994; 27:94-103.
54- Bootorf M, Hansten P. Long-term safety of hepatic hydroxymethyl glutaryl coenzyme A reductase inhibitors. Arch Intern Med 2000;160:2273-2280
55- Azie NE, Brater DC, Becker PA, et al. Interaction of diltiazem with lovastatin and pravastatin. Clin Pharmacol Therap 1998;64:369-377.
56- Kantola T, Kivist KT, Neuvonen PJ. Effect of itraconazole on the pharmacokinetics of atorvastatin. Clin Pharmacol Ther
1996;60:54-61.
57- Michalets EL. Update: clinically significant cytochrome P-450 drug interactions. Pharmacotherapy 1998;18:84-112.
58- Black DM, Bakker-Arkema RG, Nawrocki JW. An overview of the clinical safety profile of atorvastatin (Lipitor), a new HMG-CoA reductase inhibitor. Arch Intern Med 1998;158:577-584.
59- Bradford RH, Shear CL, Chremos AN, et al. Expanded Clinical Evaluation of Lovastatin (EXCEL) Study results: two-year efficacy and safety follow-up. Am J Cardiol 1994;74:667-673.
60- Lofberg M, Jankala H, Pautau A, et al. Metabolic causes of recurrent rhabdomyolysis. Acta Neurol Scand 1998;98:268-275.
61- Flint O, Masters B, Gregg R, et al. HMG CoA reductase inhibitor-induced myotoxicity: pravastatin and lovastatin inhibit the
geranylgeranylation of the low molecular weight proteins in neonatal rat muscle culture. Toxicol Appl Pharmacol 1997;145:99-110.
63- Backman JT, Kyrklund C, Kivisto KT, et al. Plasma concentrations of active simvastatin acid are increased by gemfibrozil. Clin Pharmacol Ther 2000;68:122-129.
64- Iso H, Jacobs DR Jr, Wentworth D, et al. Serum cholesterol levels and six-year mortality from stroke in 350,977 men screened for the múltiple risk factor intervention trial. N Eng J Med 1989;320:904-910.
65- Yano K, Reed DM, MacLean CJ. Serum cholesterol and hemorrhagic stroke in the Honolulu Heart Program. Stroke
1989;20:1460-1465.
66- Hebert PR, Gaziano M, Chan KS, et al. Cholesterol lowering with statins drugs, risk of stroke, and total mortality: an overview of randomized trials. JAMA 1997;278:31-321.
67- Blais L, Desgagné A, LeLorier J. 3-Hydroxy-3-methylglutaryl coenzyme A reductase inhibitors and the risk of cancer. Arch Intern Med 2000;160:2363-2368.
68- Pedersen TR, Wilhelmsen L, Faergeman O, et al. Follow-up study of patients randomized in the Scandinavian simvastatin survival study (4S) of cholesterol lowering. Am J Cardiol 2000;86:257-262.
69- Downs JR, Clearfield M, Weis S, et al., for the AFCAPS/TexCAPS Research Group. Primary prevention of acute coronary events with lovastatin in men and women with average cholesterol levels. Results of AFCAPS/TexCAPS. JAMA 1998;279:1615-1622. [ Links ]
70- Expert working group (efficacy) of the international conference on harmonization requirements for registration of pharmaceuticals for human use. Clinical safety data management: definitions and standards for expedited reporting. Federal Register. 1995;11284-11287. [ Links ]
71- Ioannidis J, Lau J. Completeness of safety reporting in randomized trials. An evaluation of 7 medical areas. JAMA 2001;285:437-443. [ Links ]*Depto. de Farmacología y Toxicología Clínica,
Escuela de Medicina, Universidad de Costa Rica.
Tel: 207-4492, Fax: 207-4489 jaguarcr@racsa.co.cr














