¿Qué es la acrilamida? ¿Cómo se forma?
La 2-propenamida (acrilamida) es utilizada ampliamente (Matthäus, 2008) en la industria para la síntesis de poliacrilamidas (Lineback, et al., 2012; Matthäus, 2008; Yu, 2007; Arribas, et al., 2012). Es un polvo blanco cristalino que se disuelve en agua, etanol, dimetiléter, metanol, acetona, pero no en heptano ni benceno (Valenzuela et al., 2007, Arribas, et al., 2012, Lingnert et al., 2002).
La acrilamida es considerada por la Agencia Internacional de Investigaciones en Cáncer (International Agency for Cancer Research IARC por sus siglas en inglés) (Clauss, et al., 2008) como "probable cancerígeno para los humanos”, esto basándose en estudios realizados en animales. De momento no se tiene claro que estos resultados puedan extrapolarse al ser humano, pero se sabe que la exposición a altas dosis causa daño al sistema nervioso y que este compuesto químico tiene propiedades mutagénicas y carcinogénicas (Clauss, et al., 2008, Matthäus, 2008, Masson, et al., 2007, Jackson, et al., 2005).
Al día de hoy se sabe que la formación de acrilamida en los alimentos involucra al aminoácido asparragina y a azúcares reductores (Figura 1), los cuales mediante la reacción de Maillard dan como resultado el mencionado compuesto, denominado actualmente como un contaminante del proceso o un contaminante neo formado La mayor cantidad de acrilamida ha sido detectada en alimentos fritos, asados u horneados con alto contenido de carbohidratos (papas, cereales) que son sometidos a temperaturas mayores a 120°C (Matthäus, 2008, Pedreschi, 2009). La literatura (Masson, et al., 2007) describe que al calentar cantidades equimolares de asparragina y glucosa a 180°C por un período de media hora es posible obtener 368 μmol de acrilamida (Stadler, et al., 2002). Se ha observado que la formación del compuesto es independiente de la temperatura desde los 120°C hasta los 170°C y que a temperaturas más elevadas se da lugar a un proceso de autodegradación poco estudiado hasta el momento (Stadler, et al., 2002; Jackson, et al., 2005). Lo que sí es conocido y reportado por la literatura es la existencia de una alta relación entre el tipo de procesamiento del alimento (valores tiempo- temperatura), el pH, la humedad y la tasa de formación de la acrilamida (Arribas, et al., 2012). Así mismo, también se ha logrado observar que la manera en que el calor es transmitido al alimento (conducción, convección o radiación) no es determinante en la formación de acrilamida (Jackson, et al., 2005). Otros aminoácidos como alanina, arginina, ácido aspártico, cisteína, glutamina, metionina, treonina y valina, pueden producir acrilamida bajo las mismas condiciones, pero en menores cantidades que la asparragina (Zhang, et al., 2007).
Algunos investigadores (Valenzuela, et al., 2007) también han propuesto que a partir del ácido acrílico (presente en alimentos ricos en lípidos) es posible obtener acroleína y ésta puede aportar a la reacción de Maillard su grupo carbonilo el cual, en presencia de asparragina, da como resultado la formación de acrilamida. Adicionalmente, se reporta que la acroleína en presencia de amoníaco mediante reacciones de oxidación puede ser una vía para la obtención de acrilamida (Gertz, et al., 2002; Lingnertet al., 2002), sin embargo, su generación mediante estas vías debe aún ser más estudiada.
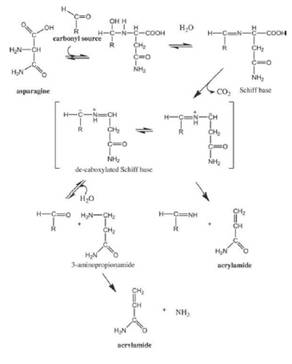
Figura 1 Mecanismo de formación de acrilamida a partir de la descarboxilación del compuesto de Amadori. Fuente: Clauss et al., 2008
1. Toxicidad de la acrilamida
La acrilamida puede ser absorbida por el ser humano mediante tres rutas diferentes: oral, inhalación o contacto dérmico (Arribas, et al., 2012). La mayoría de los estudios disponibles a la fecha, se han realizado en trabajadores expuestos a la inhalación de acrilamida y su absorción por piel, lo que impide valorar en que forma está vía de contacto puede ser comparada con la exposición mediante el consumo de alimentos que contengan acrilamida ya que en éstos últimos las interacciones con otros elementos de la matriz (ej: proteínas) podrían influir en su absorción (Valenzuela et al., 2007; Clauss, et al., 2008). Se han realizado pruebas en las que la acrilamida se administró, a ratas, disuelta en agua, obteniéndose un porcentaje de absorción de 60 a 90%, pero cuando se administró mediante alimentos fortificados la absorción solo fue del 28 al 47% (Doerge et al., 2005; Arribas, et al., 2012).
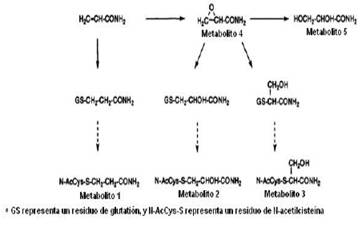
Se conoce que, debido a su polaridad, solubilidad en agua y bajo peso molecular la acrilamida se distribuye rápidamente en todo el cuerpo vía circulación sanguínea y puede ser detectada en timo, hígado, riñones e incluso en leche materna (Clauss, et al., 2008; Lineback, et al., 2012). En el hígado mediante la vía del citocromo P450, la acrilamida puede ser conjugada a glutatión y epoxidada a glicidamida (Figura 2). La formación de este derivado es considerada un paso crítico ya que éste compuesto es el responsable de la genotoxicidad de la acrilamida (Clauss, et al., 2008).
Se ha descrito que la exposición a altas dosis de acrilamida, genera daños a nivel del sistema nervioso, sin embargo, vía ingestión de alimentos estas altas dosis no se alcanzan por lo que el mayor efecto mediado por el consumo de alimentos que contengan acrilamida será mutagénico y carcinogénico (Clauss, et al., 2008), donde la glicidamida parece ser la responsable de tales efectos. Los investigadores en el campo, al parecer piensan que el mecanismo por el cual la acrilamida causa daño es una combinación de daño en el ADN, interferencia con la mitosis y meiosis y estrés oxidativo (Arribas, et al., 2012). Este último fenómeno al parecer, logra inducir un estado proinflamatorio que es considerado, un factor de riesgo para la progresión del aterosclerosis (Naruszewicz, et al., 2009).
En este punto es importante tener en cuenta que, en todos los estudios realizados con animales, se emplearon altas dosis de acrilamida por lo que éste factor aunado a las diferentes rutas de exposición y las diferencias metabólicas entre especies, hace que sea muy difícil realizar la extrapolación de los datos al ser humano (Arribas, et al., 2012).
2. Procesos y alimentos asociados a la formación de acrilamida
Está establecido que la formación de acrilamida se asocia a alimentos ricos en carbohidratos y relativamente pobres en proteínas (Carrieri, et al., 2009) que son sometidos a operaciones unitarias que presentan temperaturas elevadas. Estos procesos relacionados con la producción de 2-propenamida son: la fritura, el horneado, el tostado y el asado principalmente.
Predecir la cantidad de acrilamida que se formará durante el proceso de freído de un alimento es realmente complejo, ya que hay que considerar muchos parámetros que juegan un papel importante en este sistema (Barutcu, et al., 2009, Carrieri, et al., 2009). El duo tiempo- temperatura debe ser vigilado, además el pH y la concentración de sales también tienen su influencia en la reacción de formación de la acrilamida (Carrieri, et al., 2009). Adicionalmente, es importante mencionar que muchas investigaciones (Barutcu, et al., 2009; Clauss, et al., 2008; Arribas, et al., 2012) informan que el contenido de acrilamida en el interior de los alimentos es más bajo que el contenido en la capa externa de productos fritos y horneados (Suaterna, 2008).
Debido al hecho, que los resultados obtenidos hasta la fecha no son concluyentes, la acrilamida debe seguir siendo considerada como un agente “potencialmente cancerígeno” para el ser humano, por lo cual los niveles de este compuesto en los alimentos deben ser los mínimos posibles. Para lograr ese objetivo es primordial aclarar las rutas de formación de la acrilamida en los alimentos y a partir de ello elaborar estrategias dirigidas a conseguir los más bajos niveles de acrilamida que sea posible obtener.
Otro factor importante en la fritura es el tipo de aceite utilizado, así como su estado de oxidación e hidrólisis. Aparentemente, este parámetro no afecta de manera significativa la cantidad final de acrilamida que se pueda producir durante la operación (Masson, et al., 2007; Suaterna, 2008), aunque si se reporta un aumento de 10 veces su cantidad cuando se utilizó aceite reusado a 150°C para la producción de papas fritas (Masson, et al., 2007).
Las papas, tanto fritas como chips, son uno de los alimentos más relacionados con la formación de acrilamida y por tanto también más estudiados en este parámetro. Se sabe que las papas contienen asparragina (Pedreschi, 2009), precursor de la formación de acrilamida, sin embargo, la cantidad de este aminoácido y de los azúcares presentes en las papas son dependientes de su variedad, de las condiciones del suelo donde se cultive, de los fertilizantes utilizados, del período en que se coseche y el manejo y almacenamiento post cosecha que se realice (Pedreschi, 2009; Masson, et al., 2007; Matthäus, 2008; Jackson, et al., 2005). La cantidad de azúcares reductores se ve afectada por la temperatura de almacenamiento que se emplee, ya que los azúcares comienzan a acumularse cuando se da un desequilibrio entre la degradación del almidón, la síntesis de almidón y la tasa de respiración, este fenómeno se presenta a temperaturas menores a 10°C (Pedreschi, 2009; Masson, et al., 2007). Aunque este proceso está bien estudiado y descrito para los azúcares presentes en la papa, se sabe que el contenido de asparragina, no se ve afectado por la temperatura utilizada para el almacenamiento de los tubérculos antes de su procesamiento industrial (Olson, et al., 2004; Masson, et al., 2007).
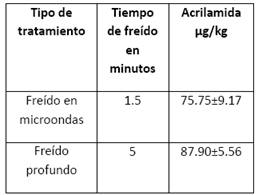
Como es lógico pensar, luego de observar el panorama muchos investigadores han propuesto diferentes opciones para tratar de reducir la formación de acrilamida durante la fritura, una de estas opciones es la fritura en microondas que no solo logra una reducción importante sino también una disminución en el tiempo de la operación (Cuadro 1) (Barutcu, et al., 2009).
Cuadro 1 Cantidad de acrilamida presente en pollo frito en microondas o por fritura profunda tradicional (Barutcu et al.)
Los alimentos a base de cereales son otro grupo que llama la atención en cuanto a porcentajes de acrilamida se refiere. En este sentido, el trigo y el centeno son dos de los cereales más utilizados en la dieta de muchos seres humanos. Se ha reportado que el trigo posee cantidades significativas de asparragina libre y azúcares reductores (Zhang et al., 2007). Sin embargo, los datos para la cantidad de aminoácidos libres y azúcares reductores del centeno no son tan claros (Zhang et al., 2007). Al igual que con las papas las condiciones de cultivo, fertilización y almacenamiento de los granos parecen tener influencia en los niveles de acrilamida que se encuentran en estos productos y sus derivados (Clauss, et al., 2008).
El proceso de tostado que conlleva la producción de café es otra operación relacionada con la formación de acrilamida. Este proceso utiliza temperaturas de aproximadamente 220- 250°C (Summa, et al., 2007) con niveles de acrilamida de 45 a 539 mgk-1 (Summa, et al., 2007), pero al parecer estas cantidades no son estables y decrecen con el tiempo (Gökmen, 2006). El café ha llamado también la atención de la comunidad científica no sólo por la presencia de acrilamida, sino también por su poder antioxidante que incluso pareciera relacionarse con baja incidencia de algunos tipos de cáncer (George et al., 2008). Tanto la formación de acrilamida como la presencia de sustancias con poder antioxidante se relación estrechamente con la reacción de Maillard, por lo cual si se toman medidas para tratar de reducirla, probablemente se estarían disminuyendo ambas sustancias en el producto final (Summa, et al.,2006), razón por la cual investigaciones recientes (Summa, et al.,2007; Summa, et al.,2006) alertan sobre la importancia de valorar el impacto que pueden tener ciertas medidas de mitigación de la formación de acrilamida, en otros componentes del producto, como es el caso de la capacidad antioxidante del café.
3. Métodos de detección de acrilamida en alimentos
Paralelamente al anuncio en 2002 de la existencia de acrilamida en alimentos, se desarrolló también un gran movimiento para contar con metodologías lo suficientemente exactas y sensibles que permitieran determinar los niveles de acrilamida en diferentes matrices alimentarias. En este sentido, los reportes en la literatura indican que existe uniformidad en cuanto a las técnicas de detección, siendo las más comúnmente utilizadas la cromatografía de gases acoplada a la espectrometría de masas (GC-MS) con un límite de detección de 10-30 mgkg-1 (Yusá et al., 2006) y la cromatografía líquida acoplada, también a la espectrometría de masas (LC-MS) con una detección límite de 30-50 mgkg-1 (Yusá et al., 2006; Linebacket al., 2012). Existen también otra serie de metodologías no oficiales que han mostrado un buen desempeño en cuanto a detección de acrilamida en alimentos, entre ellas se menciona la electroforesis capilar (CE), análisis inmunoenzimáticos y más recientemente biosensores (Oracz, et al; 2011).
En lo que respecta a los procedimientos de extracción y purificación de las muestras se reporta que existen notables diferencias (Valenzuela, et al., 2007; Oracz, et al; 2011), las cuales van a estar marcadas principalmente por la matriz alimentaria que vaya a ser analizada. Los procedimientos de extracción que comúnmente se utilizan van desde sonicación, dispersión y agitación a alta velocidad hasta agitación en rotor o extracción con fluidos supercríticos (Oracz, et al; 2011), utilizando en todos los casos (excepto en extracción de fluidos supercríticos donde se utiliza CO2), agua como disolvente (Yusá et al., 2006). Posterior a la extracción se debe realizar la purificación, para lo que se recomienda el uso de dos diferentes pasos de extracción de fase sólida (SPE), lentos y laboriosos.
Sin importar cual metodología se emplee siempre el disolvente utilizado es el agua. Esto representa un importante problema para realizar la concentración del extracto (Yusá et al., 2006), ya que, aunque utilizar el agua como disolvente es bastante económico y eficaz, es poco específico. Otras sustancias como almidón, proteínas y azúcares pueden competir con la acrilamida dependiendo de las condiciones aplicadas durante la extracción (Gökmenet al., 2009).
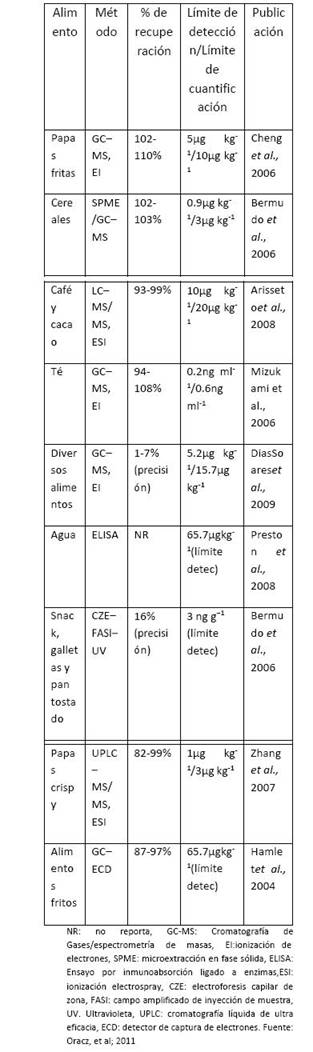
Oracz y colaboradores en su revisión del 2011, mencionan algunos de los métodos de detección de acrilamida en alimentos más utilizados (Cuadro 2).
Cuadro 2 Metodologías más empleadas para la detección de acrilamida en diferentes matrices alimentarias (Oracz, et al; 2011).
4. Estrategias para reducir la formación de acrilamida en alimentos
Existen diferentes estrategias centralizadas en reducir la formación de la 2-propenamida (Gökmenet al., 2007; FAO, 2009; FAO/WHO 2002; Lineback et al., 2012; Clauss, et al., 2008), pero casi todas se basan en la modificación de los siguientes parámetros: materias primas, control/adición de otros ingredientes, elaboración y tratamientos térmicos (FAO, 2009).
Hay que tener en cuenta que debido a la heterogeneidad de los alimentos que pueden presentar formación de acrilamida las estrategias de mitigación pueden ser muy diversas.
Con respecto a materias primas (en general) existe una base de datos bastante importante (FAO 2009; Clauss, et al., 2008; Matthäus, 2008; Jackson, et al., 2005). Las principales medidas a tomar pueden ser aplicadas desde el campo haciendo elección de la variedad de alimento (papa, grano de cereal) que posea menor cantidad de azúcares reductores y evitando la fertilización con abonos ricos en nitrógeno ya que se ha visto que estos ayudan a generar mayor cantidad de asparragina libre (Jackson, et al., 2005; Clauss, et al., 2008; Matthäus, 2008). Adicional a estas medidas también se reporta como deseable el almacenamiento, sobre todo de la papa a temperaturas mayores a los 6°C ya que esta medida previene la acumulación de azúcares reductores en el tubérculo (Clauss, et al., 2008; Matthäus, 2008; Lineback et al 2012 .,; FAO, 2009). Otra estrategia al parecer bastante viable es realizar pre- procesos como remojo, blanqueado y lavado con la idea de disminuir por lixiviación azúcares reductores (Matthäus, 2008; Lineback et al., 2012; FAO, 2009; Lineback et al., 2012; FAO, 2009). Aplicando estos pre-tratamientos algunos autores (Jackson, et al., 2005) reportan hasta un 50% de disminución de los azúcares reductores.
Referente al control/adición de otros ingredientes se hace mención de varias estrategias cuyo propósito es reducir la formación de acrilamida (Valenzuela et al., 2007; Clauss, et al., 2008; Matthäus, 2008; Lineback et al., 2012; FAO, 2009; Jackson, et al., 2005). Una de ellas es la adición de asparraginasa, la cual es capaz de degradar la asparragina a ácido aspártico y amonio (Lineback et al., 2012). Esta estrategia parecer ser importante en productos de panadería donde se reportan (Jackson, et al., 2005) disminuciones de hasta 75% de asparragina libre y 55% de formación de acrilamida en productos de panadería.
Se conoce también que disminuir el pH del medio desfavorece la reacción de Mailllard y por tanto la formación de acrilamida. Sin embargo, se reporta que la adición de ácidos como el cítrico, combinado con algunos pre-tratamientos como el blanqueado o escaldado, aunque logran reducir hasta en un 70% los niveles de acrilamida, afectan la calidad sensorial sobre todo de los productos a base de papa (Clauss, et al., 2008; Matthäus, 2008, Zhang et al., 2007). Otra posibilidad, que al parecer es prometedora en los productos de panadería, es extender el tiempo de fermentación con ayuda de levaduras capaces de desdoblar la asparragina y los azúcares reductores disminuyendo así la cantidad de reactantes para que se lleve a cabo la formación de acrilamida (Lineback et al., 2012; Clauss, et al., 2008). Se ha ensayado también la adición de cationes divalentes y trivalentes (sales de calcio), y adición de antioxidantes (extractos de hojas de bambú) entre otras estrategias a éste nivel (Lineback et al., 2012; Zhang et al., 2007; Gökmenet al., 2007).
5. Conclusiones
Las investigaciones realizadas hasta la fecha permiten concluir que la acrilamida no se encuentra en la mayoría de las materias primas, si no que es formada como consecuencia de ciertas operaciones unitarias que se realizan para conservar o dar mejor sabor a algunos alimentos. La formación de acrilamida durante dicho procesamiento, está íntimamente ligada a la conocida reacción de Maillard, y se genera cuando el aminoácido asparragina reacciona con azúcares reductores en presencia de temperaturas mayores a los 120°C (Arribas, et al., 2012; Pedreschi, 2009).
Finalmente, con respecto a los procesos de elaboración y tratamientos térmicos se recomienda vigilar muy bien el tiempo y temperatura utilizados, ya que estos son el catalizador de la reacción de formación de acrilamida y se mencionan estrategias como la fritura en microondas o al vacío con el fin de reducir la cantidad de acrilamida en el producto final (Zhang et al., 2007; Barutcu, et al., 2009).
Clauss, et al., y Zhang et al, (Clauss, et al., 2008; Zhang et al., 2007) recopilan en sus investigaciones algunos de los trabajos más relevantes en cuanto a estrategias de mitigación de formación de acrilamida se refiere.
Hasta el momento, se considera a la acrilamida como un potencial cancerígeno para el ser humano ya que aunque existen estudios científicos que sugieren que la exposición a éste tóxico genera daño en el ADN, dichos estudios han sido llevados a cabo en modelos animales y hasta la fecha no se ha publicado ningún estudio epidemiológico que afirme que las cantidades de acrilamida consumidas en los alimentos, por la población en general, aumenten significativamente el riesgo de sufrir algún tipo de cáncer por ésta causa. Sin embargo, las autoridades mundiales en inocuidad alimentaria recomiendan utilizar estrategias tendientes a la disminución de ésta sustancia en los alimentos (FAO, 2005). tecnologías que permitan detectar esta sustancia en diversos alimentos. Actualmente existen dos métodos oficiales para la detección de acrilamida en matrices alimentarias, la cromatografía de gases acoplada a la espectrometría de masas (GC-MS) y la cromatografía líquida acoplada, también a la espectrometría de masas (LC-MS) (Yusá et al., 2006; Lineback et al., 2012). Actualmente el mayor traspié en cuanto a detección de acrilamida se refiere es la complejidad y laboriosidad que presentan las técnicas de extracción de acrilamida (Gökmen et al., 2009; Oracz, et al; 2011; Lineback et al., 2012).
Finalmente existen prometedoras investigaciones en el campo que deben seguir siendo incentivadas con el fin de lograr comprender el fenómeno de integral, para así poder tomar decisiones adecuadas en el ámbito de la salud pública y la inocuidad alimentaria.