Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Médica del Hospital Nacional de Niños Dr. Carlos Sáenz Herrera
Print version ISSN 1017-8546
Rev. méd. Hosp. Nac. Niños (Costa Rica) vol.36 n.1-2 San José Jan. 2001
Introducción
Las bacterias han evolucionado a un ritmo tan acelerado que la industria farmacéutica se ha visto obligada, día a día, a vencer el reto que nos plantean los microorganismos, ante la adquisición de resistencia por parte de éstos.
Esta resistencia puede atribuirse a diversas causas: el uso incorrecto de los antibióticos por desconocimiento del agente causal de la infección, especialmente debido a la múltiple propaganda comercial, que favorece el que se ingiera un determinado antibiótico, sin realizarse un cultivo y una prueba de sensibilidad previa o la utilización de antibióticos como aditivos de engorde en alimentos para animales de carne, de consumo humano (5,11,18, 22, 29).
Cualquiera de estas modificaciones repercute en el cromosoma bacteriano, favorece la reproducción de cepas mutantes capaces de ser seleccionadas al entrar en estrés, eliminándose la población bacteriana sensible, y favoreciendo la proliferación de las resistentes (12, 24).
Las técnicas disponibles para detectar diferentes tipos de resistencia se encuentran limitadas debido a que las diferentes mutaciones en la cadena de aminoácidos pueden acarrear cambios en la velocidad de hidrólisis hacia los -lactámicos, que podrían llevamos a confusiones, sin poder dilucidar el tipo de inhibición (4,10,13).
El presente trabajo pretende hacer un resumen de las -lactamasas que se han descrito y proporcionar las mejores técnicas diagnosticas en el laboratorio.
Sin embargo, es necesario retomar algunos aspectos en la resistencia bacteriana para poder comprender la evolución de las -lactamasas.
I.- La resistencia bacteriana.
Se han utilizado modelos matemáticos para acertar la relación que existe, entre la incidencia del tratamiento por antibióticos y la frecuencia de resistencia bacteriana, en la flora normal del hombre y al mismo tiempo, la frecuencia con que podría declinar esta resistencia al cesar el uso de éstos.
Por estudios epidemiológicos se ha observado que cuanto menor es la proporción de individuos tratados con un antibiótico (15,19), menor es la tasa de resistencia hacia éste. De otro modo, grandes poblaciones de sujetos infectados con cepas sensibles protegen a la población de la aparición de resistentes, debido a densidad de población. Por otro lado, entre mayor sea la prevalecido de una cepa patógena, mayor será el número de sujetos tratados, aumentando la probabilidad de crear cepas resistentes (20).
Se ha podido determinar que la frecuencia de la resistencia está ligada a la tasa de mutación; ésta es bastante baja, del orden de 108 a 109, por lo que la aparición de un germen resistente en el medio, será el producto del tamaño de la población (15, 23, 28).
Si la bacteria resistente está presente en la población bacteriana de un grupo de humanos afectados por ella y si éstos a su vez, son tratados con antibiótico que le permitan a la bacteria ser seleccionada, la resistencia bacteriana podría ascender hacia frecuencias altas muy rápidamente. De otro modo, no es improbable la existencia de un mutante antes de la administración de un antibiótico, pero la probabilidad para que sea seleccionado dependerá del resto de la población bacteriana, durante el tratamiento (15).
Es así como, la presión de selección estará determinada por varios elementos como lo son las condiciones ambientales al entrar en contacto la bacteria con el antibiótico (11), por los factores epidemiológicos (21,30), por el uso de otros medicamentos (11,21,30) o por la presencia de contaminantes en el medio, (plásmidos o transposones), favoreciendo la proliferación de mutantes con respecto a las cepas sensibles (11,23,30).
Ahora, si el mutante resistente no está presente desde el inicio del tratamiento, la probabilidad de que surja un resistente es muy escasa (23).
Cuando estos mutantes existen en un individuo que está bajo tratamiento con antibióticos y éste lo interrumpe, la cantidad de bacterias resistentes disminuye pero no implica su desaparición, ya la cepa resistente existe. La toma irregular del antibiótico, favorece por ende, que las bacterias sensibles puedan volver a iniciar su crecimiento en presencia de concentraciones sub inhibitorias aumentando la probabilidad de que cepas sensibles puedan transformarse en cepas resistentes (11).
En el caso de que se administre un antibiótico durante períodos cortos de tratamiento, se favorece la disminución de resistencia que inicialmente podría ser elevado. Por otro lado, si el antibiótico se utiliza en concentraciones sub terapéuticas de modo continuo, la incidencia de cepas resistentes y la tasa de aparición de multi resistentes será más elevada, este hecho lo podemos observar en el uso de la tetraciclina durante períodos prolongados, sin embargo, este efecto dependerá del antibiótico y de las condiciones epidemiológicas de cada zona (23).
Se ha tratado de aplacar la resistencia bacteriana con la utilización de varios antibióticos, en conjunto; de este modo, cada antibiótico se dirigirá hacia el mutante resistente, sin embargo éstas asociaciones son armas de doble filo (24), debido a que si los antibióticos no se encuentran presentes al mismo tiempo y en el mismo lugar de la infección, en donde se localizan las bacterias, puede que no ejerzan una acción adecuada (11,30).
La rapidez con que una cepa resistente desaparece dependerá de su capacidad relativa de reproducción y de su difusión con respecto a la cepa sensible (19). Si la capacidad de reproducción es escasa, la tasa de resistencia disminuye hasta alcanzar el equilibrio, pero si esta capacidad no difiere, la tasa de resistencia permanecerá estable incluso en ausencia de tratamiento (19,26).
II.- Un poco de historia en las -lactamasas.
La vigilancia de la resistencia bacteriana se inició desde los años 30, con la introducción de las sulfamidas para el tratamiento de la enfermedad gonocócica y meningocócica. El descubrimiento de un compuesto llamado PRONTOSIL una azoanilina que contenía el grupo sulfamida llevó al Sr. Domagk en 1938 a obtener el Premio Nobel de Medicina, cit. en (12). Sin embargo, con el paso de los años el gonococo al igual que cepas meningocócicas, adquirieron en forma gradual, un cierto nivel de resistencia, por lo que decaen como tratamiento de elección, para este tipo de infecciones (12).
En 1928 fue Fleming cit. en (17), quien estudiando las variantes de Staphylococcus en el laboratorio, observó que un hongo contaminante de sus cultivos, producía lisis bacteriana a su alrededor; el hongo contenía una acción inhibitorio notable para muchos
microorganismos; como el hongo pertenecía al género Penicillium sp., Fleming llamó penicilina a la sustancia antibacteriana encontrada.
Una década después, la penicilina se desarrolló como un agente terapéutico sistémico por la investigación de un grupo de científicos de la Universidad de Oxford, encabezados por Florey, Chain y Abraham cit en (12). Para el año de 1940, el descubrimiento real de la resistencia bacteriana fue dado a conocer por Abraham y Chain cit. en (2), quienes observaron en ciertos extractos de Escherichi. coli la inactivación de soluciones de penicilina. Es aquí donde nacen las llamadas penicilinasas.
En 1944 Kirby cit. en (12), observa que la producción de penicilinasas correlaciona con la resistencia a la penicilina en cultivos de Staphylococcus aureus.
Para el año de 1960 se introducen las primeras penicilinas sintéticas tale como; meticilinas y ampicilinas, el primero contra cocos Gram positivo y el segundo contra bacilos Gram negativo y además, se desarrolló la primera generación de la familia de las cefalosporinas (12).
Poco después del uso a gran escala de la penicilina G aparecen las primeras cepas de Staphylococcus aureus resistentes a este tipo de antibiótico, como resultado de la elaboración de una -lactamasa, enzimas capaces de hidrolizar irreversiblemente el enlace amida del núcleo betalactámico de la penicilina.
A partir de 1960 y hasta 1978 se inicia la era de las penicilinas semisintéticas y viene el desarrollo de la otra generación de las cefalosporinas.
Para el año de 1963 se aislan las primeras betalactamasas, la -lactamasa de Ecoli la TEM- 1, posteriormente la SHV-1 y la PSE-1 (2,17, 25).
Esta aparición se ha ido diseminando por la producción bacteriana de plásmidos capaces de transferir genes que confieren resistencia a antibióticos betalactámicos. Estas -lactamasas mediadas por plásmidos confieren un alto nivel de resistencia hacia las penicilinas y un bajo nivel de resistencia a las cefalosporinas de primera generación. El nivel de resistencia depende de la cantidad de
-lactamasas producida.
La primera generación de cefalosporinas fue más resistente a las -lactamasas y se infiltró más rápidamente en la membrana externa de bacilos Gram negativo que las penicilinas haciendo a los antibióticos más efectivos.
Para finales de 1977 e inicios de 1978, comienza a observarse pérdida de genes productores de porinas como el OmpC que produce disminución en la permeabilidad de la membrana y la aparición de cefalosporinasas. Por ese entonces las infecciones con bacilos Gram negativos aumentan en su prevalencia (3,17).
A partir de 1978 hasta 1995 comienza la era de las cefamicinas, oxyimiocefalosporinas, monobactams, carbapenems y los inhibidores de -lactamasas como el ácido clavulánico, ácido penicilánico y sulfonas.
En octubre de 1978 ya había sido aprobado el uso de la cefoxitina en los Estados Unidos, antibiótico producido por un hongo llamado Streptomyces clavulgerus. Este antibiótico era muy resistente a la hidrólisis por los plásmidos conocidos, que mediaban la producción de -lactamasas. Sin embargo, existía aún un grupo de bacterias resistentes tales como:
Enterobacter, Serratia, Citrobacter, Morganella y Burkholderia (17).
Poco después, se introdujo el cefuroxime una droga sintética -lactámica resistente a las
-lactamasas mediadas por plásmidos. Una modificación en el anillo beta lactámico, aumentó la vida media de la droga creando un nuevo antibiótico, el ceftriaxone (antibiótico
-lactámico de tercera generación) con igual espectro antibacteriano.
De nuevo aparece un mecanismo de resistencia, donde la hiperproducción de-lactamasa especie específica de la clase A (penicilinasa) cromosomal se hacen presentes (4,17).
Todos estos antibióticos fueron utilizados ampliamente en la clínica en hospitales de los Estados Unidos, pero el más utilizado fue el ceftriaxone por la conveniencia de una dosis diaria lo que pudo muy probablemente causar la aparición de la resistencia (17).
Con el descubrimiento de un antibiótico monocíclico natural el monobactain de bacterias como Pseudomonas acidophila, Agrobacterium sp., Flavobacterium sp. y Chromobacterium violaceum y la modificación sintética de la molécula, se genera un nuevo antibiótico: el aztreonam con actividad en presencia de muchas de las -lactamasas producidas por bacilos Gram negativo, y actividad antipseudomónica, pero sin actividad contra bacterias Gram positivo y organismos anaeróbicos (12).
Otra nueva molécula, los carbapenems producidos por Streptomyces cattylea fue estudiada y mejorada hasta producir el imipenem. Ninguna betalactamasa del grupo A ni el C podía inactivarlo, solamente unas pocas bacterias productoras de metaloenzimas podían hacerlo (Stenotrophomonas maltophilia) (4,17).
Para 1982 se comienza a observar mutaciones estructurales por plásmidos que determinaban la afinidad de las -lactamasas a las cefalosporinas de tercera generación y monobactames. Por otro lado se encontró que especies de Enterobacter y Serratia eran capaces de producir carbapenemasas ( 17).
En 1983 la SHV-2 fue la primera -lactamasa de espectro extendido que se reporta en la literatura, la cual fue descubierta en Alemania y siete aflos después reportada en Francia. Por último aparece reportada en los Estados Unidos (3,17).
En 1984 el ácido clavulánico comienza a utilizarse junto con la penicilina con el objetivo de inactivar el sitio de unión de la betalactamasa bacteriana evitando hidrólisis de la penicilina en combinación con esta droga.
Comienzan a aislarse -lactamasas derivadas del TEM en Francia la TEM-3 evidenciando nuevas mutaciones (serina cambia por glicina en la posición 238 en el sitio activo). Se encuentran cuatro variantes naturales TEM-4, TEM-8, TEM-15 y TEM-25 con la misma sustitución. La TEM-12 aparece en 1987 con la sustitución de la serina en vez de la arginina en la posición 164, estas cepas eran mucho más resistentes a ceftazidime y aztreonam que las cepas productoras de TEM- 1 y TEM-2 (3,4,17).
Se encuentran nuevas variantes como la de lisina por serina en la posición 204, lo que da origen a las -lactamasas TEM-5, TEM-10 y TEM-27. Por otro lado, la sustitución de lisina por serina en la posición 104 da origen a TEM-6, TEM-9, TEM-26 y por último la sustitución de treonina por alanina en la posición 237 origina a TEM-5.
La TEM-26 surge de mutaciones silenciosas en bacterias causantes de brotes tanto en Estados Unidos como en Inglaterra, lo que sugiere una evolución convergente. La TEM-12 aparece por una sola mutación en la TEM-10 o la TEM-26, ambas fueron encontradas en una misma bacteria (4,17).
Para 1985 se comienza a utilizar el imipenem combinado con otras drogas, el cual era adecuado para B-lactamasas de clase A (penicilinasa), y clase C (cefalosporinasas) pero eran inactivadas por metaloenzimas.
En ocho años las bacterias comensales y patógenas de humanos habían sido expuestas a seis nuevas clases de agentes B-lactámicos de los cuales, tres eran de origen natural a partir de Streptomyces (cefamicinas, carbapenems y clavams); uno totalmente sintético el monobactam; y dos semisintéticos (oxyminobetalactámicos , sulfonas del ácido penicilánico) (4,17). Durante esta era muchos mecanismos de resistencia hacia los nuevos agentes emergieron de cepas aisladas en la clínica.
En 1988 comienzan a aparecer cepas de Klebsiella pneumoniae resistentes a cefoxitina, ceftibuten, y a combinaciones a cefotaxime, ceftazidine y aztreonam, estas cepas habían adquirido plásmidos que codificaban -lactamasas tipo cefalosporinasas MIR-1, con una alta secuencia de homología a las
-lactamasas cromosomales de Citrobacter freundii (BIL-1, CMY-2, LAT-1), observándose la presencia de plásmidos en la transferencia de la mutación.
También para 1988 en Japón emergen plásmidos que determinan metalobetalactamasas que hidrolizan carbapenems, la bacteria involucrada fue Pseudomonasaeruginosa que era capaz de hidrolizar imipenem por conjugación a través de la betalactamasa IMP-1 (1,4,17).
Para 1991 aparecen los primeros derivados de -lactamasa TEM con alta afinidad para el ácido clavulánico, (SHV-6), este fenómeno se describe en sangre de neonatos donde se aísla Escherichia coli resistente ( 17).
Dos -lactamasas de espectro expandido son descritas, la OXA-11 y la OXA-14 (3) aislada de P. aeruginosa, el aspartato reemplaza la glicina en la posición 143 en la primera, y la posición 157 en la segunda, ambas proporcionan un alto nivel de resistencia a ceftazidime pero no a aztreonam. También aparecen cepas de P. aeruginosa que producían una
-lactamasa con resistencia a ambos antibióticos a la que se le llamó PER-1, éstas fueron reportadas en París y en Turquía. En Istambul también fue reportada en cepas de Salmonella sp. (3,4).
Para 1999 comienza a observarse resistencia múltiple a antibióticos (18). Esta resistencia es fácilmente transferida a miembros de la familia Enterobacteriaceae, en el mismo paciente produciendo resistencia a una gran variedad de antibióticos no solamente 13lactámicos sino también a quinolonas, en donde la resistencia no es mediada por plásmidos. Es muy probable que esta multirresistencia se deba a la capacidad de la bacteria a modificar sus proteínas de membrana sobre todo en el caso de K. pneumoniae (30).
Cuando las -lactamasas de espectro extendido fueron identificadas inicialmente, fue en K. pneumoniae y ocasionalmente en Enterobacteriaceae en Francia (17), luego en Estados Unidos y por último en el resto de Europa. Esta mutación fue mediada por plásmidos (16,18) en dos géneros diferentes inicialmente aisladas en infecciones en hospitales y seleccionadas por la utilización de cefalosporinas de espectro extendido. Hoy en día las encontramos colonizando tanto pacientes ambulatorios, como en hospitalizados.
Históricamente al inicio de la resistencia bacteriana, solo se encontraban cepas con genes capaces de producir una o dos -lactamasa, sin embargo hoy en día, tienen diferentes mutaciones que les permiten sintetizar tres o cuatro
-lactamasas (7,26). Cuando múltiples enzimas son producidas por un mismo organismo, las propiedades biológicas pueden reflejar una mezcla compleja de parárnetros hacia una variedad en la cinética enzimática y en la cantidad de enzima a producir. Esto implica una problemática en la identificación en el laboratorio, de organismos productores de
-lactamasas (4).
La aparición de nuevos genes que generen resistencia hacia los antibióticos existentes irá en aumento si no se logra controlar adecuadamente el uso de éstos, a su vez la mortalidad y morbilidad podría llegar a números difíciles de controlar y caeríamos en una "crisis de resistencia bacteriana". Es necesario que las nuevas investigaciones giren alrededor de la creación de protocolos capaces de mantener una eficiencia terapéutica para el bienestar de la humanidad (13).
Los siguientes cuadros son una reseña histórica de las -lactamasas que se han encontrado.

III.- ¿Qué son las betalactamasas?
Son enzimas, producidas por bacterias con peptidoglucano y por algunos hongos, utilizadas para defenderse de antibióticos betalactámicos, o bien son utilizadas por la bacteria para sintetizar su pared bacteriana. El hombre las ha utilizado como terapéutico en la clínica (7,12,13).
Se han descrito más de 190 enzimas de tipo -lactamasa, y constituyen la mayor causa de resistencia bacteriana hacia antibióticos con anillos betalactámicos (14).
Las -lactamasas son proteínas especializadas con estructura cuatemaria de
-hoja. Están divididas en clases de acuerdo a su peso molecular, punto isoeléctrico y sitio activo entre otros (3,4,17).
Las clases A, C, D tienen serina en su sitio activo, la clase B son metaloenzimas (3,4,8,13).
Las -lactamasas clase A, C, y D tienen secuencias de aininoácidos similares, sobre todo con las proteínas peptidasas (14) encargadas de unir penicilina (PBPs), que son los blancos de acción de los antibióticos
-lactámicos (8).
La estructura terciaria de estas enzimas es muy similar (17). El sustrato natural de estas peptidasas está en la pared celular, éste es un dipéptido con terminaciones D-alanil-D-alanina (13) que foitna el final de la mureína.
Con la producción de la penicilina G, Tipper y Strominger cit. en (3,4) proponen que la conformación terciaria del carboxilo terminar de la D-alanil-D-alanina es de estructura similar al de la conformación - de los betalactárnicos por lo que ésta podía interferir con la formación de la pared celular al poderse unir al sitio activo de las enzimas
-lactamasas de las bacterias (12).
Dentro de la clase A hay cuatro subclases de -lactamasas: primero podemos citar a la PCI de S. aureus, la segunda a 749/C de Bacillus ticheniformis, la tercera a la tipo G de Streptomyces albus y la cuarta la TEM-1 de E. coli (17).
En la clase C hay dos subclases: en la primera se puede citar la 1203 de Citrobacter freundii, y al P99 de Enterobacter cloacas y en la segunda a las PBP de especies de Streptomyces R61. Todas éstas son solubles en agua, de bajo peso molecular y los D-alanyl-D-alanina son extracelulares (17).
Las enzimas que reconocen penicilina tienen una secuencia de cuatro aminoácidos: serina-X-X-Iisina; las X representan algún aminoácido diferente.
La estructura terciaria de la Clase A presenta las siguientes característica:
El sitio activo está ubicado en el aminoácido de serina, posición 70 (Ser-70).
Dentro de la Clase A existe otra tríada de aminoácidos, en las enzimas que reconocen penicilinas, ésta es: lisina-treonina-glicina (Lys-234), esta tríada forman parte de la hoja beta que delimita una de las paredes del sitio de actividad o sitio de unión con el sustrato (3,4,17).
Existe también otra tríada de aminoácidos en las Clase A: serina-ácido aspárticoaspargina (Ser-130); ésta se encarga de estabilizar el sitio activo por puentes de hidrógeno unidos a una lisina en posición 234 en el lado opuesto de la cavidad (3,4,17).
En la Clase C la estructura terciaria se caracteriza por:
El sitio activo está ubicado en el animoácido de serina, posición 64 ( Ser-64).
Existe una triada de arninoácidos, en las enzimas que reconocen penicilinas en la clase C; ésta es histidina, serina-glicina (Lys-315), la cual forma parte de la hoja beta que delimita una de las paredes del sitio de actividad o sitio de unión con el sustrato (17).
También hay otra tríada de aininoácidos en la Clase C: tirosina-ácido aspárticoaspargina. (Tyr-150), ésta se encarga de estabilizar el sitio activo por puentes de hidrógeno, unidos a una lisina en posición 234, en el lado opuesto de la cavidad del sitio activo.
En ambas clases (clase A y clase C), la serina del sitio activo se encuentra en lo más profundo de la cavidad. La estructura cuatemaria tiene forma de la letra griega "omega", cuyos péptidos contienen la secuencia de aminoácidos: arginina-X-glutamato-X-X-Ieucina-asparagina (serina), muy conservada en las -lactamasas clase A, pero alterada para todas las otras enzimas que reconocen penicilina (17).
Esta estructura define la otra pared del sitio activo, de estructura delgada en la cual se lleva a cabo el ataque nucleofilico. Sin embargo, en la clase A puede haber una arginina en la posición 244 que sirve de punto de ataque para aquellas drogas -lactámicas que no tienen el anillo betalactamasa. La clase C, pierde una contraparte, por lo que la hace relativamente imnune a los inhibidores (3,17).
Tanto las proteínas que unen penicilinas como las -lactamasas clase C tienen sitios activos dentro de la cavidad que le permite al sustrato formar puentes de unión con la serina. Sin embargo la principal función de las proteínas que unen penicilinas (PBPS) es la de partir (actividad carboxipeptidasa y endopeptidasa) y unir (actividad transpeptidasa) pequeños péptidos. Algunas son capaces de dividir por la mitad enlaces glicosídicos (actividad transglicosilasa) en la pared celular; algunas pueden hidrolizar uniones
-lactámcas (actividad
-lactamasa) pero de foma inesciente y lenta (3,4,17).
La composición del péptidoglicano cambia conforme se produce el crecimiento de la pared; por esto es que los antibióticos -lactámicos requieren inhibir a más de una de las PBPs (proteínas que unen penicilinas).
La mayoría de las PBPs de los bacilos Gram negativo producen -lactamasas de tipo especie-específica y la cantidad que produce cada bacteria, está determinada por genes cromosomales sobre todo ampC ( 3,27).
Las metaloenzimas forman la clase B de las -lactamasas, éstas son hidrolasas (1) formadas por dos subdominios, cada uno separado por una alfa -hoja y un par de hélices que caen hacia el exterior de cada una de ellas. Cada subdominio está dividido en dos sectores (1) y el primer subdominio está formado por los sectores 1 y 2.
El primer sector es muy conservado y está tipificado por una alfa-hoja que contiene un aspartato terminar. Este aspartato participa en la estabilización de las cargas positivas entre los sectores 1 y 2 (1).
El segundo sector es el más característico de la super familia de metaloenzimas, con actividad de glioxilasa y alfa -lactamasa. Este sector tiene una estructura HxHxDH, donde la primera H corresponde a un aspartato que se mantiene invariante, en todos los miembros activos de esta familia. La segunda H es reemplazada por residuos acídicos en varios miembros de las flavoproteínas. Mientras que la tercera H es remplazada por arginina en las alfa-lactamasas típicas (1).
En este segundo sector se encuentra el sitio activo, en el cual se produce la reacción de hidrólisis. Está formado por zinc, estabilizado por dos histidirias y fuertemente protegido por una estructura muy conservada de aspartato (1). El segundo subdominio está formado por los sectores 3 y 4.
El sector 3 se caracteriza por la presencia de una histidina, que es precedida por un pequeño residuo. Esta histidina actúa como un ligando coordinador de zinc, sosteniéndolo en el sitio activo.
El sector 4 es muy similar al 3, caracterizado por histidina asociada a un nitrógeno tertninal. La histidina tiene la función de proteger el sitio activo con actividad alfa-lactamasa, además de interaccionar con las cargas negativas del sustrato (1).
Las betalactamasas pueden ser enzimas inducidas, al ser codificadas por un gen no funcional que se activa en presencia de un inductor, por esta razón, pueden activarse directamente en el paciente. O por otro lado, pueden ser enzimas de tipo constitutivas, no requiriendo la presencia de un inductor para producirse (7,19).
Pueden actuar como exoenzimas excretándose al medio o podrían ser enzimas intracelulares retenidas en los espacios periplásmicos (11, 19).
En, el caso de -lactamasas de las bacterias Gram negativo podemos distinguir dos tipos: constitutivo o inducible, codificadas por genes cromosómicos o extracromosómicos; por ejemplo Haemophilus sp., Neisseria sp., y Bacteroides fragilis. Por otro lado las betalactamasas se encuentran en cantidades más bien pequeñas y están localizadas en el espacio periplásmico (9).
Para las -lactamasas de las bacterias Gram positivo se pueden citar dos tipos, las exoenzima inducible, producidas por genes o del tipo extracromosómico situadas en plásmidos pequeños no autotransferibles, con actividad de tipo penicilinasa (9).
Las bacterias Gram positivo producen una gran cantidad de betalactamasas, que se secretan al medio extracelular (19).
IV.- Mecanismos de resistencia de las -lactamasas.
La producción de betalactamasas ocurre por diversas modificaciones en la información genética (3,4). Estas modificaciones ocurren por dos tipos de mutaciones: cromosómicas o por elementos extracromosómicos (7).
En el tipo cromosómica, la resistencia ocurre por mutaciones en los genes de la bacteria, que controlan las funciones y estructuras sobre las que actúan los distintos antibióticos, modificando la susceptibilidad de la bacteria a ellos. En este caso, ocurre una modificación, en la secuencia de bases del ácido nucléico de la bacteria, transmitiendo esta información a su descendencia (resistencia en un solo escalón) o en el transcurso de varias generaciones (resistencia en varios escalones), haciendo a la bacteria totalmente resistente a la droga (7).
Estas mutaciones ocurren espontáneamente y pueden dar lugar a la alteración o superproducción de una enzima específica (7), o afectar proteínas que participan en la permeabilidad de la membrana alterando la entrada del antibiótico o bien, acumulación de éste, en el espacio periplásmico situado entre la membrana externa e interna de la bacteria (18).
El otro mecanismo de resistencia ocurre por elementos extracromosómicos, portadores de determinada información, como lo son los plásmidos y los trasposones, que tienen la capacidad de transferirse de una bacteria a otra, de igual o diferente género y especie (11, 18). Estos mecanismos extracromosómicos se manifiestan por tres procesos: el primero por conjugación con el paso de un plásmido o de un trasposon, de una bacteria a otra, involucro el contacto de ADN de célula a célula; la segunda por transformación en la cual hay incorporación en el cromosoma bacteriano, de ADN presente en el medio; en este caso el ADN se adquiere del medio directamente, éste sale hacia alguna célula, por ejemplo, el factor deresistencia RTF, que es transferido de una bacteria a otra, por medio de un plásmido, a la hora del cruce de dos bacterias. Y la tercera, por transducción en donde el ADN proveniente de un bacteriófago se incorpora al ADN bacteriano (18).
La resistencia a los inhibidores de betalactamasas en patógenos productores de este tipo de enzimas se debe principalmente a los siguientes mecanismos:
1.- Disminución de la permeabilidad hacia el antibiótico por alteración de canales de porinas.
2.- Inactivación enzimática del antibiótico (eromosomal o plasmídica).
3.- Modificación química de la diana sobre la que actúa el antibiótico (alteración en las PBPS)
4.- Tolerancia.
1.- Disminución de la permeabilidad hacia el antibiótico por modificación en una barrera preexistente.
La membrana externa de las bacterias Gram negativo es una barrera natural que favorece a la insensibilidad hacia varios antibióticos, que no son capaces de atravesar las porinas(12). Sin embargo no todas las bacterias Gram negativo son igualmente impermeables a los mismos antibióticos, entre las menos impermeables podemos citar a: Haemophilus sp. y Neisseria sp., que dejan pasar a numerosos -lactámicos; las Enterobacteriacea suelen ser intermedias (19).
En otros casos, la resistencia se debe a alteraciones en la cápsula, como en el caso de algunos neumococos resistentes (12). Pero el mecanismo adquirido por las bacterias para favorecer la incapacidad o disminución de la entrada del antibiótico se debe a modificaciones en las proteínas productoras de porinas, situadas en la membrana citoplasmática (15).
La activación de genes escondidos (crípticos) es producida por la activación del promotor o por la activación de secuencias de inserción (segmentos de ADN menor que los transposones) delante del gen de resistencia, produciendo modificaciones en la formación de proteínas, denominadas porinas, capaces de determinar la entrada y salida de sustancias a la célula (23).
En las bacterias Gram negativo los productos del gen MAR inhibe al gen SOX-RS, en presencia de -lactámicos causando una disminución en los genes que codifican la formación de porinas. Se ha observado en especies de Salmonella en donde la pérdida de un segmento genético se traduce en la pérdida de la porina OmpC, esto confiere resistencia a la cefalotina (7).
En K. pneumoniae la pérdida de porinas facilita la resistencia de TEM-3 hacia los antibióticos (18). Sin embargo, se ha observado con mucha más frecuencia la pérdida de porinas al utilizar imipenem en P Aeruginosa (con la pérdida de porina D2) y también en cepas de Enterobacter cloacae (18).
Por otra parte, la resistencia a carbapenemes es un ejemplo de resistencia mediada por hidrólisis del agente antimicrobiano y por cambios en las porinas que reducen la permeabilidad de la pared bacteriana.
Existen diferentes niveles de resistencia, que están determinados por la capacidad de la -lactamasas para hidrolizar el antibiótico y por el número de mecanismos de resistencia presentes. Los organismos pueden producir más de una enzima para hidrolizar y pueden presentar modificaciones en más de una porina produciendo altos niveles de resistencia.
La modificación en las proteínas de membrana externa OmpF y/o OmpC, limitan la penetración de las asociaciones de betalactámicos e inhibidores de betalactamasas confiriendo resistencia (7,17).
2.- Inactivación enzimática del antibiótico.
Este tipo de mecanismo está mediado cromosómicamente o por plásmidos.
La forma más común de resistencia hacia -lactámicos es la producción de penicilinasa (
-lactamasa) capaces de abrir el anillo
-lactámico de la penicilina con la formación de un producto incapaz de tener actividad (ácido peniciloico), por ejemplo en antibióticos como las cefalosporinas, donde la
-lactamasa (cefalosporinasa) genera un producto inestable e inactivo, que se descompone rápidamente (12).
La naturaleza de la cadena lateral (grupo acilo, R) influye notablemente en la susceptibilidad de rotura del anillo -lactámico por las lactamasas, un ejemplo de esto son las
-lactamasas codificadas cromosómicamente del tipo TEM (11, 17).
Mecanismo cromosómico:
Este tipo de resistencia está muy distribuida en bacterias Gram negativo confiriendo resistencia a penicilinas y cefalosporinas. Se basa en la exposición de la bacteria durante mucho tiempo al antibiótico (13), seleccionándose determinadas mutaciones en genes cromosómicos que codifican proteínas parecidas a las del tipo PBPS, adquiriendo un fuerte promotor, que le permite su expresión a alto nivel. Este tipo de -lactamasa es excretada al medio en donde inactiva al antibiótico
-lactámico (19).
El gen que codifica la -lactamasa se induce por pequeñas cantidades de penicilina o cefalosporina, y produce enormes cantidades del antibiótico, que se excreta, de modo que inactiva al
-lactámico en el entorno de la bacteria (19).
Mecanismo mediado extracomosómicamente por plásmidos.
En este caso, la resistencia es producida porque el gen responsable, es portado por plásmidos de tipo R (que llevan genes de resistencia para otros antibióticos). En las bacterias Gram-negativas, se han descubierto unos 20 tipos de -lactamasas de codificación plasmídica (S). Suelen ser enzimas de síntesis constitutiva que se expresan a bajos niveles, y cuya localización es periplásmica; esta localización permite que el antibiótico sea inactivado antes de que llegue a la membrana citoplásmica, donde se localizan las proteínas diana de los
-lactámicos.
Algunas de ellas vienen codificadas por genes plasmídicos que forman parte de transposones (p. ej., el Tnl o el Tn4) (8).
La hiperproducción de la enzima:
La hiperproducción de enzima -lactamasa causa inactivación de antibiéticos
-lactámicos.
El aumento en la cantidad de enzimas betalactamasas está ligada a la ausencia de una membrana externa en el caso de las bacterias Gram positivo para poder resistir al antibiótico (19).
Consecuentemente, otras bacterias son capaces de adquirir secuencias de inserción de plásmidos, que se ubican en el promotor de -lactamasas, al incorporarse al gen bacteriano provocando una hiperproducción de éstas. Por ejemplo las
-lactamasas cromosomales TEM1 de E. coli y K- 1 de K. pneumoniae que pueden obtenerse por la presencia de plásmidos multicopia o a la existencia de un promotor muy fuerte.
La hiperproducción de -lactamasas por el gen AmpC (2) ocurren en un 18% de las cepas E. coli aisladas en infecciones hospitalarias y se deben a una activación del promotor (segmento de ADN esencial para que éste se exprese) por medio de transferencia horizontal (adquisición de resistencia de un organismo a otro por procesos de selección genética) (23).
En la familia Enterobacteriaceae por ejemplo, Salmonella, pierde un gen estructural para la producción de -lactamasas, produciendo menor cantidad de enzima. Por otro lado en E. coli, las
-lactamasas son especie específicas clase C determinadas por genes cromosomales AmpC ligados a otros genes. El producto de AmpR (regulador transcripcional) aumenta la transcripción de AmpC cuando son activados los fragmentos de la pared celular (GIcNac-anhidro MurNac-tripéptido), que penetra al citoplasma bajo el control de una permeasa (AmpG). Una amidasa (AmpD) corta los péptidos para reciclarlos luego y hacer nueva pared. Solo algunos fragmentos de los que se escapan del reciclaje pueden volver a activar al AmpR. Cuando los antibióticos
-lactámicos se disparan sobre la pared bacteriana rompiéndola, se produce una sobrecarga en la amidasa, facilitando una superproducción de
-latamasas (17). Mutaciones en la AmpD produce modificaciones en la amidasa causando el efecto contrario, disminución, en la producción de
-lactamasas (4).
Estas mutaciones ocurren espontáneamente y con una frecuencia de 10-4 a 10-6 en cepas aisladas de infecciones hospitalarias en E. cloacae produciendo subpoblaciones altamente resistentes que pueden ser seleccionadas con antibióticos -lactámicos de tercera generación (4).
Con el descubrimiento de las enzimas que regulan la producción de la pared bacteriana, el reciclaje de los fragmentos de mureína y la producción de -lactamasas clase C, se sugiere que la mutación se produce, como una función relacionada con el crecimiento celular ( 4,17 ).
En el caso de bacterias Gram positivo como S. aureus y Bacillus licheniformis secretan grandes cantidades de -lactamasas clase A, fuera de la célula, lo que les ayuda a mantener poblaciones resistentes.
Podemos citar a K. oxytoca como otro ejemplo de hiperproducción de enzimas -lactamasa especie específica clase A cromosomal (11).
3.- Modificación química de la diana sobre la que actúa el antibiótico (alteración en las PBPs penicillin-binding-portein)
Los antibióticos betalactámicos van dirigidos a blancos llamados proteínas de unión de penicilina "PBPs". (12,23); si el antibiótico es capaz de unirse a ellas provoca la destrucción de la bacteria.
El microorganismo puede tener una resistencia intrínseca a causa de diferencias estructurales en las proteínas PBPS, sin embargo, esta resistencia puede obtenerse por mutación, como en el caso de los cocos Grwn positivo (17). La modificación de las proteínas de unión a la penicilina (PBPS) causa disminución en la capacidad de fijación del antibiótico a éstas.
La mutación es conocida desde 1982, cuando se introducen los antibióticos -lactámicos de espectro extendido y con el reporte de un brote de K pneumoniae que fue dificil de controlar. Esta mutación aparecía por diferentes mutaciones silenciosas favorecidas por plásmidos que llevó a una mutación convergente (4).
En este mecanismo, lo que sucede es que cambia la secuencia de uno o dos aminoácidos, en el sitio activo de las -lactamasas, esto los hace resistentes ya que el antibiótico
-lactámico no pude unirse a ellas (17).
Estas mutaciones ocurren en los genes E104K, E240K o el A237T, en donde los residuos de lisina en el sitio activo, favorece una disminución en la afinidad del antibiótico hacia dicho sitio, por lo que pierde la actividad. Entre este tipo de -lactamasas podemos citar a TEM- 10, TEM- 12, TEM-26, TEM-24, SHV-2, SHV-5 y SHV-4 (3,4,17).
La producción de estas proteínas se ve regulada por la transducción de señales de proteínas de membrana y por represores transcripcionales (31). El transductor de señal se compone de una fusión de proteínas con dominios de metaloproteasa de zinc y de uniones de penicilina. La señal para la expresión de la proteína se transmite por una división proteolítica específica del lugar de ambos trasductores, que se autoactivan y el represor que se inactiva, sin bloquear la transcripción del gen. Un ejemplo de esto es la resistencia a oxaciclina en donde el gen meca, provoca una alteración en la proteína de unión de la penicilina PBP2a, que no le permite a los -lactámicos unirse bien a la célula bacteriana causando la resistencia (23,31).
4. Resistencia por tolerancia.
Las bacterias que son capaces de producir valores de una dilución doble más alta que de Concentración Inhibitoria Mínima (CIM) son llamadas tolerantes (MCB> ó = 32). Ocurre cuando las bacterias tienen una pérdida de autolisinas y toleran la concentración del antibiótico (19,23).
V.- Aspectos importantes sobre la resistencia a asociaciones de -lactámicos.
La resistencia a las asociaciones de betalactámico e inhibidor de betalactamasas se debe a la sobreproducción de la cefalosporinasa cromosómica del grupo 1. El patrón de resistencia incluye aminopenicilinas, amoxicilina-ácido clavulánico, cefalosporinas de primera y segunda generación y cefainicinas. Se elevan discretamente las CMI de las carboxipenicilinas y ureidopenicilinas, y pueden encontrarse cepas con sensibilidad disminuida a todos los betalactámicos excepto los carbapenémicos (11).
La cloxacilinasa OXA-1 no es tan bien inhibida como la TEM-1 por los diferentes inhibidores de betalactamasas. La hiperproducción de esta enzima, además de elevar la CMI de amoxicilina-ácido clavulánico, disminuye la sensibilidad a la cefpiroma (2-8 µg/ml) y a la cefotaxima (0,5-2 µg/ml),sin afectar a la ceftazidima ni al aztreonam (4). Se puede sospechar su presencia en cepas resistentes a aminopenicilinas, carboxipenicilinas y asociaciones de betalactámico e inhibidor de betalactamasas, y en sensibles a cefalotina (15). El fenotipo de las cepas hiperproductoras de betalactamasas del grupo 2b incluye CMI muy elevadas para aininopenicilinas, carboxipenicilinas, ureidopenicilinas y en menor grado para la amoxicilina-ácido clavulánico y las cefalosporinas de primera y segunda generación. Puede producirse también un ligero aumento de las CMI de ceftazidima y aztreonam (11, 17,18).
Las cepas productoras de IRBL son resistentes a las penicilinas de amplio espectro, solas y en combinación con inhibidores de betalactamasas. Se mantienen sensibles a las cefalosporinas de primera y segunda generación y a las cefamicinas. La resistencia a amoxicilina-ácido clavulánico, junto con la sensibilidad completa a la cefazolina y la cefoxitina, sugieren la presencia de un mecanismo enzimático de resistencia diferente de la hiperproducción de TEM o de las alteraciones de la membrana (24).
VI.-Clasificación de las -lactamasas
La clasificación de las betalactamasas se origina cuando se separan las cefalosporinasas de las penicilinasas.
Entre las clasificaciones que han sido aceptadas para las -lactamasa figuran las de:
* 1968 Sawai et al cit. en (13). En la cual describe cefalosporinasas y penicilinasas utilizando la respuesta a antisueros como discriminante.
* 1970 Jack y Richmond cit. en (18), las clasifican de acuerdo al espectro de actividad antimicrobiana en tres grandes grupos: Grupo I: Cefalosporinasas, Grupo II Penicilinasa, y Grupo III: AE.
* 1973 Richmond y Sykes cit. en (3,18), incluyen todas las -lactamasas de bacterias Gram-negativas clasificándolas en cinco grandes grupos, basado en el sustrato de hidrólisis para cada enzima y su capacidad inhibitorio hacia algunos compuestos como cloxacilina, carbenicilina, PCMB (p-eloromercuribenzoato) y cloruro de sodio.
* 1976 Sykes y Matthew cit. en (3,9,11) utilizan una clasificación de acuerdo a la localización cromosómica o plásmica, tomando en cuenta el espectro y el punto isoeléctrico dividiéndolo en dos grupos.
Grupo I Cromosómicas: en ella figuran: las penicilinasas y cefalosporinasas .*1980 Ambler cit. en (3,18), propone una clasificación de estructura molecular clasificándolas en dos: Clase A enzimas serinas, donde ubicaGrupo II Plasmídicas: inhibidas por oxaciclinasas, no inhibidas por oxaciclinasas y el resto.
* 1981 Jaurin y Grundstrom cit. en (10), incluyen la clase C, cefalosporinasas y la clase D, enzimas que hidrolizan oxacilinas.
Con el aporte de Ambier, Jaurin y Grundstrom queda propuesta una clasificación basada en el peso molecular, espectro y grado de homología en secuencias de aminoácidos, postulándose las cuatro clases:
Clase B: Metaloenzimas con actividad preferentemente cefalosporinasas.
Clase C: Cefalosporinasas cromosómicas de bacterias Gram negativo.
Clase D: Enzimás serinas que hidrolizan oxaciclina.
Grupo II Enzimas serina inhibidas por ácido clavulánico, incluyendo 6 subgrupos.
Grupo III Metaloenzimas no inhibidas por ácido clavulánico.
Grupo IV Penicilinasas no inhibidas por ácido clavulánico.
Inhibición por EDTA y por PCMB (-cloromercuribenzoato); peso molecular, clase molecular, punto isoeléctrico y secuenciación de nucleótidos.
Mantienen la clasificación de cuatro grupos, pero generan nuevos subgrupos, ésta es la clasificación vigente y enseguida un pequeño resumen de cada grupo (3,4, 10).
-Iactamasas del Grupo I
Se colocaron dentro de este grupo todas las enzimas serina con actividad cefalosporinasas, capaces de hidrolizar benzilpenicilina, no inhibidas por ácido clavulánico, pero sí son inhibidas por aztreonam (ATM).
Casi siempre cromosómicos, aunque hay algunos que se integran al gen por plásmidos.
Pueden ser inducibles o constitutivas. Clase molecular C (formadas por proteínas básicas con un peso molecular > 30 kD y punto isoeléctrico >7,0).
Se incluyen la mayoría de cefalosporinasas de Enterobacteriaceae Incluyen 32 cefalosporinasas. (E. coli, K. pneumoniae, P aeruginosa, Enterobacter spp, Serratia spp, Citrobacterfreudii.). Ejemplo: P99 de E. cloacas, MIR-1 de E. cloacas, FOX-1 K. pneumoniae
-Iactamasas del Grupo II
Es la categoría más grande.
Son penicilinasas que se agrupan de acuerdo a el porcentaje de hidrólisis a la carbenicilina, cefalosporinas, cloxacilina (oxacilina) o carbapenems.
Dentro de este grupo se colocan todas las enzimas serina con actividad penicilinasa e inhibidas por ácido clavulánico. La mitad son de codificición plasmídica.
Se incluyen 138 -lactamasas.
Se incluyen K pneumniae, Klebsiella oxytoca, E. coli, E. vulgaris, E. cloacas, S. marcescens., S. aureus, P aeruginosa, C. Freundii y Stenotrophomonas maltophilia.
Se designan 8 subgrupos:
Subgrupo2a: Con actividad penicilinasa, inhibida por ácido clavulánico, clase de acuerdo al peso molecular: "clase molecular A".
Ejemplos: penicilinasas de bacterias Gram positivo como la estafilocóccica vistas en S. aureus y S. albus
Subgrupo2b: Con actividad penicilinasa y cefalosporinasas, inhibida por ácido clavulánico, con una clase molecular A, generalmente plasmídicas y constitutivas.
Ejemplos: Se incluyen las enzimas más frecuentes de bacterias Gram negativo, TEM 1 de E. coli; TEM2 de P aeruginosa; SHV- 1 de E.coli. y la cantidad de enzima secretada depende del número de copias del plásmido, del número de copia del gen y de la eficiencia del promotor del gen.
Subgrupo2be: Se agruparon todas aquellas enzimas con un porcentaje de hidrólisis mayor al 10% hacia la ceftazidina, cefotaxime o aztreonain que a la bencilpenicilina.
En ellas se agrupan penicilinasas de amplio espectro, cefalosporinasas y monobactamas.
Son enzimas de espectro amplio, derivadas estructuralmente del grupo 2b, inhibidas por ácido clavulánico. Varían en el nivel de resistencia conferida. Clase molecular A.
Se incluyeron -lactamasas como TEM-7 de C. freundii y TEM-2, que son resultado de mutaciones puntuales en genes que producen las enzimas TEM- 1, y TEM-2.
Ejemplos: Se incluyen las enzimas de bacterias Gram-negativas TEM-3 a TEM-27; SHV-2 a SHV-7; KI de Klebsiella oxytoca. Se aíslan con más frecuencia de E. coli y K. pneumoniae.
Subgrupo2br: Derivadas estructuralmente del grupo 2b, con actividad sobre penicilinasa, son de tipo plasmídica, con una reducida afinidad por el ácido clavulánico y otros inhibidores. Clase molecular A.
Ejemplos: Se incluyen las enzimas de bacterias Gram negativo TEM-30 a TEM-36, TRC- 1.
Subgrupo2c: Se incluyen todas las enzimas que hidrolizaron un 60% más la carbenicilina que las bencilpenicilinas; y un 50% menos cloxacilina que bencilpenicilina.
Estas enzimas tienen actividad sobre las penicilinasas, y en especial a carbenicilinasas, inhibidas por ácido clavulánico, de codificación generalmente plasmídica y solo ocasionalmente cromosómica. Clase molecular A
Ejemplos: Se incluyen las enzimas AER-1,PSE-1,PSE-3,PSE-4,CARB-3.
Subgrupo2d: Se incluyen todas las enzimas que hidrolizaron un 50% más la cloxaciclina que las bencilpenicilinas; y que también hidrolizan la carbenicilina.
Estas enzimas tienen actividad sobre las penicilinasas, y en especial a las oxaciclinasas. Inhibidas por ácido clavulánico en menor grado. Clase molecular D.
Codificación en general plasmídica.
Ejemplos: Se incluyen las enzimas de P. aeruginosa OXA-1 a la OXA-7; LCR-1.
Subgrupo2e: Son cefalosporinasas que hidrolizaron cefotaxime (cefuroximasas) pero que pierden la actividad hidrolítica sobre las penicilinasas. Inhibidas por ácido clavulánico pero con baja afinidad por el monobactam. Inhibidas por ácido clavulánico. Clase molecular A.
Codificación cromosómica o plasmídica. Se incluyen las cefalosporinas inducibles de P vulgaris y la enzima L-2 de Stenotrophomonas maltophilia.
Subgrupo2f. Actividad sobre penicilinasas, cefalosporinasas, y carbapenemasas. Inhibidas débilmente por ácido clavulánico. Clase molecular A. Codificación cromosómica e inducible. Ejemplos: Se incluyen las enzimas IMI-1,NMC-A y Sme-1 de E. cloacas y S. marcescens.
-Iactamasas del Grupo III.
Incluye la mayoría de las -lactamasas que son inhibidas por EDTA pero no inhibidas por ácido clavulánico. Compuesto por metaloenzimas incluyendo carbapenems.
Clase molecular B. Se incluyen P aeruginosa, B. fragilis, S. maltophilia, algunas especies de Aeromonas sp, Flavovacterium sp. y Serratia sp.
Codificación generalmente cromosómica, algunas de tipo plasmídica.
Se incluyen las enzimas L- 1 de Stenotrophomonas maltophilia, CcrA de B. fragilis.
- Iactamasas del Grupo IV
Son penicilinasas que no son inhibidas por ácido clavulánico. Son poco estudiadas por lo que no se ha determinado su clase molecular. Se incluyen en este grupo la penicilinasa cromosómica de Burkholderia cepacia, y algunas de codificación plasmídica.
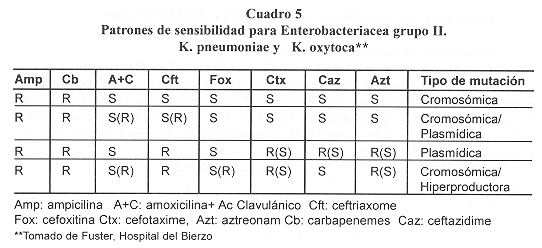
El Cuadro 3 resume la clasificación de Bush, Jacoby y Madeiros de 1995.
Técnicas de detección de las -lactamasas.
El fundamento de la detección de las -lactamasas es el de enfrentar la bacteria en estudio con los preparados betalactámicos para poner en evidencia la estabilidad (mayor o menor) de éstos frente a las enzimas
-lactamasas producidas por dichas bacterias (6).
Los métodos utilizados varían de acuerdo a la especie bacteriana a ser estudiada, el antibiótico a ensayar y el tipo de enzima a detectar (6,11,20).
Hay diferentes tipos de técnicas de detección entre ellas tenemos: 1.- las bioquímicas, subdivididas en las yodométricas, cromogénicas, y las técnicas de tipo 2.- microbiológicas (9).
Técnicas bioquímicas.
a. Acidimétrica: Son poco específicas, se basa en que los grupos carboxilo formados por hidrólisis, acidifica el medio.
b. Yodométricas: Se basan en las propiedades reductoras que poseen los productos de hidrólisis del anillo -lactámico hacia una mezcla de yodo - almidón. Esta técnica es útil para detectar penicilinasas.
c. Cromogénicas: La hidrólisis de determinados preparados -lactámicos da lugar a la formación de productos, con un espectro de absorción en la región visible, diferente a la del compuesto inicial. El compuesto más utilizado es la nitrocefina la cual cambia de color amarillo al rojo oscuro al ser hidrolizado. Esta técnica es de gran sensibilidad (detecta cantidades muy pequeñas de enzima) y se utiliza frecuentemente.
Técnicas Microbiológicas.
Se basan en la pérdida de actividad animicrobiana de los antibióticos al ser hidrolizados por la -lactamasa de la bacteria en estudio.
Se utiliza una cepa control denominada S (sensible) y una cepa problema denominada R (resistente). Si la resistencia es enzimática la cepa R problema, destruye al antibiótico de su entorno, permitiendo crecer a la cepa reveladora (S) (4,6, 10).
Esta técnica requiere más tiempo que la técnica bioquímica, sin embargo es de mayor utilidad.
Entre estas técnicas podemos citar la más utilizada como screening para detección de resistencia, la técnica disco-placa (10).
Otra técnica utilizada frecuentemente es la sinergia en doble disco (10, 11). Se utiliza para la detección de enzimas de espectro ampliado y se basa en la propiedad del ácido clavulánico de inhibir estas enzimas.
En esta técnica se inocula una placa con agar Mueller Hinton con la cepa problema a probar y se coloca un disco de amoxicilina- clavulánico en el centro de la placa y discos de cefotaxime, ceftazidina, ceftriaxone y aztreonam a su alrededor y a 30 mm exactos, del disco central.
La prueba se considera positiva cuando hay disminución hacia alguno de los preparados cuando se combina con sinergia para el ácido clavulánico.
Para la detección de -lactamasas de bacterias Gram negativo como H. influenzae, Neisseria y Bacteroides son útiles todas las técnicas ya que las enzimas que se producen son extracelulares. Para las bacterias Gram negativo, las
-lactamasas tienen sustratos fáciles de obtener, por lo que la técnica cromogénica es la más utilizada. En el caso de bacterias Gram negativo en que la membrana externa dificulta el acceso del sustrato al espacio periplásmico es necesario recurrir a la ruptura mecánica o química de la célula bacteriana (9).
Las técnicas que se utilizan para la caracterización de las -lactamasas son (4):
1.- Espectro de hidrólisis. 2.- Inhibición de la actividad hidrolítica hacia diferentes sustancias. 3.- Peso Molecular. 4.- Punto isoeléctrico. 5.- Hiperproducción de enzimas. 6.- Secuencia de aminoácidos. 7.- Secuencia de nucleótidos. 8.- Hibridación de ADN-ADN.
El papel del laboratorio de microbiología es crucial en el reconocimiento de resistencia por enzimas -lactamasas en las diferentes infecciones, por lo que debe de estar alerta ante la presencia de un fenotipo poco habitual e iniciar un plan racional para.el control de las infecciones que pudieran producirse.
Sin embargo, no existe una metodología que reúna sensibilidad, especificidad y sencillez para la detección de las -lactamasas de amplio espectro y de sus variantes, por lo qu es importante el criterio profesional del microbiólogo a la hora de seleccionar las pruebas más convenientes a utilizar en cada caso (6).
Otros aspectos importantes en la detección de -lactamasas
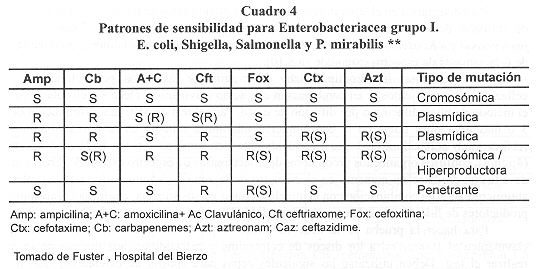
-Iactamasas de Enterobacteriacea Grupo I:
En este grupo podemos citar a E. coli, Shigella, Salmonella y P mirabilis.
Producen generalmente niveles insignificantes de -lactamasa cromosómica AmpC no inducible que no causa resistencia a los preparados
-lactámicos, aunque en casos ocasionales E. coli podría producirlo por mutaciones a nivel del locus del promotor, o del atenuador o ambos, en este caso se producen cantidades importantes de enzima-cepas hiperproductoras, estas cepas suponen menos del 2% (9,20).
La resistencia en estos casos va siempre ligada a plásmidos en el 50% de las E. coli siendo la enzima más frecuente la TEM- 1 en el 90% de los casos (9).
Algunas E. coli son resistentes al ácido clavulánico con hiperproducción de enzima TEM, o hiperproducción por mecanismos cromosómicos. También se han encontrado enzimas resistentes a otros inhibidores sobre todo tipo OXA (20).
-lactamasas de Enterobacteriaceac Grupo lI:
En este grupo podemos citar a K. pneumoniae y a K. oxytoca.
La mayor parte de las cepas producen enzimas cromosómicas constitutivas y a bajos niveles que confieren resistencia a aminopenicilinas y carbapenemes pero son inhibidas en presencia de clavulónico.
Median resistencia a cefalosporinas de tercera generación (ceftazidime, cefotaxime y ceftriaxone) y monobactames (aztroenam). No actúan sobre cefamicinas (cefoxitina y cefotetan) ni sobre carbapenemes.
La respuesta hacia ureidopenicilinas y cefalosporinas de primera generación es variable y a veces altamente dependiente del inóculo por lo que hay que considerar la resistencia.
Las -lactamasas de K pneumoniae suelen ser de tipo SHV-1 mientras que en K.oxytoca los tipos más frecuentes son K- 1 y KOXY (18).
La hiperproducción de enzima cromosómica se da especialmente en K. oxytoca, la K-1 ocasionando resistencia en un 10% a 20% de los preparados (18).
Esta bacterias algunas veces pueden producir enzimas de tipo plasmídicas que suman su acción a las cromosómicas incrementando la resistencia (9).
Para detectarlos en el laboratorio se han desarrollado caldos de microtitulación y el test de difusión de disco utilizando agentes antimicrobianos seleccionados. Todas las K pneumoniae y a K oxytoca o E. coli deben de considerarse como potencialmente productoras de
Para confirmar los fenotipos debe de examinarse las cepas por cefotaxime y ceftazidime solos y juntos; y en combinación con ácido clavulánico. Debe ser ejecutado por el método de microdilución o por difusión de disco. Para el test de MIC una disminución de 3 o más diluciones doble en la concentración inhibitorio mínima en ambos antibióticos (cefotaxime y ceftazidime) tratados individualmente y en combinación con ácido clavulánico (4µg/ml), confirma organismos productores de -lactamasas de espectro extendido. En el test de difusión de disco un aumento en el diámetro de la zona de >5mm para ambos agentes antimicrobianos en combinación con ácido clavulánico versus su zona, confirma organismos productores de
-lactamasas de espectro extendido (10).
Para hacer la prueba se le debe de añadir 10µl de una solución stock de ácido clavulánico al 1000µg/ml a los discos de cefotaxime y ceflazidime cada día que se va a realizar el test. Deben utilizarse las siguientes cepas para control de calidad del test: K pneumoniae ATCC 700603 como control positivo y E. coli ATCC 25922 como control negativo (6, 10).
El examen para la confirmación fenotípica no detecta todas las -lactamasas de espectro extendido, algunos organismos pueden contener otras que pueden enmascarar las
-lactamasas que se buscan por lo que el resultado podría revelar falsos negativos. Estas
-lactamasas incluyen AmpC y los inhibidores-resistentes TEMS. La hiperproducción de TEM o SHV también pueden producir falsos negativos en la confirmación fenotípica. Para poder confirmar se debe realizar métodos de isoelectroenfoque y secuenciación de ADN (9, 10).
De otro modo, si en un aislamiento se confirman cepas productoras de -lactamasas de espectro extendido, se debe hacer el reporte de rutina y no hacer interpretaciones de penicilina, cefalosporinas y aztreonam si no se ha confirmado adecuadamente.
Existen otras especies de Enterobacteriacea que producen -lactamasas de espectro extendido, como Salmonella sp. y Proteus mirabilis, además de P aeruginosa pero el NCCLS aún no ha determinado el test fenotípico confirmatorio para ellas (20).
-lactamasas de Enterobacteriacea Grupo III:
Dentro de este grupo podemos citar Enterobacter sp, C freundii, Serratia spp., Morganella morganii, Providencia stuartii, Providencia rettgeri.
Estas bacterias producen enzimas cromosómicas ampC de expresión inducible, con actividad cefalosporinasas y no inhibidas por clavulánico. Son resistentes a aminopenicilina, cefalosporinas de 1° generación y algunas veces a cefalosporinas de 2° generación (9).
Se pueden aislar cepas mutantes con producción de -lactamasas constitutivas y de tipo hiperproductoras de enzima con relativa frecuencia.
La producción de -lactamasas plasmáticas es poco frecuente y suele ser del tipo TEM-1 que da lugar a resistencia a carbapenemes y piperacilina (6, 10).
Las cepas hiperproductoras de enzima se pueden seleccionar en el curso del tratamiento con preparados poco inductores como lo son las cefalosporinas de 3° generación, ureidopeniciiinas y aztreonam. La hiperproducción de enzima causa resistencia a cefalosporinas de 3° generación, a aztreonam y a veces a carbapenemes (6, 10).
Dentro de este grupo III de Enterobacteriaceae podemos citar a P vulgaris y C. diversos como productoras de enzimas cromosómicas inducidas (grupo 2e) tipo cefuroximasas, capaces de activarse frente a penicilina, cefuroxima, cetotoxime y ceftriaxona. No son activas frente a ceftazidime, cefoxitina y carbapenemes. Son inhibidas por ac. clavulánico (9).
El grado de resistencia conferido depende de la cantidad de enzima reflejando el número de copias del gen o la eficiencia del promotor.
Son resistentes a aminopenicilina y carboxipenicilinas, tienen resistencia variable a ureidopenicilinas, piperazina y cefalosporinas de 1° generación (6, 10).
Hay que interpretar la sensibilidad con precaución, porque puede depender de la cantidad de inóculo. Se debe considerar las cepas como resistentes en infecciones graves.
-lactamasas de Staphylococeus coagulase negativo resistentes a oxacilina
Hay 20 especies diferentes de Staphylococcus sp., sin embargo se les considera dentro de un solo grupo. Algunas especies son más resistentes hacia los agentes antibacterianos que otras, por lo que es necesaria la identificación de especie, sobre todo para identificar los diferentes brotes y seguir su pista hacia la resistencia, además de que limitan las opciones de tratamiento ya que son resistentes a todos los -lactámicos incluyendo penicilinas, cefalosporinas,carbapenems y algunas veces a vancomicina (6).
S. epidermidis es el Staphylococcus coagulase negativo más frecuente, pero usualmente S. haemolyticus y S. hominis son los que se reportan con multiresistencia hacia antibióticos (6,10).
La detección en el laboratorio puede ser dificil ya que el tamaño de las colonias de los Staphylococcus coagulase negativo resistentes son más pequefias que los S. aureus lo que dificulta la lectura.
Por otro lado, pueden subsistir dos poblaciones juntas, resistentes y no resistentes en el mismo cultivo. Todas las células del mismo cultivo pueden llevar información genética de resistencia, pero solo un pequeño número puede expresarías in vitro. A esto se llama hetero resistencia (6,20).
La hetero resistencia ocurre en los Staphylococcus resistentes a oxacilina.
Otro aspecto importante es que las células que expresan resistencia pueden crecer más lentamente que la población susceptible, por lo que se recomienda incubar a 35°C por 24 horas exactas antes de leer (6, 10).
En 1999 el Comité Nacional para Laboratorios Clínicos (NCCLS) determina que los puntos de corte en la prueba de sensibilidad para Staphylococcus coagulase negativos es diferente a los puntos de corte de S. aureus; esto debido a que las cepas de este último contienen un gen denominado meca el cual codifica para la modificación de la proteína PBP2a, que no permite a la droga oxacilina o meticilina unirse a ella causando la resistencia a agentes -lactámicos (10).
Las -lactamasas de Staphylococcus son enzimas del grupo 2°, activas frente a la penicilina G, aminopenicilinas y carboxipenicilina, además son resistentes a meticilina en cepas hiperproductoras de enzima.
Tienen cierta labilidad hacia cefazolina y otras cefalosporinas como el tazobactam (6).
Aproximadamente el 5% de las cepas de S. aureus son susceptibles a la penicilina. En los EEUU la mayoría de las cepas son resistentes a penicilina pero susceptibles a oxacilina y meticilina (cepas llamadas MRSA) y son resistentes a todos los agentes -lactámicos incluyendo cefalosporinas y carbapenemens. También pueden ser multiresistentes a drogas como la eritromicina, clindamicina y teraciclina.
Se han encontrado unas pocas cepas con susceptibilidad disminuida a vancomicina (20).
Estas cepas MRSA son importantes de diagnosticar debido a que son cepas patogénicas y en la mayoría de los casos aisladas en infecciones adquiridas en los hospitales.
Las opciones de tratamiento son limitadas, donde la vancomicina es la única droga de elección.
Para poder detectar cepas de Staphylococcus aureus oxacilino resistentes se debe de usar un agar de Mueller-Hinton conteniendo 6jig/ml de oxacilina y suplementado con NACI 4% (6,10).
La detección será dificil si en el cultivo se encuentran mezcladas cepas resistentes y susceptibles por lo que se recomienda (NCCLS) incubaciones a 35°C por 24 horas completas antes de la lectura y además utilizar en la prueba discos de oxacilina, meticilina y nafcilina (20).
Para poder detectar cepas conteniendo MRSA se debe de utilizar caldo base y agar base y se recomienda utilizar platos con oxacilina junto con la técnica de rutina para suceptibilidad como un método de respaldo.
Existen pruebas utilizando la reacción en cadena de la polimerasa para detectar el gen meca. Esta prueba se utiliza solo para confirmar la resistencia a oxacilina/meticilina.
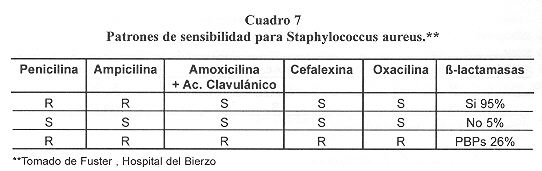
Se producen por difusión de plásmidos que codifican -lactamasas de Staphylococcus a enterococos. La frecuencia de producción es muy baja.
Son resistentes a ampicilina y piperacilina, son sensibles a amoxicilina, ácido clavulánico, tazobactam y carbapenems (9).
En el caso de Enterococcus faecium la resistencia se debe a modificación de las proteínas de unión por lo que es resistente a todos los -lactámicos.
-lactamasas de Haemophilus, Neisseria y B. catarrhalis.
Son de producción plasmídica generalmente del tipo TEM- 1. En EEUU H. influenzae es productora de una -lactamasa ROB-1 con mucha frecuencia. En B. catarrhalis los tipos más frecuentes son: BRO-1 y el BRO-2 y aún cuando todas son de difícil detección, la técnica utilizada es la cromogénica (9).
.



Son B-lactamasas del tipo cromosómica inducible ampC similar a la de Enterobacter. La selección de cepas hiperproductoras puede ocurrir durante la terapia con inductores débiles y lábiles como la piperacilina y cefalosporinas de 3°generación (9).
También pueden tener -lactamasas del tipo plasmídicas o por mecanismos de permeabilidad de la membrana.
-lactamasas de Stenotrophomonas maltophilia.
Produce dos -lactamasas cromosómicas inducibles la L-1 y la L-2.
La L-1 es activa frente a la mayoría de los -lactámicos excepto por aztreonam y cefsulodina. En el caso de la L-2 es una cefalosporinasa que puede hidrolizar todas las cefalosporinas y monobactames. Son inhibidas por clavulánico (9).
-lactamasas de Acinetobacter sp.
Es poco claro el papel que desempeñan en la resistencia hacia los antibióticos Blactámicos, sin embargo se conoce de modificaciones en las proteínas de unión a las penicilinas (PBPS) y alteraciones en la permeabilidad.
-lactamasas de Bacteroidesfragilis.
Las -lactamasas son de tipo cromosómico, inhibidas por clavulánico, tazabactam y sulbactam.
Producen resistencia a penicilinas y cefalosporinas de 3°generación, pero se han encontrado algunas cepas que presentan cierta actividad por lo que es necesario utilizar combinaciones de inhibidores o compuestos estables como las cefamicinas o carbapenems.
Ocasionalmente podrían producir otras enzimas con actividad frente a cefamicinas, carbapenems.
-lactamasas carbapenemasas
Son producidas por bacterias Gram negativo como P Aeruginosa, Pmiriabilis, P vulgaris, y M morganii. Frecuentemente estos organismos son detectados con un valor de MICs >16 µg/ml (intermedios) para P aeruginosa, y de 1-4µg/mL para Pmirabilis; P vulgaris, y M morganii. La mayoría de las otras especies de Enterobacteriaceae son susceptibles (9,20).
Para detectar estas enzimas pueden aplicarse los métodos de microtitulación, pero se debe de tener cuidado con la interpretación de imipemen (falsa resistencia), por degradación de la droga al almacenaría.
Como el imipemen se degrada fácilmente puede utilizarse meropenem (9).
Problemas de identificación de -lactamasas
Problemas en la identificación de -lactamasas ocurren por dos mecanismos: el primero, es que la bacteria puede llevar un promotor muy fuerte asociado con los genes productores de
-lactamasa. Este promotor puede ocasionar bajos niveles de la actividad
-lactamasa disminuyendo los valores de MCI si se compara con la actividad de cepas que solo contienen un promotor fuerte, por lo que debe tenerse cuidado para no pasarlo por alto en el antibiograma (4).
El efecto inóculo es twnbién importante. Se ha observado valores significativainente altos de MICs con inóculos de 5X107 UFC comparados con valores bajos para inóculos de 5X10 5 UFC. Como la NCCLS recomienda utilizar inóculos bajos muchas veces el nivel de bacteria podría no producir problema de resistencia por parte de las -lactamasas de espectro extendido. Por esto la cantidad de inóculo debe ser la adecuada para evitar estos errores, sobre todo con K. pneumoniae más que con E. coli (9,20).
Conclusiones
La escasa eficacia de las medidas instauradas en las últimas décadas para combatir la aparición de cepas bacterianas insensibles o poco sensibles a los antibióticos convencionales, indica que este fenómeno de la resistencia bacteriana es inevitable. Sin embargo, sí es posible modificar la velocidad con que se desarrolla la resistencia, por medio de diversas medidas como lo es el uso racional de estos medicamentos y la educación de los pacientes, dirigida a evitar la automedicación y hacia el cumplimiento exacto de los esquemas de antibioterapia ordenados por el médico.
Otra estrategia importante es la selección adecuada del régimen antibiótico, para lo cual es importante conocer la clase de flora microbiana predominante y la prevalencia de cepas resistentes a un determinado antibiótico, en la comunidad o en la institución de salud correspondiente.
"La resistencia bacteriana es un problema constante, desde los- primeros años de la era antibiótico y uno de los factores que más preocupación genera, es que cada vez es menor el intervalo entre la introducción de un nuevo antibiótico y la aparición de cepas resistentes. La presión selectiva ejercida sobre el ecosistema de las bacterias y la utilización abusiva e incontrolado de los antibióticos, permite la selección de gérmenes con mecanismos de resistencia más refinados y complejos, de manera que la aparición de "superbacterias", es una posibilidad cada vez más cercana y no es descabellado augurar un futuro sombrío, en que los antibacterianos perderán una gran parte de su utilidad actual" (13).
Ello ha promovido la investigación de novedosas alternativas para combatir las bacterias, entre ellas el uso de las moléculas naturales de defensa (cecropinas, magaminas, melitinas, etcétera), producidas por varias especies de organismos superiores, así como el diseño de péptidos canónicos sintéticos. Los primeros resultados promisorios indican que en este campo está la base para el desarrollo de los antimicrobianos del futuro.
Bibliografía
1. Aravind L.: An evolution classification of the metallo--Lactamases fold proteins. National Center for Biotechnology. National Library of Medicine. Página web, 1988 [ Links ]
2. Bishop R. & Weiner J.: Coordinate regulation of murein peptidase activity and AmpC -lactamase synthesis in E. coli. Natl. Acad. Sci. USA. 304:103, 1992. [ Links ]
3. Bush K, Jacoby G. & Medeiros A.: A funcional classification scheme for -lactamases and its corelation with molecular structure. Antimicrobial Agents and Chemotherapy. 39:1211,1995. [ Links ]
4. Bush K.: Is it important to identify extended-spectrum -lactamase-producing? Eur.J Clin. Microbiol. Inf. Dis. 15:361, 1996. [ Links ]
5. Carrasco E.: Cefalosporinas de segunda y tercera generación. Boletín de Información Farmacéutica de Navarra. 2: 1,1993. [ Links ]
6. CDC. Laboratory Capacity to detect antimicrobial resistance. CDC Publication. 48:1167, 2000. [ Links ]
7. Chartone E.: Las bacterias resistentes. Revista de divulgación y Tecnológica de la Asociación Ciencia Hoy. 9:1, 1999.
8. Fierer J. & Guiney D.: Extended -Spectrum -Lactamases "A plague of plasmids". JAMA. 281: 563, 1999. [ Links ]
9. Fuster C.: Betalactamasas. Características y papel en la resistencia a los antibióticos. Hospital del Bierzo. Página web, 1999. [ Links ]
10. García J., Cantón R. et al: Procedimientos en Microbiología Clínica. Recomendaciones de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica. Página web, 2000. [ Links ]
11. Giménez M., Matas L. et al: Antibióticos en Atención Primaria. Resistencia a los antimicrobianos relacionada con el consumo. JANO. 55: 55, 1988. [ Links ]
12. Goodman & Gilman: Las Bases Farmacológicas de la Terapéutica. En: Agentes antimicrobianos. 1035-1064. Editorial Médica Panamericana. México, 1991. [ Links ]
13. Jacques F.: Consequences of Bacterial Resistance to Antibiotics in Medical Practice. Clin. Infect. Dis. 24 Sup 1, S 17-S 1 8, 1997.
14. Kobayashi & Takahashi.: Diffusion of -lactam antibiotics through liposome membranas containing purified porins. Antimicrob. Agents Chemother. 22:775, 1982. [ Links ]
15. Levin B., Lipsitch Y et al: The population Genetics ofantibiotic Resistance. Clin. Infect Dis. 24 Sup 1, S9-S 16, 1977. [ Links ]
16. Malouin F. & Bryan L.: Modification of penicillin-binding proteins as mechanisms of -lactam resistance. Antimicrob. Agents Chemother. 30: 1, 1986. [ Links ]
17. Medeiros A.: Evolution and dissemination of -Lactamases by generations of
-Lactam. Antibiotics. Clin. Infect. Dis. 24. (24) Sup 1, S 19- S 45, 1997. [ Links ]
18. Mulgrave L.: Extended Spectrum -Lactamase Detection in the Clinical Laboratory: A Mini-Review. Australian Society for Antimicrobials newsletter 200: 35, 1999. [ Links ]
19. Nagel R.: La resistencia de las bacterias a los antibióticos ¿Un camino sin retomo?. Revista de divulgación y Tecnológica de la Asociación Ciencia Hoy. 10:59, 2000.
20. National Committee for Clinical Laboratory Standards. Performance standards for animicrobial susceptibility testing: Laboratory detection of oxacillin-resistant coagulasenegative Staphylococcus spp, Laboratory detection of extended- spectrum B-lactamases (ESBLs), Laboratory detection of Imipemen or Meropenem Resistance in gram-negative organisms, Laboratory detection of oxacillin/methicillin-resistant Staphylococcus aureus (MRSA).NCCLS approved estandar M100-S9. National Committee for Clinical Laboratory Standardes, Wayne, PA. Páginas web, 1999.
21. Pérez J. & Gimeno C.: B -lactamasas plasmídicas de espectro ampliado: Experiencia del programa de control de calidad, dos años después. Página web, 1999. [ Links ]
22. Piroth L., Aubé H. et al: Spread of Extended-Spectrum -lactamase-Producing Klebsiella pneumoniae: Are
-Lactamase Inhibitors of Therapeutic value?. Clin. Infect. Dis. 27 Sup 1, S76-S80, 1998.
23. Sanders P.: Tratamientos terapéuticos y antibiorresistencia. Le point veterinaria. 30: 203, 1999. [ Links ]
24. Schentag J., Strenkoski L. et al: Pharmacodynarnic Interactions of Antibiotics Alone and in combination. Clin. Infect. Dis. 27 Sup 1, S17-S18, 1998. [ Links ]
25. Spratt B.: Distinct penicillin binding proteins involved in the division, elongation and shape of E. coli K 12. Proc. Natl. Acod. Sci. USA. 72:2999, 1975. [ Links ]
26. Tabau F., Palláres R. et al: Detección de la resistencia en Streptococcus pneumoniae y consideraciones sobre el tratamiento de la infección respiratoria por neumococos resistentes. Control de calidad SEIMC. Página web, 2000. [ Links ]
27. Trehan l.: Inhibition of AmpC beta-Lactamase through a Destabilizing Interaction in the Active Site. Biochemistry. 40:7992, 2001.
28. Turnidge J.: The pharmacodynamics of -Lactams. Clin. Infect. Dis. 27:10, 1998. [ Links ]
29. Washinton J.: Functions and activities of the area committee on microbiology of the National Committee for Clinical Laboratory Standards. Clin. Microbiol. Rev. 4: 150, 1994. [ Links ]
30. Wiener J.,Quirm J. et al: Multiple Antibiotic-Resistant Kiebsiella and Escherichia coli in Nursing Homes. JAMA 281: 517, 1999. [ Links ]
31. Zhang H.: Determinan cómo se produce la resistencia a betalactámicos. Diario Médico. Página web, 2001.
* Laboratorio de Tamizaje Neonatal.
** División de Microbiología
Hospital Nacional de Niños "Dr. Carlos Sáenz Herrera" Caja Costarricense de Seguro Social, San José, Costa Rica - Correo Electrónico: mherrera@hnn.sa.cr