Introducción
La pimienta es una planta perenne de los trópicos, originaria de la Costa de Malabar, situada en Kerala al sur de la India. Pertenece a la familia Piperaceae y al género Piper, el cual abarca más de 100 especies distintas, sin embargo, la variedad económicamente más importante es la pimienta negra (Piper nigrum L.) (Maistre, 1969, Ahmad et al., 2012, Da Luz et al., 2017).
Los principales países productores son Brasil, India, Indonesia, Malasia y Sri Lanka (Andújar y Moya 2009). En Costa Rica, las principales plantaciones de pimienta se localizan desde Upala hasta Talamanca, además en toda la franja costera y la parte baja de Sarapiquí (Araya 2014).
En el 2014, según el VI Censo Nacional Agropecuario, se estimaron un total de 316 fincas productoras de pimienta con una extensión total de 665,8 hectáreas, de las cuales el 93,3% se ubica en la provincia de Heredia y Alajuela. Otra característica importante de la producción de pimienta, en este país, es su potencial para la exportación, ya que según un estudio de factibilidad realizado en 2013 destaca que la pimienta producida en Costa Rica presenta altos niveles de piperina, que pueden llegar a superar el 7%, mientras que en otros países solamente alcanzan como máximo el 5% (Monge et al., 2013).
La piperina es responsable del sabor picante de la pimienta utilizada como condimento. También posee propiedades analgésicas y antinflamatorias, las cuales son utilizadas como ingrediente activo de medicamentos orales por su fácil absorción, incluso por sus propiedades antioxidantes, se utiliza como anticancerígeno. También es un compuesto importante para la formulación de repelentes, ovicidas, insecticidas para algunas moscas, escarabajos, gorgojos y larvas (Ravindran 2005).
A pesar de lo anterior, la producción nacional solo es capaz de abastecer el 30% de la demanda del grano para la exportación. Las enfermedades vasculares representan una seria limitante para el cultivo de pimienta, ya que reducen los rendimientos e incluso pueden ocasionar la pérdida total de las plantaciones. En Brasil, por ejemplo, enfermedades producidas por Fusarium redujeron en un 32,4% la producción entre el 2006 y 2016 (Da Costa et al. 2019).
En los países productores de pimienta como India, Malasia, Indonesia, Brasil y Tailandia, se reporta que uno de los problemas más importantes en las plantaciones de la pimienta negra es la enfermedad del amarillamiento, también conocida como muerte lenta. En 1988 se identificó como agente causal de esta enfermedad a Fusarium solani f. sp. piperis (teleomorfo: Nectria haematococca f. sp. piperis) (Salgado et al. 2016, Shahnazi et al. 2014).
A nivel nacional, Céspedes (1988) y Villalobos et al. (2009) indican la presencia de la especie F. oxysporum ha causado marchitez y F. solani ha afectado el sistema radical, aunque no se indica cuáles fueron las bases que se utilizaron para realizar la identificación de estas especies.
La identificación de las especies de Fusarium, desde el punto de vista taxonómico tradicional, se basa en estudios de la morfología de las estructuras reproductivas asexuales del hongo; los macroconidios, los microconidios, las clamidosporas y la célula conidiógena (Šišić et al. 2018).
Sin embargo, varios autores coinciden en que la identificación morfológica es compleja, ya que muchas especies no presentan diferencias morfológicas entre sí. La identificación molecular, mediante la extracción de ADN y la secuenciación de genes informativos, permite separar estas especies (Summerell 2019). Por ejemplo, el gen EF-1α (Factor de Elongación 1α) se utiliza para este fin, porque tiende a evolucionar a nivel de esta especie a una velocidad superior en comparación con otros genes de uso común (Choi et al. 2018).
Además, según Geiser et al. (2004), O΄Donnell et al. (2008) e Ismail et al. (2015) el gen EF-1α en el genoma de Fusarium está presente en una única copia, no se han detectado copias ortólogas, posee una riqueza de regiones intrónicas y un alto nivel de polimorfismo entre las especies estrechamente cercanas. Por estas razones, esta región genómica tiene una alta utilidad filogenética (Choi et al. 2018).
Realizar estudios que combinen las técnicas morfológicas y moleculares enfocados a la caracterización a nivel de especie tienen gran importancia, ya que permiten generar información más robusta de las características de los patógenos. Esto permite determinar un problema fitosanitario, a lo largo del tiempo y en diferentes regiones a nivel mundial.
Mediante esta investigación, se logró determinar el impacto causado por Fusarium spp. en las plantaciones muestreadas y el escaso conocimiento que existe de este cultivo en Costa Rica. La producción de pimienta (Piper nigrum) es una actividad económica realizada por pequeñas personas productoras, las cuales no cuentan con información técnica actualizada (Monge et al. 2013). Por estas razones, el objetivo de esta investigación fue el aislamiento, la identificación morfológica y molecular de las especies de Fusarium asociadas al cultivo de la pimienta (Piper nigrum L.) en 2 de las principales zonas productoras del país.
Recolección de las muestras
La recolección de muestras se realizó en 14 fincas localizadas en Sarapiquí y Guatuso. En cada finca se observaron los diferentes síntomas asociados con Fusarium spp; el material vegetal fue llevado al Laboratorio de Fitopatología del Centro de Investigación en Protección de Cultivos (CIPROC) de la Universidad de Costa Rica.
Descripción de los síntomas
En el laboratorio se realizó una descripción detallada de los síntomas generales e internos de los tejidos afectados, el sistema radical y/o la base del tallo, esto para cada una de las plantas recolectadas.
Se analizaron 30 muestras de plantas enfermas de las distintas fincas; los códigos utilizados para la identificación se conformaron por las iniciales de la zona de procedencia de la planta (PV o PSC) y el número de planta de la cual se obtuvo el tejido enfermo. Sin embargo, en las muestras 19, 22, 26 y 28 en una misma planta se observaron 2 síntomas distintos. Para calificarlos se agregó al código de identificación las iniciales de cada síntoma; RA: Rama aérea, R: Raíz, T: Tallo, RH: Raíz hilachada, HV: Haces vasculares, RL: Raíz larga y RI: Raíz interna. Por lo tanto, se trabajó con un total de 34 muestras sintomáticas.
Aislamientos de Fusarium spp
A partir del material vegetal, extraído de cada uno de los síntomas, se realizaron los aislamientos. La desinfección del material se realizó con hipoclorito de sodio al 1% y alcohol al 70% durante un minuto. Posteriormente, se realizaron 3 lavados con agua destilada.
De cada muestra, se colocaron en un plato Petri con medio de cultivo papa dextrosa agar (PDA) 5 fragmentos provenientes de la zona de avance. Se incubaron en una cámara a temperatura ambiente (23 a 26°C) en condiciones de oscuridad durante 15 días.
A partir de los 170 fragmentos procesados, se tuvieron 105 crecimientos de micelio relacionado a Fusarium spp. Finalmente, se seleccionaron las colonias según los distintos colores observados en el plato petri de cada muestra. De esta selección, se obtuvieron 21 aislamientos de Fusarium spp.
En los restantes 65 fragmentos, 4 correspondieron a Phytophthora spp. (muestra PV 3), en 10 se aisló Trichoderma spp. en las muestras PV 6 y PV 9, en 5 solamente hubo crecimiento bacteriano (PV 13), 10 fragmentos tuvieron crecimiento de Lasidiplodia spp, (muestras PV 21 y PV 27) y en los restantes 35 fragmentos correspondiente a las muestras PV 4, PV 7, PV 14, PV 15, PV 16, PSC 20 y PV 29, no hubo crecimiento de ningún organismo asociado al síntoma analizado.
Caracterización molecular
Extracción de ADN
La extracción de ADN se realizó a partir de micelio puro según la metodología de Trout et al. (1997).
A una pequeña porción de micelio se le agregó 150 µL del buffer de extracción y posteriormente se maceró fuertemente. Luego, se agregó 150 µL del buffer de lisis CTAB (Hexadecyltrimethyl ammonium bromide) y se agitó por 15 segundos en vortex. La mezcla se incubó por 60 minutos a 65ºC. Luego en cámara de gases se agregó 300 µL de cloroformo isoamyl alcohol (24:1) a cada muestra; se mezcló manual y suavemente (50 veces) y se centrifugó a 14 000 rpm durante 15 minutos. Seguidamente, se extrajo el supernadante (fase líquida de la suspensión) a un nuevo tubo Eppendorf de 1,5 mL.
Al nuevo tubo se le agregó 300 µL de choroformo isoamyl alcohol que se volvió a mezclar manual y suavemente, 50 veces y se centrifugó a 14 000 rpm durante 10 minutos. Posteriormente, se extrajo el supernadante a un nuevo tubo Eppendorf de 1,5 mL, se agregó 20 µL de acetato de sodio 3M y 300 µL de etanol puro de 95% frío, se mezcló de forma manual y se almacenó por 24 horas a -20ºC.
Las muestras se centrifugaron a 14 000 rpm durante 20 minutos, luego se eliminó el acetato y el etanol, se limpió el pellet de ADN con 150 µL de etanol al 70% frío. A continuación, se centrifugó a 12 000 rpm por 10 minutos, se decantó cuidadosamente el etanol, se dejó boca abajo cada eppendorf sobre una toalla estéril para eliminar el exceso de etanol y se dejó secar por 30 minutos. Para almacenarlo se disolvió el pellet en 50 µL de buffer TE y se almacenó a -20ºC.
Se determinó con un espectrofotómetro Eppendorf BioPhotometer Plus, la concentración y pureza del ADN extraído de cada muestra.
Amplificación por medio de PCR
Para la amplificación (PCR) de la región parcial del gen que codifican para el Factor de Elongación 1α (EF-1α), se utilizaron los siguientes cebadores específicos: EF1 (5'ATGGGTAAGGA(A/G)GACAAGAC3') y EF2 (5'GGA(G/A)GTACCAGT(G/C)ATCAT TT3') (Karlsson et al. 2015).
El perfil término utilizado consistió en 3 fases: una desnaturalización inicial a 96ºC durante 2 minutos, seguido por 35 ciclos de desnaturalización a 96ºC durante 1 minuto con una temperatura de anillamiento de 50°C, finalmente una extensión a 72ºC por 1 minuto, seguidos de una extensión final, también a 72ºC durante 10 minutos (Abd-Elsalm et al. 2003).
Los productos del PCR se visualizaron mediante electroforesis, se utilizó un gel de agarosa (0,8%), el buffer de corrida TBE (1X), un marcador de peso molecular de 100 bp y un control negativo (sin ADN). El fragmento a amplificar tuvo un tamaño de 700 pb.
Secuenciación
El producto de PCR se purificó mediante la endonucleasa Exonuclease I (Fermentas), se llevó a una concentración de 50 ng.μL-1 y, posteriormente, se envió a secuenciar a la empresa Macrogen Inc, en Corea del Sur.
Se obtuvieron secuencias en ambas direcciones para cada muestra generadas a partir de ciclos fluorescentes utilizando un secuenciador modelo 3730XL (Applied Biosystems).
Alineamiento de las secuencias
La calidad de las secuencias se confirmó con un alineamiento bidireccional y por comparación con los cromatogramas con el programa BioEdit, además, se cortaron las terminaciones 5’ y 3’ de las cadenas para facilitar el alineamiento. Se utilizó la herramienta informática BLAST (Basic Local Alignment Search Tool del National Center for Biotechnology Information (NCBI), por sus siglas en inglés) a partir de la cual se comparó la secuencia generada frente a las secuencias que se encuentran en la base de datos GenBank.
Caracterización morfológica
Las características morfológicas macroscópicas, como el color y la textura de las colonias, así como las características microscópicas de los microconidios (la forma, el número de septos y la abundancia), se determinaron a partir del crecimiento de los aislamientos en medio de cultivo PDA incubados en una cámara a temperatura ambiente y en condiciones de oscuridad durante 15 días.
A partir del crecimiento en el medio de cultivo Carnation Leaf-piece Agar (CLA), se determinó la presencia, la forma, la posición y la abundancia de las clamidosporas; la forma de la célula apical y la célula basal; la forma, la abundancia y el número de septos de los macroconidios, así como el tipo de células conidiógenas,
Para identificar y describir estas estructuras se utilizó un microscopio óptico y las claves taxonómicas de Booth (1971) y Leslie y Summerell (2006).
Resultados
Caracterización de los síntomas observados a nivel de campo
Los síntomas generales observados en las plantaciones muestreadas fueron una clorosis generalizada de las plantas, en algunos casos también se observó necrosis del follaje en la parte superior (Figura 1).

Figura 1 Síntomas en plantas enfermas de pimienta negra A) Clorosis generalizada en toda la planta y B) Necrosis parcial del follaje.
En la parte interna del tallo, se observaron 2 síntomas diferentes: el primero, consistió en áreas necróticas de color café o negro limitadas al sistema vascular (Figura 2A) y, el segundo, una necrosis general de la base del tallo y la raíz, en ambos casos las plantas enfermas no producen olores desagradables. A nivel de la base de la planta se da una descomposición del tejido con un aspecto “deshilachado” (Figura 2B).
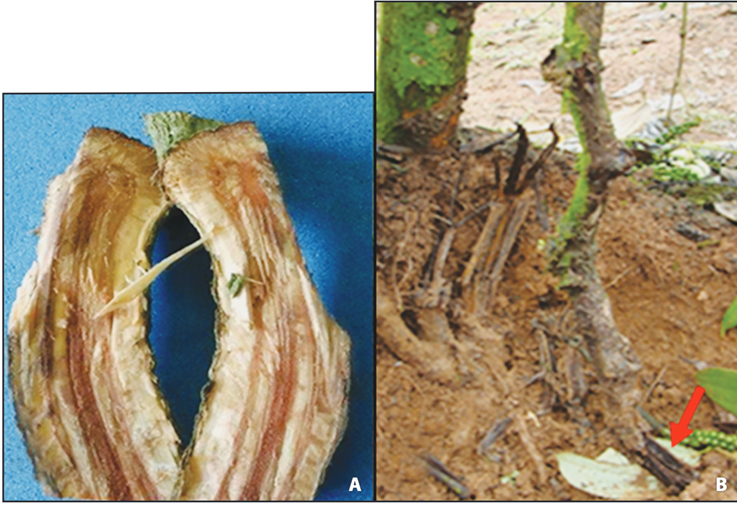
Figura 2 Síntomas en plantas enfermas de pimienta negra A) Lesiones necróticas de color café o negro limitadas al sistema vascular y B) “Deshilachamiento” necrótico en la raíz.
Los síntomas asociados a Fusarium oxysporum fueron lesiones internas, que no tienden a estar limitadas alrededor de los haces vasculares. Se observa en la Figura 3, que la necrosis del tejido avanza progresivamente en todo el tallo, lo que causa una afectación completa del tejido vascular.

Figura 3 Daño vascular a nivel del tallo observada en plantas enfermas de pimienta negra asociadas a Fusarium oxysporum.
En el caso de las muestras con síntomas asociados a F. solani (Figura 4A) provenientes de Sarapiquí, se observaron lesiones internas restringidas al sistema vascular (Figura 4B). En las muestras de Guatuso, además, del síntoma anterior se observó una necrosis generalizada en el tejido vascular (Figura 5).

Figura 4 Sintomatología asociada a Fusarium solani observada en muestras de plantas enfermas de pimienta negra de Sarapiquí A) Clorosis aleatoria del follaje y B) Daño vascular localizado a nivel de tallo.

Figura 5 Sintomatología asociada a Fusarium solani en muestras de plantas enfermas de pimienta negra de Guatuso A) Clorosis aleatoria del follaje y B) Necrosis generalizada en el tallo.
Los síntomas asociados a Fusarium concentricum (Figura 6) fueron lesiones necróticas internas localizadas en los haces vasculares, pero no se observó un "deshilachamiento" necrótico en la raíz o en la base de la planta. El follaje presentó una necrosis sin ninguna distribución clara y un leve amarillamiento de las hojas.

Figura 6 Sintomatología asociada a Fusarium concentricum en plantas enfermas de pimienta negra A) Síntomas a nivel de follaje y B) Daño vascular del sistema radical.
Los síntomas asociados a Fusarium proliferatum están relacionados a un amarillamiento generalizado de la parte área. En la raíz y la base del tallo se observó un deshilachamiento necrótico del tejido e internamente, en la zona de avance, una necrosis de color café claro generalizada que abarca todo el tejido (Figura 7), además, es importante destacar que no se percibió mal olor.

Figura 7 Sintomatología asociada Fusarium proliferatum en plantas enfermas de pimienta negra A) Crecimiento vegetativo reducido y clorosis del follaje, B) “Deshilachamiento” necrótico en la base del tallo, C) Daño vascular interno a nivel de tallo y D) “Deshilachamiento” necrótico en la raíz principal.
A partir de este estudio, se analizaron 30 plantas enfermas y 34 síntomas asociados a Fusarium spp. localizadas en provenientes de Sarapiquí y Guatuso. A partir de 170 fragmentos de la zona de avance, se tuvieron 105 crecimientos de micelio relacionado a Fusarium. Finalmente, para cada muestra se seleccionaron los aislamientos tomando en cuenta los distintos colores presentes. De esta selección se obtuvieron los 21 aislamientos de Fusarium spp (Tabla 1).
Tabla 1 Código de identificación, procedencia, coordenadas geográficas y área afectada de las plantas de pimenta negra (Piper nigrum) muestreadas.
| Código de identificación | Procedencia | Coordenadas geográficas | Área afectada |
| PV 1 | La Virgen de Sarapiquí | N 10.47268º W 084.10876º | Base del tallo |
| PV 2 | La Virgen de Sarapiquí | N 10.47268º W 084.10876º | Base del tallo |
| PV 3 | La Virgen de Sarapiquí | N 10.54769º W 084.12753º | Base del tallo |
| PV 4 | La Virgen de Sarapiquí | N 10.54769º W 084.12753º | Base del tallo |
| PV 5 | La Virgen de Sarapiquí | N 10.55591º W 084.15514º | Base del tallo |
| PV 6 | La Virgen de Sarapiquí | N 10.46852º W 084.21631º | Raíz |
| PV 7 | La Virgen de Sarapiquí | N 10.46937º W 084.21589º | Base del tallo |
| PV 8 | La Virgen de Sarapiquí | N 10.46450º W 084.20999º | Base del tallo |
| PV 9 | La Virgen de Sarapiquí | N 10.46450º W 084.20999º | Raíz |
| PV 10 | La Virgen de Sarapiquí | N 10.39518º W 083.9607º | Raíz |
| PV 11 | La Virgen de Sarapiquí | N 10.39518º W 083.9607º | Base del tallo |
| PV 12 | La Virgen de Sarapiquí | N 10.40121º W 084.16311º | Base del tallo |
| PV 13 | La Virgen de Sarapiquí | N 10.40121º W 084.16311º | Raíz |
| PV 14 | La Virgen de Sarapiquí | N 10.40237º W 084.15678 º | Base del tallo |
| PV 15 | La Virgen de Sarapiquí | N 10.39996º W 084.15465º | Raíz |
| PV 16 | La Virgen de Sarapiquí | N 10.39996º W 084.15465º | Base del tallo |
| PVS 17 | La Virgen de Sarapiquí | N 10.39996º W 084.15465º | Base del tallo |
| PV 18 | La Virgen de Sarapiquí | N 10.39996º W 084.15465º | Base del tallo |
| PSC 19 RA | Guatuso de San Carlos | N 09.53339º W 083.52349º | Parte aérea |
| PSC 19 R | Guatuso de San Carlos | N 09.53339º W 083.52349º | Raíz |
| PSC 20 | Guatuso de San Carlos | N 10.4942.2º W 0850030.3º | Raíz |
| PSC 21 | Guatuso de San Carlos | N 10.4942.2º W 0850030.3º | Base del tallo |
| PSC 22 T | Guatuso de San Carlos | N 10.4942.2º W085.0030.3º | Tallo |
| PSC 22 R | Guatuso de San Carlos | N 10.4942.2º W085.0030.3º | Raíz |
| PSC 23 | Guatuso de San Carlos | N 10.4608º W 084.54144 º | Raíz |
| PSC 24 | Guatuso de San Carlos | N 10.46089º W 084.54144 º | Base del tallo |
| PSC 25 | Guatuso de San Carlos | N 10.46089º W 084.54144 º | Base del tallo |
| PSC 26 RH | Guatuso de San Carlos | N 10.46089º W 084.54144 º | Raíz |
| PSC 26 RI | Guatuso de San Carlos | N 10.46089º W 084.54144º | Raíz |
| PSC 27 | Guatuso de San Carlos | N 10.46089º W 084.54144º | Tallo |
| PV 28 H | La Virgen de Sarapiquí | N 10.54769º W 084.12753º | Base del tallo |
| PV 28 RL | La Virgen de Sarapiquí | N 10.54769º W 084.12753º | Raíz |
| PV 29 | La Virgen de Sarapiquí | N 10.46873º W 084.21891º | Base del tallo |
| PV 30 | La Virgen de Sarapiquí | N 10.46852º W 084.21631º | Base del tallo |
Identificación molecular
Mediante la amplificación del ADN de un fragmento del gen del Factor de Elongación 1α (EF-1α) y la comparación entre las secuencias obtenidas para los veintiún aislamientos con las secuencias almacenadas en la base de datos GenBank, procesados con la herramienta informática BLAST, que posibilitó determinar la presencia de 4 especies de Fusarium presentes en las plantaciones de pimienta negra de Costa Rica.
Las secuencias de Fusarium oxysporum del aislamiento PV 1 tuvo un 99% de similitud con la accesión MK172058.1 (Taylor et al. 2019), las secuencias de los aislamientos PV 5 y PV 10 fueron en un 100% y 99% similares, respectivamente, a la accesión MG018805.1 (Maldonado-Bonilla et al. 2019) y la secuencia de los aislamientos PSC 26 RH tuvo un porcentaje de 99% similitud con la accesión MG018803.1 (Maldonado-Bonilla et al. 2019).
Los aislamientos identificados como Fusarium solani PV 2, PV 11, PSC 24 y PSC 25 presentaron un porcentaje de similitud de 99%, 99%, 98% y 98%, respectivamente, con la accesión KF255995 (Wang et al. 2014) las secuencias de los aislamientos PV 12, PV 17, PSC 19 R, PV 23 y PSC 26 RI tuvieron un porcentaje de similitud que osciló entre 98 y 100% con la accesión HQ731056 (Jiménez-Fernández et al. 2011).
Los aislamientos de Fusarium proliferatum PSC 19 RA y PSC 22 R fueron similares en un 99% y 100%, respectivamente, a la accesión JX869017.1 (Hawa et al. 2013). Los aislamientos identificados como Fusarium concentricum (PV 8, PSC 28 HV, PSC 28 RL y PV 30 fueron 99% similares a la accesión JF740760.1 (O΄Donnell et al. 2012).
Identificación morfológica
Las 4 especies de Fusarium spp., identificadas a partir de los 21 aislamientos, fueron Fusarium oxysporum, Fusarium solani, Fusarium concentricum y Fusarium, proliferatum, las características morfológicas de cada especie se describen en la Tabla 2, Tabla 2.1, Tabla 2.2 y las Figuras 8, 9, 10 y 11.
Tabla 2 Características morfológicas de los macroconidios, los micronidios, las células conidiógenas, las clamidosporas y la coloración de la colonia de las cuatro especies de Fusarium asociadas a plantas enfermas de pimienta negra, según las claves taxonómicas de Booth (1971) y Leslie y Summerell (2006).
| Especie | Macroconidios | - | - | - | - |
|---|---|---|---|---|---|
| - | Forma | Célula apical | Célula basal | Número de septos | Abundancia |
| Fusarium oxysporum | PV 1, PV 5, PV 26 RH: Semicurvos. PV 10: casi rectos (Figura 8C) | Forma redondeada, ligeramente encorvada (Figura 8C) | Forma de pie (Figura 8C) | Septados con 3 a 5 septos, pero predominaron con 3 septos | Abundantes |
| Fusarium solani | Rectos y robustos. PV 2 y PV 12: ligeramente curvos (Figura 9C) | PV 2, PV 12: Aguda. PV 11, PV 17 y PV 18: Ligeramente encorvada (Figura 9C) | Forma de pie (Figura 9C) | Septados con 3 a 7 septos | PV 2, PV 12 y PV 18: Abundantes. PV 11 y PV 17: Escasos |
| Fusarium concentricum | PSC 28 RL y PV 30: Casi rectos PV 8 y PV 28 HV: curvos (Figura 10C) | Forma de pico ligeramente encorvada (Figura 10C) | Forma de pie (Figura 10C) | Septados con 3 a 5 septos | PSC 28 RL y PV 30: Abundantes PV 8 y PSC 28 HV: Escasos |
| Fusarium proliferatum | Delgados, casi rectos a ligeramente curvos (Figura 11B) | Curvada (Figura 11B) | Ligeramente redonda (Figura 11B) | Septados con 3 a 5 septos | Abundantes |
| Especie | - | Microconidios | - | Célula conidiógena | - |
| - | Forma | Número de septos | Abundancia | - | - |
| Fusarium oxysporum | Ovalados | Sin septos | Abundantes | PV 10 y PV 5: Monofiálides cortas y simples (Figura 8B) PV 1: Esporodoquios ramificados (Figura 8D) | - |
| Fusarium solani | Ovalados, algunos ovoides truncados (Figura 9B) | Sin septos | Abundantes en todos los aislamientos PV 12: Escasos | Predominaron monofiálides simples y cortas (Figura 9B) PV 17 y PV 18: Esporodoquios cortos | - |
| Fusarium concentricum | Ovalados (Figura 10B) | Sin septos | Abundantes | PV28 RL y PV 28 HV: Monofiálides simples y cortas (Figura 10E) PV 8 y PV 30: Esporodoquios ramificados y simples (Figura 10D) | - |
| Fusarium proliferatum | Piriformes (Figura 11E) | Sin septos o con un sólo septo | Escasos | Polifiálides y monofiálidas, con menor frecuencia en falsas cabezas (Figura 11C y Figura 11D) | - |
| Especie | - | Clamidosporas | - | Coloración de la colonia | - |
| - | Posición | Forma | Abundancia | - | - |
| Fusarium oxysporum | PV 1 y PV 5: Terminales PV 10: Intercalares (Figura 8D) | Esférica de paredes lisas | Abundantes | Micelio aéreo: Blanco (Figura 8A) | - |
| Fusarium solani | PV 12: Intercalares PV 17: Terminales | Esférica de paredes rugosas | Sólo los aislamientos PV 12 y PV 17 (Figura 9E) | Micelio aéreo: PV 2, PV 8, PV 11, PSC 24 y PSC 25 T: Tonalidades beige a café PV 12 y PSC 26 RI: Rojo. PV 17 y PV18: Blanco (Figura 9A) | - |
| Fusarium concentricum | - | Ningún aislamiento produjo clamidosporas | - | - | Micelio aéreo blanco posteriormente se torna gris-violeta (Figura 10A) |
| Fusarium proliferatum | - | Ningún aislamiento produjo clamidosporas | - | - | Micelio aéreo blanco con leves tonalidades rosadas (Figura 11A) |
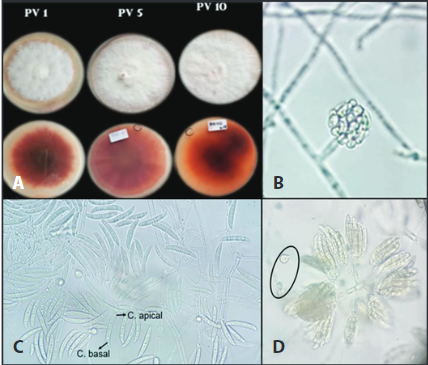
Figura 8 Características morfológicas de los aislamientos Fusarium oxysporum A) Color de la colonia en PDA, B) Monofiálide corta, C) Macroconidios, C. apical; célula apical, C. basal; célula basal. D) Esporodoquio ramificado y clamidosporas terminales en medio de cultivo CLA. (40X).
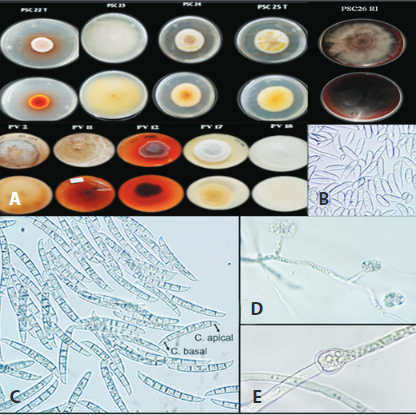
Figura 9 Características morfológicas de los aislamientos de Fusarium solani A) Color de la colonia en PDA B) Microconidios, C) Macroconidios C. apical; célula apical, C. basal; célula basal, D) Monofiálides cortas y E) Clamidospora intercalar en medio de cultivo CLA (40X).
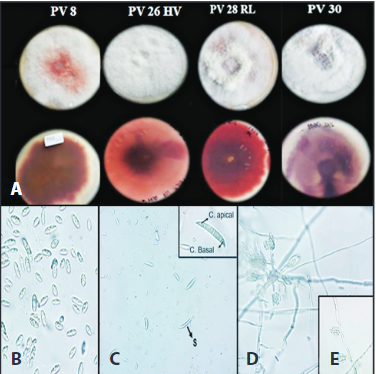
Figura 10 Características morfológicas de los aislamientos de Fusarium concentricum A) Color de la colonia en PDA B) Microconidios en el micelio aéreo (en PDA) C) Macroconidios, C. apical; célula apical, C. basal; célula basal, D) Esporodoquio ramificado y E) Conidióforos simples y cortos en medio de cultivo CLA (40X).
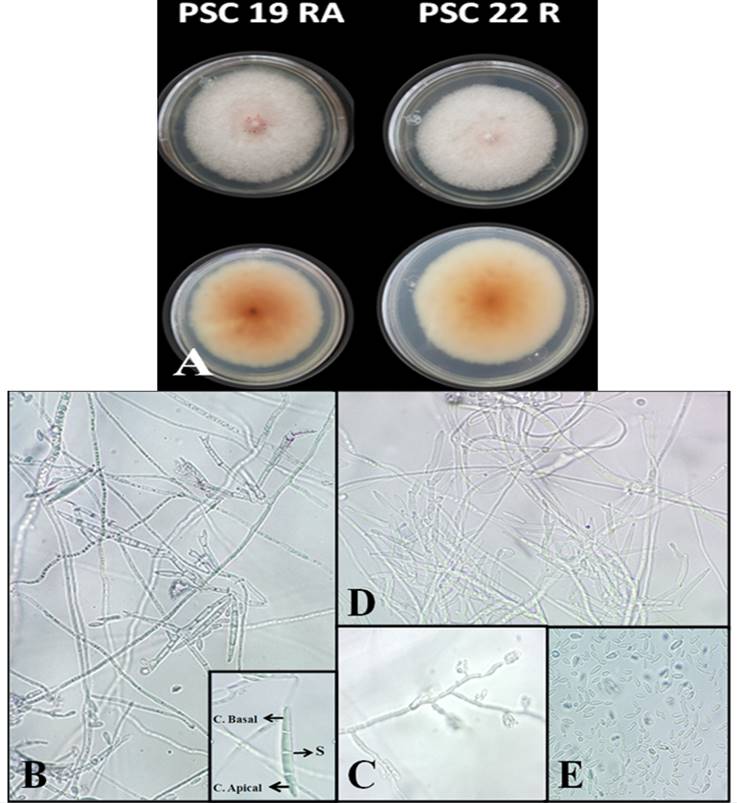
Figura 11 Características morfológicas de los aislamientos de Fusarium proliferatum A) Color de la colonia (PDA), B) Macroconidios, C. apical; célula apical, C. basal; célula basal, S: septos, C) Conidióforos simples y cortos D) Conidióforos en falsas cabezas y E) Microconidios en el micelio aéreo en medio de cultivo CLA (40X).
Discusión
El género Fusarium comprende especies endófitas, saprófitas y patógenas de plantas, humanas y animales (Leslie y Summerell 2006, Chandra et al. 2011). Para definir una especie existen varias clasificaciones, unas basadas en la morfología (especies morfológicas), otras en experimentos cruzados (especies biológicas), y también en marcadores moleculares (especies filogenéticas) (Chandra et al. 2011) y según la especificidad del huésped (Coleman 2016).
En la práctica, es difícil distinguir las especies de Fusarium que se encuentran dentro de los complejos de especies, porque están estrechamente relacionadas y tienden a tener ninguna o pocas diferencias morfológicas entre sí. Para estos casos la identificación molecular permite distinguir con mayor precisión estas especies (Chandra et al. 2011).
La identificación molecular se basa en la extracción de ADN y la secuenciación de genes informativos que permiten separar las especies (Summerell 2019). Las secuencias más comúnmente utilizadas para distinguir especies de Fusarium son porciones de las secuencias genómicas que codifican el factor de elongación1-α (EF-1α), β-tubulina (tub2), calmodulina, regiones espaciadoras transcritas internamente en la región de repetición ribosómica (ITS1 e ITS2) y la región espaciadora intergénica (IGS) (Chandra et al. 2011).
En esta investigación, se utilizó el gen EF-1α, el cual es el más aceptado porque tiende a evolucionar a nivel de esta especie a una velocidad superior en comparación con otros genes de uso común (Choi et al. 2018). Además, otros marcadores tienen algunas limitantes, por ejemplo, las regiones ITS no funcionan bien dentro de la sección Liseola y ß-tub2 no funciona bien dentro del complejo de especies Fusarium solani (Chandra et al. 2011).
Respecto a la identificación molecular y el análisis morfológico, se confirmó la presencia de la especie Fusarium oxysporum en los aislamientos provenientes de plantas enfermas de pimienta negra en las 2 localidades muestreadas.
Al observar los síntomas asociados a esta especie en las plantas de pimienta negra analizadas (Figura 3), se identificó que no concuerdan precisamente con lo descrito por Duarte et al. 2001 y Sarma et al. 2013, quienes indican que este patógeno invade las raíces de las plantas de pimienta a través de heridas o durante la aparición de nuevas raíces. Posteriormente, se da la colonización y la necrosis de los haces vasculares, que evitan así, la absorción de agua y nutrientes. Externamente, las plantas enfermas muestran coloración amarillenta cuando se infectan varias raíces, la planta se colapsa y el follaje se mantiene adherido a las ramas.
Según Rana et al. (2017) y Dean et al. (2014), Fusarium oxysporum es el hongo más abundante y ubicuo del suelo; se han encontrado en diversos ecosistemas, incluidos pastizales, bosques, desiertos, que van desde los trópicos hasta el Ártico. Aunque son comúnmente conocidos como fitopatógenos, también pueden sobrevivir como saprófitos, como colonizadores endófitos de plantas asintomáticas (se han encontrado Fusarium oxysporum endófito en casi 100 especies de plantas), incluso como inductores de resistencia. Según estas personas autoras la mayoría de los aislamientos Fusarium oxysporum se presume que no son patógenos.
Aunado a lo anterior, la capacidad de degradar la lignina y los hidratos de carbono complejos, asociados con los desechos del suelo, que poseen las especies saprofíticas de Fusarium oxysporum (Rana et al. 2017 y Dean et al. 2014), podrían explicar los síntomas asociados a F. oxysporum observados en las muestras analizadas (Figura 3).
Además, dada la baja frecuencia de aparición de esta especie en este estudio (4 muestras de un total de 34), podría sugerir que los aislamientos obtenidos F. oxysporum corresponden a saprófitos. Otro dato para tomar en cuenta, es que hasta el momento no se ha reportado una forma especial para pimienta negra dentro del complejo Fusarium oxysporum (FOSC).
En esta investigación también se confirmó la presencia de la especie F. solani en las 2 localidades muestreadas. Además, fue la especie que se presentó en mayor frecuencia. Este resultado coincide con los múltiples reportes nacionales e internacionales que la señalan como uno de los patógenos más importante en el cultivo de la pimienta, específicamente, en la forma especial piperis (Sitepu y Mustika 2006, Andújar y Moya 2009, Villalobos et al. 2009, Shahnazi et al. 2012, Vaz et al. 2012, Sarma et al. 2013, Shahnazi et al. 2014 y Salgado et al. (2016).
Fusarium solani f. sp. piperis (teleomorfo: Nectria haematococca f. sp. piperis) causa graves pérdidas en la mayoría de los países productores de pimienta negra, incluidos India, Malasia, Indonesia, Brasil y Tailandia. Se informa que la infección por Fusarium en una plantación de pimienta negra reduce la vida económica de la plantación de 20 años a 6 -8 años (Shahnazi et al. 2012).
Los daños asociados a Fusarium solani observados en las fincas muestreadas fueron 2; lesiones del sistema vascular y el daño necrótico de la base del tallo y la raíz (Figuras 4 y 5). Estos resultados concuerdan con las investigaciones realizadas en Brasil, que describen 2 enfermedades causadas por Fusarium solani; la primera de ellas se conoce como como fusariosis y corresponde a la infección de las raíces de la pimienta negra (Piper nigrum L.) y la segunda es un daño conocido como tizón del tallo, que como su nombre lo sugiere, es una enfermedad que afecta los tallos (Da Costa 2019).
La tercera especie presente en cultivo de pimienta, en Costa Rica, es la especie F. concentricum; la misma no ha sido reportada en el cultivo de pimienta negra hasta el momento, por lo que este es el primer reporte de esta especie asociada al daño vascular y a la posterior muerte de las plantas de pimienta negra.
Esta especie fue descrita por primera vez por Nirenberg y O'Donnell en 1998, a partir de aislamientos provenientes de Musa sapientum (ex T) de Costa Rica y Guatemala. Además, en el 2009 fue identificada en piña de Costa Rica (Waśkiewicz y Stepień 2012). Pero, en términos generales, se sabe poco de su ecología y biología reproductiva (Leslie y Summerell 2006).
Según Paparu et al. (2003) y Barrios (2006), Fusarium concentricum puede encontrarse de forma endófita en algunas musáceas, incluso puede presentar una actividad benéfica (inductor de resistencia), ya que según estudios realizados en Uganda en el 2000, se observó un incremento significativo de la biomasa de plantas de banano cultivadas en campo e inoculadas con esta especie de Fusarium.
Con base en las investigaciones que reportan la presencia de esta especie en varios cultivos en nuestro país y tomando la necrosis de los haces vasculares observadas en las plantas de pimienta enfermas (Figura 6), es necesario investigar aún más su ecología y biología (capacidad patogénica o actividad benéfica).
La última especie identificada en este estudio fue Fusarium proliferatum. Esta se reportó por primera vez en 1387 como una especie de Cephalosporium y fue descrita como una especie de Fusarium hasta 1566 (Leslie y Summerell 2006). En el cultivo de la pimienta solo se ha reportado aislado de la rizósfera de plantaciones de pimienta en Malasia y, según las pruebas de patogenicidad realizadas, no presentó actividad patogénica (Shahnazi et al. 2012). En Costa Rica, no existe registro de su presencia en el cultivo de pimienta negra.
Sin embargo, en otros cultivos como soya y espárragos, se reporta como causante de pudrición de la raíz (Costa et al. 2016), también se reporta como patógeno en banano, mango (Campos 2013), arroz, tomate, ajo, piña y cebolla (Stępien et al. 2015). Además, produce diferentes micotoxinas, entre ellas están moniliformina, beauvericina, ácido fusárico, fusaroproliferina y fumonisinas (Saha 2002, Fanelli et al. 2012, De la Torre et al. 2014). También produce enzimas relacionadas con la degradación de lignina y xileno (Saha 2002, Leslie y Summerell 2006).
Las especies F. concentricum y Fusarium proliferatum también están reportadas como endófitas en cultivos como gramíneas, trigo, orquídeas y arroz (Leslie y Summerell 2006). La información anterior resulta relevante si se toma en cuenta que se ha demostrado que las plantas de P. barbatum y P. nigrum son hospedantes de múltiples microorganismos endófitos, como por ejemplo los hongos Colletotrichum spp., Bipolaris spp., Lasiodiplodia spp., Phoma spp., Phomopsis spp., (Orlandelli et al. 2012), Alternaria spp., Colletotrichum gloeosporioides (Chithra et al. 2014) y bacterias promotoras del crecimiento (Jasim et al. 2013).
En Costa Rica, se reportó Colletotrichum gloeosporioides como endófito en plantas de Piper nigrum (González 2017) y, al considerar que se han logrado aislar Fusarium spp. de tejidos asintomáticos de plantas de Piper silvestres, es posible que alguna de las especies identificadas en este estudio pueda encontrarse como endófitas en las plantaciones nacionales.
Es importante señalar que en una misma planta fue posible confirmar la presencia de 2 especies distintas de Fusarium (muestras PSC 19 y PSC 22), en ambos casos se aisló F. solani y F. proliferatum en distintos estratos enfermos de la planta (parte aérea y raíz, respectivamente). Debido a que se desconoce la capacidad infectiva de los aislamientos, tampoco se debe descartar que al menos alguna de las especies sea un organismo endófito.
Conocer la biología de las especies de Fusarium identificadas, en este estudio, es esencial para comprender la enfermedad que se observa en las plantaciones. En aquellas especies patogénicas es necesario investigar su dinámica epidemiológica, el grado de especialización y los cambios en la capacidad patogénica. Toda esta información podrían ser la base para investigar nuevas estrategias de manejo integrado, incluso como lo sugiere Chandra et al. (2011) para iniciar proyectos de mejoramiento genético.
Las medidas de control que recomiendan las personas autoras, para el manejo de las enfermedades vasculares en pimienta, son un diseño adecuado de un drenaje sobre todo en épocas con altas precipitaciones, porque la acumulación de agua promueve las condiciones anaeróbicas, las cuales reducen el nivel de oxígeno y aumentan la susceptibilidad del huésped, debido a la disminución de la producción de fenol oxidasas, la producción reducida de fitoalexina, la supresión de las micorrizas y la reducción de la fijación de nitrógeno (Ravidra 2005).
La eliminación de plantas infectadas reduce el nivel de inóculo y la propagación del hongo y el manejo de la sombra en la temporada de lluvias es esencial para facilitar la penetración de la luz solar y la reducción de la alta humedad. Agregar materia orgánica para aumentar la diversidad de los suelos, proporcionar una nutrición adecuada y realizar un manejo integrado de Radopholus similis y Meloidogyne incognita son prácticas que se deben incluir en manejo integrado de la enfermedad (Ravidra 2005, Shahnazi et al. 2012).
En futuras investigaciones se realizará el análisis filogenético de los aislamientos descritos en este artículo, esto para contribuir al diseño de los programas manejo integrado de la enfermedad.















