Introducción
La Poza La Arenilla (Malecón Pardo, distrito de La Punta, en la Provincia Constitucional del Callao, Perú) se caracteriza por ser un ecosistema marino artificial creado con dos rompeolas, lo que ocasiona que tenga escasa circulación del agua. Los dos canales de entrada y salida del agua interactúan con el agua de la bahía del Callao. En estas aguas desembocan los ríos Rímac y Chillón, así como efluentes domésticos e industriales, los cuales pueden acarrear diferentes residuos tóxicos o peligrosos (Sánchez, Orozco, & Guzmán, 2002; Correa, Tam, Pasapera, Saavedra, & Ingunza, 2008). Entre los residuos tóxicos depositados en ambientes acuáticos destacan los hidrocarburos de petróleo y metales tóxicos como cadmio, cobre, plomo y arsénico, como consecuencia de actividades antropogénicas (desarrollo industrial, agrícola y/o urbano) o de forma natural (lluvias, escorrentía de los ríos, erosión, etc.) (Fu-hong & Qi-xing, 2008) acumulándose en los sedimentos costeros, donde pueden alcanzar altas concentraciones (Ankley, Thomas, DiToro, Hansen, Mahony, Berry, Swartz, Hoke, Garrison, Allen, & Zarba, 1994). En estas áreas, los organismos bentónicos pueden acumular Cd a través del agua y, sobre todo, de partículas ingeridas (Selck, Forbes, & Forbes, 1998). Los niveles de Cd en el agua en ambientes marinos pueden fluctuar entre 0.005 ug L-1 (Nürnberg, 1977) y 130 ug de L-1 (Förstner & Wittmann, 1981). El Cd se encuentra como CdCl2, siendo la salinidad un factor importante que puede modificar la actividad del ion libre del Cd (+2) y, por consiguiente, la biodisponibilidad, el metabolismo y toxicidad en los sistemas marinos (Jenkins & Sanders, 1986).
Los poliquetos (Clase Polychaeta, Phylum Annelida), son excelentes indicadores de perturbación ambiental (Tovar-Hernández, Salazar-Silva, de León-González, Carrera-Parra, & Salazar-Vallejo, 2014; Fernández-Rodríguez & Londoño-Mesa, 2015). Destaca la familia Spionidae (Grube, 1850) por su alta diversidad, por presentar un mayor número de especies descritas y por presentar una amplia distribución en sistemas bentónicos (Tomassetti & Porrello, 2005). Los miembros de Polydora (Bosc, 1802), son sedimentívoros (Blake & Woodwick, 1971; Fauchald & Jumars, 1979), y son considerados como indicadores de contaminación por materia orgánica (Dean, 2008) y metales traza, como el cadmio e hidrocarburos (Ajao & Fagade, 1990). Además, tienen ciclos de vida cortos y su mantenimiento y cultivo en el laboratorio son sencillos (Dean, 2008).
La toxicidad relativa de metales en poliquetos en orden decreciente es cobre, mercurio, zinc, arsénico, cromo y cadmio (Reish, 1988). Sin embargo, existen relativamente pocos estudios sobre el efecto del Cd en poliquetos. Reish & Carr (1978) demostraron que el efecto del Cd sobre la supervivencia, reproducción, desarrollo y ciclos de vida de los poliquetos Ctenodrilus serratus (Schmidt, 1857) y Ophryotrocha diadema Åkesson, 1976, es mínimo en comparación con otros metales pesados como el cobre y mercurio. Los miembros de varias especies crípticas del complejo de Capitella capitata han sido objeto de estudio del efecto del Cd en varias respuestas fisiológicas. Los estudios pioneros demostraron que el Cd disuelto en agua es uno de los metales pesados menos dañinos para la supervivencia de Capitella spp. (Reish, Martin, Piltz, & Word, 1976; Reish & Le May, 1991). Estudios más recientes han demostrado la ausencia de efectos significativos del Cd incorporado en agua y sedimentos sobre las tasas de crecimiento, tasa de egestión y alometría de Capitella sp I (Selck et al., 1998; Selck, Decho, & Forbes, 1999), mortalidad, producción de heces fecales y masa corporal de Capitella sp. I y Capitella sp. B (Méndez & Baird, 2002) y mortalidad de juveniles de Capitella sp. Y (Méndez & Green-Ruiz, 2005). Sin embargo, el estudio de Méndez & Green-Ruiz (2006), demostró efectos del Cd sobre la mortalidad y metamorfosis de larvas de Capitella sp. Y.
A pesar de la relativamente baja toxicidad del Cd observada en algunos poliquetos, se espera que el elemento cadmio tenga efecto sobre la mortalidad de otras especies de poliquetos no estudiadas, demostrando así el impacto que este elemento puede tener en los ecosistemas naturales. Por otro lado, este estudio aportará nuevos conocimientos, debido a que los únicos trabajos de poliquetos en el Perú se restringen a estudios ecológicos y de diversidad, siendo el grupo menos estudiado en comparación con otros invertebrados bentónicos como moluscos, crustáceos y equinodermos, entre otros (Aguirre & Canales, 2017; Vera, Tam, Vera, & Pinto, 2001).
Por lo tanto, en este trabajo se pretende evaluar el efecto tóxico del Cd sobre la mortalidad de adultos de Polydora sp, el cual puede ser un buen candidato como especie prueba en futuros estudios ecotoxicológicos.
Materiales y métodos
El ensayo sobre el efecto del Cd en la mortalidad adultos de Polydora sp. se realizó durante la época de verano, entre diciembre del 2016 a marzo del 2017 en el Laboratorio de Ecotoxicología Acuática, Área Funcional de Investigaciones Marino Costeras (AFIMC) de la Dirección General de Investigaciones en Acuicultura (DGIA) del Instituto del Mar del Perú (IMARPE), Callao, Perú.
Individuos adultos de Polydora sp. (entre 5 y 5.3 cm de longitud, con 20 a 25 segmentos) se recolectaron en diciembre de 2016 en la zona intermareal del humedal Poza de la Arenilla, Malecón Pardo, distrito de La Punta, Callao (12°04’24.1” S - 77°09’38.2” W). Los sedimentos en esta zona son predominantemente fangosos con contenidos de materia orgánica entre 2.53 y 22.8 % (Velasco & Solís, 2013). El estudio de Sánchez, Flores, & Henostroza (2014) reveló concentraciones de Cd en sedimento entre 0.14 y 1.08 µg/g con valor medio de 0.68 µg/g. En general el 100 % de los valores registrados no superaron el Nivel Probable de Efecto estipulado en la Tabla de Protección Costera de EE UU (4.21 µg/g).
El sedimento superficial (15 cm de profundidad) se recolectó con una espátula de aluminio y se tamizó con una malla de 500 µm. El material biológico retenido en el tamiz se colocó en envases de plástico de 500 ml con agua de mar para su traslado al laboratorio. La temperatura superficial del agua de mar fue de 32 °C y la salinidad de 29.6 ups, obtenidas con un equipo multiparamétrico portátil (Hach HQ40D). Estas mediciones fueron importantes para mantener condiciones similares en el laboratorio.
En el laboratorio, los especímenes fueron identificados utilizando un microscopio estereoscopio (Olympus SZ-61 ILST 1K36156). El género Polydora, junto con otros cinco géneros de la familia Spionidae, forma parte del complejo de especies de Polydora. El género Polydora se caracteriza por la presencia de setas modificadas en el setígero cinco (con espinas grandes de un solo tipo dispuestas en una sola hilera curveada, con setas de acompañamiento delgadas) y branquias a partir del setígero seis a 11. El setígero uno carece de notosetas. Los ganchos cubiertos neuropodiales son bidentados a partir de los setígeros siete al 14. El prostomio puede ser entero o con incisión y se extiende posteriormente como carúncula, la cual está rodeada de órganos nucales. La forma del pigidio es variable (Blake & Woodwick, 1971; Delgado-Blas, 2008).
Para el mantenimiento de los especímenes en el laboratorio se acondicionaron mesas de enfriamiento reguladas a 20 °C. Se utilizaron: i) Dos vasos de precipitados de 1 L de capacidad y en cada uno se colocó una capa de 2 a 4 cm de sedimento experimental (Linke-Gamenick, Forbes, & Méndez, 2000; Méndez, 2005; Méndez, 2006a; Méndez, 2006b); ii) 500 ml de agua de mar filtrada (< 1 µm) con salinidad de 30 ups; iii) se colocaron 150 individuos en cada vaso. El periodo de aclimatación a las condiciones de laboratorio duró dos semanas (Kenny, 1969). Para ello, los individuos adultos de Polydora sp se colocaron en envases de plástico de 1 L de capacidad con sedimento experimental y aireación constante durante dos semanas. Durante este periodo los organismos se alimentaron mediante la adición semanal de 0.5 g de alimento artificial seco que consistía en una mezcla, a partes iguales, de espinaca y comida para peces (Méndez, 2006a; Méndez, 2006b). Posteriormente, permanecieron tres días en agua de mar sin sustrato (Gopalakrishnan, Thilagam, & Raja, 2007).
El sedimento experimental utilizado para la aclimatación de los especímenes se recolectó en el área de estudio, simultáneamente con las muestras biológicas, se secó en estufa a 80 °C durante 24 h (To-orn & Paphavasit, 2017) y se tamizó a través de una malla de 250 µm para utilizar la parte menor de esta fracción (Méndez, Lacorte, & Barata, 2013), la cual corresponde a arena fina (Folk, 1965).
Diseño experimental: Se eligió el Cd con fines comparativos con otros poliquetos. Debido a la escasez de datos en la literatura sobre concentraciones subletales de Cd en solución para experimentos con poliquetos, se consideró la concentración mínima utilizada por Méndez & Green-Ruiz (2006) con larvas de Capitella sp Y (0.035 mg/L) y, como concentración máxima, se consideró la CL50 a 96 horas de 75 mg/L registrada para el poliqueto Eurythoe complanata por Reish, Asato, & LeMay (1989). Con el fin de determinar las concentraciones nominales de Cd, se analizó un intervalo de cinco concentraciones de manera logarítmica, a fin de obtener un amplio intervalo de concentraciones, considerando estos valores máximo y mínimo. La ventaja de la escala logarítmica es que permite analizar los impactos en las tasas de mortalidad en función de diversos órdenes de magnitud en el cambio de la concentración. La concentración mayor (75 mg/L), se multiplicó por el factor de 0.15 (Yacomelo, 2014) y las multiplicaciones sucesivas por este factor permitieron calcular las cuatro concentraciones restantes. Así, las concentraciones nominales para el experimento fueron 75, 11.25, 1.69, 0.25; 0.04 mg/L y un control.
La preparación de las cinco concentraciones se realizó por separado mediante la dilución de diferentes cantidades CdCl2 (tóxico de referencia considerado por Ingersoll et al. (1994)) en 3L agua de mar filtrada (<1 µm), con 30 a 32 ups, 20 a 21 °C y 8 a 9 mg/L de oxígeno disuelto. Para la preparación del tratamiento de 75 mg/L, se diluyeron 225 mg de CdCl2, para el segundo tratamiento se utilizaron 33.75 mg de CdCl2, y así sucesivamente, para el resto de las concentraciones.
Durante el bioensayo, se colocaron diez individuos adultos en 1 L de solución de Cd con las diferentes concentraciones (y 1L de agua de mar para los controles) y se realizaron tres réplicas por tratamiento. El experimento tuvo una duración de 72 horas, durante el cual no se colocó sedimento ni se administró alimento artificial a los especímenes para evitar la posible interacción con las soluciones de Cd. Los especímenes fueron contados cada 24 horas utilizando un microscopio estereoscópico, a fin de determinar su supervivencia.
Análisis Estadístico de los datos: El porcentaje de mortalidad para cada réplica se determinó de acuerdo con la expresión propuesta por Horng, Wang, & Cheng (2009):
S= (nf/ni) * 100,
Donde:
nf = número final de individuos vivos
ni = número inicial de individuos vivos
S = % de supervivencia
Los datos de supervivencia fueron expresados como porcentaje de mortalidad, los cuales fueron utilizados para el cálculo de la la CL50, mediante el programa Probit (USEPA) en SPPS ver. 2.1, a fin de determinar la concentración letal media (CL50).
Debido a que los datos no eran normales (prueba de Kolmogorov-Smirnov), se realizó una prueba de Kruskal-Wallis para observar si existen diferencias significativas entre los tratamientos. Posteriormente, se realizó la prueba de U-Man Whitney para detectar las diferencias entre pares de tratamientos. Para ambas pruebas se utilizó el programa SPPS ver. 2.1.
Resultados
La tabla 1 muestra los resultados de mortalidad registrados durante los tres días que duró el bioensayo. La supervivencia disminuyó al aumentar la concentración de Cd y el efecto negativo del Cd fue mucho más evidente en los tratamientos 11.25 y 75 mg/L. En ambos tratamientos, el efecto del tiempo de exposición fue más evidente a partir de las 24 horas experimentales, mientras que la mortalidad en los tratamientos con menores concentraciones de Cd fue evidente a partir del segundo día de exposición. Estos resultados fueron confirmados con la prueba de Kruskal-Wallis que mostró diferencias entre los tratamientos (Chi cuadrado = 10.536; gl = 4; p = 0.032) y la prueba de U-Man Whitney en la que los tratamientos 11.25 y 75 mg/L presentaron diferencias con los tres tratamientos restantes. El control presentó diferencias con todos los tratamientos de Cd. La CL50 de Cd durante 72h fue de 2.59 mg/L, con límite superior de y 16.39 mg/L y límite inferior de 1.37 mg/L (Fig. 1).
Tabla 1 Table 1 Mortalidad (%) registrada durante el bioensayo sobre adultos de Polydora Mortality (%) registered during the bioassay on adults of Polydora
| Tiempo | Réplicas | Control | 0.04 mg/L | 0.25 mg/L | 1.6 mg/L | 11.25 mg/L | 75 mg/L |
| 24 horas | R1 | 0 | 0 | 0 | 0 | 0 | 0 |
| R2 | 0 | 0 | 0 | 0 | 0 | 0 | |
| R3 | 0 | 0 | 0 | 0 | 0 | 0 | |
| 48 horas | R1 | 0 | 0 | 0 | 0 | 100 | 100 |
| R2 | 0 | 20 | 0 | 0 | 100 | 100 | |
| R3 | 0 | 0 | 0 | 0 | 100 | 100 | |
| 72 horas | R1 | 0 | 10 | 10 | 40 | 100 | 100 |
| R2 | 0 | 30 | 100 | 0 | 100 | 100 | |
| R3 | 0 | 0 | 20 | 30 | 100 | 100 |
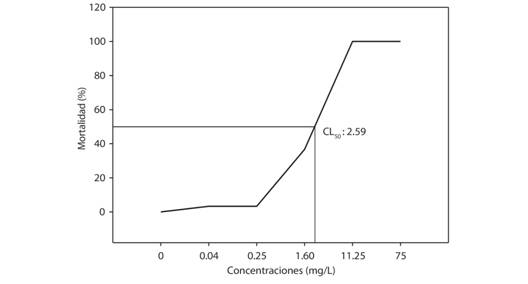
Fig. 1 Fig. 1 Concentración letal media (CL50) a 72h durante el bioensayo sobre adultos de Polydora. Median lethal dose (LC50) at 72h during the bioassay on adults of Polydora.
La mortalidad fue comprobada al estimular a los organismos con una varilla de vidrio y observar la carencia de movimiento Los síntomas de mortalidad fueron más evidentes en los tratamientos 11.25 y 75 mg/L, ya que los organismos disminuyeron su movilidad paulatinamente hasta la muerte Asimismo, tendían a agruparse y a formar tubos de sedimento. La mayoría de los especímenes de estos tratamientos cambiaron su coloración de rojiza a verde y algunos organismos presentaron pequeñas carnosidades en los setígeros.
Discusión
En la actualidad únicamente existen dos estudios de impacto ambiental en el área de estudio. Troll (2000), realizó una evaluación y ordenamiento ambiental para el establecimiento de un área protegida en la Poza de La Arenilla, mediante cuatro puntos de monitoreo de agua. Estos resultados fueron comparados con los estándares de calidad ambiental correspondientes y concluyó que las concentraciones de Cd en todos los puntos fueron inferiores a 0.001 mg/L, lo que indica que estos valores se encuentran muy por debajo de la cuantificación del método del laboratorio Estos resultados coinciden con los registros de Sánchez et al. (2014) en el estudio de calidad ambiental del humedal Poza La Arenilla-Callao en 2008, en el cual los valores de Cd estuvieron por debajo del límite de detección del equipo, lo que explica la supervivencia de Polydora sp. en ese ambiente.
Dada la escasez de estudios ecotoxicológicos con poliquetos, los datos de referencia de concentraciones de Cd experimentales son escasos, por lo que nuestras concentraciones nominales fueron calculadas en base a las escalas de otras especies de poliquetos registradas por Reish et al (1989) y Méndez & Green-Ruiz (2006). Los valores de mortalidad mostraron que el intervalo de concentraciones nominales elegido en este estudio preliminar superó los valores de concentraciones subletales, ya que en las concentraciones 11.25 y 75 mg/L murieron todos los organismos durante las primeras 24 horas. Por el contrario, los resultados de mortalidad en los tratamientos menores a 0.25 mg/L están en el mismo orden de magnitud que las concentraciones utilizadas por Selck et al (1998; Selck et al, 1999) y por Méndez & Green-Ruiz (2005), Méndez & Green-Ruiz (2006) con Capitella sp. I y Capitella sp. Y, respectivamente. Estos resultados sugieren que para futuros estudios en los que se analicen otras respuestas de este organismo se deberían utilizar concentraciones subletales de Cd menores a 1.6 mg/L, ya que en este tratamiento se observó mortalidad después de dos días. Idealmente, deberían realizarse más estudios preliminares detallados utilizando concentraciones bajas entre 0.04 y 1.6 mg/L, de preferencia con individuos identificados a nivel de especie (ya que las respuestas podrían verse enmascaradas a niveles taxonómicos superiores).
La comparación de la CL50 con otros poliquetos expuestos a Cd en solución (procedentes de cultivos realizados en Los Ángeles, EE UU) muestra que el valor obtenido con Polydora sp. durante 72 horas (2.59 mg/L) está en el mismo orden de magnitud que los valores registrados para adultos de Capitella capitata (Fabricius, 1780) (2.8 mg/L) y Pectinaria californiensis Hartman, 1941 (2.6 mg/L) (Reish & Le May, 1991) y de Neosabellaria clandestinus (Menon & Sareen, 1966) (2.8 mg/L; como Sabellaria clandestinus en Mohan, Menon, & Gupta, 1984) en sus experimentos de 96 horas de exposición. Estos valores resultaron menores que los de los poliquetos Neanthes arenaceodentata (14.1 mg/L) Nereis grubei (4.7 mg/L) y Ophryotrocha labronica Bacci & La Greca, 1961 (3.7 mg/L), de los mismos autores, así como los de C serratus y O diadema (10 mg/L) de Reish & Carr (1978). Estas comparaciones indican que los adultos de Polydora sp. presentan mayor sensibilidad al Cd que otras especies, ya que existe mortalidad en menores concentraciones de Cd, lo que la señala como una buena especie de prueba para futuros estudios de ecotoxicología. Por el contrario, la CL50 de Polydora sp. resultó mayor que la obtenida para larvas trocóforas de C. capitata durante 96 horas (0.22 mg/L; Reish et al., 1976) y para larvas metatrocóforas de Capitella sp. Y procedentes de Mazatlán, México (0.035 mg/L, Méndez & Green-Ruiz, 2006) en un periodo de 10 días. Esto sugiere que dentro del grupo de los poliquetos, el Cd tiene un impacto mayor en estados larvarios, ya que la mortalidad ocurre a menores concentraciones que en los adultos.
De acuerdo con Delgado-Blas (2009), los miembros de la familia Spionidae, en el medio natural, tienen la capacidad de cambiar su patrón de consumidores de depósito a suspensívoros. Esto podría explicar el éxito del experimento, ya que los controles sobrevivieron sin sedimento durante los tres días experimentales, lo que indica que probablemente cambiaron el patrón de alimentación para sobrevivir, mientras que los organismos expuestos recibieron el efectƒo adverso del Cd provocándoles la muerte. Estos resultados concuerdan con las características establecidas por Reish (1980) sobre el valor de los poliquetos en estudios de laboratorio (relativamente fácil recolección, manipulación, cultivo y transporte y ciclos de vida relativamente cortos). Nuestros resultados apoyan la sugerencia de utilizar Polydora spp. como otra especie prueba dentro del grupo de los poliquetos, en experimentos de ecotoxicología en ecosistemas marino-costeros en Perú o en otras localidades. Además, se podrán sentar las bases para realizar estudios ecotoxicológicos y fisiológicos con otros géneros de poliquetos frente a otros tóxicos, así como estudios de bioacumulación y biomarcadores enzimáticos o moleculares incentivando mayor interés de estudio sobre la clase Polychaeta.
Los estudios ecotoxicológicos son importantes, ya que permiten identificar problemas ambientales, establecer controles de contaminación, establecer límites, identificar apropiadamente acciones correctivas y monitorear los efectos de efluentes contaminados (Wall & Hanmer, 1987; Fent, 2003). La presente investigación preliminar constituye el primer estudio ecotoxicológico en Perú con el grupo Polychaeta en condiciones de laboratorio. Este estudio puede contribuir a sentar las bases para futuros estudios de ecotoxicología, monitoreo biológico y calidad ambiental utilizando el complejo de especies de Polydora, así como otros géneros de la familia Spionidae.
Declaración de ética: los autores declaran que todos están de acuerdo con esta publicación y que han hecho aportes que justifican su autoría; que no hay conflicto de interés de ningún tipo; y que han cumplido con todos los requisitos y procedimientos éticos y legales pertinentes. Todas las fuentes de financiamiento se detallan plena y claramente en la sección de agradecimientos. El respectivo documento legal firmado se encuentra en los archivos de la revista.












 uBio
uBio 

