Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.61 n.1 San José Mar. 2013
Variabilidad ambiental y respuestas fisiológicas de Polylepis cuadrijuga (Rosaceae) en un ambiente fragmentado en el Páramo de la Rusia (Colombia)
Environmental variability and physiological responses from Polylepis cuadrijuga (Rosaceae) in a fragmented environment in the Páramo de la Rusia (Colombia)
Environmental variability and physiological responses from Polylepis cuadrijuga (Rosaceae) in a fragmented environment in the Páramo de la Rusia (Colombia)
*Dirección para correspondencia:
Abstract
Polylepis cuadrijuga is an endemic woody species from the Colombian Eastern range, being the only tree species with capacity to live on mountainous environments beyond 4 000m of altitude. Grazing and agriculture have transformed at least 30% of the Guantiva-La Rusia region, turning continuous extensions of high Andean forest in a fragmented landscape, and P. cuadrijuga remnants have become smaller and more isolated. The aim of this study was to establish the environmental differences between a matrix of grazing pastures and the interior of fragments, to evaluate the physiological responses of P. cuadrijuga and determining the edge effect. Air temperature and humidity, soil water holding capacity and photosynthetic active radiation, were measured along two 50X2m transects from the matrix toward the center of fragment. Six trees inside the transects were chosen in each one of three sites (matrix, edge and interior) to measure the index chlorophyll content and to sample leaves to assess the leaf area, leaf biomass, specific leaf area, anatomy, health condition and pubescence. Results showed significantly differences between the matrix and the interior and intermediate conditions in the edge. Radiation, temperature and air desiccation were higher in the matrix than in the interior, submitting P. cuadrijuga trees to a stressing environment, where they presented stratification of epidermis and palisade parenchyma, and a higher leaf area, leaf thickness, chlorophyll content and pubescence than in the interior of fragments. All these physiological traits allow avoiding the photoxidation and damages by freezing or desiccation to which trees are exposed in a grazing pasture matrix. Nevertheless, there was a higher frequency of healthy leaves in the interior of fragments, showing that high irradiations and extreme air temperature and humidity reach adversely affect to P. cuadrijuga. Individuals in the edge had ecophysiological traits similar to the matrix ones, which confirm an edge effect that could penetrate 17m inside the fragments. We conclude that P. cuadrijuga is a plastic species, able to overcome the stress conditions from anthropogenic transformations, species able to be used in high Andean forest restoration programs.
Key words: chlorophyll, edge, high Andean forest, leaf biomass, photosynthetic active radiation, plasticity, pubescence, specific leaf area.
Resumen
Polylepis cuadrijuga es una especie leñosa endémica de la cordillera oriental de Colombia, donde la agricultura y el pastoreo han generado la fragmentación de sus bosques. Para determinar si existe un efecto borde en fragmentos ubicados en el Páramo de la Rusia, se establecieron diferencias ambientales y se evaluó las respuestas ecofisiológicas de P. cuadrijuga entre matriz de pastura, borde e interior de los fragmentos, a través de la medición de temperatura ambiental, humedad relativa, capacidad de retención de agua del suelo y radiación fotosintéticamente activa, a lo largo de dos transectos de 50m desde la matriz hacia el interior. En cada sitio se escogieron seis árboles para evaluar el contenido de clorofila, área foliar, biomasa foliar, área foliar específica, anatomía foliar, sanidad y pubescencia. En matriz fue mayor la temperatura y la radiación, condiciones relacionadas con la disminución del AFE y el aumento del contenido de clorofilas, evidenciado por la presencia de un parénquima en empalizada biestratificado. Características ecofisiológicas similares a las expuestas en borde, confirman un efecto de borde que podría penetra unos 17m en el interior de los fragmentos. Se concluye que P. cuadrijuga es una especie plástica, capaz de enfrentar condiciones de estrés generadas por actividades antropogénicas.
Palabras clave: área foliar específica, biomasa foliar, bosque altoandino, clorofila, efecto borde, plasticidad, pubescencia, radiación fotosintéticamente activa.
Los bosques tropicales sufren el permanente impacto de actividades humanas como la ganadería, la explotación de minas, la construcción de carreteras, la tala, la agricultura y las quemas inducidas, trayendo como consecuencia su fragmentación (Schlaifer 1993, Wade et al. 2003). La deforestación de bosques tropicales alcanza 13 millones de hectáreas al año, en Sudamérica (Tucker et al. 2001, Wade et al. 2003, Cayuela 2006, Alexandratos 2010). Con relación a los bosques montanos neotropicales, se estima que éstos se han reducido hasta en un 66%, afectando la diversidad vegetal (Cayuela 2006), y contribuyendo a la emisión de carbono a la atmósfera (Melillo et al. 1996).
A pesar de ser uno de los ecosistemas naturales más importantes del planeta por mantener la regulación hídrica y climática, en Colombia el impacto de las actividades antrópicas ha reducido considerablemente la cobertura de bosques andinos (Armenteras et al. 2003). La alta degradación y fragmentación a la que están actualmente sujetos junto con los páramos, generan cambios en la heterogeneidad intrínseca y en la capacidad de auto-recuperación (López 2004), reduciendo la diversidad alfa y beta (Vandermeer et al. 1998, Chapin et al. 2000).
Un modo de establecer los efectos directos de la fragmentación es estudiar las respuestas fisiológicas sobre las especies vegetales que dominan en el fragmento; se mencionan entre otras, el aumento de la transpiración, del ciclaje de nutrientes y de la productividad (Harper et al. 2005). Como resultado de la evapotranspiración, un efecto borde de desecación de dosel penetra incluso hasta varios kilómetros hacia el interior del fragmento (Briant et al. 2010). Las plantas en el borde pueden estar siendo sometidas a condiciones de estrés hídrico, en cuyo caso son esperables altos registros de conductancia estomática y bajos contenidos relativos de agua en las hojas (Kapos et al. 1997, Giambelluca et al. 2003). La presencia de pastizales en escenarios fragmentados dificulta la germinación, el establecimiento y la sobrevivencia de especies arbóreas (Zimmerman et al. 2000, Asbjornsen et al. 2004), especialmente debido a que el ganado explota recursos en los bordes de los fragmentos de bosque.
Polylepis (Rosaceae) es un género de plantas de forma de vida arbórea o arbustiva, de 1-6m de altura y un diámetro de copa de 3-5m (Azócar et al. 2007), característico por sus for- mas retorcidas, una corteza gruesa y escamosa de color rojizo, y pequeñas hojas de color verde grisáceo. El bosque de Polylepis representa la vegetación natural de gran parte de los Andes por encima de los 2 800m (Kessler 2006, Azócar et al. 2007), llegando fácilmente a superar los 4 000m en la franja andina desde Colombia – Ecuador - Perú - Bolivia (Smith 1994). Sin embargo, su distribución se ha reducido en más de un 80%, restringiéndose a afloramientos rocosos inaccesibles al fuego (Hensen 2002, Purcell & Brelsford 2004, Kessler 2006). Ya que su madera es valiosa como combustible, hoy en día es evidente la reducción constante de los fragmentos de Polylepis, siendo el ecosistema boscoso más amenazado de Sudamérica (Fjeldsa 2002, Renison et al. 2002, Kessler 2006).
La importancia de estos bosques se basa en que son considerados islas ecológicas de diversidad biológica, proporcionando micro- climas óptimos para un gran número de especies de fauna y flora (Hensen 2002, Servat et al. 2002, Kessler 2006, Azócar et al. 2007). Por otro lado, reducen la erosión del suelo, aumentan la captación de agua y retienen la precipitación (Renison et al. 2002), además de tener usos medicinales (Fjeldsa 2002). Existen varias adaptaciones morfológicas y fisiológicas del género Polylepis ante su entorno. Entre ellas se han descrito respuestas de ajuste del potencial hídrico y osmótico, cambios en área foliar específica (AFE) y cambios en la presencia de carbohidratos solubles (Rada et al. 1985, Rada et al. 2001, Ely et al. 2005). Además se han descubierto mecanismos de resistencia a temperaturas de congelación, a través del intercambio de gases, las relaciones hídricas de la hoja y la eficiencia fotosintética (Azócar et al. 2007). Algunos de los rasgos que varían con relación a la altitud, incluyen el grosor de las hojas, la conductividad estomática, el AFE, los contenidos de nitrógeno y fósforo en las hojas, la proporción C/N y el área foliar (AF) (Macek et al. 2009).
El género está representado por tres especies en Colombia, siendo P. cuadrijuga la única especie endémica, presente exclusivamente en la cordillera oriental del país (Azócar et al. 2007). Aunque se ha estudiado su representatividad biogeográfica y diversidad asociada, se conoce muy poco con relación a su capacidad adaptativa o de ajuste a forzantes ambientales. Teniendo en cuenta que la expansión de las fronteras agropecuarias son la principal causa de fragmentación de los ecosistemas altoandinos, en este estudio se planteó evaluar los cambios ambientales diurnos generados por la potrerización en el Páramo de la Rusia, determinar si existe un efecto borde, y establecer cómo esos cambios pueden influir en las respuestas morfo-fisiológicas de P. cuadrijuga a lo largo de un gradiente desde la matriz de pasturas hacia el interior de un fragmento de bosque.
Materiales y Métodos
Área de estudio: El estudio se realizó durante el año 2011, en un área de fragmentos de P. cuadrijuga (5˚55’42.37” N-73˚04’52.48” W), que hacen parte del Páramo de la Rusia, en el corredor de conservación Altoandino Guantiva - La Rusia - Iguaque, ubicado en el flanco occidental de la cordillera oriental entre los 2 900-3 800msnm, con una extensión de 187km2. Presenta un régimen de lluvias bimodal comprendido entre abril-mayo y octubre-noviembre; y las épocas secas en diciembre-marzo y junio-septiembre con un promedio anual de precipitación de 1 950mm, temperaturas entre los -4°C-9.7°C, suelos poco fértiles con pH ácido y una alta acumulación de materia orgánica en el horizonte superficial (Morales et al. 2007, Meneses & González 2008). El escenario es heterogéneo y fragmentado, con presencia de matorrales de Asteraceae, bosques achaparrados con Polylepis, formaciones abiertas con Espeletia y pajonales de Calamagrostis, además de pastizales, prados, turberas, chuscales y tremedales (Rangel 2000).
El género Polylepis ha permanecido en la cordillera oriental por lo menos desde el plioceno superior, hace más de un millón de años (Van der Hammen & Hooghiemstra 1995). Actualmente, los remanentes de P. cuadrijuga se hallan restringidos a pendientes pronunciadas, donde persiste la influencia de la radiación solar, variable con la orientación geográfica, la inclinación, y la elevación del sol (Azócar et al. 2007).
Caracterización ambiental: A lo largo de dos transectos lineales de 50m orientados desde la matriz de pasturas hacia el interior de un fragmento de bosque, fueron ubicados seis termo-higrómetros digitales. En cada sitio se tomaron dos lecturas de humedad y temperatura ambiental, en intervalos de una hora, desde las 10:50 hasta las 14:50, rango diurno en el cual se registra la mayor radiación en páramos. Adicionalmente, en nueve sitios al azar en los transectos se colectaron muestras de suelo con cilindros de 5cm de diámetro, con el fin de determinar en laboratorio la capacidad de retención de agua (CRA) por método gravimétrico.
En puntos del transecto donde se encontraban árboles de P. cudrijuga, y a una altura de 1.5-2m de altura desde el suelo, se tomaron tres a seis mediciones de luz con un cuantificador de densidad RFA (radiación fotosintéticamente activa) Apogeé MQ-100. Estas mediciones se hicieron al mismo tiempo que las observaciones fisiológicas, abarcando entre las 10:30 y las 15:00 horas.
Evaluadores fisiológicos: Se escogieron árboles adultos de P. cuadrijuga ubicados dentro de 1m a cada lado de los transectos, completando un total de seis individuos por sitio (matriz de pasturas, borde e interior) para la medición en campo del índice de contenido de clorofilas (ICC; clorofilómetro OptiScience CCM-200), la revisión de adaptaciones foliares y del estado sanitario foliar. En cada árbol fueron colectadas al azar un total de 5-6 hojas para medir el área foliar (AF; medidor BioScientific SKT-103), la biomasa foliar (BF) y calcular el área foliar específica (AFE: cm2 de lámina foliar/g de biomasa). Dos hojas por árbol fueron usadas para establecer diferencias entre sitios en características morfo-anatómicas mediante cortes transversales de lámina y nervadura. Dichos cortes fueron realizados con un micrótomo de rotación manual y tratados con la técnica de transpenetración en xilol y tinción con safranina fast-green (Montero 2001, Sandoval 2005); los mejores cortes se usaron para fotografía y mediciones de grosor de lámina foliar. Desde la colecta, todas las muestras foliares fueron conservadas en cámara húmeda y a baja temperatura (2-5˚C) hasta su tratamiento en laboratorio.
Se evaluó en forma cualitativa la pubescencia de las hojas usando cuatro categorías, desde ausente hasta abundante. El estado sanitario de P. cuadrijuga fue clasificado en tres categorías, de acuerdo al porcentaje observado de área foliar con síntomas como clorosis, quemazón y necrosis, del siguiente modo:
• Sanidad alta: Síntomas en menos del 10% de área foliar.
• Sanidad media: Síntomas entre el 10% y 50% de área foliar.
• Sanidad baja: Síntomas en más del 50% de área foliar.
En cuanto al análisis estadístico de la información, los datos fisiológicos y de caracterización ambiental fueron promediados y analizados empleando ANDEVAS a una vía para establecer si existen diferencias entre sitios. Cuando no se cumplió normalidad u homocedasticidad de los datos, se procedió a un análisis no paramétrico de Kruskal - Wallis y test a posteriori de contrastes múltiples de Dunn. Las variables área foliar y biomasa foliar fueron normalizadas mediante √x, mientras la variable contenido de clorofilas requirió una transformación tipo Log10 (x+1). Todos los análisis se realizaron utilizando los programas SigmaStat 3.1 (Systat, ®) y STATISTICA 6.0 (StatSoft ®).
Resultados
Las características ambientales fueron diferentes entre sitios, y en el caso de la matriz y el borde las mediciones de radiación foto- sintéticamente activa (RFA) fueron incluso distintas entre mañana y tarde (Cuadro 1, Fig. 1). La temperatura y RFA en el interior del fragmento (11.8±2.1°C; 50-165µmol/m2s) fueron menores a lo registrado en la matriz de pasturas (31.2±0.4°C; 524-785µmol/m2s en la mañana y 900-941µmol/m2s en la tarde), mientras que en este último sitio la humedad ambiental (27±2.1%) fue menor con relación al interior del fragmento (72±13.6%). La capacidad de retención de agua en el suelo de los dos sitios fue similar (55.4±2.4% en la matriz y 59.8±4.1% en el interior). El borde se diferenció del interior del fragmento, registrando una mayor RFA durante la mañana (498-540µmol/m2s), mayor temperatura (16.2±1.5°C) y menor CRA (38.4±5.6%).
El desempeño fisiológico de P. cuadrijuga fue afectado significativamente por la fragmentación (Fig. 2). Los árboles de la matriz tuvieron una mayor biomasa foliar (0.22±0.05g), área foliar (11.9±2.7cm2) y contenido de clorofilas (10.7-48.1) que los árboles del interior (BF: 0.15±0.05g; AF: 2.07±0.43cm2; ICC: 7.6- 27.2). Sin embargo la medida alométrica AFE, que relaciona el área y la biomasa foliar, fue menor en la matriz (54.22±13.8cm2/g) que en el interior del fragmento (67.15±18.57cm2/g). Los árboles en el borde mostraron una respuesta fisiológica similar a los individuos de la matriz, pero con un AFE notoriamente menor (BF: 0.22±0.07g; AF: 3.73±0.68cm2; ICC: 19.2-42; AFE: 49±10.55cm2/g).
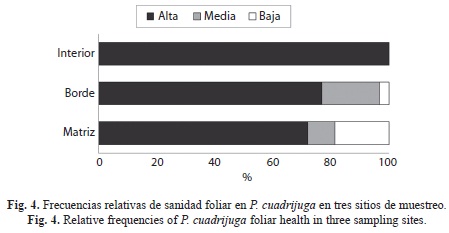
La pubescencia, el estado sanitario y la anatomía foliar también denotaron patrones de diferenciación entre sitios. El 16.7% de las hojas de matriz y el 33.3% de las de borde presentaron pubescencia abundante, pero no en el interior, donde en la mayoría de las hojas la pubescencia apenas era notoria (72%). Por otra parte, en la matriz el 50% de las hojas carecían de pubescencia y había una alta frecuencia de síntomas que cubren más de la mitad de la lámina foliar (19%) (Fig. 3, 4). La clorosis o amarillamiento generalizado fue el síntoma más común, seguido por la necrosis de ramas completas en algunos individuos de la matriz. Únicamente en el interior del fragmento el 100% de las hojas revisadas exhibió una sanidad alta (Fig. 4).
Los cortes transversales mostraron que existen dos tipos anatómicos de hoja (Fig. 5): En la matriz y el borde el grosor de la lámina foliar midió entre 330-450 micras, la epidermis adaxial y el parénquima de empalizada eran predominantemente biestratificados y la reacción del método de tinción fue más intenso y de colores rojizos oscuros. El segundo tipo provino del interior del fragmento, y consiste en una lámina foliar más delgada (menor a 300 micras de espesor), con epidermis y parénquima típicamente uniestratificado; la tinción suave y de tono gris-verdoso en toda la lámina foliar, excepto en la epidermis adaxial y abaxial, donde hubo coloración rojo-brillante.
Discusión
Los resultados mostraron que P. cuadrijuga está expuesta a condiciones ambientales contrastantes como resultado de la fragmentación. La matriz de pasturas alcanzó temperaturas hasta 14°C superiores a la temperatura media en el interior del fragmento, ocasionando una reducción de la humedad ambiental de más del 40%. La RFA promedio que recibió la matriz durante un día despejado superó los 600µmoles/m²s, cantidad alrededor de la cual se encuentra el umbral para la fotoinhibición en la mayoría de plantas C3 (Fitter & Hay 2002, Taiz & Zeiger 2004). Bajo continuas y prolongadas exposiciones a estas condiciones de luz, el fotosistema II sufre daños que llegan a ser irreversibles (Biswal 2005). La retención de humedad en el suelo alcanzo el 55% en matriz, favoreciendo el crecimiento de P. cuadrijuga a pesar de la alta radiación.
La matriz de pasturas genera un efecto borde en el microambiente del bosque, el cual se caracterizó por condiciones intermedias de humedad del aire, temperatura y RFA. Los cambios observados en las mediciones ambientales a lo largo de los transectos permitieron estimar que el efecto borde penetra unos 17m hacia el interior del fragmento, distancia mucho menor a la que se reporta para otros ecosistemas boscosos fragmentados (Kapos et al. 1997, Mesquita et al. 1999, Davies-Colley et al. 2000, Harper et al. 2005). La única variable ambiental para la cual el borde no mostró un efecto atenuante fue la capacidad de retención de agua en el suelo, la cual fue significativamente menor a la que presentaron la matriz y el interior, posiblemente debido a una fuerte competencia radical por agua y nutrientes, a causa de la alta densidad y reclutamiento de especies de rápido crecimiento en el borde (Sizer & Tanner 1999, Casanova et al. 2007).
Se encontraron claras diferencias fisiológicas de P. cuadrijuga asociadas a la fragmentación, mostrando que los árboles se comportan de manera más similar en borde y matriz, desarrollando características en común como una alta biomasa foliar, la presencia de hipodermis adaxial y la presencia de un parénquima de empalizada biestratificado que ocasiona a su vez el engrosamiento de la lámina foliar. En contraparte, las hojas de P. cuadrijuga en el interior de los fragmentos exhiben una única capa de epidermis, predominancia de un solo estrato de parénquima de empalizada y lámina foliar más angosta. Algunas características de composición celular se lograron determinar gracias a la reacción con la tinción safranina – fast Green; la coloración roja oscura en hojas de matriz y borde sugiere que las paredes del parénquima tienen mucha más lignina y sustancias antioxidantes que las hojas provenientes del interior, mientras que la superficie adaxial podría estar cubierta de una capa de súber que típicamente tiñe en tonos rojo brillante (Ruzin 1999, Sandoval 2005).
El engrosamiento de la lámina foliar en individuos de borde y matriz es congruente con el área foliar específica, de tal modo que cada gramo de biomasa abarca un área foliar menor, en comparación con las hojas en el interior de los fragmentos. Al haber más parénquima de empalizada los contenidos de clorofila fueron significativamente mayores en la matriz que en el interior del fragmento, convirtiéndose en una estrategia para maximizar el aprovechamiento de la luz que llega en altas cantidades a lo largo del día (Valladares et al. 2002, Colmenares et al. 2005). Todas las diferencias mofo-fisiológicas apuntan a establecer una clara estrategia de ajuste de los individuos de P. cuadrijuga a las condiciones de alta irradiación, bajas temperaturas nocturnas y viento, a las que están sometidos en la matriz y el borde, consistente en (1) aumentar el tejido fotosintético en cuanto a área foliar, biomasa y clorofila para un máximo aprovechamiento de la luz y (2) emplear paredes suberizadas y epidermis biestratificadas con sustancias antioxidantes para reducir la pérdida de agua y el daño de los tejidos por foto-oxidación (Colmenares et al. 2005, Rada et al. 1985, Larcher 2003).
La pubescencia foliar parece ser un elemento adicional de aclimatación para las condiciones de estrés en la matriz y el borde, donde se encontró una mayor variabilidad en la presencia de tricomas, y en particular una mayor frecuencia de hojas con pubescencia abundante. Se ha descrito que el desarrollo de pubescencia permite que las hojas conserven durante más tiempo una temperatura interna superior al umbral de congelamiento (Luttge 1997, Colmenares et al. 2005, Ely et al. 2005), reduciendo así la probabilidad de daño en los tejidos, que aumenta por encima de los 3 000m de altitud (Rundel 1994). Las temperaturas en el Páramo de la Rusia podrían alcanzar hasta -4°C durante la noche (Morales et al. 2007). Junto con su corteza, que se desprende como finas hojas alrededor del tronco, otros mecanismos que podrían permitirle a P. cuadrijuga soportar las bajas temperaturas se han descrito para sus congéneres Polylepis sericea (Venezuela) y Polylepis tarapacana (Bolivia), e incluyen reducir el potencial osmótico a un punto superior pero cercano al de congelamiento, o supercongelar los tejidos (Goldstein et al. 1994, Rada et al. 2001, Rada et al. 2009). Esto es posible manteniendo tasas metabólicas altas, de tal manera que la respiración celular durante la noche brinde la suficiente energía para acumular azúcares de función osmolítica en el pre-alba, la hora del día con menor temperatura (Rada et al. 1985, Goldstein et al. 1994, Rada et al. 2001).
La presencia de sustancias antioxidantes en P. cuadrijuga, que bien podrían ser flavonoides y catequinas, sugiere que los árboles de P. cuadrijuga desarrollan una estrategia de alta protección frente a dos factores: La herbivoria y la radiación UV-B, que tienden a aumentar con la altitud (Vélez et al. 1998). En este estudio, el 100% de las hojas del interior presentaron alta sanidad foliar en contraste con matriz y borde, donde con una frecuencia del 20-30% se encuentran hojas con un estado sanitario medio y bajo (Fig. 4). Esto demuestra que si los árboles en la matriz no estuvieran dotados de estrategias de aclimatación, su sobrevivencia en una matriz de pasturas podría ser muy baja.
En general, nuestro estudio comprobó que P. cuadrijuga responde a la fragmentación con una amplia plasticidad morfo-fisiológica, retrasando los efectos negativos que normalmente las actividades antrópicas trae sobre otras especies arbóreas (Kapos et al. 1997, Mesquita et al. 1999, Zimmerman et al. 2000). En la zona de estudio se observó por ejemplo reclutamiento de plántulas y juveniles de P. cuadrijuga dentro del pastizal, y esto cobra importancia si se tiene en cuenta que el corredor altoandino Guantiva – La Rusia hace parte de un área prioritaria para la conservación en Colombia (Armenteras et al. 2003). Hacia el año 2 000 se estimaba que en un 30% de su extensión, el corredor ha sufrido transformaciones con fines productivos como la ganadería, la agricultura y las plantaciones forestales (Morales et al. 2007); y es positivo postular que gracias a su capacidad de aclimatación, su potencial regenerativo en el borde de los fragmentos (Cierjacks et al. 2007) y al proveer hábitat para la avifauna (Meneses & González 2008), P. cuadrijuga tiene un alto potencial de uso con fines de recuperación ecosistémica.
Agradecimientos
A Clara Marisol Cespedes Gil, por el apoyo en el procesamiento y tinción de cortes histológicos de hojas de P. cuadrijuga, y a Luz Andrea Menesses Ortegón por su acompañamiento al sitio de estudio y por el aporte de material fotográfico.
Referencias
Alexandratos, A. 2010. Agricultura mundial: hacia el año 2010. Estudio de La FAO. Grupo Mundi-prensa, Madrid, España. [ Links ]
Armenteras, D., F. Gast & H. Villareal. 2003. Andean forest fragmentation and the representativeness of protected natural areas in the Eastern Andes, Colombia. Biol. Conserv. 113: 245-256. [ Links ]
Asbjornsen, H., M. Ashton, D. Vogt & S. Palacios. 2004. Effects of habitat fragmentation on the buffering capacity of edge environments in a seasonally dry tropical oak forest ecosystem in Oaxaca, Mexico. Agricult. Ecosys. Environ. 103: 481-495. [ Links ]
Azócar, A., F. Rada & C. García. 2007. Functional characteristics of the arborescent genus Polylepis along a latitudinal gradient in the high Andes. Interciencia 32: 663-668. [ Links ]
Biswal, B. 2005. Photosynthetic Response of Green Plants to Environmental Stress: Inhibition of Photosynthe- sis and Adaptational Mechanisms, p. 739-750. In M. Pessarakli (eds.). Handbook of photosynthesis. Taylor and Francis Group, Boca Raton, EE.UU. [ Links ]
Briant, G., V. Gond & S. Laurance. 2010. Habitat fragmentation and the desiccation of forest canopies: a case study from Eastern Amazonia. Biol. Cons. 143: 2763-2769. [ Links ]
Casanova, F., L. Ramírez & F. Solario. 2007. Interacciones radiculares en sistemas: mecanismos y opciones de manejo. AIA 11: 41-52. [ Links ]
Cayuela, L. 2006. Deforestación y fragmentación de bosques tropical montanos en los altos de Chiapas, México. Efectos sobre la diversidad de árboles. Eco- sistemas 15: 192-198. [ Links ]
Chapin, F.S., E.S. Zavaleta, V.T. Eviner, R.L. Naylor, P.M. Vitousek, H.L. Reynolds, D.U. Hooper, S. Lavorel, O.E. Sala, S.E. Hobbie, M.C. Mack & S. Diaz. 2000. Consequences of changing biodiversity. Nature 405: 234-242. [ Links ]
Cierjacks, A., K. Karsten & I. Hensen. 2007. Potential lateral expansion of Polylepis forest fragments in central Ecuador. For. Ecol. Manage. 242: 477-486. [ Links ]
Colmenares, M., F. Rada & R. Luque. 2005. Anatomía foliar de Polylepis sericea wedd. (Rosaceae) a dos altitudes en los Altos andes venezolanos. Plantula 3: 141-148. [ Links ]
Davies-Colley, R.J., G. Payne & M. van Elswijk. 2000. Microclimate gradients across a forest edge. New Zeal. J. Ecol. 24: 111-121. [ Links ]
Ely, F., F. Torres & J. Gaviria. 2005. Morfología y anatomía foliar de Monochaetum meridense (Melastomataceae). Acta Bot. Venez. 28: 197-12. [ Links ]
Fitter, A. & R. Hay. 2002. Environmental physiology of Plants. Academic, Londres, Inglaterra. [ Links ]
Fjeldsa, J. 2002. Polylepis forests-vestiges of a vanishing ecosystem in the Andes. Ecotropica 8: 111-123. [ Links ]
Giambelluca, T.W., A.D. Zieger, M.A. Nullet, D.M. Truong & L.T. Tran. 2003. Transpiration in a small tropical forest patch. Agric. For. Meteorol. 117: 1-22. [ Links ]
Goldstein, G., F.C. Meinzer & F. Rada. 1994. Environmental Biology of a tropical treeline species, Polylepis sericea, p. 129-149. In P.W. Rundel, A.P. Smith & F.C. Meinzer (eds.). Tropical alpine environments: Plant form and function. Cambridge University, Cambridge, Inglaterra, Reino Unido. [ Links ]
Harper, K.A., S.E. Macdonald, P.J. Burton, J. Chen, K.D. Brosofske, S.C. Saunders, E.S. Euskirchen, D. Roberts, M.S. Jaiteh & P. Essen. 2005. Edge influence on forest structure and composition in fragmented landscapes. Conserv. Biol. 19: 768-782. [ Links ]
Hensen, I. 2002. Impacts of antropogenic activity on the vegetation of the Polyplepis woodlands in the region of Cochabamba, Bolivia. Ecotropica 8: 183-203. [ Links ]
Kapos, V., E. Wandelli, J.L. Camargo & G. Ganade. 1997. Edge related changes in environmental and plant responses due to forest fragmentation in Central Amazonia, p. 33-44. In W.F. Laurance & R.O Bierregaard (eds.). Tropical Forest Remnants. Chicago University, Chicago, EE.UU. [ Links ]
Kessler, M. 2006. Bosques de Polylepis, p. 110-120. In M Moraes, B. Ollgaard, L.P. Kvist, F. Borchsenius & H. Balslev (eds.). Botánica Económica de los Andes Centrales. Universidad Mayor de San Andrés, La Paz, Bolivia. [ Links ]
Larcher, W. 2003. Physiological Plant Ecology: Ecophysiology and Stress Physiology of Functional Groups. Springer-Verlag Berlín, Heidelberg, Germany. [ Links ]
López, F. 2004. Estructura y función en bordes de bosque. Ecosistemas 13: 67-77. [ Links ]
Luttge, U. 1997. Physiological Ecology of Tropical Plants. Springer-Verlag Berlin, Heidelberg, Germany. [ Links ]
Macek, P., J. Macková & F. De Bello. 2009. Morphological and ecophysiological traits shaping altitudinal distribution of three Polylepis treeline species in the dry tropical Andes. Acta Ecol. 35: 778-785. [ Links ]
Melillo, J., R. Houghton & D. Kicklighter. 1996. Tropical deforestation and the global carbon budget. Rev. Energy. Environ. 21: 293-310. [ Links ]
Meneses, L.A. & D.A. González. 2008. Relación entre la diversidad de avifauna y la estructura y composición florística de los bosques de Polylepys cuadrijuga del páramo de La Rusia, Duitama (Boyacá-Colombia). Tesis de pregrado, Universidad Pedagógica y Tecnológica de Colombia, Tunja, Colombia. [ Links ]
Mesquita, R., P. Delamônica & W. Laurance. 1999. Effect of surrounding vegetation on edge-related tree mortality in Amazonian forest fragments. Biol. Cons. 91: 129-134. [ Links ]
Montero, W. 2001. Estudio morfogénico e histológico de Echinaceae purpurea in vitro. Instituto tecnológico de Costa Rica, Cartago, Costa Rica. [ Links ]
Morales, M., J. Otero, T. Van der Hammen, A. Torres, C. Cadena, C. Pedraza, N. Rodríguez, C. Franco, J.C. Betancourth, E. Olaya, E. Posada & L. Cárdenas. 2007. Atlas de páramos de Colombia. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt, Bogotá D.C., Colombia. [ Links ]
Purcell, J. & A. Brelsford. 2004. Reassessing the Causes of decline of Polylepis, a tropical subalpine forest. Ecotropica 10: 155-158. [ Links ]
Rada, F., G. Goldstein, A. Azocar & F. Meinzer. 1985. Daily and seasonal osmotic changes in a tropical treeline species. J. Exp. Bot. 36: 989-1000. [ Links ]
Rada, F., C. García, C. Boero, M. Gallardo, M. Hilal, J. Gonzales, F. Prado, M. Liberman & A. Azocar. 2001. Low-temperature resistance in Polylepis tarapacana, a tree growing at the higest altitudes in the world. Plant. Cell. Environ. 24: 377-381. [ Links ]
Rada, F., C. García & S. Rangel. 2009. Low temperature resistance in saplings and ramets of Polylepis sericea in the Venezuela Andes. Acta Oecologica 35:610-613. [ Links ]
Rangel, O. 2000. Colombia: Diversidad Biótica III: La región de la vida paramuna. Universidad Nacional de Colombia, Facultad de Ciencia, Instituto de Ciencias Naturales, Bogotá, Colombia. [ Links ]
Renison, D., A. Cingolani & R. Suarez. 2002. Efectos del fuego sobre un bosquecillo de Polylepis australis (Rosaceae) en las montañas de Córdoba, Argentina. Rev. Chil. Hist. Nat. 75: 719-727. [ Links ]
Rundel, P. 1994. Tropical alpine climates, p. 21-44. In P.W. Rundel, A.P. Smith, F.C. Meinzer (eds.). Tropical Alpine Environments: Plant Form and Function. Cambridge University, Cambridge, Inglaterra, Reino Unido. [ Links ]
Ruzin, S.E. 1999. Plant Microtechnique and Microscopy. Oxford University, New York, EEUU. [ Links ]
Sandoval, E. 2005. Técnicas aplicadas al estudio de la anatomía vegetal. Instituto de Biología, Universidad Nacional Autónoma de México, México D.F., México. [ Links ]
Schlaifer, M. 1993. Las especies nativas y la deforestación en los andes: una visión histórica, social y cultural en Cochabamba, Bolivia. Bull. Inst. Fr. Études Andin. 22: 585-610. [ Links ]
Servat, G.P., W. Mendoza & J.A. Ochoa. 2002. Flora y fauna de cuatro bosques de Polylepis (Rosaceae) en la Cordillera de Vilcanota (Cusco, Perú). Ecol. Apl. 1: 25-35. [ Links ]
Sizer, N. & V.J. Tanner. 1999. Responses of woody plant seedlings to edge formation in a lowland tropical rainforest, Amazonia. Biol. Conserv. 91: 135-142. [ Links ]
Smith, A.P. 1994. Introduction to tropical alpine vegetation. In P.W. Rundel, A.P. Smith & F.C. Meinzer (eds.). Tropical alpine environments: Plant form and function. Cambridge University, Cambridge, Inglaterra, Reino Unido. [ Links ]
Taiz, L. & E. Zeiger. 2004. Fisiología Vegetal. Porto Alegre, Artmed, Brasil. [ Links ]
Tucker, C., M. Steininger, D. Slayback & D. Gran. 2001. Measuring the state of the world´ is forest: an introduction to the scientific analysis of forest cover and forest loss. Environmental Defense, New York, EE.UU. [ Links ]
Valladares, F., J.M. Chico, I. Aranda, L. Balaguer, P. Dizengremel, E. Manrique & E. Dreyer. 2002. The greater seedling high-light tolerance of Quercus robur over Fagus sylvatica is linked to a greater physiological plasticity. Trees 16: 395-403. [ Links ]
Van der Hammen, T. & H. Hooghiemstra. 1995. Cronoestratigrafía y correlación del Plioceno y Cuaternario en Colombia. Anál. Geogr. 24: 51-68. [ Links ]
Vandermeer, J., M. Van Noordwijk, J. Andreson, C. Ong & I. Perfecto. 1998. Global-change and multi-species agroecosystems. Concepts and issues. Agr. Ecosyst. Environ. 67: 1-22. [ Links ]
Vélez, V., J. Cavelier & B. Devia. 1998. Ecological traits of the tropical treeline Species Polyepis cuadrijuga (Rosaceae) in the Andes of Colombia. J. Trop. Ecol. 14: 771-787. [ Links ]
Wade, T., K. Riiters, J. Wickham & K. Jones. 2003. Distribution and causes of global forest fragmentation. Conserv. Ecol. 7: 7-23. [ Links ]
Zimmerman, J., J. Pascarella & T. Aide. 2000. Barriers to forest regeneration in an abandoned pasture in Puerto Rico. Restor. Ecol. 8:350-360. [ Links ]
*Correspondencia a:
Carolina Ramos. Grupo de investigación en Manejo Integrado de Ecosistemas y Biodiversidad, Escuela de Ciencias Biológicas, Universidad Pedagógica y Tecnológica de Colombia, Av. Central Norte Tunja, Colombia; carolina.ramos@uptc.edu.co.
Sindy P. Buitrago. Grupo de investigación en Manejo Integrado de Ecosistemas y Biodiversidad, Escuela de Ciencias Biológicas, Universidad Pedagógica y Tecnológica de Colombia, Av. Central Norte Tunja, Colombia; kalisahe@hotmail.com.
Karen L. Pulido. Grupo de investigación en Manejo Integrado de Ecosistemas y Biodiversidad, Escuela de Ciencias Biológicas, Universidad Pedagógica y Tecnológica de Colombia, Av. Central Norte Tunja, Colombia; biopao.k18@gmail.com.
Leidy J. Vanegas. Grupo de investigación en Manejo Integrado de Ecosistemas y Biodiversidad, Escuela de Ciencias Biológicas, Universidad Pedagógica y Tecnológica de Colombia, Av. Central Norte Tunja, Colombia; leidyvanegas_8915@hotmail.com.
1. Grupo de investigación en Manejo Integrado de Ecosistemas y Biodiversidad, Escuela de Ciencias Biológicas, Universidad Pedagógica y Tecnológica de Colombia, Av. Central Norte Tunja, Colombia; carolina.ramos@uptc.edu.co, kalisahe@hotmail.com, biopao.k18@gmail.com, leidyvanegas_8915@hotmail.com
Recibido 13-XII-2011. Corregido 23-VII-2012. Aceptado 20-VIII-2012