Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.60 n.1 San José Mar. 2012
Biología reproductiva del pargo Lutjanus inermis (Perciformes: Lutjanidae), en el Pacífico central mexicano
Gabriela Lucano-Ramírez1*, Salvador Ruiz-Ramírez1, Gaspar González-Sansón1 & Bertha Patricia Ceballos-Vázquez2*
*Dirección para correspondencia
Abstract
Reproductive biology of the Golden snapper Lutjanus inermis (Perciformes: Lutjanidae) in the central Mexican Pacific. Reproductive aspects and information on the effect of fishery activities over this species stock are scarce, despite the imperative need of effective protection and resource management programs. To support the possible establishment of closed seasons and catch levels for the area, our study aimed to evaluate the spawning season of the Golden snapper (Lutjanus inermis). For this, fish caught by artisanal fisheries in the Navidad, Tenacatita and Chamela bays (Jalisco, Mexico) were sampled monthly from 1999-2008, and analyzed sex ratios, spawning season and size at first maturity. A total of 311 (53.1%) females and 275 (46.9%) males were caught, and the observed sex ratio was 1:0.88. The total length range was 14.4-37.0cm and total weight range from 48-575g. The length at first maturity was 23.9cm TL for females and 23.6cm TL for males. The gonadosomatic index showed two principal reproductive periods in the year (February-April and September- November), when the largest number of mature gonads were observed. Ovaries were of asynchronic development type and seven oocyte development stages were identified. Testicles showed lobular development and spermatozoa were observed in the center of the cysts and in the collecting ducts. It is important to mention that our results support the current suitable exploitation of this species in the area.
Key words: Lutjanidae, sex ratio, maturation stages, gonadosomatic index, sexual maturity.
Resumen
Debido a los escasos antecedentes del efecto de las pesquerías y manejo del pargo Lutjanus inermis, es importante conocer la época reproductiva para el establecimiento de temporadas de veda, ya que la biomasa de los peces en fase de reproducción, es usada como punto de referencia para evaluar la condición del stock explotado y para establecer futuros niveles de captura. Por ello, el objetivo de este trabajo fue analizar algunos aspectos reproductivos como proporción sexual, época reproductiva, talla de madurez de L. inermis en las costas de Jalisco, México. Durante 1999-2008, se llevaron a cabo muestreos mensuales de los ejemplares capturados por la pesca artesanal en las bahías de Navidad, Tenacatita y Chamela (Jalisco, México). Se recolectaron 311 (53.1%) hembras y 275 (46.9%) machos y, la proporción de sexos (1:0.88) no presentó diferencia significativa. El intervalo de longitud total fue 14.4 a 37.0cm y el peso total de 48 a 575g. L. inermis presentó los máximos valores del IGS en dos periodos, febrero-abril y septiembre-noviembre, también en estos periodos se presentaron los mayores porcentajes de organismos en estadio de maduración. El ovario presentó el tipo de desarrollo asincrónico y se reconocieron siete fases del desarrollo de los ovocitos. En los testículos se observó el tipo de desarrollo lobular, se observaron espermatozoides en el centro de los cistos y en el conducto recolector. La talla de madurez (L50) fue de 23.9cm LT para hembras y 23.6cm LT para machos. Considerando el periodo de muestreo de este estudio, los antecedentes descritos podrían ser de utilidad en la formulación de planes o estrategias de manejo de esta especie.
Palabras clave: Lutjanidae, reproducción, proporción sexual, estadios de madurez, índice gonadosomático.
Reproductive biology of the Golden snapper Lutjanus inermis (Perciformes: Lutjanidae) in the central Mexican Pacific. Reproductive aspects and information on the effect of fishery activities over this species stock are scarce, despite the imperative need of effective protection and resource management programs. To support the possible establishment of closed seasons and catch levels for the area, our study aimed to evaluate the spawning season of the Golden snapper (Lutjanus inermis). For this, fish caught by artisanal fisheries in the Navidad, Tenacatita and Chamela bays (Jalisco, Mexico) were sampled monthly from 1999-2008, and analyzed sex ratios, spawning season and size at first maturity. A total of 311 (53.1%) females and 275 (46.9%) males were caught, and the observed sex ratio was 1:0.88. The total length range was 14.4-37.0cm and total weight range from 48-575g. The length at first maturity was 23.9cm TL for females and 23.6cm TL for males. The gonadosomatic index showed two principal reproductive periods in the year (February-April and September- November), when the largest number of mature gonads were observed. Ovaries were of asynchronic development type and seven oocyte development stages were identified. Testicles showed lobular development and spermatozoa were observed in the center of the cysts and in the collecting ducts. It is important to mention that our results support the current suitable exploitation of this species in the area.
Key words: Lutjanidae, sex ratio, maturation stages, gonadosomatic index, sexual maturity.
Resumen
Debido a los escasos antecedentes del efecto de las pesquerías y manejo del pargo Lutjanus inermis, es importante conocer la época reproductiva para el establecimiento de temporadas de veda, ya que la biomasa de los peces en fase de reproducción, es usada como punto de referencia para evaluar la condición del stock explotado y para establecer futuros niveles de captura. Por ello, el objetivo de este trabajo fue analizar algunos aspectos reproductivos como proporción sexual, época reproductiva, talla de madurez de L. inermis en las costas de Jalisco, México. Durante 1999-2008, se llevaron a cabo muestreos mensuales de los ejemplares capturados por la pesca artesanal en las bahías de Navidad, Tenacatita y Chamela (Jalisco, México). Se recolectaron 311 (53.1%) hembras y 275 (46.9%) machos y, la proporción de sexos (1:0.88) no presentó diferencia significativa. El intervalo de longitud total fue 14.4 a 37.0cm y el peso total de 48 a 575g. L. inermis presentó los máximos valores del IGS en dos periodos, febrero-abril y septiembre-noviembre, también en estos periodos se presentaron los mayores porcentajes de organismos en estadio de maduración. El ovario presentó el tipo de desarrollo asincrónico y se reconocieron siete fases del desarrollo de los ovocitos. En los testículos se observó el tipo de desarrollo lobular, se observaron espermatozoides en el centro de los cistos y en el conducto recolector. La talla de madurez (L50) fue de 23.9cm LT para hembras y 23.6cm LT para machos. Considerando el periodo de muestreo de este estudio, los antecedentes descritos podrían ser de utilidad en la formulación de planes o estrategias de manejo de esta especie.
Palabras clave: Lutjanidae, reproducción, proporción sexual, estadios de madurez, índice gonadosomático.
Los miembros de la familia Lutjanidae, se conocen como pargos, habitan aguas tropicales y subtropicales, incluye 21 géneros y 125 especies reconocidas. La mayoría de los pargos viven en aguas someras, aunque hay especies que se encuentran entre los 100 y 500m de profundidad. En el Pacífico oriental, diez especies de pargos se agrupan en dos géneros, Hoplopagrus y Lutjanus el cual está representado por nueve especies. El pargo rabirrubia del pacífico, Lutjanus inermis (Peters 1869), se distribuye en el Pacífico desde México hasta Colombia, es común encontrarlo en costas rocosas y arrecifes de coral hasta los 40m de profundidad, durante el día forman grupos de 30 o más individuos, que a veces permanecen inmóviles. Se alimentan de crustáceos y peces, también zooplancton, especialmente larvas de peces (Amezcua-Linares 1996, Allen & Robertson 1998). En el Pacífico tropical mexicano se captura con redes agalleras, de arrastre y línea de mano, principalmente en áreas costeras. Con importancia económica, se comercializa localmente entero. La captura comercial ribereña (en Jalisco) ha presentado oscilaciones que van de 0.5 a 1.0 tonelada por año (Amezcua-Linares 1996, Espino-Barr et al. 2004). Rojo-Vazquéz et al. (2008), enlista a L. inermis entre las 30 especies más abundantes en un periodo de 47 meses de muestreo. Hasta el momento solo se ha reportado de esta especie aspectos como: descripción, distribución, redescubrimiento en el golfo de California y listados de especies en el Pacífico (Amezcua-Linares 1996, Allen & Robertson 1998, Tavera & De la Cruz-Agüero 2006, Rojo-Vázquez et al. 2009).
Los antecedentes sobre la biología, ecología y el efecto de las pesquerías en la especie no se encontraron, a pesar de que los mismos son necesarios para desarrollar programas efectivos de protección y manejo del recurso. En este sentido, el reconocimiento de la época reproductiva es necesaria para el establecimiento de vedas de captura, ya que comúnmente la biomasa de los peces en fase de reproducción, es usada como uno de los puntos de referencia para evaluar la condición del stock explotado y para establecer futuros niveles de captura (Vitale et al. 2006). Por ello, se analizan e interpretan algunos aspectos reproductivos (proporción sexual, época reproductiva, talla de primera madurez) de Lutjanus inermis en las costas de Jalisco, México, durante un periodo de nueve años de muestreos.
Materiales y métodos
Recolecta de muestras: Las muestras se obtuvieron entre enero de 1999 y diciembre de 2008 (excepto 2001) durante cinco días de cada mes. Los organismos analizados provinieron de la captura comercial realizada con redes agalleras de diferente luz de malla (3.0”, 3.5”, 4.0” y 4.5”), las cuales se colocaban a las 19:00 y se levantaban al otro día a las 7:00 por pescadores ribereños en las Bahías de Navidad (19°12’34” N - 104°41’24” W), Tenacatita (19°18’08” N - 104°48’21” W) y Chamela (19°33’29” N - 105°05’35” W), ubicadas en el estado de Jalisco, México. Los organismos de L. inermis fueron separados del resto de la fauna capturada, se le registró la longitud total (LT±1mm) y el peso total (PT±0.1g). El sexo se identificó mediante la observación directa de las gónadas y se registró el peso de las mismas (PG±0.01g). Las gónadas se fijaron en formol neutro al 10% para su posterior análisis histológico.
Para conocer la temporada reproductiva se aplicaron dos métodos complementarios. El primero consistió en el cálculo del índice gonadosomático como la relación porcentual del peso de la gónada con respecto al peso del organismo (Sánchez-Cárdenas et al. 2007). El otro método consistió en la aplicación de la escala morfocromática de cuatro fases de desarrollo gonádico (inmaduro, en maduración, maduro y desovado) de acuerdo a los criterios de Everson et al. (1989).
Para describir la organización interna de la gónada se hicieron cortes histológicos de ovarios y testículos en diferentes grados de desarrollo. El proceso histológico consistió en la deshidratación en una serie de soluciones de alcohol etílico en concentraciones crecientes, inclusión en paraplast, cortes de 5mm y tinción con hematoxilina-eosina (Lucano-Ramírez et al. 2001a). La observación y análisis de las gónadas se realizó con un microscopio Axiostar Plus (Zeiss). Se clasificaron los diferentes tipos de ovocitos de acuerdo a Yamamoto & Yamazaki (1961), Cerisola (1984) y Lucano-Ramírez et al. (2001a). La organización de los testículos se describió de acuerdo a Hyder (1969) y Lucano-Ramírez et al. (2001b).
Se calculó el índice gonadosomático (IGS) de cada individuo mediante la expresión:
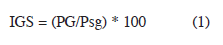
donde: PG es el peso de la gónada, Psg es el peso sin el peso de la gónada.
Se obtuvo el factor de condición (FC) para cada uno de los organismos, mediante la expresión:
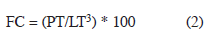
donde: PT= peso total, LT= longitud total.
La existencia de diferencias significativas entre los valores medios de estos índices se verificó mediante el análisis de varianza (ANDEVA) y la correlación entre índices mediante el coeficiente de correlación por rangos de Spearman (rs). En todas las pruebas se utilizó el programa STATISTICA. 7.0, fijando un nivel de significación de 0.05.
Se calculó la proporción sexual como la razón del número de hembras entre el número de machos, considerando la muestra total, anual, y por frecuencia de tallas. Se utilizó la prueba de bondad de ajuste Chi cuadrada con corrección para continuidad de Yates (Zar 2010) para comparar y determinar si la proporción de sexos difieren del esperado 1:1.
La talla de maduración sexual (L50) se estimó como la longitud a la cual el 50% de los individuos han alcanzado la madurez sexual. Para ello se ajustó un modelo logístico a la frecuencia relativa acumulada de peces maduros (en intervalos de 2cm). El valor L50 para cada sexo se obtuvo a partir de los parámetros estimados en cada caso, según la expresión
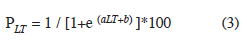
donde: PLT es el porcentaje de individuos maduros a la longitud x, a y b son parámetros del modelo logístico ajustado (Echeverria 1987). Este modelo se ajustó mediante un método no lineal basado en el algoritmo de Levenberg-Maquard, utilizando el programa STATISTICA 7.0.
Resultados
En total se recolectaron 586 organismos. La longitud total de las hembras varió entre 7.0 y 37.0cm con un promedio de 28.2±0.26cm y el peso total varió entre 54 y 575g con promedio de 275.9±6.92g. Los machos presentaron un intervalo de longitud total entre 14.4 y 36.7cm, con promedio de 27.5±0.26cm y el peso total varió entre 48 y 564g con un promedio de 252.4±6.79g. Al parecer las hembras son más grandes que los machos, ya que al realizar un ANDEVA, este presentó diferencia significativa entre las tallas (F=3.92, p=0.04). Las longitudes promedio, encontradas en los diferentes años de muestreo, fluctuaron desde 24.9cm hasta 32.1cm. En hembras y en machos se observó la talla promedio máxima (32.0 y 32.1cm) en 2007, y la mínima (24.9 y 25.1cm) en 1999.
De los organismos recolectados, 311 fueron hembras (53.1%) y 275 machos (46.9%). Las proporciones sexuales para cada uno de los años de muestreo, así como la total (1H:0.88M) no fueron significativamente diferentes de la esperada 1:1 (x2=2.21, p>0.05). Al realizar el análisis por talla, sólo se presentó diferencia significativa en la frecuencia de longitud de 32-33.9cm (x2=3.88, p=0.049), esta proporción no influye sobre la anual ni la total en donde no se presentó diferencia significativa (Fig. 1).
Variación mensual de porcentajes de madurez gonádica (Fig. 2). Estadio Inmaduro: Se presentó en todos los meses tanto en hembras como en machos, con porcentaje máximo en mayo (60% y 76.9% respectivamente). Estadio en Maduración: En hembras el mayor porcentaje se observó en marzo (20.4%) y en machos en abril (44.4%). Estadio Maduro: Abril (64.3%) y noviembre (46.2%) fueron los meses con el mayor porcentaje en hembras; en machos abril (44.4%) y octubre (42.9%). Estadio Desovado: En junio (85.0% y 85.7%) se presentaron los porcentajes altos tanto en hembras como en machos.
La variación mensual de los porcentajes de madurez gonádica y del índice gonadosomático (IGS) sugieren que la especie se reproduce en dos temporadas del año (Figs. 2, 3), la primera febrero-abril y la segunda septiembre-noviembre.
El IGS presentó una variación estacional significativa en hembras (F=10.68, p<0.05) y en machos (F=6.58, p<0.05). Entre ambos sexos se presentó una tendencia similar; sin embargo, los valores del IGS de los machos fueron significativamente menores a los de las hembras (F=26.83, p<0.05). Los promedios altos del IGS en hembras se presentaron en febrero y abril (3.03 y 4.28) y en septiembre y noviembre (3.28 y 3.60) y, en los machos, en marzo y abril (1.98 y 2.76) y septiembre y noviembre (2.23 y 1.81). Aunque en hembras el IGS disminuyó en marzo y octubre, estos no se igualan a los mínimos registrados después de dichos periodos (Fig. 3).
El factor de condición presentó valores altos en mayo y junio tanto en hembras (1.17 y 1.19) como en machos (1.22 y 1.23), ocurriendo en la temporada no reproductiva (Fig. 3). Los valores promedios del FC presentaron diferencia significativa de manera temporal tanto en hembras (F=4.57, p<0.05), como en machos (F=5.34, p<0.05), los promedios variaron entre 1.09 y 1.19 en las hembras, y de 1.08 a 1.23 en los machos. Se presentó correlación positiva significativa entre los valores promedio mensuales del IGS de hembras y del IGS de machos (rs=0.916, p=0.000028) y entre los valores promedio mensuales del FC de hembras y del FC de machos (rs=0.741, p=0.0058), pero no se encontró correlación entre el IGS y el FC entre hembras (rs=0.011, p=0.834) y machos (rs=0.047, p=0.430).
Descripción microscópica de las gónadas: Los ovarios están envueltos por una túnica que penetra en el ovario formando lamelas ovígeras. En el interior del ovario se observaron ovocitos en diferentes grados de desarrollo por lo que se puede considerar que L. inermis presenta un desarrollo asincrónico (Fig. 4). Se identificaron siete fases de desarrollo de los ovocitos: 1) ovocitos cromatina nucléolo con diámetro promedio de 57.1±0.54μm, se caracterizan por tener poco citoplasma y un núcleo grande con nucléolos; 2) en perinucléolo con diámetro de 81.5±2.40μm, los nucléolos se observan en la periferia del núcleo; 3) con vesículas vitelinas con diámetro promedio de 133.5±2.50μm, en el citoplasma se forman gotas de aceite, con ellos se inicia la formación de vitelo; 4) en vitelogénesis primaria el diámetro promedio fue de 236.7±2.95μm, se observan glóbulos de vitelo en el citoplasma; 5) en vitelogénesis secundaria con diámetro de 304.4±3.59μm, en todo el citoplasma se encuentran glóbulos de vitelo; 6) vitelogénesis terciaria diámetro de 321.2±7.13μm, los glóbulos de vitelo se empiezan a fusionar y el núcleo se encuentra en proceso de migración hacia el polo animal y 7) maduros con diámetro de 334.7±13.34μm, vitelo completamente fusionado, no se observa el núcleo.
El interior de los testículos se encuentra organizado por lóbulos, los cuales están formados por varios cistos dentro de los cuales se lleva a cabo la espermatogénesis. Una vez formados los espermatozoides son liberados al interior del lóbulo y posteriormente se agrupan en el conducto receptor para ser expulsados. A este tipo de organización que tienen las células del testículo se le denomina desarrollo lobular.
En las gónadas en estadio inmaduro (Figs. 4A, 5A), se observaron principalmente ovocitos en cromatina nucléolo y en perinucléolo y en los machos el testículo presentó cistos con poco desarrollo celular y el conducto receptor libre de espermatozoides. En el estadio en maduración (Figs. 4B, 5B), los ovarios presentan ovocitos cromatina nucléolo, en perinucléolo, con vesículas vitelinas, vitelogénesis primaria y pocos en vitelogénesis secundaria y los testículos presentan desarrollo celular en los cistos y espermatozoides en el conducto receptor. En el estadio maduro (Figs. 4C, 5C), el ovario está constituido principalmente por ovocitos en vitelogénesis secundaria, pero se pueden identificar otras fases como en cromatina nucléolo, perinucléolo, vesículas vitelinas y vitelogénesis primaria. Por su parte, el testículo presenta una gran cantidad de espermatozoides en el conducto receptor. El estadio desovado (Figs. 4D, 5D) presenta en el ovario ovocitos en cromatina nucléolo y algunos en vitelogénesis secundaria, y en el testículo se observan cistos semivacíos y pocos espermatozoides en el conducto receptor.
Talla de maduración sexual (L50): La hembra y el macho más pequeños con gónadas maduras fueron de 20.1 y 21.3cm LT, respectivamente. Por su parte, los organismos más grandes con gónadas inmaduras fueron de 27.0cm LT, la hembra y 26.6cm LT, el macho. Considerando las frecuencias relativas acumuladas, se encontró que las hembras con talla promedio de 28.2cm, representaron el 99.1% del total de hembras maduras y los machos con talla promedio de 27.4cm representaron el 97.3% del total de machos maduros. La longitud de madurez sexual (L50) calculada utilizando todos los individuos muestreados fue de 23.9cm LT para las hembras y 23.6cm LT para los machos (Fig. 6).
Discusión
El intervalo de longitud que se obtuvo en el presente trabajo (14.4 a 37.0cm LT), es similar al reportado por Espino-Bar et al. (2004) para la costa de Jalisco (18.6 a 37.3cm LT). La longitud máxima reportada por Amezcua- Linares (1996) y Allen & Robertson (1998) en el Pacífico oriental tropical, es inferior (35.0cm LT) a la encontrada en el presente trabajo. La talla promedio encontrada por Espino-Bar et al. (2004), es similar (27.7cm LT) a la observada en el presente trabajo (27.8cm LT). Esta coincidencia puede deberse a que los organismos muestreados para ambos casos provinieron de la pesca comercial.
Un aspecto importante en la reproducción de los peces es la proporción de hembras y machos que integran una población. Se encontró diferencia significativa en la distribución de tallas (32-33.9cm), en donde se observó un mayor número de hembras que machos, como lo mencionan varios autores en otras especies, esto puede estar ligado a varios aspectos como la supervivencia, la distribución y preferencia del hábitat, la profundidad, la distribución de tallas, o bien en los aspectos alimenticios y reproductivos (Nikolsky 1963, Rojas et al. 2004, Piñón et al. 2009).
El periodo reproductivo de L. inermis, descrito en el presente estudio (febrero-abril y septiembre-noviembre) constituye el primer reporte sobre este aspecto de la biología de la especie, autores como Sánchez-Cárdenas et al. (2007), mencionaron que el IGS es un buen indicador del periodo reproductivo, además ha sido utilizado para establecer dichos periodos en diversas especies (González & Oyarzún 2002, Palomera-Sánchez 2004, Lucano-Ramírez et al. 2006, Piñón et al. 2009). El IGS y el FC no están correlacionados entre sí en L. inermis, este mismo resultado también se encontró en las especies Holacanthus passer (Arellano-Martínez & Ceballos-Vázquez 2001) y en Pinguipes chilensis (González & Oyarzún 2002). Esto puede deberse a que el FC está relacionado con la condición fisiológica y requerimientos energéticos de un pez, tal como se detectó en el bacalao del Atlántico. Además, el FC presenta independencia de la energía almacenada en la producción de ovocitos (González & Oyarzún 2002).
El desove asincrónico (parcial o fraccionado) que presentó L. inermis es similar al que presentan otras especies que se distribuyen en regiones tropicales y subtropicales como Scomberomorus sierra (Palomera-Sánchez 2004), Pseudupeneus grandisquamis (Lucano- Ramírez et al. 2006) y Diodon holocanthus (Lucano-Ramírez et al. 2011); en contraste con el mostrado por los peces de las regiones templadas, los cuales tienen periodos cortos, desove total y desarrollo de la gónada sincrónico (Nikolsky 1963, Granados-Lorencio 2002). Los peces que presentan desarrollo asincrónico, como en el caso de L. inermis, por lo general desovan en varias ocasiones en una temporada reproductiva prolongada (Nagahama et al. 1995, Maack & George 1999) y los ovarios contienen ovocitos en diferentes fases de desarrollo.
En el presente trabajo, como en otros realizados en la región (Palomera-Sánchez 2004, Lucano-Ramírez et al. 2001a, 2006, 2011), se han identificado de cinco a siete fases de desarrollo de los ovocitos los cuales representan la vitelogénesis como tal. González et al. (1979) describieron cinco fases del desarrollo de los ovocitos en la especie Lutjanus griseus. Según los autores, las fases de la I a la IV, son no maduras, las cuales se observaron en organismos capturados en el medio natural, mientras que la fase V (ovocitos maduros), se observó sólo en hembras tratadas con la hormona GCH.
Microscópicamente el testículo de L. inermis presentó el desarrollo de tipo lobular, coincidiendo con lo descrito para L. peru (Lucano-Ramírez et al. 2001b), P. grandisquamis (Lucano-Ramírez et al. 2006) y Diodon holocanthus (Lucano-Ramírez et al. 2011) en la costa sur de Jalisco.
La talla de madurez (L50) fue similar en ambos sexos y constituyen los primeros reportes de este parámetro para L. inermis, cabe resaltar que la L50, es inferior a la talla promedio del total de organismos capturados y a las tallas promedio encontradas en los distintos años de muestreo, por lo tanto podemos inferir que cerca o mas del 50% de los organismos ya se habían reproducido por lo menos una vez.
Agradecimientos
Los autores agradecen a Daniel Kosonoy, Gerardo Kosonoy y Manuel Díaz por su ayuda en la realización de las actividades de pesca. A las cooperativas “Rivera Melaque” y “Punta Farallón” por facilitarnos sus instalaciones. A la Universidad de Guadalajara por financiar el proyecto “Reproducción de los peces de la familia Lutjanidae colectados en el Pacífico tropical mexicano” y a los estudiantes del Departamento de Estudios para el Desarrollo Sustentable de Zonas Costeras, que colaboraron en los muestreos.
Los antecedentes sobre la biología, ecología y el efecto de las pesquerías en la especie no se encontraron, a pesar de que los mismos son necesarios para desarrollar programas efectivos de protección y manejo del recurso. En este sentido, el reconocimiento de la época reproductiva es necesaria para el establecimiento de vedas de captura, ya que comúnmente la biomasa de los peces en fase de reproducción, es usada como uno de los puntos de referencia para evaluar la condición del stock explotado y para establecer futuros niveles de captura (Vitale et al. 2006). Por ello, se analizan e interpretan algunos aspectos reproductivos (proporción sexual, época reproductiva, talla de primera madurez) de Lutjanus inermis en las costas de Jalisco, México, durante un periodo de nueve años de muestreos.
Materiales y métodos
Recolecta de muestras: Las muestras se obtuvieron entre enero de 1999 y diciembre de 2008 (excepto 2001) durante cinco días de cada mes. Los organismos analizados provinieron de la captura comercial realizada con redes agalleras de diferente luz de malla (3.0”, 3.5”, 4.0” y 4.5”), las cuales se colocaban a las 19:00 y se levantaban al otro día a las 7:00 por pescadores ribereños en las Bahías de Navidad (19°12’34” N - 104°41’24” W), Tenacatita (19°18’08” N - 104°48’21” W) y Chamela (19°33’29” N - 105°05’35” W), ubicadas en el estado de Jalisco, México. Los organismos de L. inermis fueron separados del resto de la fauna capturada, se le registró la longitud total (LT±1mm) y el peso total (PT±0.1g). El sexo se identificó mediante la observación directa de las gónadas y se registró el peso de las mismas (PG±0.01g). Las gónadas se fijaron en formol neutro al 10% para su posterior análisis histológico.
Para conocer la temporada reproductiva se aplicaron dos métodos complementarios. El primero consistió en el cálculo del índice gonadosomático como la relación porcentual del peso de la gónada con respecto al peso del organismo (Sánchez-Cárdenas et al. 2007). El otro método consistió en la aplicación de la escala morfocromática de cuatro fases de desarrollo gonádico (inmaduro, en maduración, maduro y desovado) de acuerdo a los criterios de Everson et al. (1989).
Para describir la organización interna de la gónada se hicieron cortes histológicos de ovarios y testículos en diferentes grados de desarrollo. El proceso histológico consistió en la deshidratación en una serie de soluciones de alcohol etílico en concentraciones crecientes, inclusión en paraplast, cortes de 5mm y tinción con hematoxilina-eosina (Lucano-Ramírez et al. 2001a). La observación y análisis de las gónadas se realizó con un microscopio Axiostar Plus (Zeiss). Se clasificaron los diferentes tipos de ovocitos de acuerdo a Yamamoto & Yamazaki (1961), Cerisola (1984) y Lucano-Ramírez et al. (2001a). La organización de los testículos se describió de acuerdo a Hyder (1969) y Lucano-Ramírez et al. (2001b).
Se calculó el índice gonadosomático (IGS) de cada individuo mediante la expresión:
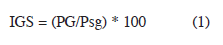
donde: PG es el peso de la gónada, Psg es el peso sin el peso de la gónada.
Se obtuvo el factor de condición (FC) para cada uno de los organismos, mediante la expresión:
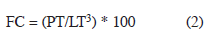
donde: PT= peso total, LT= longitud total.
La existencia de diferencias significativas entre los valores medios de estos índices se verificó mediante el análisis de varianza (ANDEVA) y la correlación entre índices mediante el coeficiente de correlación por rangos de Spearman (rs). En todas las pruebas se utilizó el programa STATISTICA. 7.0, fijando un nivel de significación de 0.05.
Se calculó la proporción sexual como la razón del número de hembras entre el número de machos, considerando la muestra total, anual, y por frecuencia de tallas. Se utilizó la prueba de bondad de ajuste Chi cuadrada con corrección para continuidad de Yates (Zar 2010) para comparar y determinar si la proporción de sexos difieren del esperado 1:1.
La talla de maduración sexual (L50) se estimó como la longitud a la cual el 50% de los individuos han alcanzado la madurez sexual. Para ello se ajustó un modelo logístico a la frecuencia relativa acumulada de peces maduros (en intervalos de 2cm). El valor L50 para cada sexo se obtuvo a partir de los parámetros estimados en cada caso, según la expresión
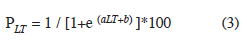
donde: PLT es el porcentaje de individuos maduros a la longitud x, a y b son parámetros del modelo logístico ajustado (Echeverria 1987). Este modelo se ajustó mediante un método no lineal basado en el algoritmo de Levenberg-Maquard, utilizando el programa STATISTICA 7.0.
Resultados
En total se recolectaron 586 organismos. La longitud total de las hembras varió entre 7.0 y 37.0cm con un promedio de 28.2±0.26cm y el peso total varió entre 54 y 575g con promedio de 275.9±6.92g. Los machos presentaron un intervalo de longitud total entre 14.4 y 36.7cm, con promedio de 27.5±0.26cm y el peso total varió entre 48 y 564g con un promedio de 252.4±6.79g. Al parecer las hembras son más grandes que los machos, ya que al realizar un ANDEVA, este presentó diferencia significativa entre las tallas (F=3.92, p=0.04). Las longitudes promedio, encontradas en los diferentes años de muestreo, fluctuaron desde 24.9cm hasta 32.1cm. En hembras y en machos se observó la talla promedio máxima (32.0 y 32.1cm) en 2007, y la mínima (24.9 y 25.1cm) en 1999.
De los organismos recolectados, 311 fueron hembras (53.1%) y 275 machos (46.9%). Las proporciones sexuales para cada uno de los años de muestreo, así como la total (1H:0.88M) no fueron significativamente diferentes de la esperada 1:1 (x2=2.21, p>0.05). Al realizar el análisis por talla, sólo se presentó diferencia significativa en la frecuencia de longitud de 32-33.9cm (x2=3.88, p=0.049), esta proporción no influye sobre la anual ni la total en donde no se presentó diferencia significativa (Fig. 1).
Variación mensual de porcentajes de madurez gonádica (Fig. 2). Estadio Inmaduro: Se presentó en todos los meses tanto en hembras como en machos, con porcentaje máximo en mayo (60% y 76.9% respectivamente). Estadio en Maduración: En hembras el mayor porcentaje se observó en marzo (20.4%) y en machos en abril (44.4%). Estadio Maduro: Abril (64.3%) y noviembre (46.2%) fueron los meses con el mayor porcentaje en hembras; en machos abril (44.4%) y octubre (42.9%). Estadio Desovado: En junio (85.0% y 85.7%) se presentaron los porcentajes altos tanto en hembras como en machos.
La variación mensual de los porcentajes de madurez gonádica y del índice gonadosomático (IGS) sugieren que la especie se reproduce en dos temporadas del año (Figs. 2, 3), la primera febrero-abril y la segunda septiembre-noviembre.
El IGS presentó una variación estacional significativa en hembras (F=10.68, p<0.05) y en machos (F=6.58, p<0.05). Entre ambos sexos se presentó una tendencia similar; sin embargo, los valores del IGS de los machos fueron significativamente menores a los de las hembras (F=26.83, p<0.05). Los promedios altos del IGS en hembras se presentaron en febrero y abril (3.03 y 4.28) y en septiembre y noviembre (3.28 y 3.60) y, en los machos, en marzo y abril (1.98 y 2.76) y septiembre y noviembre (2.23 y 1.81). Aunque en hembras el IGS disminuyó en marzo y octubre, estos no se igualan a los mínimos registrados después de dichos periodos (Fig. 3).
El factor de condición presentó valores altos en mayo y junio tanto en hembras (1.17 y 1.19) como en machos (1.22 y 1.23), ocurriendo en la temporada no reproductiva (Fig. 3). Los valores promedios del FC presentaron diferencia significativa de manera temporal tanto en hembras (F=4.57, p<0.05), como en machos (F=5.34, p<0.05), los promedios variaron entre 1.09 y 1.19 en las hembras, y de 1.08 a 1.23 en los machos. Se presentó correlación positiva significativa entre los valores promedio mensuales del IGS de hembras y del IGS de machos (rs=0.916, p=0.000028) y entre los valores promedio mensuales del FC de hembras y del FC de machos (rs=0.741, p=0.0058), pero no se encontró correlación entre el IGS y el FC entre hembras (rs=0.011, p=0.834) y machos (rs=0.047, p=0.430).
Descripción microscópica de las gónadas: Los ovarios están envueltos por una túnica que penetra en el ovario formando lamelas ovígeras. En el interior del ovario se observaron ovocitos en diferentes grados de desarrollo por lo que se puede considerar que L. inermis presenta un desarrollo asincrónico (Fig. 4). Se identificaron siete fases de desarrollo de los ovocitos: 1) ovocitos cromatina nucléolo con diámetro promedio de 57.1±0.54μm, se caracterizan por tener poco citoplasma y un núcleo grande con nucléolos; 2) en perinucléolo con diámetro de 81.5±2.40μm, los nucléolos se observan en la periferia del núcleo; 3) con vesículas vitelinas con diámetro promedio de 133.5±2.50μm, en el citoplasma se forman gotas de aceite, con ellos se inicia la formación de vitelo; 4) en vitelogénesis primaria el diámetro promedio fue de 236.7±2.95μm, se observan glóbulos de vitelo en el citoplasma; 5) en vitelogénesis secundaria con diámetro de 304.4±3.59μm, en todo el citoplasma se encuentran glóbulos de vitelo; 6) vitelogénesis terciaria diámetro de 321.2±7.13μm, los glóbulos de vitelo se empiezan a fusionar y el núcleo se encuentra en proceso de migración hacia el polo animal y 7) maduros con diámetro de 334.7±13.34μm, vitelo completamente fusionado, no se observa el núcleo.
El interior de los testículos se encuentra organizado por lóbulos, los cuales están formados por varios cistos dentro de los cuales se lleva a cabo la espermatogénesis. Una vez formados los espermatozoides son liberados al interior del lóbulo y posteriormente se agrupan en el conducto receptor para ser expulsados. A este tipo de organización que tienen las células del testículo se le denomina desarrollo lobular.
En las gónadas en estadio inmaduro (Figs. 4A, 5A), se observaron principalmente ovocitos en cromatina nucléolo y en perinucléolo y en los machos el testículo presentó cistos con poco desarrollo celular y el conducto receptor libre de espermatozoides. En el estadio en maduración (Figs. 4B, 5B), los ovarios presentan ovocitos cromatina nucléolo, en perinucléolo, con vesículas vitelinas, vitelogénesis primaria y pocos en vitelogénesis secundaria y los testículos presentan desarrollo celular en los cistos y espermatozoides en el conducto receptor. En el estadio maduro (Figs. 4C, 5C), el ovario está constituido principalmente por ovocitos en vitelogénesis secundaria, pero se pueden identificar otras fases como en cromatina nucléolo, perinucléolo, vesículas vitelinas y vitelogénesis primaria. Por su parte, el testículo presenta una gran cantidad de espermatozoides en el conducto receptor. El estadio desovado (Figs. 4D, 5D) presenta en el ovario ovocitos en cromatina nucléolo y algunos en vitelogénesis secundaria, y en el testículo se observan cistos semivacíos y pocos espermatozoides en el conducto receptor.
Talla de maduración sexual (L50): La hembra y el macho más pequeños con gónadas maduras fueron de 20.1 y 21.3cm LT, respectivamente. Por su parte, los organismos más grandes con gónadas inmaduras fueron de 27.0cm LT, la hembra y 26.6cm LT, el macho. Considerando las frecuencias relativas acumuladas, se encontró que las hembras con talla promedio de 28.2cm, representaron el 99.1% del total de hembras maduras y los machos con talla promedio de 27.4cm representaron el 97.3% del total de machos maduros. La longitud de madurez sexual (L50) calculada utilizando todos los individuos muestreados fue de 23.9cm LT para las hembras y 23.6cm LT para los machos (Fig. 6).
Discusión
El intervalo de longitud que se obtuvo en el presente trabajo (14.4 a 37.0cm LT), es similar al reportado por Espino-Bar et al. (2004) para la costa de Jalisco (18.6 a 37.3cm LT). La longitud máxima reportada por Amezcua- Linares (1996) y Allen & Robertson (1998) en el Pacífico oriental tropical, es inferior (35.0cm LT) a la encontrada en el presente trabajo. La talla promedio encontrada por Espino-Bar et al. (2004), es similar (27.7cm LT) a la observada en el presente trabajo (27.8cm LT). Esta coincidencia puede deberse a que los organismos muestreados para ambos casos provinieron de la pesca comercial.
Un aspecto importante en la reproducción de los peces es la proporción de hembras y machos que integran una población. Se encontró diferencia significativa en la distribución de tallas (32-33.9cm), en donde se observó un mayor número de hembras que machos, como lo mencionan varios autores en otras especies, esto puede estar ligado a varios aspectos como la supervivencia, la distribución y preferencia del hábitat, la profundidad, la distribución de tallas, o bien en los aspectos alimenticios y reproductivos (Nikolsky 1963, Rojas et al. 2004, Piñón et al. 2009).
El periodo reproductivo de L. inermis, descrito en el presente estudio (febrero-abril y septiembre-noviembre) constituye el primer reporte sobre este aspecto de la biología de la especie, autores como Sánchez-Cárdenas et al. (2007), mencionaron que el IGS es un buen indicador del periodo reproductivo, además ha sido utilizado para establecer dichos periodos en diversas especies (González & Oyarzún 2002, Palomera-Sánchez 2004, Lucano-Ramírez et al. 2006, Piñón et al. 2009). El IGS y el FC no están correlacionados entre sí en L. inermis, este mismo resultado también se encontró en las especies Holacanthus passer (Arellano-Martínez & Ceballos-Vázquez 2001) y en Pinguipes chilensis (González & Oyarzún 2002). Esto puede deberse a que el FC está relacionado con la condición fisiológica y requerimientos energéticos de un pez, tal como se detectó en el bacalao del Atlántico. Además, el FC presenta independencia de la energía almacenada en la producción de ovocitos (González & Oyarzún 2002).
El desove asincrónico (parcial o fraccionado) que presentó L. inermis es similar al que presentan otras especies que se distribuyen en regiones tropicales y subtropicales como Scomberomorus sierra (Palomera-Sánchez 2004), Pseudupeneus grandisquamis (Lucano- Ramírez et al. 2006) y Diodon holocanthus (Lucano-Ramírez et al. 2011); en contraste con el mostrado por los peces de las regiones templadas, los cuales tienen periodos cortos, desove total y desarrollo de la gónada sincrónico (Nikolsky 1963, Granados-Lorencio 2002). Los peces que presentan desarrollo asincrónico, como en el caso de L. inermis, por lo general desovan en varias ocasiones en una temporada reproductiva prolongada (Nagahama et al. 1995, Maack & George 1999) y los ovarios contienen ovocitos en diferentes fases de desarrollo.
En el presente trabajo, como en otros realizados en la región (Palomera-Sánchez 2004, Lucano-Ramírez et al. 2001a, 2006, 2011), se han identificado de cinco a siete fases de desarrollo de los ovocitos los cuales representan la vitelogénesis como tal. González et al. (1979) describieron cinco fases del desarrollo de los ovocitos en la especie Lutjanus griseus. Según los autores, las fases de la I a la IV, son no maduras, las cuales se observaron en organismos capturados en el medio natural, mientras que la fase V (ovocitos maduros), se observó sólo en hembras tratadas con la hormona GCH.
Microscópicamente el testículo de L. inermis presentó el desarrollo de tipo lobular, coincidiendo con lo descrito para L. peru (Lucano-Ramírez et al. 2001b), P. grandisquamis (Lucano-Ramírez et al. 2006) y Diodon holocanthus (Lucano-Ramírez et al. 2011) en la costa sur de Jalisco.
La talla de madurez (L50) fue similar en ambos sexos y constituyen los primeros reportes de este parámetro para L. inermis, cabe resaltar que la L50, es inferior a la talla promedio del total de organismos capturados y a las tallas promedio encontradas en los distintos años de muestreo, por lo tanto podemos inferir que cerca o mas del 50% de los organismos ya se habían reproducido por lo menos una vez.
Agradecimientos
Los autores agradecen a Daniel Kosonoy, Gerardo Kosonoy y Manuel Díaz por su ayuda en la realización de las actividades de pesca. A las cooperativas “Rivera Melaque” y “Punta Farallón” por facilitarnos sus instalaciones. A la Universidad de Guadalajara por financiar el proyecto “Reproducción de los peces de la familia Lutjanidae colectados en el Pacífico tropical mexicano” y a los estudiantes del Departamento de Estudios para el Desarrollo Sustentable de Zonas Costeras, que colaboraron en los muestreos.
Referencias
Allen, G.R. & D.R. Robertson. 1998. Peces del Pacífico oriental tropical. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad y Agrupación Sierra Madre, México, D.F., México. [ Links ]
Amezcua-Linares, F. 1996. Peces demersales de la plataforma continental del Pacífico Central de México. Instituto de Ciencias de Mar y Limnología, UNAM, Comisión Nacional para el Conocimiento y Uso de la Biodiversidad, México, D.F., México. [ Links ]
Arellano-Martínez, M. & B.P. Ceballos-Vázquez. 2001. Reproductive activity and condition index of Holacanthus passer (Teleostei: Pomacanthidae) in the Gulf of California, México. Rev. Biol. Trop. 49: 939-943 (También disponible en línea: http://www.scielo.sa.cr/scielo.php?script=sci_arttext&pid=S0034-77442001000300013&lng=es&nrm=iso&tlng=en). [ Links ]
Cerisola, H. 1984. Cambios estructurales del folículo ovárico durante su maduración en el pejesapo Sicyases sanguineus, Muller y Troschel 1843. (Gobiescocidae: Teleostei). Rev. Biol. Mar., Valparaíso 20: 1-21. [ Links ]
Echeverria, W.T. 1987. Thirty-four species of California rockfishes: maturity and seasonality of reproduction. Fish. Bull. 85: 229-250. [ Links ]
Espino-Barr, E., E.G. Cabral-Solís, A. García-Boa & M. Puente-Gómez. 2004. Especies marinas con valores comerciales de la costa de Jalisco, México. CRIP, Manzanillo, México. [ Links ]
Everson, A.R., H.A. Williams & B.M. Ito. 1989. Maturation and reproduction in two Hawaiian eteline snappers, uku, Aprion virescens, and onaga, Etelis coruscans. Fish. Bull. 87: 877-888. [ Links ]
Granados-Lorencio, C. 2002. Ecología de peces. Secretariado de publicaciones. Universidad de Sevilla, España. [ Links ]
González, E., T. Damas, N. Millares & M. Borrero. 1979. Desove inducido en el caballerote (Lutjanus griseus Linné, 1758) en condiciones de laboratorio. Rev. Cub. Inv. Pesq. 4: 43-63. [ Links ]
González, P. & C. Oyarzún. 2002. Variabilidad de índices biológicos en Pinguipes chilensis Valenciennes 1833 (Perciformes, Pinguipedidae): ¿Estan realmente correlacionados? Gayana, 66: 249-253. [ Links ]
Hyder, M. 1969. Histological studies on the testis of tilapia leucosticta and other species of the genus Tilapia (Pisces:Teleostei). Trans. Amer. Microsc. Soc. 88: 211-231. [ Links ]
Lucano-Ramírez, G., E. Peña-Pérez, S. Ruiz-Ramírez, J.A. Rojo-Vázquez & G. González-Sansón. 2011. Aspectos reproductivos del pez erizo, Diodon holocanthus (Pisces: Diodontidae) en la plataforma continental del Pacífico Central Mexicano. Rev. Biol. Trop. 59: 217-232 (También disponible en línea: www.ots.ac.cr/tropiweb/intpages/vols/vol59-1.html). [ Links ]
Lucano-Ramírez, G., S. Ruiz-Ramírez & J.A. Rojo-Vázquez. 2006. Composición por tallas y ciclo reproductivo de Pseudupeneus grandisquamis (Pisces: Mullidae) en el Pacífico central Mexicano. Rev. Biol. Trop. 54: 195-207 (También disponible en línea: www.ots.ac.cr/tropiweb/attachments/volumes/vol54-1/20-LUCANO-Composici.pdf). [ Links ]
Lucano-Ramírez, G., M. Villagrán-Santa Cruz, S. Ruiz-Ramírez & M.T. López-Trujillo. 2001a. Histología de los ovocitos de Lutjanus peru (Nichols y Murphy, 1922) (Pisces: Lutjanidae). Cienc. Mar. 3: 335-349 (También disponible en línea: redalyc.uaemex.mx/redalyc/html/480/48027302/48027302.html). [ Links ]
Lucano-Ramírez, G., M. Villagrán-Santa Cruz & S. Ruiz- Ramírez. 2001b. Cambios estructurales en las gónadas de Lutjanus peru (Pisces:Lutjanidae), en la Costa sur de Jalisco, México. Bol. Centro Invest. Biol. 35: 295-316. [ Links ]
Maack, G. & M.R. George. 1999. Contributions to the reproductive biology of Encrasicholina punctifer Fowler, 1938 (Engraulidae) from West Sumatra, Indonesia. Fish. Research 44: 113-120. [ Links ]
Nagahama, Y., M. Yoshikuni, T. Yamashita, M. Tokumoto & Y. Katsu. 1995. Regulation of oocyte growth and maturation in fish. Current Topics Develop. Biol. 30: 103-145. [ Links ]
Nikolsky, G. 1963. The ecology of fishes. Academic, Londres, Inglaterra. [ Links ]
Palomera-Sánchez, F.I. 2004. Características reproductivas de Scomberomorus sierra Jordan y Starks 1895 (Pisces: Scombridae) en Bahía Navidad, Jalisco, México. Tesis de Licenciatura, Universidad de Guadalajara, México. [ Links ]
Piñón, A., F. Amezcua & N. Duncan. 2009. Reproductive cycle of female yellow snapper Lutjanus argentiventris (Pisces, Actinopterygii, Lutjanidae) in the SW Gulf of California: gonadic stages, spawning seasonality and length at sexual maturity. J. Appl. Ichthyol. 25: 18-25. [ Links ]
Rojas, P.A., F.C. Gutiérrez & V. Puentes. 2004. Aspectos de la biología y dinámica poblacional del pargo coliamarillo Lutjanus argentiventris en el Parque Nacional Natural Gorgona, Colombia. Invest. Mar. Valparaíso 32: 23-36. [ Links ]
Rojo-Vázquez, J.A., C. Quiñonez-Velázquez, H.A. Echavarria-Heras, G. Lucano-Ramírez, E. Godínez- Domínguez, S. Ruiz-Ramírez, V.H. Galván-Piña & O. Sosa-Nishizaki. 2008. The fish species composition and variation of catch from the small-scale gillnet fishery before, during and after the 1997-1998 ENSO event, central Mexican Pacific. Rev. Biol. Trop. 56:133-152 (También disponible en línea: www.biologiatropical.ucr.ac.cr/attachments/volumes/vol56-1/09-Rojo-Fish.pdf). [ Links ]
Rojo-Vázquez, J.A., G. Lucano-Ramírez & S. Ruiz- Ramírez. 2009. Length-Weight relationships for coastal fish species from the gillnet artisanal fishery in the central Mexican Pacific. J. Appl. Ichthyol. 25: 497-498. [ Links ]
Sánchez-Cárdenas, R., B.P. Ceballos-Vázquez, M. Arellano-Martínez, M.C. Valdez-Pineda & R.E. Morán-Angulo. 2007. Reproductive aspects of Sphoeroides annulatus (Jenyns, 1842) (Tetraodontiformes, Tetraodontidae) inhabiting the Mazatlan coast, Sinaloa, Mexico. Rev. Biol. Mar. Oceanogr. 42: 385-392. [ Links ]
Tavera, J.J. & J. De la Cruz-Agüero. 2006. Rediscovery of the golden snapper Lutjanus inermis (Peters, 1869) (Perciformes: Lutjanidae) in the gulf of California. Ocean Sci. J. 41: 191-193. [ Links ]
Vitale, F., H. Svedäng & M. Cardinale. 2006. Histological analysis invalidates macroscopically determined maturity ogives of the Kattegat cod (Gadus morhua) and suggests new proxies for estimating maturity status of individual fish. J. Mar. Sci. 63: 485-492. [ Links ]
Yamamoto, K. & M. Yamazaki. 1961. Rhythm of development in the oocyte of the gold-fish, Carassius auratus. Bull. Fac. Fish. Hokkaido Univ. 12: 93-114. [ Links ]
Zar, J.H. 2010. Biostatistical analysis. Prentice Hall, Nueva Jersey, EEUU. [ Links ]
*Correspondencia a: Gabriela Lucano-Ramírez, Salvador Ruiz-Ramírez & Gaspar González-Sansón: Departamento de Estudios para el Desarrollo Sustentable de Zonas Costeras, Universidad de Guadalajara, V. Gómez Farias 82, San Patricio-Melaque, Jalisco, México, CP 48980; lucanorg@costera.melaque.udg.mx, sruizram@costera.melaque.udg.mx, gaspargonzalez2001@yahoo.es
Bertha Patricia Ceballos-Vázquez: Laboratorio de Invertebrados Marinos, Centro Interdisciplinario de Ciencias Marinas, Instituto Politécnico Nacional, Apartado Postal 592, 23000, La Paz, Baja California Sur, México; bceballo@ipn.mx
1. Departamento de Estudios para el Desarrollo Sustentable de Zonas Costeras, Universidad de Guadalajara, V. Gómez Farias 82, San Patricio-Melaque, Jalisco, México, CP 48980; lucanorg@costera.melaque.udg.mx, sruizram@costera.melaque.udg.mx, gaspargonzalez2001@yahoo.es
2. Laboratorio de Invertebrados Marinos, Centro Interdisciplinario de Ciencias Marinas, Instituto Politécnico Nacional, Apartado Postal 592, 23000, La Paz, Baja California Sur, México; bceballo@ipn.mx
Allen, G.R. & D.R. Robertson. 1998. Peces del Pacífico oriental tropical. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad y Agrupación Sierra Madre, México, D.F., México. [ Links ]
Amezcua-Linares, F. 1996. Peces demersales de la plataforma continental del Pacífico Central de México. Instituto de Ciencias de Mar y Limnología, UNAM, Comisión Nacional para el Conocimiento y Uso de la Biodiversidad, México, D.F., México. [ Links ]
Arellano-Martínez, M. & B.P. Ceballos-Vázquez. 2001. Reproductive activity and condition index of Holacanthus passer (Teleostei: Pomacanthidae) in the Gulf of California, México. Rev. Biol. Trop. 49: 939-943 (También disponible en línea: http://www.scielo.sa.cr/scielo.php?script=sci_arttext&pid=S0034-77442001000300013&lng=es&nrm=iso&tlng=en). [ Links ]
Cerisola, H. 1984. Cambios estructurales del folículo ovárico durante su maduración en el pejesapo Sicyases sanguineus, Muller y Troschel 1843. (Gobiescocidae: Teleostei). Rev. Biol. Mar., Valparaíso 20: 1-21. [ Links ]
Echeverria, W.T. 1987. Thirty-four species of California rockfishes: maturity and seasonality of reproduction. Fish. Bull. 85: 229-250. [ Links ]
Espino-Barr, E., E.G. Cabral-Solís, A. García-Boa & M. Puente-Gómez. 2004. Especies marinas con valores comerciales de la costa de Jalisco, México. CRIP, Manzanillo, México. [ Links ]
Everson, A.R., H.A. Williams & B.M. Ito. 1989. Maturation and reproduction in two Hawaiian eteline snappers, uku, Aprion virescens, and onaga, Etelis coruscans. Fish. Bull. 87: 877-888. [ Links ]
Granados-Lorencio, C. 2002. Ecología de peces. Secretariado de publicaciones. Universidad de Sevilla, España. [ Links ]
González, E., T. Damas, N. Millares & M. Borrero. 1979. Desove inducido en el caballerote (Lutjanus griseus Linné, 1758) en condiciones de laboratorio. Rev. Cub. Inv. Pesq. 4: 43-63. [ Links ]
González, P. & C. Oyarzún. 2002. Variabilidad de índices biológicos en Pinguipes chilensis Valenciennes 1833 (Perciformes, Pinguipedidae): ¿Estan realmente correlacionados? Gayana, 66: 249-253. [ Links ]
Hyder, M. 1969. Histological studies on the testis of tilapia leucosticta and other species of the genus Tilapia (Pisces:Teleostei). Trans. Amer. Microsc. Soc. 88: 211-231. [ Links ]
Lucano-Ramírez, G., E. Peña-Pérez, S. Ruiz-Ramírez, J.A. Rojo-Vázquez & G. González-Sansón. 2011. Aspectos reproductivos del pez erizo, Diodon holocanthus (Pisces: Diodontidae) en la plataforma continental del Pacífico Central Mexicano. Rev. Biol. Trop. 59: 217-232 (También disponible en línea: www.ots.ac.cr/tropiweb/intpages/vols/vol59-1.html). [ Links ]
Lucano-Ramírez, G., S. Ruiz-Ramírez & J.A. Rojo-Vázquez. 2006. Composición por tallas y ciclo reproductivo de Pseudupeneus grandisquamis (Pisces: Mullidae) en el Pacífico central Mexicano. Rev. Biol. Trop. 54: 195-207 (También disponible en línea: www.ots.ac.cr/tropiweb/attachments/volumes/vol54-1/20-LUCANO-Composici.pdf). [ Links ]
Lucano-Ramírez, G., M. Villagrán-Santa Cruz, S. Ruiz-Ramírez & M.T. López-Trujillo. 2001a. Histología de los ovocitos de Lutjanus peru (Nichols y Murphy, 1922) (Pisces: Lutjanidae). Cienc. Mar. 3: 335-349 (También disponible en línea: redalyc.uaemex.mx/redalyc/html/480/48027302/48027302.html). [ Links ]
Lucano-Ramírez, G., M. Villagrán-Santa Cruz & S. Ruiz- Ramírez. 2001b. Cambios estructurales en las gónadas de Lutjanus peru (Pisces:Lutjanidae), en la Costa sur de Jalisco, México. Bol. Centro Invest. Biol. 35: 295-316. [ Links ]
Maack, G. & M.R. George. 1999. Contributions to the reproductive biology of Encrasicholina punctifer Fowler, 1938 (Engraulidae) from West Sumatra, Indonesia. Fish. Research 44: 113-120. [ Links ]
Nagahama, Y., M. Yoshikuni, T. Yamashita, M. Tokumoto & Y. Katsu. 1995. Regulation of oocyte growth and maturation in fish. Current Topics Develop. Biol. 30: 103-145. [ Links ]
Nikolsky, G. 1963. The ecology of fishes. Academic, Londres, Inglaterra. [ Links ]
Palomera-Sánchez, F.I. 2004. Características reproductivas de Scomberomorus sierra Jordan y Starks 1895 (Pisces: Scombridae) en Bahía Navidad, Jalisco, México. Tesis de Licenciatura, Universidad de Guadalajara, México. [ Links ]
Piñón, A., F. Amezcua & N. Duncan. 2009. Reproductive cycle of female yellow snapper Lutjanus argentiventris (Pisces, Actinopterygii, Lutjanidae) in the SW Gulf of California: gonadic stages, spawning seasonality and length at sexual maturity. J. Appl. Ichthyol. 25: 18-25. [ Links ]
Rojas, P.A., F.C. Gutiérrez & V. Puentes. 2004. Aspectos de la biología y dinámica poblacional del pargo coliamarillo Lutjanus argentiventris en el Parque Nacional Natural Gorgona, Colombia. Invest. Mar. Valparaíso 32: 23-36. [ Links ]
Rojo-Vázquez, J.A., C. Quiñonez-Velázquez, H.A. Echavarria-Heras, G. Lucano-Ramírez, E. Godínez- Domínguez, S. Ruiz-Ramírez, V.H. Galván-Piña & O. Sosa-Nishizaki. 2008. The fish species composition and variation of catch from the small-scale gillnet fishery before, during and after the 1997-1998 ENSO event, central Mexican Pacific. Rev. Biol. Trop. 56:133-152 (También disponible en línea: www.biologiatropical.ucr.ac.cr/attachments/volumes/vol56-1/09-Rojo-Fish.pdf). [ Links ]
Rojo-Vázquez, J.A., G. Lucano-Ramírez & S. Ruiz- Ramírez. 2009. Length-Weight relationships for coastal fish species from the gillnet artisanal fishery in the central Mexican Pacific. J. Appl. Ichthyol. 25: 497-498. [ Links ]
Sánchez-Cárdenas, R., B.P. Ceballos-Vázquez, M. Arellano-Martínez, M.C. Valdez-Pineda & R.E. Morán-Angulo. 2007. Reproductive aspects of Sphoeroides annulatus (Jenyns, 1842) (Tetraodontiformes, Tetraodontidae) inhabiting the Mazatlan coast, Sinaloa, Mexico. Rev. Biol. Mar. Oceanogr. 42: 385-392. [ Links ]
Tavera, J.J. & J. De la Cruz-Agüero. 2006. Rediscovery of the golden snapper Lutjanus inermis (Peters, 1869) (Perciformes: Lutjanidae) in the gulf of California. Ocean Sci. J. 41: 191-193. [ Links ]
Vitale, F., H. Svedäng & M. Cardinale. 2006. Histological analysis invalidates macroscopically determined maturity ogives of the Kattegat cod (Gadus morhua) and suggests new proxies for estimating maturity status of individual fish. J. Mar. Sci. 63: 485-492. [ Links ]
Yamamoto, K. & M. Yamazaki. 1961. Rhythm of development in the oocyte of the gold-fish, Carassius auratus. Bull. Fac. Fish. Hokkaido Univ. 12: 93-114. [ Links ]
Zar, J.H. 2010. Biostatistical analysis. Prentice Hall, Nueva Jersey, EEUU. [ Links ]
*Correspondencia a: Gabriela Lucano-Ramírez, Salvador Ruiz-Ramírez & Gaspar González-Sansón: Departamento de Estudios para el Desarrollo Sustentable de Zonas Costeras, Universidad de Guadalajara, V. Gómez Farias 82, San Patricio-Melaque, Jalisco, México, CP 48980; lucanorg@costera.melaque.udg.mx, sruizram@costera.melaque.udg.mx, gaspargonzalez2001@yahoo.es
Bertha Patricia Ceballos-Vázquez: Laboratorio de Invertebrados Marinos, Centro Interdisciplinario de Ciencias Marinas, Instituto Politécnico Nacional, Apartado Postal 592, 23000, La Paz, Baja California Sur, México; bceballo@ipn.mx
1. Departamento de Estudios para el Desarrollo Sustentable de Zonas Costeras, Universidad de Guadalajara, V. Gómez Farias 82, San Patricio-Melaque, Jalisco, México, CP 48980; lucanorg@costera.melaque.udg.mx, sruizram@costera.melaque.udg.mx, gaspargonzalez2001@yahoo.es
2. Laboratorio de Invertebrados Marinos, Centro Interdisciplinario de Ciencias Marinas, Instituto Politécnico Nacional, Apartado Postal 592, 23000, La Paz, Baja California Sur, México; bceballo@ipn.mx
Recibido 04-II-2011. Corregido 12-V-2011. Aceptado 14-VI-2011.














