Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.59 n.4 San José Dec. 2011
Reproducción de Joturus pichardi y Agonostomus monticola(Mugiliformes: Mugilidae) en ríos de la Sierra Nevada de Santa Marta, Colombia
Pedro Eslava Eljaiek1 & Roy Díaz Vesga2
1. Programa de Ingeniería Pesquera, Universidad del Magdalena, Carrera 32 No. 22-08 Santa Marta, Magdalena, Colombia; ingpesqueraunimagdalena@gmail.com2. Laboratorio de Investigaciones Pesqueras Tropicales, Universidad del Magdalena, Carrera 32 No. 22-08 Santa Marta, Magdalena, Colombia; rdiazvesga@gmail.com
Abstract
Key words: mugilids, Joturus pichardi, Agonostomus monticola, reproductive biology, Sierra Nevada de Santa Marta, Colombia.
Resumen
Para los mugílidos de agua dulce Joturus pichardi y Agonostomus monticola se han documentado aspectos ecológicos y de distribución, principalmente para las poblaciones de América Central, sin embargo, hay poca información disponible de sus aspectos reproductivos, especialmente en ambientes de agua dulce de Colombia. Por lo tanto para ambas especies se estudió la biología reproductiva en ríos de la Sierra Nevada de Santa Marta durante julio de 2005 y diciembre de 2006. En total, 14 especímenes de J. pichardi y 320 A. monticola fueron capturados. Proporción sexual, índice gonadosomático, talla media de madurez, fecundidad y diámetros de los ovocitos fueron evaluados. Se realizó un bioensayo para observar el efecto de la salinidad sobre la movilidad espermática y su posible relación con el área de desove de las especies. Estos mugílidos comparten un hábitat con características ecológicas similares, de corrientes fuertes y claras y zonas pedregosas. Indicadores de madurez gonadal y evidencias indirectas son presentados y con los cuales se comprueba que el periodo reproductivo se encuentra relacionado con los mayores valores de precipitación de la zona (septiembre a noviembre), así como, la migración catádroma de J. pichardi y A. monticola. Estas especies representan un potencial de cultivo, dado su alimentación basada en vegetales y macroinvertebrados, la calidad de su carne y las tallas que pueden alcanzar, por lo cual, se deben efectuar estudios más profundos que revelen mayor información sobre su comportamiento y reproducción en cautividad.
Palabras clave: mugílidos, Joturus pichardi, Agonostomus monticola, biología reproductiva, Sierra Nevada de Santa Marta, Colombia.
La Sierra Nevada de Santa Marta, declarada por la UNESCO Reserva del Hombre y la Biosfera en 1986, es la formación montañosa litoral más alta del mundo (FPSNSM 1997). En ella, existe una amplia variedad de especies ícticas, muchas de las cuales hacen parte de la pesca de subsistencia de sus habitantes que en su mayoría son campesinos e indígenas. De estas especies, Joturus pichardi y Agonostomus monticola (conocidos por las comunidades locales como "besote" y "rayado", respectivamente), presentan una muy buena preferencia de pesca, debido a las buenas características organolépticas de su carne (Eslava 2009) y las tallas que alcanzan en el medio; considerados peces muy populares entre los pescadores fluviales (Garzón & Wedler 1997).
J. pichardi y A. monticola son peces dulceacuícolas que pertenecen a la Familia Mugilidae, la cual incluye generalmente especies marinas y estuarinas (Harrison 2002). Estas dos especies habitan las partes cálidas de los ríos montañosos, donde se presentan corrientes fuertes, grandes rocas y aguas claras y al parecer requieren del agua marina en los estados iniciales de su ciclo de vida (Cruz 1987, Garzón & Wedler 1997).
Materiales y métodos
La identificación taxonómica de las especies se realizó con base en las claves de Harrison (2002). Cada ejemplar fue evaluado morfométricamente así: longitud total (LT), longitud horquilla (LH) y longitud estándar (LS), al milímetro más cercano con un ictiómetro convencional, y el peso total (WT) al gramo más cercano con una balanza electrónica con capacidad de 2 000g (±1g). Para el análisis de los ejemplares capturados, los peces fueron eviscerados y las gónadas se separaron del resto de órganos, registrándose fecha, sitio de captura, sexo, peso eviscerado, peso de las gónadas y estado de madurez sexual de acuerdo con la escala de Vazzoler (1996). Para el caso del peso de las gónadas se utilizó una balanza analítica con precisión de ±0.001g.
Estimación de la proporción sexual: La proporción sexual total y mensual se estimó de acuerdo con la ecuación:
% hembras= 100*(Nm/Nt),
donde Nm es el número hembras y Nt es el número total de individuos.
La proporción sexual fue expresada como el número de hembras por cada macho. La proporción sexual a la talla se calculó con la técnica de Holden & Raitt (1975) utilizando intervalos de clase de 20mm.
Índice gonadosomático (IGS): Se estimó con base en las ecuaciones de Vazzoler (1996) y Tresierra & Culquichicón (1993), y fue graficado en función del mes de muestreo:
IGS1=100*(WG/WT),
donde WG es el peso de las gónadas y WT es el peso total del pez.
IGS2=100*(WG/WE),
donde WE es el peso eviscerado del pez. Este índice se conoce como gonadosomático corregido.
Estimación de las tallas de madurez sexual: La talla media de madurez sexual fue estimada separadamente para hembras y machos, a través de la curva que relaciona la frecuencia relativa de individuos adultos por clase de longitud total, según Sparre & Venema (1995) y ajustada a la ecuación planteada en Andrade (1998):
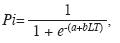
donde Pi es la frecuencia relativa de individuos maduros, e la base del logaritmo neperiano, a y b los coeficientes estimados por el método de mínimos cuadrados y LT la longitud total.
Diámetro de ovocitos maduros: Por medio de un microscopio de luz con reglilla micrométrica se midió el diámetro de los ovocitos de muestras de gónadas maduras. Los valores fueron expresados como la media ± desviación estándar.
Estimación de la fecundidad: Luego de pesadas las gónadas, se tomaron submuestras de cada una de ellas (0.12-0.25g) y se guardaron en frascos rotulados, los cuales contenían solución de Gilson. La fecundidad total (F) se estimó aplicando el método gravimétrico (Vazzoler 1996) a partir de la siguiente ecuación:
F=nG/g,
donde n es el número de ovocitos maduros en la muestra, G es el peso de todos los ovocitos y g es el peso de la muestra. También se estimó la fecundidad relativa con respecto a la talla, peso del pez y peso de las gónadas.
Área de desove: Se realizaron muestreos en la parte baja de los ríos Toribio y Piedras y en su desembocadura, con el fin de capturar ejemplares maduros en estas zonas dado su comportamiento catádromo (Anderson 1957, Cruz 1987, 1989, Phillip 1993, Ditty & Shaw 1996, Aiken 1998).
Efecto de la salinidad sobre la activación de espermatozoides de J. pichardi y A. montícola y su relación con el área de desove: Un bioensayo piloto se realizó para observar el efecto de la salinidad sobre la movilidad espermática y su posible relación con el área de desove de las especies de estudio. Para ello, se utilizaron cuatro individuos maduros (con liberación de esperma a una leve presión en el abdomen) de J. pichardi (un individuo) y A. monticola (tres individuos). Los especímenes fueron mantenidos vivos en el Centro de Desarrollo Pesquero y Acuícola de Taganga de la Universidad del Magdalena, registrando su talla y peso. Los animales ayunaron 24h para evitar contaminación de las muestras de semen. Para los ensayos en laboratorio, se utilizaron soluciones activadoras distribuidas en salinidades de 0, 10, 20, 30 y 36 (agua de mar) UPS (unidades prácticas de salinidad), que se obtuvieron a partir de una dilución de agua de mar filtrada con agua destilada. Para la extracción de las muestras de semen de los ejemplares analizados se siguió la metodología propuesta en González & Díaz (2001). Sobre cada salinidad experimental, con un cronómetro digital se registró el tiempo de activación espermática en segundos desde el momento en que el activador y la gota de semen entraron en contacto hasta que la mayoría de los espermatozoides cesaron el movimiento o presentaron un leve temblor (Cruz-Casallas 2001, González & Díaz 2001). Sumado a ello, se registraron la motilidad espermática, estimación del número de espermatozoides por conteo en cámara Neubauer, prueba de viabilidad con tinción Eosina-Nigrosina, coloración y viscosidad (Rodríguez 1992, Cruz-Casallas 2001) sobre las muestras de semen evaluadas.
Se utilizó estadística descriptiva y las variables fueron expresadas como promedio±desviación estándar. Se estimó la relación entre las variables LT vs F, WT vs F y WG vs F, al igual que los coeficientes de correlación para cada una de ellas. Se utilizó un análisis de varianza a una vía (previa comprobación de los supuestos de normalidad de los datos y homogeneidad de varianzas usando la prueba de Levene) para verificar diferencias entre los estados de maduración de los indicadores IGS1 e IGS2 y entre los tiempos de activación espermática y motilidad evaluados a partir del efecto de salinidad sobre las muestras de semen. Cuando existieron diferencias estadísticas significativas en el ANOVA, se efectuó una prueba post-hoc empleando el test de Tukey para establecer entre cuales tratamientos se presentaron los contrastes. Para comprobar si la proporción sexual estimada se ajustaba a la esperada, se aplicó la prueba G (Zar 1996). Para llevar a cabo los diferentes procedimientos estadísticos se utilizaron los software SPSS© versión 11.5 y Statgraphics Plus© versión 4.0. En los análisis se empleó un nivel de confianza del 95%.
Resultados
Durante el periodo de estudio, las variables fisicoquímicas no sufrieron variaciones relevantes. Sin embargo, los altos valores registrados, principalmente en la conductividad y caudal, estuvieron relacionados con los mayores valores de pluviosidad de la zona. Los rangos de los parámetros fisicoquímicos medidos en los sitios muestreados durante el estudio son presentados en el Cuadro 1. J. pichardi y A. monticola prefieren aguas cristalinas, habitan los rápidos o zonas inmediatamente río abajo donde todavía la corriente es torrentosa y la velocidad es de moderada a fuerte.
Áreas de desove: No se logró la captura de ejemplares de J. pichardi durante los muestreos realizados entre la desembocadura y las partes baja próxima a esta zona, en los ríos de estudio en el periodo de septiembre, octubre y noviembre de 2005 y 2006. Especímenes de A. monticola fueron capturados en octubre y noviembre de 2006 en el área de desembocadura cercana a la zona de mezcla del río con el ecosistema marino, diez machos y cuatro hembras todos sexualmente maduros. Posterior a la captura en estas zonas del río, se verificó que los machos presentaron inmediata liberación de esperma con una leve presión abdominal y las hembras mostraron el enrojecimiento de la papila genital y abultamiento del abdomen.
Proporción sexual e índice gonadosomático: Durante el periodo de estudio, en total se capturaron 14 individuos de J. pichardi (tamaño de muestra no representativo) y 320 de A. monticola.
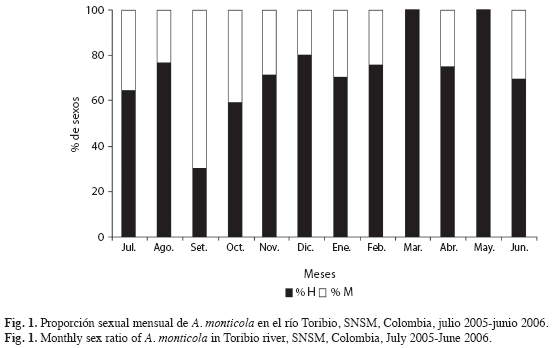
Para J. pichardi se registraron tallas y pesos que oscilaron entre 160 y 550mm de longitud total (LT) y 35.0 y 1 779.0g de peso total (WT). Nueve individuos fueron hembras, tres machos y dos indiferenciados. Se calculó una proporción sexual total de tres hembras: un macho. De los ejemplares analizados, las hembras presentaron las tallas más grandes en comparación con los machos. De A. monticola se obtuvieron tallas y pesos comprendidos en un rango de 45 y 312mm de longitud total (LT) y 1.0 y 275.0g de peso total (WT). Se presentaron 185 hembras, 81 machos y 54 indiferenciados. La proporción sexual total fue de 2.3 hembras: 1 macho (Gcal: 41.76, p<0.05, g.l.=1). Se observó predominancia de hembras a lo largo del estudio, salvo en septiembre cuando el número de machos sobrepasó el de las hembras (Gcal: 4.936, p<0.05, g.l.=1). Durante junio, julio y octubre, la proporción sexual fue similar a la esperada (1:1) (Fig. 1). La proporción sexual a la talla evidenció una predominancia de los machos con tamaños pequeños hasta el intervalo 97-117mm de LT y se observó ausencia de machos en tallas mayores de 200mm de LT.
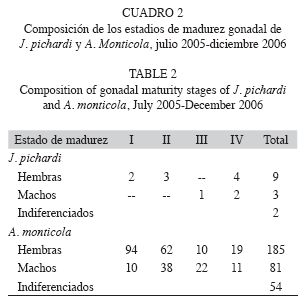
De los individuos de J. pichardi capturados que mostraron avanzado estado gonadal, se registró como menor talla el valor correspondiente a 484mm LT (389mm LS) para hembras y 251mm LT (208mm LS) en machos. El mayor registro fue de 550mm LT (436mm LS) y 451mm LT (356mm LS) en hembras y machos, respectivamente. El índice de madurez (IGS) osciló entre 0.16 y 5.19, este último correspondio a un individuo macho maduro de 208mm de LS (Cuadro 2).
Estimación de las tallas de madurez sexual: Debido a los escasos registros de J. pichardi, no se logró inferir la talla de madurez sexual de esta especie. Para A. monticola, la talla de inicio de madurez sexual (TIM) encontrada fue de 122mm en hembras y 76mm de LT en machos. La talla media de madurez sexual (TMM) fue estimada en 172mm de LT para hembras (Fig. 2A), en la cual las hembras adultas fueron el 49% del total de la muestra, mientras que para los machos fue 108mm LT (Fig. 2B), y la cantidad de machos adultos representó un 51% de la muestra total.
Diámetro de los ovocitos: En A. monticola se midieron 525 ovocitos, provenientes de gónadas maduras, con un diámetro que osciló entre 270 y 450μm, con un valor promedio de 362±40μm.
Efecto de la salinidad sobre la activación de espermatozoides y su relación con el área de desove: Los resultados sobre el individuo analizado de J. pichardi, mostraron que las variables tiempo de activación y motilidad espermática tuvieron los valores más bajos en los tratamientos 0, 10 y 30 UPS e inactividad con agua de mar (36 UPS). Sin embargo, el tratamiento con salinidad de 20 UPS se registró un mayor tiempo de activación (845s) y motilidad (90%).
No se registró movilidad espermática de A. monticola en el tratamiento de salinidad 0. En la salinidad de ensayo de 20 UPS se registraron los valores mayores para tiempo de activación y movilidad espermática con 535±116 segundos y 97±3% respectivamente. El análisis estadístico no reveló diferencias significativas entrelas salinidades 10, 20, 30 y 36 (p>0.05) para las variables evaluadas. Las características de semen para A. monticola fueron: 3 113±74x107 espermatozoides/mL, vitalidad de 87.5±10.5% (porcentaje de espermatozoides vivos), coloración espermática blanca y viscosidad de 3.4±0.6.
Discusión
Evidencias de la distribución en los sistemas fluviales que drenan al mar en Mesoamérica de J. pichardi (Bussing 1987, Cruz 1987, Cruz 1989) y A. monticola (también registrado en Venezuela, Florida e islas del Caribe y Galápagos) han sido ampliamente documentados (Cruz 1987, Phillips 1993, Ditty & Shaw 1996, Aiken 1998, Cotta-Ribeiro & Molina- Ureña 2009). En Colombia se ha comprobado la presencia J. pichardi y A. monticola en los ríos de la vertiente norte de la SNSM (Garzón & Wedler 1997), evidenciándose en los ríos de estudio, que J. pichardi y A. monticola, comparten un hábitat de similares características ecológicas, de corrientes fuertes y claras y zonas pedregosas, que complementan con la zona de desembocadura hacia el mar, en franjas estuarinas, que soportan de forma indirecta su condición migratoria. En relación a esto, Anderson (1957), registra la captura de larvas y pre-juveniles de A. monticola en el mar a un kilómetro de la costa, lo cual fue corroborado posteriormente por Ditty & Shaw (1996) al recolectar individuos de 3.6 a 25.5mm de LS mar afuera en el golfo de México. A la fecha, no existe evidencia que J. pichardi entre en el mar, sin embargo, en A. monticola los estudios consideran que la especie migra mar adentro para reproducirse (Ditty & Shaw 1996, Cruz 1987). En este estudio, esta conducta catádroma estuvo soportada por la captura de prejuveniles recolectados en los meses posteriores al proceso reproductivo, en el área de desembocadura del río e inclusive a pocos metros de mar (lugar conocido como "pluma").
A pesar de no observar dimorfismo sexual en ejemplares de J. pichardi, las hembras mostraron un mayor tamaño, coincidiendo con lo encontrado por Cruz (1987). Para A. monticola, Bussing (1987) comenta haber recolectado animales de coloración, tamaño y forma del labio diferente; es posible que en su momento estas características correspondieran a las diferencias entre sexos observadas en este trabajo. Al igual que en J. pichardi, la hembras de A. monticola presentaron una longitud mayor. Tal vez, una de las categorías más comunes de dimorfismo sexual en los peces sea la variación del tamaño del cuerpo. Para los mugílidos (e.g.: género Mugil), en general las hembras presentan mayor tamaño en relación con sus opuestos masculinos (Vazzoler 1996).
En lo relacionado con la biología reproductiva de las especies, se observó dominancia de hembras y mayores valores de longitud en J. pichardi, lo cual concuerda con Cruz (1987), en estudios sobre poblaciones hondureñas. El autor menciona que la proporción de hembras fue mayor para tallas superiores a 250mm de LS. Por otra parte, A. monticola, mostró una mayor proporción de hembras, lo cual es similar a lo reportado en Trinidad por Phillip (1993), quien registra una dominancia de hembras en tallas superiores a 100mm de LS y a su vez, difiere de lo encontrado por Aiken (1998), en Jamaica, quien señala una mayor proporción de machos. Vazzoler (1996), considera que en algunas especies de la familia Mugilidae, la relación sexual es varios machos por hembra, lo cual únicamente se evidenció durante los muestreos realizados en el mes de septiembre y en el análisis por tamaño en las tallas pequeñas (individuos menores de 118mm LT).Cruz (1987), establece que el periodo de precipitación máxima se encuentra relacionado con el proceso de reproducción en estas especies, lo cual se demostró en los registros de las dos especies estudiadas, observándose que el ciclo de desarrollo gonadal de J. pichardi ha finalizado en diciembre, etapa de post-desove, y que su periodo de desove osciló entre los meses de septiembre a noviembre, periodo con los valores más altos de precipitación para la zona (IDEAM 2005). Las tallas de las hembras de J. pichardi, en estado post-desove fueron similares a las anotadas en el trabajo de Cruz (1987) en Honduras y éstas presentaron también un mayor tamaño frente a los machos.
Por otro lado, Phillip (1993) en Trinidad, encuentra que el periodo de reproducción para A. monticola ocurre entre junio y octubre, coincidiendo también con la estación lluviosa de la zona. En Jamaica, Aiken (1998), estableció una estación de desove de mayo a julio, periodo que también se relaciona con la época lluviosa. Estas observaciones concuerdan con los resultados de este trabajo, mostrando una sincronía entre el periodo de mayor precipitación (septiembre a noviembre) (IDEAM 2005) y la época de desove de ambas especies.
Aiken (1998), registra una TIM para hembras y machos de A. monticola de 123 y 96mm LH, constituyéndose el valor de 72mm LH encontrado en este estudio en los machos, como un referente menor para las poblaciones examinadas. Mientras que en las hembras el resultado fue similar. La TMM de este trabajo se asemeja a lo registrado por Aiken (1998), de 166mm LH en las hembras y diferentes para el caso de los machos (148mm LH). Phillip (1993), solo determina la TMM en las hembras con un valor de 135mm de LH, valor diferente a lo hallado en este trabajo.
Las estimaciones de fecundidad para las poblaciones del Caribe colombiano de A. monticola, se aproximaron a lo encontrado por Phillip (1993), quien registra valores de 1 000 000 ovocitos para 70g de gónada, mientras que Aiken (1998) estima un número de 340 000 ovocitos para 25g de gónada y Cruz (1987) en Honduras determina 300 000 ovocitos en 75g de gónada. Según Vazzoler & Rossi-Wongtschowski (1976) y Wootton (1991), la fecundidad puede alterarse por el tipo de desove, duración de la época reproductiva, el grado de madurez de los ovocitos y su reabsorción. Así mismo, consideran que la fecundidad es un parámetro extremadamente influenciado, debido a que sufre cambios por factores fisiológicos, metabólicos y ambientales, siendo un reflejo de la relación entre estos factores sobre cada organismo. De acuerdo con Nikolsky (1963), la fecundidad en especies de peces puede variar de una estación reproductiva a otra por causa de condiciones alimentarias, longevidad y tamaño de la primera madurez sexual. Las consideraciones anteriores pueden verse reflejadas en los resultados de este trabajo, los cuales indican que la longitud total es relativamente homogénea, mientras que el peso total, el eviscerado y de las gónadas no lo son. A. monticola presenta ovocitos de mediano tamaño y alta fecundidad (>10 000 ovocitos/año).
Es posible que la salinidad guarde relación con el lugar de desove y sea condición para llevar a cabo este proceso reproductivo en las especies de estudio. Son variados los factores físicos, químicos y fisiológicos que activan la movilidad espermática y dependen de la especie y del medio donde habitan (Billard 1978, Billard & Cosson 1986). Al respecto, Cosson et al. (1999), tras realizar una revisión bibliográfica, registran la inducción en medios hipertónicos de la movilidad espermática en seis especies marinas (incluyendo el mugílido Mugilcephalus); así mismo, anotan que en los salmónidos, de comportamiento anádromo, la movilidad espermática puede ser activada en medios hipotónicos, isotónicos y en cierto grado, hipertónicos. En contraste, en especies completamente dulciacuícolas la movilidad espermática es activada en medios hipotónicos (Morisawa & Suzuki 1980, Cruz- Casallas et al. 2006, Tabares et al. 2006). De los resultados hallados en este estudio, para J. pichardi, es probable que el desove suceda en aguas estuarinas (entre el río y el mar), y que el animal no migre a ambientes completamente marinos. Se tiene conocimiento de la captura de animales maduros a pocos metros de la desembocadura (Cruz 1989), pero en Colombia, aún no existe un registro de su presencia en el mar en alguna fase de su ciclo vital. En A. monticola, los resultados sugieren que soporta un amplio rango de salinidad, lo cual coincide con larvas y pre-juveniles recolectados mar adentro (Anderson 1957, Ditty & Shaw 1996), lo que propone que su freza ocurra en un lugar de intermedia a total salinidad, condición que podría encontrarse en la unión del río con el mar o inclusive en el mar propiamente dicho.
Sigue siendo escaso el conocimiento acerca de aspectos biológicos y ecológicos sobre las poblaciones colombianas de J. pichardi y A. monticola, compresible en alguna manera para J. pichardi, si se tiene en cuenta que su distribución se restringe a los ríos de la vertiente norte de la SNSM y que hasta hace poco se certificó su presencia en Suramérica (Garzón & Wedler 1997). Estas especies presentan una tendencia migratoria catádroma. Es posible que la freza se lleve a cabo en ambientes estuarinos. Posiblemente exista una disminución en las poblaciones de J. pichardi aunque no se conocen las causas, tal vez producto de la presión de pesca y el deterioro de los ambientes. Estas especies presentan un proceso reproductivo condicionado por la época con mayores valores de pluviosidad en la SNSM, tal como se ha reportado en otras latitudes, así como en otros géneros de la familia. Por otro lado, su alimentación a base de vegetales y macroinvertebrados, la calidad de su carne y las tallas que pueden alcanzar hacen de estas especies un potencial de cultivo (Garzón & Wedler 1997, Eslava 2009), por lo cual, se deben efectuar estudios más profundos que revelen mayor información sobre su comportamiento y reproducción en cautividad.Agradecimientos
Este estudio fue desarrollado en el marco del proyecto "Estudio sobre la biología, ecología y posibilidades de piscicultura del besote Joturus pichardi (Pisces: Mugilidae) de los ríos de la vertiente norte de la Sierra Nevada de Santa Marta, Colombia" auspiciado por COLCIENCIAS, la Universidad del Magdalena y la Asociación Caoba (Código 3356- 09-13549). Los autores agradecen también a Eberhard Wedler, Francisco Correa Polo y Jhon Perdomo Balaguera.
Referencias
Aiken, A.K. 1998. Reproduction, diet and population structure of the mountain mullet, Agonostomus monticola, in Jamaica, West Indies. Env. Biol. Fish. 53: 347-352. [ Links ]
Álvarez-Lajonchere, L. 1976. Contribución al estudio del ciclo de vida de Mugil curema Valenciennes (Pisces: Mugilidae). Ciencias Serie 8, Invest. Mar. 28: 1-130. [ Links ]
Anderson, W.W. 1957. Larval forms of the fresh-water mullet (Agonostomus monticola) from the open ocean off the Bahamas and south Atlantic coast of the United States. Fish. Bull. 120: 415-425. [ Links ]
Andrade, J.P. 1998. Age and growth of the bastard sole, Microchirusazevia (Capello, 1868) (Pisces, Soleidae) from the south coast of Portugal. Fish. Res. 34: 205-208. [ Links ]
Billard, R. 1978. Changes in structure and fertilizing ability of marine and freshwater fish spermatozoa diluted in media of various salinities. Aquaculture 14: 187-198. [ Links ]
Billard, R. & M.P. Cosson. 1986. Sperm motility in rainbow trout, Parasalmomykiss; effects of pH and temperature. Reprod. Fish. 44: 10-12 [ Links ]
Bussing, W.A. 1987. Peces de las aguas continentales de Costa Rica. Universidad de Costa Rica, San José, Costa Rica. [ Links ]
Cosson, J., R. Billard, C. Cibert, C. Dreanno & M. Suquet. 1999. Ionic factors regulating the motility of fish sperm, p. 161-186. In C. Gagnon (ed.). The Male Gamete: From basic knowledge to clinical applications. Cache River, Paris, Francia. [ Links ]
Cotta-Ribeiro, T. & H. Molina-Ureña. 2009. Ontogenic changes in the feeding habits of the fishes Agonostomus monticola (Mugilidae) and Bryconbehreae (Characidae), Térraba River, Costa Rica. Rev. Biol. Trop. 57: 285-290. [ Links ]
Cruz-Casallas, P.E. 2001. Técnicas de laboratorio para la evaluación de la calidad seminal en peces. Rev. Orinoquía 5: 155-163. [ Links ]
Cruz-Casallas, P.E., V.M. Medina-Robles & Y.M. Velasco- Santamaría. 2006. Protocolo para la crioconservación de semen de yamú (Bryconamazonicus Spix&Agassiz 1829). Rev. Colom. Cienc. Pecua. 19: 146-151. [ Links ]
Cruz, G.A. 1987. Reproductive biology and feeding of Cuyamel Joturus pichardi and Tepemechin Agonostomus monticola (Pisces: Mugilidae) from Rio Platano, Mosquita, Honduras. Bull. Mar. Sci. 40: 63-72. [ Links ]
Cruz, G.A. 1989. Joturus pichardi (Pisces: Mugilidae) sexualmente maduros capturados en Laguna de Brus y en la desembocadura del Río Plátano, Honduras. Rev. Biol. Trop. 37: 107-108. [ Links ]
Ditty, J.G. & R.F. Shaw. 1996. Spatial and temporal distribution of larval striped mullet (Mugilcephalus) and white mullet (M. curema, Family: Mugilidae) in the Northern gulf of Mexico, with notes on mountain mullet, Agonostomus monticola. Bull. Mar. Sci. 59: 271-288. [ Links ]
Eslava, P.E. 2009. Estimación del rendimiento y valor nutricional del besote Joturus pichardi Poey, 1860 (Pisces: Mugilidae). Rev. MVZ 14: 1576-1586. [ Links ]
FPSNSM-Fundación Pro-Sierra Nevada de Santa Marta. 1997. Plan de desarrollo sostenible de la Sierra Nevada de Santa Marta: Estrategia de conservación de la Sierra Nevada de Santa Marta. Proyecto de cooperación Colombia-Alemán. Colombia, Graficompany. [ Links ]
Garzón, J. & E. Wedler. 1997. Primer registro del besote Joturus pichardi Poey 1860 (Pisces: Mugilidae) para Colombia y América del Sur. Boletín Ecotrópica 31: 1-9. [ Links ]
González, O.E.S. & J.A.S. Diaz. 2001. Principios básicos de criopreservación de semen de peces, p. 253-263. In H. Rodríguez, P.V. Daza & M. Carrillo (eds.). Fundamentos de Acuicultura Continental. Instituto Nacional de Pesca y Acuicultura (INPA), Colombia. [ Links ]
Harrison, I.J. 2002. Family Mugilidae, p. 1071-1085. In K. Carpenter (ed.). Species identification guide for fishery purposes the living marine resources of the Western Central Atlantic Vol. 2. FAO, Roma. [ Links ]
Holden, M.J. & D.F.S. Raitt. 1975. Manual de ciencia pesquera. Pesca 2. Métodos para investigar los recursos y su aplicación. Documento Técnico de Pesca No. 115. FAO, Roma. [ Links ]
IDEAM, 2005. Base de datos de precipitación anual total, años 2003 a 2005. Instituto de Hidrología, Metereología y Estudios Ambientales (IDEAM), Bogotá, Colombia. [ Links ]
Morisawa, M. & K. Suzuki. 1980. Osmolality and potassium ion: their roles in initiation of sperm motility in teleost. Science 210: 1145-1147. [ Links ]
Nikolsky, G. 1963. The ecology of fishes. Academic, Nueva York, EEUU. [ Links ]
Phillip, A.D. 1993. Reproduction and feeding of the mountain mullet, Agonostomus monticola, in Trinidad, West Indies. Env. Biol. Fish. 37: 47-55. [ Links ]
Rodríguez, G.M. 1992. Técnicas de evaluación cuantitativa de la madurez gonádica en peces. México. [ Links ]
Sparre, P. & S.C. Venema. 1995. Introducción a la evaluación de recursos pesqueros tropicales. Parte 1. Documento Técnico de Pesca No. 306. FAO, Roma. [ Links ]
Tabares, C.J., A.F. Montoya, L. Arboleda, A. Echeverri, L.F. Restrepo & M. Olivera-Ángel. 2006. Efecto de la pluviosidad y el brillo solar sobre la producción y características del semen en el pez Bryconhenni (Pisces: Characidae). Rev. Biol. Trop. 54: 179-187. [ Links ]
Tresierra, A. & Z. Culquichicón. 1993. Manual de biología pesquera. Universidad Nacional da Trujillo, Perú [ Links ].
Vazzoler, A.E.A. de M. 1996. Biología da reproduçâo de peixes teleósteos: teoria e prática. EDUEM, Maringa, São Paulo, Brasil. [ Links ]
Vazzoler, A.E.A. de M. & C.L.D.B. Rossi-Wongtschowski. 1976. Sardinellabrasiliensis: tipo de desova, fecundidade e potencial reprodutivo relativo. I. Área entre 23° 40´ S e 24° 40´ S, Brasil. Bol. Inst. Oceanogr. São Paulo 25: 131-155. [ Links ]
Wootton, R.J. 1991. Ecology of teleost fishes. Chapman & Hall, Londres, Inglaterra. [ Links ]
Zar, J.H. 1996. Biostatisticalanalysis. Prentice Hall, Nueva Jersey, EEUU. [ Links ]
Roy Díaz Vesga: Laboratorio de Investigaciones Pesqueras Tropicales, Universidad del Magdalena, Carrera 32 No. 22-08 Santa Marta, Magdalena, Colombia; rdiazvesga@gmail.com
Recibido 17-I -2011. Corregido 03-IV-2011. Aceptado 02-V-2011.