Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.49 n.3-4 San José Dec. 2001
Ictiofauna de la pesquería ribereña en Bahía de Navidad, Jalisco, México,
asociada al evento El Niño 1997- 1998
J. A Rojo-Vázquez1, B Aguilar-Palomino2,3, V. H Galván-Piña2,. E Godínez-Domínguez2,3, S Hernández-Vázquez2, S. Ruiz-Ramírez2 y Lucano-Ramírez. G.2
1 CICESE - Departamento de Ecología. Km. 107 Tijuana-Ensenada. Apdo. Postal 2732. Ensenada, Baja California, México. Corel: jrojo@cicese.mx
2 Centro de Ecología Costera. Universidad de Guadalajara. Gómez Farias # 82. San Patricio-Melaque, Jalisco C.P. 48980. México. Tel: (3) 355 63 30, Fax: (3) 355 63 31.
3 Sistema Nacional de Investigadores SNI.
Abstract
The ichthyofauna fished in Bahia de Navidad, Jalisco, Mexico in the Central Pacific was surveyed during 1998. 6944 organisms of 130 species were caught which weighted 3231 kg. Nearly 30% of the species belonged to Carangidae, Haemulidae and Sciaenidae. The most important species in number and biomass were Microlepidotus brevipinnins, Caranx caninus and C. caballus. Species number, abundance and biomass fluctuated during the year. The largest number of species was caught in June (61), the minimum in March (33). January had the maximum abundance (1397 organisms), while the minimum was obtained during August (251). The maximum biomass values were from January (556.5 kg), and the lowest from August (114.7 kg). 18 species accumulated 87% of the total abundance, while 20 species represented 86.3% of the biomass. There were large in differences species number, abundance and biomass nets of different mesh size.
Keywords: Diversity, El Niño event, ichthyofauna, Jalisco, Mexico
Las comunidades de peces en las zonas tropicales y subtropicales del Pacífico Mexicano están influenciadas tanto por las corrientes oceánicas como por cambios asociados a la temperatura. La corriente de California, la Contracorriente Norecuatorial y El fenómeno el Niño han sido considerados como los eventos más importantes que tienen influencia sobre la estructura de las comunidades de peces en el Pacífico Central Mexicano (Madrid y Sánchez 1997).
El fenómeno El Niño es una anomalía del sistema climático del Pacífico con efectos mundiales que aparece con intervalos de pocos años. El Niño tiene consecuencias ecológicas profundas en los ecosistemas marinos y terrestres de la región, las cuales muchas veces resultan catastróficas para las economías de las naciones colindantes del Pacífico (Arntz y Fahrbach 1996). El Niño 1997-98 esta considerado como el de mayor intensidad que se ha registrado hasta el momento (McPhaden 1999, Trasviña, et al. 1999), así como el más estudiado (Chávez et al. 1999)
El reconocimiento de la presencia del fenómeno del Niño (ENSO) en el Pacífico Oriental, entendido como una anomalía en las condiciones oceanográficas y atmosféricas, fue planteado en la segunda década de este siglo (Arntz y Fahrbach 1996). A partir del ENSO 1982-83, considerado también como de los como uno de los más intensos, se advierte un incremento notable en la literatura científica enfocada a conocer las causas y los efectos biológicos propiciados por el régimen anómalo que caracteriza a este evento de alcance global.
Entre los efectos más notables detectados en la biota marina se encuentran los cambios en los patrones de presencia-ausencia, abundancia, distribución, composición y reproducción algunas especies, los cuales se relacionan con el incremento de la temperatura del agua marina durante el largo período en que se presenta este evento y por los cambios en los patrones de circulación de las corrientes (Kong et al. 1985, Fiedler et al. 1986, Westerhagen 1993, Aurioles et al. 1994, Lluch-Cota et al. 1999).
Si bien es cierto que existe una gran cantidad de literatura sobre los peces del Pacífico Mexicano (Rojo y Ramírez 1997); existe poca información acerca del efecto que ENSO ha tenido sobre las comunidades de peces en el área del Pacífico Central Mexicano. Existen algunos estudios realizados sobre las comunidades marinas durante la presencia del Niño, los cuales hacen referencia del efecto sobre el fito y zooplancton (Torres y Alvarez 1985, Funes-Rodríguez et al. 1998), sobre las pesquerías del Pacífico Mexicano (Lluch-Cota et al. 1999), siendo muy pocos los que hacen referencia a las comunidades de peces (Torres-Villegas et al. 1995, Madrid y Sánchez 1997).
Con el fin de evaluar los posibles cambios en la ictiofauna capturada por la pesquería ribereña en la costa sur del estado de Jalisco, México, debidos a la presencia del evento El Niño 1997-98, se realizaron actividades de pesca experimental durante el año de 1998, periodo durante el cual el evento presentó una mayor intensidad en la zona (Trasviña et al. 1999), así mismo se fue durante este periodo en el que se registraron las alteraciones biológicas más severas, tales como incrementos de la mortalidad natural, fallas en el reclutamiento y crecimiento somáticos disminuidos en las principales pesquerías del país (Lluch-Cota et al. 1999).
Materiales y métodos
La Bahía de Navidad se localiza en el extremo sur de la costa del estado de Jalisco (19° 10' 30" N, 19° 12' 50" N y 104° 42' 45" W, 104° 41' 30" W). Cuenta con diferentes tipos de sustrato como fondos rocosos (Caleta Cuastecomatito y Punta Corrales), áreas de fondos blandos (Bahía de Cuastecomates y Bahía de Melaque), y fondos blandos con piedras pequeñas.
Las muestras fueron obtenidas entre enero y diciembre de 1998. Se realizaron operaciones de pesca experimental durante 60 días utilizando cuatro redes de enmalle (luz de malla de 3.0, 3.5, 4.0 y 4.5 pulgadas), de monofilamento de nilón, con una altura de 4.5 m, coeficiente de armado del 65% y una longitud aproximada de 120 m. Dichos artes de pesca fueron diseñados para operar en el fondo, de acuerdo a las características que tienen las redes más comúnmente utilizadas por los pescadores de la zona.
Las maniobras de pesca fueron realizadas durante la noche por los mismos pescadores ribereños, utilizando los cuatro tipos de redes a la vez, esto con el fin de rerecolectar la mayor cantidad de peces de la comunidad que soporta la pesquería ribereña, cubriendo así un mayor intervalo de tallas y con la posibilidad de capturar el mayor número de especies distintas. La captura fue separada en cajas por tipo de red. A todos los organismos capturados se les tomó la longitud total (cm) y el peso entero fresco (g). En cada muestreo se rerecolectaron muestras de agua utilizando una botella van-Dorn, para determinar la temperatura, salinidad y oxígeno disuelto. Las anomalías de los parámetros ambientales son analizados por Godínez et al. (en prensa).
Las especies fueron identificadas al momento de realizar las mediciones y aquellas que no fue posible reconocer se fijaron algunos organismos en solución de formaldehído al 10%, para su posterior identificación, en la cual se utilizó literatura especializada, principalmente los trabajos de Jordan & Evermann (1896-1900), Meek & Hildebrand (1923-1928), Miller y Lea (1972), Castro-Aguirre (1978), Allen y Robertson (1994), Fischer et al. (1995). Las especies registradas en el presente trabajo se encuentran depositadas en la colección biológica del Centro de Ecología Costera de la Universidad de Guadalajara.
Con el fin de observar la contribución de las especies capturadas a la abundancia y biomasa total, se calculó la importancia relativa de cada una de las especies, en forma total y por tipo de red, de acuerdo a lo recomendado por diferentes autores como Horn y Allen (1985), Ramírez y Rodríguez (1990).
La lista de especies se arregló de acuerdo a Nelson (1994), clasificación frecuentemente utilizada en listados sistemáticos de peces en el Pacífico Mexicano (Rodríguez et al. 1992, Abitia-Cárdenas et al. 1994, De la Cruz-Agüero et al. 1994).
Resultados
Se rerecolectaron 6 944 espécimenes (3 231 kg), distribuidos en 130 especies, 91 géneros, 51 familias y 18 órdenes. Las familias más diversas fueron Carangidae (n = 19), Haemulidae (n = 13) y Sciaenidae (n = 8) (Anexo 1).
La abundancia total presentó gran variación, enero (1 397 organismos) y octubre (1 228 organismos) fueron los meses con máxima captura, mientras que las menores abundancias se obtienen durante los meses de agosto (251) y mayo (263) (Fig. 1a). La máxima biomasa se captura en enero y octubre (556.5 y 534.9 kg), la menor fue en agosto (114.7 kg) (Fig. 1b). Junio y diciembre fueron los meses con el mayor número de especies (61 y 59 respectivamente). Los valores más bajos se obtuvieron en marzo y mayo (33 y 34 respectivamente) (Fig. 1c).

Microlepidotus brevipinnis, Caranx caninus, Caranx caballus, Kyphosus analogus, Caranx sexfasciatus, Scomberomorus sierra, Kyphosus elegans, Elops affinis, Haemulon flaviguttatum y Lutjanus argentiventris fueron capturadas durante los 12 meses del estudio; las especies Lutjanus guttatus, Katsuwonus pelamis y Haemulon sexfasciatus se capturaron durante 11 meses; Anisotremus interruptus apareció durante 10 meses; Caranx vinctus, Lutjanus novenfasciatus, Epinephelus labriformis, Mulloidichthys dentatus, Trachinotus rhodopus y Myripristis leiognathus durante nueve meses, 23 especies se capturaron de cinco a ocho meses y 87 se capturaron durante cuatro meses o menos (Anexo 1).
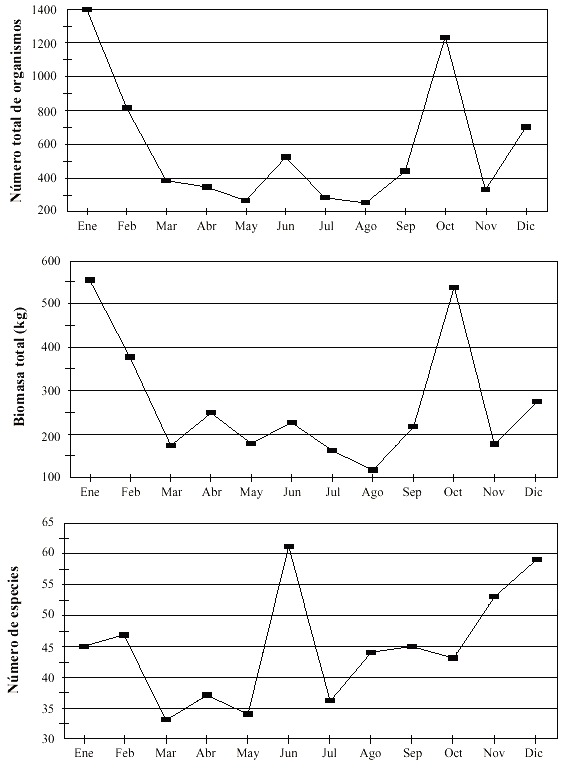
El Niño 1997-98 en Bahía de Navidad, Jalisco, México.
Fig. 1. Number of organisms, biomass and number of species caught during El Niño event 1997-97
rom Bahía de Navidad, Jalisco, México.
De las 130 especies rerecolectadas, 30 de estas fueron capturadas por las cuatro redes, 26 por tres de las redes, 24 por dos y 50 especies fueron exclusivas de una sola red, de las cuales la red de 3" capturó 22 especies, la de 3.5" capturó 14, la de 4.0" obtuvo cinco y las restantes nueve fueron capturadas únicamente por la red de 4.5" (Anexo 1).
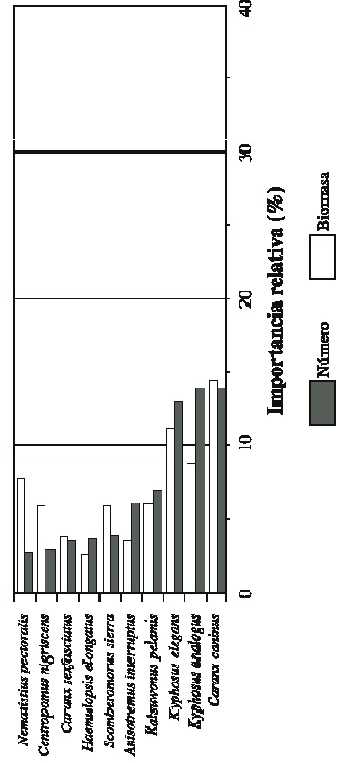
Considerando la importancia numérica relativa de cada una de las especies capturadas, se encontró que sólo 18 especies representaron el 86.7% de la abundancia total obtenida por todas las redes (Cuadro 2). La importancia biomásica relativa presentó un patrón muy similar, en este caso son 20 especies las que acumularon el 86.3% de la biomasa total capturada, mientras que el restante 13.7% fue aportado por 110 especies las cuales presentaron valores menores al 1% (Cuadro 2).
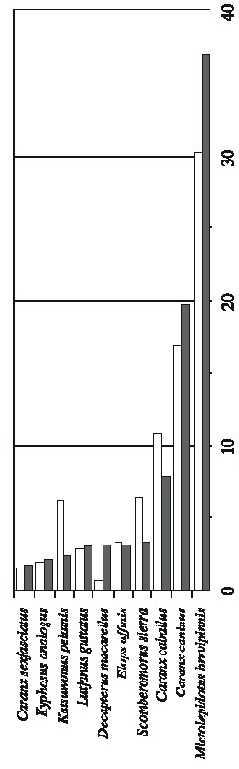
Composición por tipo de red: (3.0 pulgadas): Esta red capturó 3254 ejemplares, distribuidos en 92 especies y con un peso de 1060 kg (Cuadro 1). Las especies con mayor importancia relativa, tanto en abundancia (N) como en biomasa (B) fueron M. brevipinnis (N: 37.07%, B: 30.13%), C. caninus (N: 19.64%, B: 16.78%) y C. caballus (N: 7.84%, B: 10.75%). En abundancia, 14 especies acumularon el 88.1% del total obtenido por esta red, mientras que el resto de las especies (78) aportan 11.9%, contribuyendo con menos del 1% cada una de ellas. En biomasa se presentó un patrón muy similar, donde las mismas 14 especies aportaron el 86% de la biomasa total y las 81 especies restantes acumulan 14% (Fig. 2a).
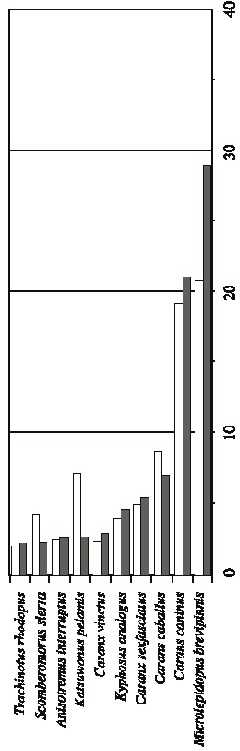
Red (3.5 pulgadas): Esta red capturó 2259 ejemplares distribuidos en 83 especies y con un peso de 986.6 kg (Cuadro 1). Importantes por su aporte en número y biomasa fueron M. brevipinnis (N: 28.88%, B: 20.72%), C. caninus (N: 20.95%, B: 19.14%) y C. caballus (N: 6.86%, B: 8.65%). En abundancia 15 especies aportaron el 86.9%, mientras que 68 especies reúnen el 13.1% restante. En biomasa estas 15 especies acumularon el 84.3% de total (Fig. 2b).
Red (3.5 pulgadas): Esta red capturó 2259 ejemplares distribuidos en 83 especies y con un peso de 986.6 kg (Cuadro 1). Importantes por su aporte en número y biomasa fueron M. brevipinnis (N: 28.88%, B: 20.72%), C. caninus (N: 20.95%, B: 19.14%) y C. caballus (N: 6.86%, B: 8.65%). En abundancia 15 especies aportaron el 86.9%, mientras que 68 especies reúnen el 13.1% restante. En biomasa estas 15 especies acumularon el 84.3% de total (Fig. 2b).
Red (4.0 pulgadas): La red de 4.0" capturó 910 ejemplares distribuidos en 70 especies y un peso de 619.4 kg (Cuadro 1). Las especies más importantes fueron C. caninus (N: 16.37%, B: 15.41%), M. brevipinnis (N: 16.04%, B: 11.73%). En este caso 20 especies aportaron el 86.37% del total en abundancia, mientras que en biomasa, las mismas especies reunieron el 83.56% del total obtenido (Fig. 2c).
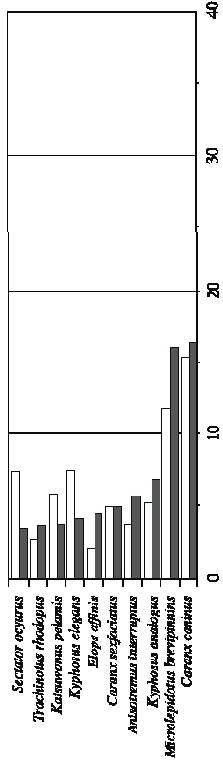
Red (4.5 pulgadas): Esta red capturó 521 ejemplares pertenecientes a 53 especies, y con un peso de 565 kg (Cuadro 1). Las principales especies fueron C. caninus (N: 13.87%, B: 14.41%), K. elegans (N: 13.87%, B: 8.87%) y K. analogus (Número: 12.9%, Peso 11.17%). En este caso 20 especies acumularon el 86.9% de la abundancia total y 86.27% de la biomasa (Fig 2d).
Fig. 2. Abundancia relativa en número y peso de las especies más importantes capturadas durante el evento El Niño 1997-
98 en Bahía de Navidad, Jalisco, México. A) Red de 3.0, B) Red de 3.5, C) Red de 4.0, D) Red de 4.5 de luz de malla.
Fig. 2. Relative abundance by number and weight of the most important species caught during El Niño event 1997-98 from Bahía de Navidad, Jalisco, México. A) Gillnet of 7.62 cm, B) Gillnet of 8.89 cm, C) Gillnet of 10.16 cm, D) Gillnet of 11.43 cm.
Discusión
Se ha observado que los cambios en los patrones de presencia-ausencia, abundancia, distribución, composición y reproducción algunas especies debidos al evento El Niño en las poblaciones de peces son notables y no son menores en los invertebrados. Esto no sólo es válido para la zona costera de la región de la corriente de Humboldt, sino hasta dentro de las zonas subpolares, en las que los efectos físicos de ENSO apenas se sienten (Arntz y Fahrbach 1996).
El análisis de la importancia relativa de la captura de peces obtenida con redes de enmalle en la zona de bahía de Navidad, Jalisco, permite determinar que un reducido número de especies contribuye de forma importante en la captura. En este caso las más importantes por su contribución en abundancia y biomasa fueron M. brevipinnis, C. caninus y C. caballus, cuyo aporte asciende a más del 50% de la abundancia total y del 42% en biomasa. En términos generales la existencia de un gran número de especies con bajas biomasas por especie, es característico de los recursos pesqueros en las zonas costeras tropicales y subtropicales; estos ecosistemas litorales son vulnerables debido al bajo número de individuos de las especies y a las complejas interrelaciones existentes entre las mismas (González et al. 1995).
En este sentido se encontró que, a pesar del impacto que sobre la comunidad de peces pudo haber tenido el evento ENSO, en términos generales, el patrón de las comunidades tropicales de peces se mantiene, dado que a pesar de que se capturó un elevado número de especies, siguen siendo pocas las que dominan en la comunidad y soportan el esfuerzo de la pesquería ribereña, de la misma forma que lo reportó Rojo-Vázquez (1997), en un estudio realizado durante un periodo en el que no se reportan anomalías de ningún tipo. Si bien este patrón no presentó cambios con la presencia del evento EN, cabe hacer notar los cambios que sufrió la composición específica en dicha comunidad.
Es evidente que ENSO propicia considerables desplazamientos en las poblaciones de peces, así como una recomposición en las comunidades. Arntz y Fahrbach (1996), mencionan este efecto para la Costa Central Peruana, Chile y las Islas Galápagos, señalando que la mayoría de las especies autóctonas desaparecieron del área de hasta 30 m de profundidad, área explotada por la pesquería artesanal. Madrid y Sánchez (1997) reportan un comportamiento similar en las comunidades de peces explotadas por la pesquería artesanal de Michoacán, México.
De los aspectos más relevantes en los que se observaron cambios debido al evento ENSO 1997-98, fue el considerable aumento en el número de especies (130 especies); Rojo-Vázquez (1997) en un estudio realizado en la misma área, en condiciones similares de esfuerzo pero durante un periodo considerado normal (1994-95), registró un total de 75 especies. Este incremento en el número de especies pudo haber sido producto de las migraciones que realizan las poblaciones de peces al presentarse un evento de esta naturaleza, así lo reportan diferentes autores como Espino (1991) y Arntz y Fahrbach (1996).
Otro aspecto a considerar es la composición específica de la captura, durante el periodo ENSO se presentó una recomposición en las especies que componen la captura, ya que de las especies que dominan regularmente en la comunidad, sólo M. brevipinnis se mantiene, esto comparado con los resultados obtenidos durante un periodo normal reportados por Rojo y Ramírez (1997), y desaparecen algunas consideradas importantes como Haemulon flaviguttatum y Lutjanus guttatus, especies que, además de su abundancia y biomasa, son importantes comercialmente. Por otro lado, durante el periodo ENSO aparecen nuevas especies importantes por su abundancia y biomasa como son C. caninus, Kyphosus analogus y Katsuwonus pelamis, además de otras especies de Carángidos como C. caballus, C. sexfasciatus.
En el caso de estas especies de Carangidos y K. pelamis se tiene como antecedente que estas especies bajo condiciones normales se encuentran más alejadas de la costa, pero durante El Niño migran con las masas de agua hacia la costa y se hacen así más vulnerables a la pesquería (Arntz y Fahrbach 1996). En el presente estudio se encontró que, tanto algunas especies de carángidos, así como el escómbrido K. pelamis presentaron un comportamiento similar en Bahía de Navidad, ya que durante el periodo considerado como normal Rojo-Vázquez (1997) y Aguilar-Palomino et al (2000) registraron una importancia relativa y frecuencia baja, sin embargo, durante EN alcanzaron altos niveles de importancia debido a su abundancia y biomasa en la zona, apareciendo prácticamente durante todo el periodo de estudio.
Otro de los efectos de ENSO sobre las comunidades de peces es la disminución del número de especies y la diversidad. En la bahía de Ancón, pescas comparativas antes y durante ENSO 1982-83 mostraron que en total el número de especies y la diversidad disminuyeron durante ENSO, aunque inmigrantes tropicales y oceánicos enriquecieron las capturas (Arntz y Fahrbach 1996). Este puede ser un patrón normal para las poblaciones de peces en donde el impacto del evento es mayor o más directo.
Sin embargo, en Bahía de Navidad esto se presentó de manera diferente, ya que en la misma área y utilizando un de esfuerzo de pesca similar, durante el evento ENSO 1997-98 se capturaron un mayor número de especies (130), comparado con las 75 especies capturadas durante un periodo normal obtenidas por Rojo y Ramírez 1997. Estos resultados concuerdan con lo propuesto por Warwick y Clarke (1993), quienes encuentran que en ciertas condiciones de estrés o impacto, la diversidad de especies tiende a incrementarse con el incremento del nivel de la perturbación.
De acuerdo a los resultados obtenidos en el presente estudio pudimos constatar que, si bien el evento El Niño 1997-98 tuvo un cierto efecto sobre la comunidad de peces explotada por la pesquería artesanal en Bahía de Navidad, Jalisco, México, al provocar la migración de algunas especies importantes para la pesquería, este efecto fue a su vez compensado por la ocurrencia de otras especies también de interés comercial. Un efecto similar es reportado, para el mismo periodo, en las pesquerías del norte del país, donde para algunas especies se presentaron aumentos considerables en las capturas y en otras disminuyo su abundancia, siendo a su vez sustituidas por especies nuevas que ampliaron su distribución (Lluch-Cota et al. 1999).
Agradecimientos
Los autores agradecen al Consejo Nacional de Ciencia y Tecnología (Conacyt), programa ACUDE de la Universidad de Guadalajara y la Sociedad Cooperativa de Producción Pesquera de Ribera "Melaque" el financiamiento proporcionado para la realización de este proyecto. También muy especialmente a la tripulación de la Embarcación "León Marino I" por su valiosa ayuda durante realización de las actividades de pesca.
Resumen
Se cuantifico la ictiofauna obtenida por la pesquería ribereña de Bahía de Navidad, Jalisco, México durante 1998. Se capturaron 6944 ejemplares distribuidos en 130 especies (3231 kg). Las familias con mayor número de especies fueron Carangidae, Haemulidae y Sciaenidae. Las especies más importantes en número y biomasa fueron Microlepidotus brevipinnins, Caranx caninus, C. caballus. El máximo número de especies se registró en junio (61), mínimo en marzo (33). En enero se capturó la mayor abundancia (1397 organismos), la menor durante agosto (251). La mayor biomasa fue en enero (556.5 kg), y la menor en agosto (114.7 kg). 18 especies acumularon el 86.7% de la abundancia total, mientras que 20 especies reúnen el 86.3% de la biomasa. De igual forma, se encontraron grandes diferencias entre el número de especies, la abundancia y la biomasa capturados en los diferentes tipos de redes.
Referencias
Abitia-Cárdenas, L. A., J. Rodríguez-Romero, F. Galván-Magaña, J. De la Cruz-Agüero & H. Chávez-Ramos. 1994. Lista sistemática de la ictiofauna de La Paz, Baja California Sur, México. Cienc. Mar. 20: 159-181.
Aguilar-Palomino, B., Pérez-Reyes, C., Galván-Magaña, F y Abitía-Cárdenas, L. A. 2000. Ictiofauna de la Bahía de Navidad, Jalisco, México. Revista de Biología Tropical. 48 (4) 2000. Universidad de Costa Rica. Costa Rica.
Allen, G.R. & D.R. Robertson. 1994. Fishes of the Tropical Eastern Pacific. Univ. Of Hawaii Press. 332 p.
Arntz W.E. & E. Fahrbach, 1996. El Niño: Experimento climático de la naturaleza. Sección de Obras de Ciencia y Tecnología. Fondo de Cultura Económica. México. 312 p. [ Links ]
Aurioles-Gamboa, D., M.I. Castro-González & R. Pérez-Flores. 1994. Annual mass strandings of pelagic red crabs, Pleuroncodes planipes (Crustacea: Anomura: Galatheidae) in Bahia Magdalena, Baja California Sur, México. Fish. Bull. 92: 464-470.
Castro-Aguirre, J.L. 1978. Catálogo sistemático de los peces que penetran a las aguas continentales de México con aspectos zoogeográficos y ecológicos. Dep. Pesca INP. Ser. Cient. 19. 1-298 p. [ Links ]
Chávez, F.P., P.G. Strutton, G.E. Friederich, R.A. Feely, G.C. Feldman. D.G. Foley & M.J. MacPhaden. 1999. Biological and chemical response of the equatorial Pacific Ocean to the 1997-98 El Niño. Science. 286: 2126-2131. [ Links ]
De la Cruz-Agüero, J., F. Galván-Magaña, L.A. Abitia-Cárdenas, J. Rodríguez-Romero & F.J. Gutiérrez-Sánchez. 1994. Lista sistemática de los peces marinos de Bahía Magdalena, B.C.S., México. Cienc. Mar.. 20: 17-31.
Espino, M. 1991. El Niño Phenomena: Its impact on the demersal fishes of Peru. Peru-Pesq. 3: 19-24. [ Links ]
Fiedler, P.C., R.D. Methot & R.P. Hewitt. 1986. Effects of California El Niño 1982-1984 on the northern anchovy. J. Mar. Res. 44: 317-338.
Fischer, W., F. Krupp, W. Schneider, C. Sommer, K.E. Carpenter & V.H. niem, 1995. Guía FAO para la identificación de especies para los fines de la pesca. Pacífico Centro-Oriental. FAO, Roma. Vols I y III. Vertebrados Parte 1 y 2: 647 – 1813. [ Links ]
Funes-Rodríguez, R, M.A Fernández-Alamo & R. González-Armas. 1998. Larvas de peces recolectados durante dos eventos El Niño en la costa occidental de Baja California Sur, México. 1958-1959 y 1983-1984. Oceánides 13: 67-75. [ Links ]
Godínez-Domíngues, E., J.A. Rojo-Vázquez, V.H. Galván-Piña & B. Aguilar-Palomino. (En prensa). Changes in the structure of a coastal fish assemblage exploited by a small scale gillnet fishery during an ElNiño-La Niña event. Estuar. Coast and Shelf Sci.
González, J.A., J.I. Santana, V. Rico, V.M. Tuset & M.M. García-Díaz. 1995. Descripción de la pesquería de enmalle en el sector Norte Noreste de Gran Canaria. Inf. Tec. Inst. Cienc. Mar. No 1. Telde (Gran Canaria). 59 p.
Horn, M.H. & L.G. Allen 1985. Fish community ecology in southern California bays and estuaries. Chap. 8: 169-190. In: A. Yáñez-Arancibia (ed). Fish community ecology in estuaries and coastal lagoons: Towards an ecosystem integration. UNAM.Mexico. 654 p.
Jordan, D.S. & B.W. Evermann. 1896-1900. The fishes of North Middle America. Bull. U.S. Natl. Mus. 47. 3313 p.
Kong, U.I, K.J. Tomicic & L.J. Zegers. 1985. Ichthyofauna associated to the 1982-83 El Niño phenomenon in the northern of Chile. Invest. Pesq. (Santiago). 32: 215-224. [ Links ]
Lluch-Cota D., D. Lluch-Belda, S. Lluch-Cota, J. López-Martínez, M. Nevárez-Martínez, G.Ponce-Díaz, G. Salinas-Zavala, A. Vega-Velázquez, J.R. Lara-Lara, G. Hammann & J. Morales. 1999. Las pesquerías y El Niño. Cap. 5: 137-178. En: Magaña (ed). Los impactos de El Niño en México. UNAM. 229 p.
Madrid-Vera, J. & P. Sánchez. 1997. Patterns in marine fish community as shown by artisanal fisheries data on the shelf off the Nexpa River, Michoacán México. Fisheries Research. 33: 149-158.
McPhaden, M.J. 1999. Genesis and evolution of the 1997-98 El Niño. Science. 283: 950-954. [ Links ]
Meek, S.E. & S.F. Hildebrand. 1923-1928. The marine fishes of Panama. Field Mus. Natl. Hist. Publ. (Zool). 15. Parts 1 – 3, 1045 p.
Miller, D.J. & R.N. Lea. 1972. Guide to the coastal marine fishes of California. Calif. Dept. Fish and Game. Fish Bull. 157: 1-249.
Nelson, J.S. 1994. Fishes of the World. Third Edition. Wiley. Nueva York. 600 p.
Ramírez-Rodríguez, M. & C. Rodríguez. 1990. Composición específica de los peces en Isla Cerralvo, B.C.S. México. Inv. Mar. Cicimar. 5: 137-141. [ Links ]
Rodríguez-Romero, J., L.A. Abitia-Cárdenas, J. De La Cruz-Agüero & F. Galván-Magaña. 1992. Lista sistemática de los peces marinos de bahía Concepción, Baja California Sur, México. Cienc. Mar. 18: 85-95.
Rojo-Vázquez, J.A. 1997. Selectividad y eficiencia de redes de enmalle en Bahía de Navidad, Jalisco, México. Tesis de Maestría. CICIMAR-IPN. México. 83 p. [ Links ]
Rojo-Vázquez, J.A. & M.E. Ramírez-Rodríguez. 1997. Composición específica de la captura con redes de enmalle en la Bahía de Navidad, Jalisco, México. Oceánides 12: 121-126. [ Links ]
Torres-Moye, G. & S. Alvarez-Borrego. 1985. Efectos de El Niño en los nutrientes y el fitoplancton de verano de 1983, en las aguas costeras de Baja California occidental. Cienc. Mar. 11: 107-113.
Torres-Villegas, J.R., R.I. Ochoa-Baez, L. Perezgomez-Alvarez & G. García-Melgar. 1995. Comparison of seasonal variability in the reproduction of Pacific sardine (Sardinox sagax) from Baja California Sur, Mexico, in the years 1982-1992. Sci. Mar. Barc. 59: 255-264. [ Links ]
Trasviña, A., D. Lluch-Cota, A.E. Filonov & A. Gallegos. 1999. Oceanografía y El Niño. Cap. 3: 69-101. En: Magaña (ed). Los impactos de El Niño en México. UNAM. 229 p.
Warwick, R.M. & K.R. Clarke. 1993. Increased variability as a symptom of stress in marine communities. J. Exp. Mar. Biol. Ecol. 172: 215-225.
Westerhagen, H.V. 1993. Climatic changes and their possible effects on fisheries. Actual problems of marine pollution. Arb. Dtsch. Verb. 58: 13-27.
Yáñez-Arancibia, A., A.L. Lara-Domínguez, A. Aguirre-León, S. Díaz-Ruíz, F. Amezcua-Linares, D. Flores-Hernández & P. Chavence. 1985. Ecología de poblaciones de peces en estuarios tropicales: Factores ambientales que regulan las estrategias biológicas y las producción. p. 311-366. In: A. Yáñnez-Arancibia (ed). Fish community ecology in estuaries and coastal lagoons: Towards an ecosystem integration. UNAM.Mexico. 654 p.
Listado sistemático de la ictiofauna de la pesquería ribereña en Bahía de Navidad. Jalisco.
México. asociada al evento El Niño 1997 - 1998. número de meses de aparición
en la captura y tipo de red que capturó cada especie.
Checklist of ji.rhes of the ichthyofauna from the small scale jishery from Bahia de Navidad.
Jalisco. Mexico associated to the El Niño event 1997 - 1998. number of months
caught and type of gillnet
| FILO CHORDATA | ||
| SUBFlLO VERTEBRATA | Numero de meses | Tipo de red |
| SUPERCLASE GNATHOSTOMATA | ||
| CLASE CHONDRICHTHYES | ||
| SUBCLASE ELASMOBRANCHI | ||
| ORDEN ORECTOLOBIFORMES | ||
| FAMILIA GINGLYMOSTOMATIDAE | ||
| Ginglymostoma cirratum (Bonnaterre, 1788) [CECUDGCP550] | 1 | A |
| ORDEN CARCHARHINIFORMES | ||
| FAMILIA CARCHARlHNIDAE | ||
| Carcharhinu.r limbatus (Valenciennes, 1839) [CECUDGCP590] | 2 | A B C D |
| Carcharbinus porosus (Ranzani, 1839) | 1 | B |
| Negaprion brevirostris (Poey, 1868) [CECUDGCP670] | 1 | B |
| Sphyrna lewini (Griffith y Smith, 1834) [CECUDGCP71O) | 7 | A B C D |
| ORDEN RAJIFORMES | ||
| FAMILIA DASYATIDAE | ||
| Dasyatis longus (Garman 1880) [CECUDGCP1O3O] | 2 | B |
| FAMILIA RHINOBATIDAE | ||
| Rhinobatos glaucostigma Jordan y Gílbert, 1883.[CECUDGCP1150] | 4 | A B C D |
| FAMILIA UROLOPHIDAE | ||
| Urotrygon asterias (Jordan y Gilbert, 1882) [CECUDGCP1370] | 2 | A D |
| Urotrygon rogersi (Jordan & Starks, 1895) [CECUDGCP1380] | 1 | C D |
| FAMILIA MOBULIDAE | ||
| Mobula japanica (Muller y Henle, 1941) [CECUDGCP1520] | 1 | D |
| CLASE OSTEICHTHYES (ACTlNOPTERYGII) | ||
| ORDEN ELOPIFORMES | ||
| FAMILIA ELOPIDAE | ||
| Elops affinis Regan, 1909 [CECUDGCP1640] | 12 | A B C D |
| ORDEN ALBULlFORMES | ||
| FAMILIA ALBULIDAE | ||
| Albula nemoptera (Fowler, 1911) [CECUDGCP1750] | 3 | A B C |
| Albula vulpes (Linnaeus, 1758) [CECUDEGCP176O] | 1 | A B |
| ORDEN ANGUILLlFORMES | ||
| FAMILIA MURAENIDAE | ||
| Gymnothorax castaneus (Jordan y Gílbert, 1882) [CECUDGCP1860] | 8 | A B C D |
| ORDEN CLUPEIFORMES | ||
| FAMILIA CLUPEIDAE | ||
| Harengula thrisina (Jordan y Gilbert, 1882) | 1 | B |
| Opisthonema liberta te (Günther, 1867) [CECUDGCP266] | 8 | ABC |
| ORDEN GONORYNCHIFORMES | ||
| FAMILIA CHANIDAE | ||
| Chanos chanos (Forsskäl, 1775) [CECUDGCP2720] | 5 | A B C |
| ORDEN SILURIFORMES | ||
| FAMILIA ARllDAE | ||
| Sciadeops troscheli (GiII, 1863) [CECUDGCP28S0] | 5 | A B |
| ORDEN AULOPIFORMES | ||
| FAMILIA SYNODONTIDAE | ||
| Synodus sechurae Hildebrand, 1946 [CECUDGCP29 10] | 1 | A B |
| Synodus scituliceps Jordan y Gilbert, 1881 [CECUDGCP2920] | 4 | A B C |
| ORDEN MUGILIFORMES | ||
| FAMILIA MUGILIDAE | ||
| Mugil ceptialus Linnaeus, 1758 [CECUDGCP3770] | 2 | A |
| Mugil curema Valenciennes, 1836 [CECUDGCP3780] | 3 | A |
| ORDEN BELONIFORMES | ||
| FAMILIA BELONIDAE | ||
| Ablennes hians (Valenciennes, 1846) [CECUDGCP3900] | 2 | A |
| Tylosurus acus pacificus (Steindachner, 1875) [CECUDGCP3930] | 8 | A B C D |
| ORDEN BERYCIFORMES | ||
| FAMILIA HOLOCENTRlDAE | ||
| Sargocentron suborbitalis (GiII, 1864) [CECUDGCP41 80] | 7 | A B C |
| Myripristis leiognathus Valenciennes, 1846 [CECUDGCP4I 90] | 9 | A B C |
| ORDEN GASTEROSTEIFORMES | ||
| FAMILIA FISTULARlIDAE | ||
| Fistularia commersonii Rüppel, 1835 [CECUDGCP431 0] | 2 | A |
| ORDEN SCORPAENIFORMES | ||
| FAMILIA SCORPAENIDAE | ||
| Scorpaena plumieri mystes Jordan y Starks, 1895 [CECUDGCP4380] | 7 | A B C D |
| FAMILIA TRlGLIDAE | ||
| Prionotus ruscarius Gilbert y Starks, 1904 [CECUDGCP451O] | 2 | A |
| ORDEN PERCIFORMES | ||
| FAMILIA CENTROPOMIDAE | ||
| Centropomus nigrescens Günther, 1864 [CECUDGCP4620] | 6 | B C D |
| Centropomus robalito Jordan y Gilbert, 1881 [CECUDGCP4630) | 3 | A B D |
| FAMILIA SERRANIDAE | ||
| Cephalopholis panamensis | 2 | A |
| Epinephelus acanthistius (Gilbert, 1892) [CECUDGCP484~ | 1 | A |
| Epinephelus labriformis (Jenyns, 1843) [CECUDGCP4890] | 9 | A B C |
| FAMILIA PRlACANTHIDAE | ||
| Heteropriacanthus cruentatus (Lacépédel, 1801)fCECUDGCP515~ | 1 | A |
| FAMILIA NEMATlSTlIDAE | ||
| Nematistius pectoralis GiII, 1862 [CECUDGCP5350] | 6 | A B C D |
| FAMILIA CARANGIDAE | ||
| Alectis cilaris (Bloch, 1788) [CECUDGCP5460] | 1 | B |
| Carangoides orthogrammus Jordan y Gilbert, 1881 [CECUDGCP5470] | 1 | B |
| Carangoides otrynter Jordan y Gilbert, 1833 [CECUDGCP5480] | 14 | A B |
| Caranx cabalIus Günther, 1869 [CECUDGCP5490] | 12 | A B C D |
| Caranx caninus Günther, 1869 [CECUDGCP5500] | 12 | A B C D |
| Caranx sexfasciatus Quoy y Gaimard, 1824 [CECUDGCP5530] | 12 | A B C D |
| Caranx vinctus Jordan y Gilbert, 1882 [CECUDGCP554O] | 9 | A B C |
| Caranx speciosus | 1 | A |
| Chioroscombrus orqueta Jordan y Gilbert, 1882 [CECUDGCP5550] | 3 | A B |
| Decapterus macarellus Cuvier, 1833 [CECUDGCP5560] | 5 | A B C |
| Decapterus macrosoma Bleeker, 1851 | 1 | A |
| Elagatis bipinnulata (Quoy y Gaimard, 1824) CECUDGCP5580 | 2 | B D |
| Hemicaranx zelotes Gilbert, 1898 | 3 | A |
| Selar crumenophthalmus (Bloch, 1793) [CECUDGCP5660] | 1 | A |
| Selene brevoortii (Gill, 1863) [CECUDGCP5670] | 4 | A B D |
| Selene peruviana (Guichenot, 1866) [CECUDGCP5690] | 7 | A B C |
| Striola peruana | 4 | A B C D |
| Trachinotus kennedyi Steindachner, 1875 [CECUDGCP57 10] | 2 | B C |
| Trachinotus rhodopus GiII, 1863 [CECUDGCP573] (3) | 9 | A B C D |
| FAMILIA LUTJANIDAE | ||
| Hoplopagrus guntheri GiII, 1862 [CECUDGCP578O] | 6 | A C D |
| Lutjanus argentiventris (Peters, 1869) [CECUDGCP581O] | 12 | A B C D |
| Lutjanus colorado Jordan y Gilbert, 1882 [CECUDGCP58OO] | 6 | C D |
| Lutjanus inermis (Peters, 1869) [CECUDGCP5820] | 3 | A B C |
| Lutjanus guttatus (Steindachner, 1869) [CECUDGCP5790] | 11 | A B C D |
| Lutjanus novemfasciatus GiII, 1862 [CECUDGCP5840] | 9 | A B C D |
| FAMILIA LOBOTIDAE | ||
| Lobotes pacificus Gilbert, 1898 | 2 | D |
| FAMILIA GERREIDAE | ||
| Eucinostomus gracilis | 1 | A |
| Diapterus peruvianus (Valenciennes, 1830) [CECUDGCP6OOO] | 3 | B C |
| Gerres cinereus (Walbaum, 1792) [OEOUDGOP605] | 7 | A B C D |
| FAMILIA HAEMULlDAE | ||
| Anisotremus caesius (Jordan y Gilbert, 1881) [CECUDGCP61OO) | 2 | A B |
| Anisotremus interruptus (GiII, 1862) [CECUDGCP612O] | 10 | A B C D |
| Haemulon flaviguttatum GiII, 1863 [CECUDGCP61 50] | 12 | A B C D |
| Haemulon maculicauda (Gill, 1863) [CECUDGCP6160] | 8 | A B C |
| Haemulon scudderi Gill, 1863 [CECUDGCP6170] | 7 | A B C D |
| Haemulon sexfasciatum GiII, 1863 [CECUDGCP61 80) | 11 | A B C D |
| Haemulon steindachneri (Jordan y Gilbert, 1882) [CECUDGCP6190] | 7 | A B C |
| Haemulopsis elongatus (Steindachner, 1879) [CECUDGCP6200] | 8 | A B C D |
| Microlepidotus brevipinnis (Steindachner, 1869) [CECUDGCP621 0] | 12 | A B C D |
| Orthopristis chalceus (Günther, 1864) [CECUDGCP624O] | 1 | D |
| Haemulopsis axillaris (Steindachner, 1869) [CECUDGCP625O) | 1 | A |
| Pomadasys branickii (Steindachner, 1879) (CECUDGCP6260] | 4 | A B D |
| Haemulopsis leuciscus (Günther, 1864) [CECUDGCP6280] | 1 | D |
| FAMILIA SPARIDAE | ||
| Calamus brachysomus (Lockington, 1880) [CECUDGCP6380] | 2 | C D |
| FAMILIA POLYNEMIDAE | ||
| Polydactylus approximans Lay y Bennet, 1839 [CECUDGCP6430] | 6 | A B C D |
| Polydactylus opercularis (GiII, 1863) [CECUDGCP6440] | 1 | B |
| FAMILIA SCIAENIDAE | ||
| Menticirrhus elongatus (Günther, 1864) [CECUDGCP6680] | 2 | A C |
| Menticirrhus panamensis (Steindachner, 1875) [CECUDGCP6690] | 3 | A B |
| Odonthoscion xanthops Gilbert, 1898 [CECUDGCP6730] | 1 | C |
| Ophioscion scierus (Jordan y Gilbert, 1881) [CECUDGCP6740) | 4 | A B |
| Ophioscion vermiculatus (Gunther, 1869) [CECUDGCP677O] | 1 | B |
| Umbrina dorsalis (GiII, 1862) [CECUDGCP6840] | 4 | A B C |
| Umbrina xanti GiII, 1862 [CECUDGCP685O) | 5 | A B C |
| Umbrina roncador Jordan y Gilbert, 1881 CECUDGCP686O | 2 | A B C |
| FAMILIA MULLIDAE | ||
| Mulloidichthys dentatus (Gill,1863) [CECUDGCP69OOJ | 9 | A B C |
| FAMILIA CHAETODONTIDAE | ||
| Chaetodon humeralis Günther, 1860 [CECUDGCP692O] | 1 | A |
| Johnrandallia nigrirostris (GiII, 1863) [CECUDGCP697O) | 1 | D |
| FAMILIA POMACANTHIDAE | ||
| Holacanthus passer Valenciennes, 1846 [CECUDGCP7O2O] | 1 | D |
| FAMILIA KYPHOSIDAE | ||
| Kyphosus analogus (GiII, 1863) [CECUDGCP7O8O] | 12 | A B C D |
| Kyphosus elegans (Peters, 1869) [CECUDGCP7 O9O) | 12 | A B C D |
| Sectator ocyurus (Jordan y Gilbert, 1881) [CECUDGCP71OO] | 7 | A B C D |
| FAMILIA CIRRHITIDAE | ||
| Cirrhitus rivulatus Valenciennes, 1855 [CECUDGCP72 OOJ] | 1 | D |
| FAMILIA POMACENTRIDAE | ||
| Abudefduf troschelli (Gill, 1862) [CECUDGCP7280O] | 2 | B |
| Microspathodon dorsalis (GiII, 1862) [CECUDGCP732O] | 4 | A D |
| FAMILIA LABRIDAE | ||
| Bodianus diplotaenia (GiII, 1862) [CECUDGCP740OO] | 4 | A B D |
| Halichoeres notospilus Günther, 1864 | 1 | B |
| FAMILIA SCARIDAE | ||
| Scarus ghobban Forsskäl, 1775 [CECUDGCP759O] | 1 | B |
| Scarus perrico Jordan y Gilbert, 1882 [CECUDGCP76OO] | 1 | D |
| Scarus rubroviolaceus Bleeker, 1847 [CECUDGCP761] | 3 | C D |
| FAMILIA URANOSCOPIDAE | ||
| Astroscopus zephyreus Gilbert y Starks, 1896 [CECUDGCP766O] | 1 | B |
| FAMILIA EPHIPPIDAE | ||
| Chaetodipterus zonatus (Girard, 1858) [CECUDGCP837O] | 3 | B |
| FAMILIA ACANTHURIDAE | ||
| Acanthurus xanthopterus Valenciennes, 1835 [CECUDGCP851O] | 5 | A B C D |
| Prionurus punctatus GiII, 1862 [CECUDGCP852O) | 4 | D |
| FAMILIA SPHYRAENIDAE | ||
| Sphyraena ensis Jordan y Gilbert, 1882 [CECUDGCP8S8O] | 1 | A 8 |
| FAMILIA SCOMBRIDAE | ||
| Auxis rochei Risso, 1810 [CECUDGCP876O) | 1 | A B C |
| Auxis thazard Lacepede, 1800 [CECUDGCP8765) | 1 | A C |
| Euthynnus lineatus Kishinouye, 1920 [CECUDGCP877O] | 2 | B C |
| Katsuwonus pelamis (Linnaeus. 1758) [CECUDGCP882O] | 11 | A B C D |
| Scomberomoru.v sierra Jordan y Starks, 1895 [CECUDGCP881O] | 12 | A B C D |
| FAMILIA STROMATEIDAE | ||
| Peprilus snyderi Gilbert y Starks, 1904 [CECUDGCP8970] | 1 | A |
| Peprilus medius (Peters, 1869) | 1 | B |
| ORDEN PLEURONECTIFORMES | ||
| FAMILIA BOTIDDAE | ||
| Bothus leopardinus (Günther, 1862) [CECUDGCP9O5O] | 1 | A |
| FAMILIA PARALICHTHYIDAE | ||
| Citharichthys gilberti Jenkins y Evermann, 1889 [CECUDGCP914O] | 4 | A B C |
| Cyclopsetta panamensis (Steindachner, 1875) [CECUDGCP91 80] | 3 | A B C |
| Cyclopsetta querna (Jordan y Boilman, 1890) [CECUDGCP919O] | 2 | A C |
| Paralichthys woolmani Jordan y Williams (en Gilbert,1897) [CECUDGCP925O] | 1 | D |
| Syacium latifrons (Jordan y Gilbert, 1862) [CECUDGCP926O] | 1 | A |
| Syacium ovale (Günther, 1864) [CECUDGCP927O] | 1 | A |
| FAMILIA ACHIRIDAE | ||
| Achirus scutum (Günther, 1862) [CECUDGCP933O] | 1 | A C |
| Trinectes fonsecensis (Günther, 1862) [CECUDGCP935O) | 1 | A |
| ORDEN TETRAODONTIFORMES | ||
| FAMILIA BALISTIDAE | ||
| Balistes polylepis Steindachner, 1876 [CECUDGCP956O] | 3 | A B C |
| Sufflamen verres (Gilbert y Starks, 1904) [CECUDGCP959O) | 2 | C D |
| FAMILIA MONACANTHIDAE | ||
| Alutera monoceros (Linnaeus, 1758) [CECUDGCP966] | 1 | C |
| FAMILIA DlODONTIDAE | ||
| Diodon holocanthus Linnaeus, 1758 [CECUDGCP992O] | 1 | C |
Clave de redes. A = 7.62 cm (3.0 pulg); B = 8.89 cm (3.5 pulg); C = 10.16 cm (4.0 pulg); D = 11.43 cm (4.5 pulg), de luz de malla. Key for gillnets. A = 7.62 cm (3.0 in); B = 8.89 cm (3.5 in); C = 1O.I6 cm (4.0 in); D = 11.43 cm (4.5 in), mesh size.