Uno de los mayores problemas globales en salud pública es la resistencia a los antibióticos. La Organización Mundial de la Salud (OMS), en su portal web, indica que la resistencia a los antimicrobianos ocurre cuando un microorganismo: bacteria, virus, hongo o parásito, cambia su forma de responder a un medicamento, y este se vuelve un tratamiento ineficaz; si un microorganismo se hace resistente a la mayoría de los antimicrobianos, se conoce como “superbug”.1
De acuerdo con la información proporcionada por la OMS, los niveles de resistencia a los antibióticos están aumentando en todo el mundo, lo que provoca que el tratamiento de neumonía, tuberculosis, septicemia, gonorrea y enfermedades de transmisión alimentaria, sea cada vez más difícil. La presión selectiva generada, entre otras causas, por el uso / abuso de antimicrobianos, tanto en la práctica clínica como en la industria, es la principal responsable de este aumento.1
En los últimos años se ha observado que la aparición de la resistencia no obedece solo al uso de fármacos, sino que la exposición de las bacterias a biocidas, particularmente los desinfectantes, puede favorecer la selección y supervivencia de microorganismos resistentes.2,3
Generalidades de los biocidas
Son biocidas aquellas sustancias químicas como: antisépticos, desinfectantes y preservantes, que no tienen actividad específica para un grupo microbiano particular y con cuya aplicación se espera reducir el número de microorganismos en el ambiente, a niveles inofensivos.4 Una misma sustancia es capaz de afectar diferentes grupos de microorganismos y distintos blancos celulares de forma simultánea, por lo que se considera inespecífica, a diferencia de un antibiótico, que se dirige a un grupo bacteriano particular y a un blanco celular específico, por citar un ejemplo.5
El objetivo de todos los biocidas es destruir o inhibir el crecimiento de los microorganismos; sin embargo, el término desinfectante se utiliza cuando el biocida es usado sobre objetos o superficies, mientras que los antisépticos se aplican sobre tejidos vivos.6
Los biocidas más comunes son los derivados del amonio cuaternario (cloruro de benzalconio), las biguanidas (clorhexidina), los fenoles (triclosán), los alcoholes, los aldehídos (glutaraldehído), los compuestos halogenados (yodo y cloro) y el peróxido de hidrógeno.7
A grandes rasgos, los derivados del amonio cuaternario (DAC) funcionan como tensioactivos (una parte de la molécula es polar y otra no polar), lo que les permite unirse de forma irreversible a fosfolípidos y proteínas de membrana, e incluso, la porción hidrofóbica puede insertarse dentro de la membrana, lo cual provoca una alteración de la permeabilidad de esta y una disfunción de la cadena respiratoria.8
Las biguanidinas se asocian fuertemente con sitios aniónicos (fosfolípidos acídicos y proteínas) expuestos sobre la membrana y pared celular, lo que produce un desplazamiento de los cationes divalentes Mg2+ y Ca2+ de estas estructuras, que implica una disminución en la fluidez de la membrana y alteraciones osmóticas en la célula bacteriana.9
En el caso de los fenoles, como el triclosán, el mecanismo de acción no solo se limita a la generación de alteraciones en la membrana bacteriana, sino que el químico puede ser absorbido por difusión hacia el citoplasma bacteriano y afectar directamente las vías metabólicas de síntesis de ácidos grasos, inhibiendo enzimas como la NADH-reductasa dependiente de ácidos grasos.10
El mecanismo de acción de los alcoholes se potencia en presencia de agua y se asocia a la generación de daños en la membrana y en las proteínas bacterianas, lo cual genera su desnaturalización y efectos metabólicos que propician la lisis de la bacteria en un corto plazo.4
Los aldehídos, como el glutaraldehído, afectan proteínas, principalmente de pared y membrana bacteriana, actuando sobre grupos tioles, aminos y sulfidrilos. Al unirse a estos grupos “fijan” estructuras y enzimas e inhiben funciones básicas de supervivencia bacteriana.9
Por último, los compuestos halogenados y el peróxido de hidrógeno son sumamente reactivos y actúan como oxidantes y radicales libres capaces de interactuar con componentes celulares como ribosomas y diversas proteínas.11
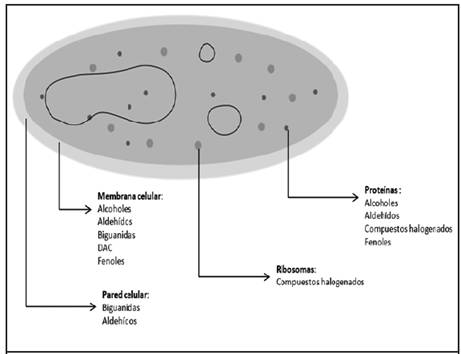
En la Figura 1 se muestra un esquema donde se resumen los principales blancos celulares de los biocidas mencionados.
Resistencia a biocidas
Desde la década de los 50 del siglo pasado, se informó de las primeras cepas bacterianas capaces de adquirir resistencia a biocidas, como por ejemplo, hacia los derivados del amonio cuaternario, y se demostró la capacidad de estos microorganismos de modificar la composición lipídica de las células para sobrevivir a la exposición a estos compuestos.12 Sin embargo, esa situación ha ido en aumento, en el Cuadro 1 se detallan algunos informes de aislamientos bacterianos resistentes a desinfectantes a nivel clínico alrededor del mundo, siendo de particular interés el incremento en la frecuencia de estos en los últimos 5 años.13-29Es necesario destacar que un aislamiento bacteriano se considera resistente cuando la concentración mínima inhibitoria que presenta es superior a la concentración de trabajo del biocida respectivo, de acuerdo con las recomendaciones del fabricante, o en su defecto, del protocolo de aplicación de estas sustancias en el centro médico donde se realizó el aislamiento.
Cuadro 1 Especies de aislamientos clínicos reportadas con resistencia a biocidas
| Bacteria | Lugar de aislamiento | Resistencia descrita | País | Referencia bibliográfica |
| Acinetobacter baumanii | Úlcera de piel, esputo, exudado de heridas, frotis de garganta, lavado bronquial, orina, lavado alveolar, punta de catéter, bilis, líquido cefalorraquídeo | Biguanidas, derivados del amonio cuaternario, biguanidas, compuestos halogenados, derivados del amonio cuaternario | España China | 13 14 |
| Bordetella pertusis | Colección de aislamientos clínicos | Alcoholes | República Checa | 15 |
| Burkholderia cepacia | Sangre | Biguanida | República de Korea | 16 |
| Enterococcus faecium | Colección de aislamientos clínicos | Bigunidas, peróxidos, derivados del amonio cuaternario | Dinamarca | 17 |
| Escherichia coli | Orina | Derivados del amonio cuaternario | Irán | 18 |
| Klebsiella pneumonie | Colección de aislamientos clínicos | Biguanidas | Reino Unido | 19 |
| Klebsiella oxytoca | Piel | Biguanida | Kuwait | 20 |
| Mycobacterium sp. | Colección de aislamientos clínicos | Derivados del amonio cuaternario | Venezuela | 21 |
| Mycobacterium tuberculosis | Colección de aislamientos clínicos | Alcoholes, biguanidas, compuestos halogenados derivados del amonio cuaternario | Japón | 22 |
| Pseudomonas aeruginosa | Esputo Muestras de endoscopios Colección de aislamientos clínicos | Compuestos halogenados Aldehídos Derivados del amonio cuaternario | Reino Unido Suiza Brasil | 23 24 25 |
| Staphylococcus sp. | Sangre, secreciones, puntas de catéter, fluidos biológicos | Biguanidas | Brasil | 26 |
| Staphylococcus aureus | Colección de aislamientos clínicos Muestras de la Unidad de Cuidados Intensivos | Biguanidas Biguanidas Fenoles Alcohol Aldehídos | Reino Unido Australia Brasil | 27 28 29 |
En general, estas bombas son transportadores dependientes de energía y se clasifican en cinco principales familias:
1. superfamilia unidora de adenosíntrifosfato (ABC, por sus siglas en inglés),32 2. familia resistencia-nodulación-división (RND, por sus siglas en inglés),33 3. familia de resistencia a multidrogas pequeñas (SMR, por sus siglas en inglés),34 4. Superfamilia de facilitadores mayores (MFS, por sus siglas en inglés),35 y 5. familia de expulsión de multidrogas y compuestos tóxicos (MATE, por sus siglas en inglés).36
Únicamente los transportadores ABC usan energía a partir del adenosíntrifosfato (ATP) para el bombeo de sustancias, mientras que las otras 4 familias emplean como fuente de energía, el flujo de protones. Las RND se encuentran sobre todo en bacterias Gram negativas, mientras que las otras familias, tanto en Gram positivos como en Gram negativos.
Para mostrar un ejemplo del tipo de proteínas que son estas transportadoras, nos enfocaremos en la familia SMR. A la fecha se han identificado más 250 genes relacionados con esta familia, la cual se divide en tres subfamilias: bombas pequeñas multidrogas (SMP, por sus siglas en inglés), bombas pequeñas de resistencia a multidrogas (PSMR, por sus siglas en inglés) y supresores de mutaciones de groEL (SUG, por sus siglas en inglés). Suelen ser altamente hidrofóbicas (poseen cuatro dominios transmembrana), se componen de 100 a 150 aminoácidos y se acoplan a transportadores de protones que les permiten transportar una amplia gama de biocidas y cationes lipofílicos (se intercalan dentro de la doble cadena del ADN).38,39
En 2009 se estimó que cerca de un 34 % de los miembros de los fila Bacteria y Archaea, poseen en promedio 2 genes de SMR por especie, siendo relevantes en Proteobacteria y Clostridia, ambos de significancia médica, ya que la mayoría de las bacterias patógenas pertenecen a estos.40
Relación entre resistencia a biocidas y resistencia a los antibióticos
A nivel bacteriano, un sistema muy exitoso en la obtención de genes de resistencia son los integrones. Los integrones son regiones del ADN compuestas de tres elementos: un gen que codifica por una tirosinrecombinasa (conocida como integrasa y codificada en el gen intI-1), un sitio específico para recombinación (attI) y reconocido por la integrasa, y un promotor (Pc) localizado corriente arriba del sitio de integración e indispensable para que se produzca la transcripción de los genes localizados en el sitio de recombinación.41
Por su secuencia genética, los integrones se pueden clasificar en tres grupos, siendo los de tipo 1 los más importantes a nivel clínico. Por ejemplo, un integrón de una cepa bacteriana de origen clínico puede transportar hasta nueve genes de resistencia a los antibióticos.42 El origen de estas estructuras se ha asociado a la fusión del gen qacE (relacionado con resistencia a aminas cuaternarias) y el gen sulI (asociado a resistencia a sulfonamidas).43
En 2005, Gaze y colaboradores analizaron muestras de agua y suelo provenientes de una pesquería en la que se usaban altas cantidades de compuestos derivados del amonio cuaternario, y la compararon con muestras de suelos agrícolas. Encontraron que las muestras provenientes de la pesquería portaban bacterias muy resistentes a derivados del amonio cuaternario, y que la presencia de integrones clase 1 era significativamente más alta en estas; demostraron que en ese ambiente se estaba coseleccionando microorganismos resistentes a biocidas y a antibióticos.44
Para 2015 un metanálisis, basado en secuenciación de 2522 genomas y 4582 plásmidos de bacterias, encontró que el 86 % de los genomas estudiados posee genes relacionados con resistencia a biocidas y metales pesados y solo un 17 % de los genomas posee tanto genes de resistencia a los biocidas como a los antibióticos, sin embargo, ese 17 % representa en principio, aislamientos de origen clínico, siendo las bacterias con más frecuencia identificadas en esa categoría:
Providencia, Citrobacter, Klebsiella, Enterobacter, Escherichia, Staphylococcus y Salmonella. Además, identificaron que los plásmidos que poseen genes de resistencia a biocidas y a los antibióticos son conjugativos, lo que favorece la movilización horizontal entre diferentes especies bacterianas, cuando están en estrecho contacto físico unas con otras.45
Es preciso mencionar que la coselección de estos microorganismos no solo se produce en ambientes clínicos, sino que el uso / abuso de desinfectantes y antibióticos a nivel domiciliar, hace que las aguas residuales y las plantas de tratamiento de éstas sean ambientes que actúan como reservorios y suplidores de resistencia a los antibióticos.46
En Costa Rica, en el INISA, se han identificado aislamientos clínicos de Shigella sp. multirresistentes con presencia de inti-1 y genes de resistencia a β-lactamasas (blaOXAyblaTEM), también se han encontrado aislamientos de Escherichia coli multirresistente, proveniente de aguas residuales domésticas, con presencia de intI-1, intI-2, sul-1, sul-2 y blaTEM.47,48A su vez, estudios preliminares realizados en el INISA han identificado concentraciones subinhibitorias de cloruro de benzalconio en muestras de lodos activados de plantas de tratamiento de aguas residuales domiciliares, y también se han encontrado aislamientos de Escherichia coli multirresistentes a los antibióticos, con presencia de genes de resistencia a biocidas y metales pesados.49-52
La existencia de microorganismos con estos perfiles representa una confirmación de la presencia de coselección de microorganismos resistentes a antibióticos y a biocidas en el país.
La utilización de biocidas a nivel doméstico, clínico e industrial, había sido una práctica recomendada en aras de minimizar la cantidad de microorganismos potencialmente nocivos. Sin embargo, en vista de la escalada en los niveles de resistencia a los antibióticos conviene replantearse los protocolos de utilización de los biocidas, con el fin de evaluar su efectividad y en particular su forma de aplicación para minimizar la selección de bacterias cada vez más resistentes a los antibióticos.
Por último, este trabajo representa un llamado de atención sobre efectos históricamente no considerados sobre el uso de desinfectantes. Se insta a la población a hacer un uso moderado de estas sustancias, evitando desperdicios y limitando su desecho en los sistemas de alcantarillado público. Se hace un llamado a la comunidad científica para desarrollar más investigación vinculada con estos temas, por su alta relevancia para la salud pública.