La colonoscopia constituye el método de preferencia para evaluar el colon. Si se realiza apropiadamente es un procedimiento seguro. Además, constituye el estándar de oro para la detección de cáncer colorrectal a nivel mundial,1 tanto para pacientes con riesgo promedio, es decir, aquellos sin factores intrínsecos que promuevan la degeneración neoplásica, así como para aquellos con riesgo aumentado portadores de síndromes polipósicos hereditarios, enfermedad inflamatoria intestinal de larga data o antecedentes heredofamilares de primer grado con cáncer colorrectal.
La eficacia de la colonoscopia depende de múltiples factores. La calidad de la preparación intestinal influye en la duración y la eficacia del procedimiento.2 Una inspección meticulosa y un tiempo de salida adecuado son factores asociados a un aumento en la tasa de detección de adenomas.3Una tasa de detección de adenomas elevada es necesaria para considerar que una colonoscopia de tamizaje es segura, y de este modo reducir el riesgo de cáncer de colon de intervalo.4 Finalmente, una capacitación adecuada y la experiencia del operador se asocian con disminución en la aparición de eventos adversos.5
Estudios recientes sugieren que la efectividad de la colonoscopia para la prevención de cáncer en el colon proximal es menor.6 Esto probablemente se encuentre vinculado con múltiples factores, tales como preparación deficiente y adenomas no detectados o resecados de forma incompleta. Mejorar la detección del cáncer de colon derecho debe ser una de las principales metas de los programas de calidad en colonoscopia.
Múltiples estudios han demostrado que los gastroenterólogos son más efectivos que los cirujanos en la prevención del cáncer colorrectal por colonoscopia.7-9Esto probablemente se encuentra relacionado con un mayor porcentaje de estudios completos (intubación cecal) y una mejor tasa de detección de adenomas en los gastroenterólogos. Es fundamental que los especialistas que realicen colonoscopia determinen con frecuencia la calidad de sus estudios.
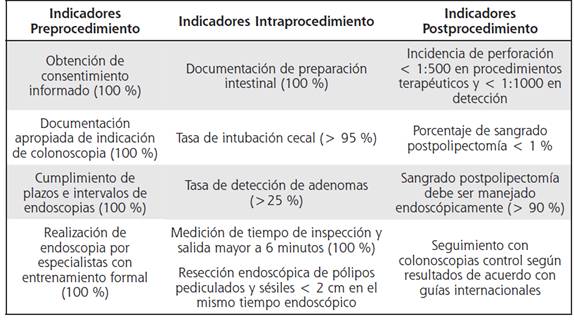
La calidad de la atención médica puede medirse al comparar el desempeño de un individuo contra un punto de referencia. El parámetro particular utilizado para comparación se denomina indicador de calidad. La Asociación Costarricense de Gastroenterología y Endoscopía Digestiva ha desarrollado este documento con el fin de estandarizar los indicadores de calidad asociados con la realización de colonoscopia en nuestro país.
Se revisaron los indicadores de calidad para colonoscopia publicados por la asociacion americana (ASGE)10 y europea (ESGE)11 de endoscopia digestiva, y se adaptaron a la realidad nacional. Los indicadores de calidad se dividieron en: preprocedimiento, intraprocedimiento y postprocedimiento.
Indicadores de calidad preprocedimiento
El periodo preprocedimiento se refiere al contacto entre el equipo de endoscopia y el paciente antes de la introducción del endoscopio. Los indicadores de calidad preprocedimiento contemplan:
1. Se obtuvo un consentimiento informado que incluye los riesgos asociados con la colonoscopia en todos los pacientes.
El consentimiento informado debe incluir los riesgos, beneficios y opciones frente a la colonoscopia. Los riesgos más frecuentes asociados con la colonoscopia incluyen sangrado, perforación, infecciones, eventos asociados a la sedación y la existencia de lesiones no observadas.
2. La colonoscopia se realizó por una indicación apropiada y esto se documentó en el reporte.
Las indicaciones apropiadas para la realización de colonoscopia incluyen:12
Alteraciones significativas en un estudio de imagen
Evaluación del sangrado digestivo bajo
Evaluación de anemia ferropénica
Tamizaje de cáncer colorrectal en pacientes mayores de 50 años
Seguimiento de pacientes con antecedente de cáncer colorrectal
Tamizaje de displasia en pacientes con enfermedad inflamatoria intestinal
Estudios por diarrea crónica
El objetivo primordial de este indicador es reducir el número de procedimientos realizados por una indicación inadecuada.13
3. Deben cumplirse los plazos establecidos según las guías para el seguimiento postpolipectomía y posterior a la resección de un cáncer, así como el intervalo establecido de 10 años en pacientes con riesgo promedio y luego de una colonoscopia negativa con preparación adecuada.14
Para que la colonoscopia sea costo efectivo y se minimicen sus riesgos, los intervalos entre procedimientos deben optimizarse. Los intervalos recomendados asumen que la colonoscopia se realizó con una preparación adecuada, que se alcanzó el ciego y que la exploración fue meticulosa. La realización de colonoscopia con un intervalo menor a 10 años en pacientes con riesgo promedio de cáncer colorrectal no es costo efectivo y expone a los pacientes a riesgos innecesarios, lo cual es injustificable.
La colonoscopia debe ser realizada exclusivamente por gastroenterólogos o especialistas de ramas afines que hayan completado un entrenamiento formal en endoscopia digestiva, que incluya al menos la realización de 275 colonoscopias supervisadas por un especialista debidamente acreditado.9
La especialidad de gastroenterología suele ofrecer el entrenamiento más intensivo en la realización de colonoscopia. La mayoría de programas de estudio y guías internacionales establece como requisito que se efectúen al menos 275 procedimientos bajo supervisión antes de establecer el nivel de competencia del estudiante. Investigaciones desarrolladas en residentes de gastroenterología han evidenciado que la tasa de intubación cecal no es confiable hasta que se practiquen más de 500 colonoscopias.15 Estos datos sugieren que debería reconsiderarse el número mínimo de colonoscopias para asignar competencia.
Se ha demostrado que los gastroenterólogos detectan y resecan adenomas con mayor frecuencia, lo cual sugiere una relación directa entre un entrenamiento intensivo y estos indicadores de calidad. La menor probabilidad de detección y resección de pólipos por no gastroenterólogos que realizan colonoscopia, reduce los beneficios potenciales de este procedimiento en la prevención del cáncer colorrectal.9,16
Indicadores de calidad intraprocedimiento
La calidad de la evaluación del colon consiste en la exploración de la totalidad del colon, incluido el ciego y el íleon terminal, así como una detallada inspección mucosa. La intubación cecal aumenta la sensibilidad y reduce el costo al eliminar la necesidad de estudios radiográficos complementarios, o de repetir la colonoscopia. Una inspección detallada y cuidadosa de la mucosa es esencial para la prevención del cáncer colorrectal. La detección de lesiones precancerosas es el objetivo primario de la mayoría de las colonoscopias.
La necesidad de repetir estudios, la aparición de eventos adversos y el manejo quirúrgico de pólipos que pueden ser resecados endoscópicamente, reducen la relación costo beneficio de la colonoscopia. Es primordial que los endoscopistas evalúen sus prácticas e implementen las mejoras necesarias para reducir los costos asociados a la detección y prevención del cáncer colorrectal.
El periodo intraprocedimiento se extiende desde que se inicia la sedación hasta que se retira el endoscopio. Abarca todos los aspectos técnicos y maniobras terapéuticas del procedimiento. Los indicadores de calidad intraprocedimiento incluyen los siguientes:
1. Debe documentarse la calidad de la preparación intestinal para la colonoscopia en todos los procedimientos y esta debe ser adecuada, de tal forma que permita el uso de los intervalos de seguimiento recomendados en las guías de detección.
La calidad de la preparación se basa en la habilidad de visualizar adecuadamente la mucosa durante la colonoscopia. El endoscopista debe documentar la calidad de la preparación en cada procedimiento.17 Deben evitarse términos no estandarizados para describir la preparación intestinal. Se recomienda el uso de la escala de Boston, validada internacionalmente, para describir la preparación de la colonoscopia.18 Según lineamientos internacionales, se define como una preparación intestinal adecuada con una escala de Boston ≥ 6.11Si la preparación colónica es inadecuada y el procedimiento es realizado para detección de cáncer colorrectal o seguimiento postpolipectomia, la colonoscopia debe repetirse en un lapso de un año o menos.
La presencia de mala preparación intestinal prolonga los tiempos de intubación cecal y de revisión durante la salida, además de reducir considerablemente la detección de pólipos pequeños y grandes.19
Se recomienda que el porcentaje de estudios que se desarrollen con una preparación inadecuada sea menor al 15 %. Múltiples estudios clínicos sugieren que el uso de preparación en dosis dividida (split dose) mejora las tasas de preparación intestinal adecuada. El factor de mayor relevancia para una preparación adecuada es el intervalo entre el final de la ingesta de la preparación y el inicio del procedimiento.20La calidad de la preparación intestinal disminuye al aumento del intervalo entre el final de la ingesta y el inicio del estudio. Esto ocurre especialmente en el colon derecho. Se recomienda el uso de preparación intestinal en dosis dividida en todos los pacientes que se vayan a someter a colonoscopia, finalizando la última toma 2 horas antes del estudio. Según las guías de ayuno de la Sociedad Americana de Anestesiología, los pacientes deben estar nada vía oral por 2 horas luego de la ingestión de líquidos claros.21 Se debe instruir a los pacientes para iniciar la segunda dosis de la preparación de 4 a 5 horas antes de la hora agendada para el procedimiento y para que lo deben finalizar 2 horas antes de esta.
2. La frecuencia con la que se logra intubar el ciego debe ser mayor al 95 % y se debe documentar fotográficamente.
La intubación cecal se define como el avance de la punta del endoscopio a un sitio proximal a la válvula ileocecal, de tal forma que todo el ciego pueda ser valorado. La necesidad de valorar completamente el ciego radica en que un porcentaje importante de neoplasias colorrectales están localizadas en el colon derecho. Bajas tasas de intubación cecal se han asociado con una mayor frecuencia de aparición de cáncer de colon proximal de intervalo.22 La intubación cecal debe documentarse mediante la captura fotográfica de la válvula ileocecal y el orificio apendicular. Los colonoscopistas experimentados están en la capacidad de identificar con un 100 % de certeza la intubación cecal.
Un colonoscopista efectivo debe ser capaz de intubar el ciego en un 95 % de las colonoscopias de tamizaje.23
3. La frecuencia con la cual se detectan adenomas en individuos asintomáticos con riesgo promedio de cáncer colorrectal debe ser mayor al 25 %.
Existe evidencia que documenta la omisión en la detección de adenomas por colonoscopistas cuando se realizan colonoscopias en tandem.24 Además, se ha demostrado que la colonoscopia falla en prevenir todos los cánceres colorrectales en cohortes seguidas por más de 3 años, siendo la mayoría de los cánceres atribuibles a lesiones no identificadas y resecciones incompletas, así como a variaciones en los patrones de crecimiento tumoral. 25
Además, se ha logrado evidenciar una marcada variación en la detección de adenomas por colonoscopistas dentro de una misma práctica clínica.26,27Esta variación fue el sustento para la creación de objetivos para la tasa de detección de adenomas (TDA).28 La TDA se define como el porcentaje de pacientes mayores de 50 años en los cuales se detecta uno o más adenomas durante su primera colonoscopia de tamizaje. Estudios han documentado que los pacientes a los que se les realiza colonoscopia de tamizaje por endoscopistas con TDA menor al 20 % tienen un cociente de riesgo 10 veces mayor para desarrollar cáncer de colon, en comparación con los que tienen su colonoscopia con endoscopistas con TDA mayor al 20 %.4
Estudios recientes sugieren que algunos colonoscopistas pueden alcanzar TDA mayores al 40 %.26 Las TDA mayores del 30 % se asocian con una reducción del riesgo de desarrollar cáncer de colon, tanto proximal como distal, tanto en hombre como en mujeres.29 Con base en esta evidencia se ha propuesto un objetivo mínimo del 25 % como TDA en pacientes mayores de 50 años sometidos a colonoscopia de tamizaje.
Todos los colonoscopistas deben tener un registro de su TDA y los que tengan una TDA menor al 25 % deben tomar medidas concretas para mejorar su desempeño.
La TDA constituye el principal indicador de calidad en colonoscopia. Existe una correlación estrecha entre la TDA y los intervalos recomendados para seguimiento y tamizaje. Los colonoscopistas con TDA elevados encuentran y resecan una mayor cantidad de lesiones precancerosas y traen de vuelta a sus pacientes a intervalos más cortos, debido a que los intervalos de seguimiento recomendados son cortos luego del hallazgo de lesiones precancerosas. Por el contrario, los colonoscopistas con TDA bajos fallan en identificar pacientes con lesiones precancerosas o múltiples y, por lo tanto, recomendaran intervalos inapropiadamente largos entre estudios. Esta interacción hace que sea esencial conocer la TDA de cada endoscopista para, de este modo, asegurar una adecuada protección del paciente.30
4. El tiempo de inspección de salida durante la colonoscopia debe ser medido y, en promedio, debe ser mayor de 6 minutos.
Estudios han demostrado un aumento en la detección de lesiones neoplásicas, cuando el tiempo de inspección durante la salida es mayor a 6 minutos. La principal utilidad de incrementar el tiempo de salida es aumentar la TDA en colonoscopistas con desempeño subóptimo.31
La exploración detallada del colon requiere tiempo y esta es la razón por la cual existe una estrecha relación entre el tiempo de inspección durante la salida de la colonoscopia y la TDA.
5. Debe procurarse la resección endoscópica de los pólipos pediculados y sésiles menores de 2 cm, durante el mismo procedimiento endoscópico.
Diferir la resección de pólipos colónicos pequeños identificados durante una colonoscopia de rutina, aumenta los costos y disminuye la relación costo beneficio del procedimiento, lo cual es inaceptable. La amplia mayoría de los pólipos menores de 2 cm son resecables endoscópicamente y no deben ser referidos para resección quirúrgica. En algunos casos, ciertos pólipos pueden ser difíciles de posicionar para una polipectomía adecuada, y lo recomendable es su envío a un centro de referencia.32 La resección endoscópica de la amplia mayoría de las lesiones polipoides es segura y más costo efectiva que la resección quirúrgica.33 Si se anticipa que la lesión va a ser referida para ser resecada por otro endoscopista, debe evitarse la toma de múltiples biopsias o una polipectomía parcial con asa, a fin de evitar el desarrollo de fibrosis que limite una posterior resección.
Las lesiones enviadas para resección quirúrgica deben ser marcadas con tinta china en 3 o 4 cuadrantes y de esta forma asegurar la resección del segmento correcto.
Indicadores de calidad postprocedimiento El periodo postprocedimiento se extiende desde que se retira el endoscopio hasta el seguimiento subsecuente. Entre los cuidados luego del procedimiento se incluyen: dar las instrucciones pertinentes al paciente, reconocimiento de eventos adversos, valoración de los hallazgos histopatológicos y determinación del grado de satisfacción del paciente. Los indicadores de calidad postprocedimiento incluyen:
1. Incidencia de perforación menor a 1 de cada 500 procedimientos terapéuticos y 1 de cada 1000 colonoscopias de detección y un porcentaje de sangrado postpolipectomia menor al 1 %. La perforación es considerada como el evento adverso más serio asociado a la colonoscopia. Cerca del 5 % de las perforaciones durante la colonoscopia son fatales.34
Las tasas de perforaciones mayores a 1 en cada 500 pacientes, debe propiciar un estudio para determinar si existen algunas prácticas inapropiadas. Entre las prácticas sugeridas para reducir el riesgo de perforación, se incluyen: no empujar en contra de una resistencia fija, quitar los loops en cuanto sea posible, utilizar un colonoscopio pediátrico en casos de enfermedad diverticular severa y utilizar dióxido de carbono en lugar de aire para la insuflación. Es preciso evitar el uso de electrocauterio en la resección de pólipos pequeños y utilizar inyección submucosa previo a la resección con electrocauterio de lesiones sésiles grandes.35Las perforaciones que ocurran intraprocedimiento pueden resolverse mediante el cierre con clips hemostáticos.36
El sangrado es el evento adverso más frecuente luego de una polipectomía. Puede ser temprano o tardío. Las distintas series sugieren que el sangrado postpolipectomía debe ser menor al 1 %.37 El riesgo de sangrado aumenta según el tamaño del pólipo, localización proximal y con el uso de anticoagulación o antiagregantes plaquetarios.38
2. El sangrado postpolipectomía debe ser manejado endoscópicamente de forma exitosa en más del 90 % de los casos. El sitio de sangrado debe tratarse con inyección en combinación con la colocación de hemoclips o el uso de cauterio.39
3. Debe brindarse una recomendación para la colonoscopia de control, según las guías de seguimiento luego de la revisión de los hallazgos histológicos.
Las guías actuales recomiendan el tamizaje por colonoscopia cada 10 años en la población general, cada 5 años en pacientes con menos de 2 adenomas tubulares pequeños y cada 3 años en pacientes con más de 3 adenomas tubulares, en adenomas vellosos, en los mayores de 1 cm o en los asociados a displasia de alto grado.40 Debe evitarse la sobreutilización de la colonoscopia para el tamizaje, ya que esta práctica no es costo efectivo y expone a los pacientes a riesgos adversos innecesarios.
Corrección del pobre desempeño
El propósito primordial de medir los indicadores de calidad es mejorar la atención del paciente al identificar a los colonoscopistas que tengan un pobre desempeño para reentrenarlos adecuadamente. Cuando un endoscopista tenga un TDA menor a lo recomendado, deberá efectuar los ajustes necesarios y demostrar mejoría en un plazo razonable. Se ha evidenciado que las intervenciones más efectivas relacionadas con mejorar la TDA, incluyen educación ligada a la apariencia endoscópica de las lesiones precancerosas e instrucción acerca de la técnica de inspección adecuada durante la fase de salida.41
Debe evitarse la realización de colonoscopia por endoscopistas que no alcancen los niveles mínimos de TDA luego de un periodo de reentrenamiento. La experiencia es concluyente en cuanto a que niveles bajos de TDA ponen en riesgo a los pacientes.
Conclusiones
Para colonoscopia, los indicadores de calidad prioritarios son una TDA mayor al 25 %, una intubación cecal mayor al 95 % y el uso correcto de los intervalos recomendados para el tamizaje y seguimiento del cáncer colorrectal. Estos 3 indicadores se asocian a desenlaces clínicos de gran relevancia y, por lo tanto, deben ser monitoreados estrictamente.
La realización de colonoscopia de alta calidad constituye el rol fundamental del colonoscopista dentro del esfuerzo multidisciplinario para reducir la incidencia y mortalidad del cáncer colorrectal.











 text in
text in