La leucemia mieloide crónica (LMC) es el trastorno neoplásico caracterizado por la presencia del cromosoma Philadelphia y la consecuente tirosina quinasa derivada BCR-ABL1.1 Esta sobreexpresión de BCR-ABL1 es eficazmente controlada con los inhibidores de tirosina quinasa (TKI; imatinib como primera línea, nilotinib y dasatinib de segunda línea), cuyo tratamiento debe ser monitorizado molecularmente, según las recomendaciones de la European LeukemiaNet (ELN). No obstante, la cura de la enfermedad se alcanza mediante el trasplante alogénico de células hematopoyéticas.2
La situación actual de la LMC en América Latina ha sido descrita en algunos estudios. Sin embargo, hasta el momento no se ha analizado la situación específica en Centroamérica, cuya situación socioeconómica difiere de manera considerable de países como México, Chile o Brasil. En Costa Rica, un país de ingreso medio superior, según lo estimado por el Banco Mundial para 2015, la Caja Costarricense de Seguro Social (CCSS) brinda cobertura sanitaria a prácticamente el 100% de la población. Como parte de esta cobertura, la Dirección de Farmacoepidemiología de la CCSS establece una “Lista Oficial de Medicamentos”, dentro de la cual se incluye al imatinib como primera línea de tratamiento para la LMC. No obstante, los medicamentos de segunda línea (nilotinib y dasatinib) deben ser solicitados por el especialista a la Dirección de Farmacoepidemiología de forma excepcional, para ser brindados a pacientes con intolerancia al medicamento, o una enfermedad refractaria al tratamiento.
El diagnóstico y seguimiento molecular de la LMC en adultos y niños de todo el país se realiza en un solo centro de referencia en el Hospital Nacional de Niños, acorde a las recomendaciones de los expertos.2 Sin embargo, no se posee un presupuesto destinado a la salud, tan alto como en otras naciones americanas, por lo que la atención de estos pacientes genera un fuerte impacto en la economía. Solo el imatinib representa el segundo medicamento de mayor costo para la seguridad social, con una inversión superior a USD $ 6 000 000 anuales.
Ante la inopia de estudios regionales y el impacto socioeconómico que tiene la LMC en países de ingreso bajo o medio, es necesario el desarrollo de estudios a nivel nacional para la caracterización de la enfermedad y efectuar comparaciones con las guías internacionales. El objetivo del estudio fue describir la epidemiología de la LMC en un país de ingreso económico medio, con énfasis en el tipo de respuesta obtenido y la valoración del seguimiento molecular que se le brinda a los pacientes.
Métodos
Pacientes
Se analizó la totalidad de pacientes pertenecientes a la CCSS diagnosticados con LMC en el período del 01 de enero de 2011 al 31 de diciembre de 2014 (n=133), y referidos al laboratorio de Diagnóstico Molecular del HNN, centro institucional para el análisis molecular de leucemias para muestras provenientes de los hospitales de adultos San Juan de Dios, Hospital México, Hospital “Dr. Rafael Ángel Calderón Guardia” y Hospital “Dr. Maximiliano Peralta”. El diagnóstico de LMC se basó en los criterios clínicos, morfológicos y moleculares aceptados acorde a las guías ELN.2 Se seleccionaron los casos de LMC basándose en los siguientes criterios de inclusión: mayoría de edad (18 años), diagnóstico confirmatorio de la enfermedad por determinación molecular por reacción de la cadena de la polimerasa con retrotranscripción, tratamiento con TKI (imatinib, nilotinib o dasatinib), y seguimiento de 12 meses mínimo. Se excluyeron del análisis molecular, los casos de fallecimiento prematuro, dado antes de 6 meses desde el diagnóstico, ya sea por causa relacionada o no con la neoplasia.
El diseño del estudio se efectuó conforme a los requerimientos del Comité Ético Científico Institucional de la CCSS (protocolo R015-SABI-00075), así como a los acuerdos en la declaración del Helsinki.
Extracción de ácido ribonucleico y retrotranscripción.
El ácido ribonucleico de las muestras fue extraído por medio de la técnica de Trizol. La cantidad de ácido ribonucleico fue cuantificado por espectrofotometría y almacenado a -80ºC hasta el momento de su procesamiento. Posteriormente, 4 μg fueron transcritos a una copia de ácido desoxirribonucleico con kit comercial (Roche Diagnostics). La cuantificación del transcrito BCR-ABL1 fue realizada por medio de la PCR acoplado a retrotranscripción en el equipo LightCycler® 480 (Roche Diagnostics), según el protocolo del programa Europe Against Cancer3 y expresado en porcentaje de estándar internacional (%IS), conforme a lo descrito por el protocolo de la ELN.2
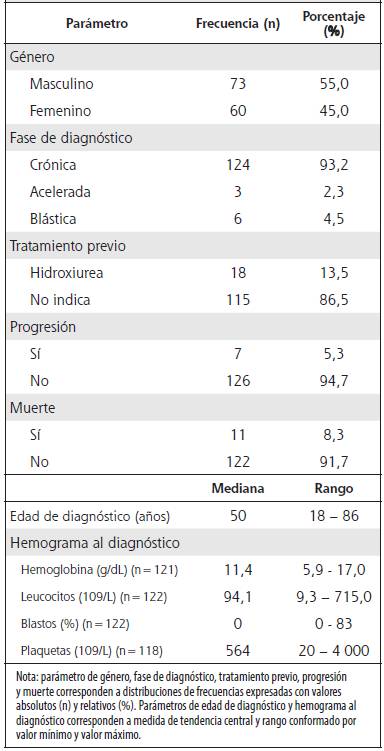
Cuadro 1 Características clínico-biológicas de 133 pacientes con LMC en Costa Rica, diagnosticados entre enero de 2011 y diciembre de 2014
Mutaciones ABL
El análisis de mutaciones en ABL fue realizado siguiendo las recomendaciones de la ELN.4 La copia de ácido desoxirribonucleico fue amplificado por PCR de acuerdo con el programa Europe Against Cancer y luego acoplado a una reacción de PCR anidada, según el protocolo de Branford.5 La reacción de secuenciación de Sanger fue realizada en el equipo Genetic Analyzer 3500 (Life Technologies), utilizando química BigDye 3.1; siendo las secuencias analizadas en ambas direcciones.
Análisis Estadístico
Las variables del estudio fueron conformadas por edad, sexo, tratamiento previo, tratamiento de primera línea, segunda línea (escalamiento o cambio de TKI), así como progresión de la enfermedad, muerte general, presencia y tipo de mutaciones. Para el seguimiento de la enfermedad se contó con valores de hemograma, así como de resultados de biología molecular, con los cuales fue posible determinar la respuesta hematológica y molecular, según las guías ELN actuales.2 La supervivencia libre de evento, supervivencia libre de progresión (SLP) y supervivencia global (SG), se determinaron por método de Kaplan-Meier, desde el momento del diagnóstico hasta la aparición del evento, recaída hematológica o muerte, respectivamente, o bien, fecha de última valoración. El evento fue definido como escalamiento de dosis, suspensión por intolerancia, cambio a segunda línea de tratamiento, progresión, muerte, pérdida de respuesta o aparición de mutaciones en ABL. Para el análisis estadístico se utilizó el programa IBM SPSS® 21.0.0, en el cual se comparaban dos grupos, respondedores al tratamiento, como aquellos que alcanzaron la RMM acorde a las normas ELN y los no respondedores que no alcanzaron el RMM en el tiempo definido. La comparación se realizó mediante el uso de la herramienta Chi cuadrado y long rank test, con un grado de libertad y una significancia de p=0,05.
Resultados
Se encontraron 133 casos portadores de la LMC que cumplieron con los criterios de inclusión establecidos. El seguimiento de los pacientes se realizó en un período total de 56 meses, con una mediana de 28 meses de seguimiento (rango 0,3 - 56,3). Las características clínico-biológicas de los pacientes se resumen en el Cuadro 1.
Con respecto a la terapia de la enfermedad, en el país un 98,5% de la población inició con 400 mg de mesilato de imatinib, y un 1,5% (2 casos) con 600 mg; además, un 13,5% de la población recibió hidroxiurea como tratamiento previo al imatinib. El escalamiento a 800 mg se produjo en un 16,5% de la población. Se tiene 28 casos (21,1%) de suspensión de la terapia, en la mayoría por causa de falla terapéutica. La segunda línea de tratamiento estuvo conformada por nilotinib (21 casos), dasatinib (3 casos) y quimioterapia convencional (4 casos).
Se observó respuesta hematológica completa (RHC) en un 97,7% de los casos (n=130); el restante 2,3% (n=3) lo obtuvieron posteriormente. Se registró 7 pacientes en los que hubo una pérdida de la RHC, 4 de ellos lograron recuperarla después, sin realizar cambio a segunda línea de tratamiento, sugiriendo una mala adherencia a este. De los 3 restantes, ninguno pudo recuperar respuesta, ya que uno presentaba la mutación T315I, otro falleció y el último no la había alcanzado al momento de finalizar el estudio (a los 21 meses de seguimiento).
Con respecto a la respuesta molecular, los pacientes presentaron una mediana de determinaciones de biología molecular de 6 (rango: 1 - 15), realizadas cada 5,55 meses, aproximadamente (rango: 2,3 - 29,6 meses). El seguimiento de los pacientes reflejó que el 68,4% de los pacientes tuvo un seguimiento de al menos cada 3-4 meses en el primer año de tratamiento; posterior al año de diagnóstico, a un 57,7% se le realizó determinaciones cada 6 meses o menos, según lo recomendado por la ELN. 2
La respuesta molecular, según las guías de la ELN actuales, se pudo evaluar en 129 pacientes. Se destaca que hubo 4 exclusiones respecto al grupo total de análisis por fallecimiento. Se observó un 43,4% (n=56) de respuesta molecular mayor (RMM) a los 12 meses (recomendado por las guías internacionales), 36 pacientes (29,7% adicional de los pacientes analizados) alcanzaron la RMM a los 12 meses, considerándose un total de 92 pacientes (76%) respondedores al tratamiento. De estos, hubo un 87,0% (n=80) que conservó la RMM hasta el final del estudio.
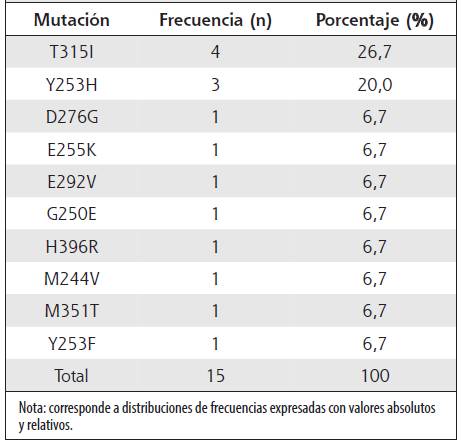
Se observó que 37 de los 73 pacientes que no alcanzaron RMM a los 12 meses (27,8% del total de pacientes del estudio), no lograron obtener respuesta óptima a lo largo del estudio. Se confirmaron 12 pacientes que perdieron la RMM en una mediana de tiempo de 5 meses de haberla adquirido, considerándose un total de 49 pacientes como no respondedores al tratamiento. Al analizar la presencia de mutaciones en el gen ABL en este subgrupo, 12 de 49 pacientes (24,5%) presentaron algún tipo de alteración concreta (Cuadro 2), siendo la T315I la mutación encontrada con más frecuencia, con un total de 4 casos. En tres pacientes con ABL1 mutado se encontró una mutación adicional posterior al cambio terapéutico de la primera mutación: Y253H posterior a una M351T en un paciente, y posterior a la G250E en otro, y una E255V posterior a una E292V.
Con respecto al análisis de supervivencia, se determinó que 59 pacientes (44,4%) presentaron al menos un tipo de evento: escalamiento en la dosis inicial de imatinib (16,5%; n=22), suspensión del imatinib por intolerancia (21,1%; n=28), cambio a nilotinib (15,8%; n=21) o dasatinib (2,2%; n=3), progresión (5,3%; n=7), muerte (8,3%; n=11), pérdida de RMM (9,0%; n=12), pérdida de RHC (5,3%; n=7), o detección de una mutación (9,0%; n=12). La supervivencia libre de evento a 3 años fue del 65,7%.
Por otra parte, la SLP en la población total en estudio fue del 92,2% en 3 años. Hubo una SLP a 3 años, menor en los pacientes que no respondieron al tratamiento según las guías ELN actuales, en comparación con los que sí lo hicieron, aunque esta no alcanza significancia estadística (87,3% contra 94,8%, respectivamente, p = 0,201; Figura 1A). La SG del grupo en estudio a los tres años fue del 89,2%; al comparar los mismos grupos se determina una SG a tres años del 96,3% para los pacientes buenos respondedores, respecto a un 77,4% en el grupo de no respondedores (p=0,002; Figura 1B).
Discusión
Los datos demográficos obtenidos de pacientes con la LMC en el presente estudio mostraron semejanzas entre la situación actual en Costa Rica con lo reportado mundialmente. En el país, la mayor proporción de la enfermedad en hombres es equiparable a lo reportado en la bibliografía mundial.6-7 La mediana de edad de presentación de la enfermedad es similar a la reportada en Argentina y Suramérica.6,8 Sin embargo, esta edad es mayor a la reportada en África y en la región sur y sureste de Asia, y menor a la reportada por Europa, Norteamérica y Oceanía.7
El porcentaje de la RHC en el país es semejante al reportado por estudios realizados en España, Italia, así como en el estudio IRIS.9-12 En aquellos pacientes que no lograron el alcance de la respuesta en el tiempo establecido, o bien, que la perdieron a lo largo del período en investigación, esto puede responder a variaciones individuales en la respuesta al tratamiento, intolerancia al medicamento o falta de adherencia al tratamiento. La falta de adherencia es considerada internacionalmente como la primera causa de fallo al tratamiento.2 Aunque en el estudio no se evaluó este parámetro, el pobre seguimiento molecular de la enfermedad en algunos pacientes, puede sugerir poco apego a las citas médicas y mala adherencia al tratamiento.
El seguimiento molecular en el país se realiza según las recomendaciones de las guías ELN actuales.2 A pesar del esfuerzo por cumplir con lo indicado en estas guías, 3 de cada 10 pacientes con LMC no cumplen con el monitoreo recomendado para la LMC, cada 3 meses durante el primer año, e incluso el mal seguimiento es más evidente una vez alcanzada la RMM, donde se recomienda una evaluación al menos cada 6 meses, según criterio médico. En el país, debido a la organización institucional de la CCSS, la mayoría de los departamentos de Hematología se encuentran en los hospitales del Gran Área Metropolitana; esto significa que hay algunos pacientes con problemas de desplazamiento hacia estos hospitales, lo cual puede incidir negativamente en la adherencia al tratamiento y a los protocolos de seguimiento.2 Existen, además, limitaciones económicas de los pacientes, diferencias en la disponibilidad de las drogas entre los centros de la institución, y un discreto repertorio de pruebas de laboratorio referentes al monitoreo de la enfermedad, que pueden contribuir a que no se alcancen las metas de las guías internacionales.13
Al clasificar la RMM acorde a las guías de la ELN actuales, se obtienen porcentajes menores a lo reportado por el estudio IRIS español, argentino e italiano.11,12Esta menor respuesta puede deberse a varias razones, como interacciones medicamentosas o falta de adherencia al tratamiento, así como al monitoreo irregular de la respuesta. También habría que tener en cuenta que, al ser una enfermedad de curso crónico en población de más de 50 años, es probable la existencia de comorbilidades que afecten la absorción gastrointestinal, el metabolismo de primer paso, la unión plasmática a proteínas, o la entrada celular del inhibidor de tirosina quinasa.14
Los pacientes que tuvieron escalamiento en el imatinib terminaron presentando intolerancia a dicha dosis, lo cual está reportado en la bibliografía como un incremento en los efectos adversos ante dosis altas de imatinib.14 Todo esto incide en que la ELN no recomiende el escalamiento a 800 mg como segunda opción de tratamiento, sino que se pase directamente a un fármaco de segunda generación. Sin embargo, en Costa Rica se realiza el escalamiento como un requisito previo para que el Comité Central de Farmacoterapia de la institución apruebe el cambio a segunda línea.
Concordante con lo encontrado en la bibliografía, la mutación T315I es la más prevalente entre los pacientes costarricenses con ABL1 mutado, siendo también la más importante, ya que es resistente a los tres TKI disponibles en el país: imatinib, nilotinib, dasatinib. Aparte de esta mutación, la Y253H también está reportada como una de las mutaciones más prevalentes entre los pacientes con LMC, aunque para esta si se encuentra disponible la opción terapéutica del dasatinib. También se presenta el hallazgo de doble mutación en tres pacientes, lo cual es conocido en la bibliografía como resistencia policlonal al imatinib,14 con respuesta solamente a fármacos no disponibles en el país, como el Ponatinib.
Al analizar la supervivencia libre de evento de la población estudiada, se nota que es similar a la reportada por Gugliotta en el estudio italiano, sin embargo, es comparativamente menor a la esperado para la población española.12,15Con este dato se puede inferir que, a tres años, menos de un 35% de la población presentará un suceso de escalamiento, suspensión, cambio de fármaco, progresión, muerte, pérdida de alguna de las respuestas o detección de mutaciones, lo cual sugiere un balance positivo en la aplicación de este tipo de terapias en los pacientes de LMC en el país.
La SLP en el país es coherente a lo esperado, según el estudio IRIS, así como lo reportado por distintas regiones geográficas. Aunque existe una diferencia porcentual entre los grupos respondedores y no respondedores a la terapia, el poder de significancia no es suficiente para definir ambos grupos como estadísticamente diferentes. Caso contrario sucede con la SG, donde existe una diferencia significativa entre los respondedores y los no respondedores al tratamiento. De igual manera, se puede comparar esta supervivencia a lo observado en otros estudios, en donde se evidencia una alta correlación de la población respondedora con lo observado mundialmente, y un contraste con respecto a los malos respondedores.9-12,15Al trabajar con una población cuyos eventos de progresión de la enfermedad representaron pocos casos, no se pudo tener una diferencia significativa entre los dos grupos de comparación, lo que constituye una limitación del estudio.
Tomando en cuenta que el Laboratorio de Diagnóstico Molecular del Hospital Nacional de Niños es el único centro hospitalario público del país que cuenta con la tecnología para diagnóstico molecular de LMC, el estudio ofrece un panorama claro de la situación de estos pacientes en el país. No obstante, debe considerarse la limitación de no incluir a la población atendida en el sector privado, así como a los pacientes diagnosticados fuera de ese peróodo, cuyo manejo clínico ha variado debido a mejoras en el seguimiento molecular, por ejemplo: detección de respuestas moleculares profundas, que pueden llevar incluso a la suspensión de tratamiento con TKI2 y los beneficios consecuentes para el paciente, e incluso para el manejo financiero de la LMC dentro de la CCSS.
El estudio exhibió el panorama epidemiológico de la LMC en el país, en donde es indispensable orientar una buena respuesta a la enfermedad en el paciente mediante el cumplimiento de las guías internacionales. Es preciso abogar por una mayor accesibilidad al medicamento y la constante educación del paciente para fomentar la adherencia, mejorar el monitoreo de la enfermedad y así detectar, oportunamente, posibles fallos en la terapia. Es necesario continuar estudiando la enfermedad, con el fin demesclarecer las razones de la baja RMM y así formar indicaciones terapéuticas y de educación para mejorar aún más la respuesta y, por ende, la supervivencia de los pacientes con LMC en el país.
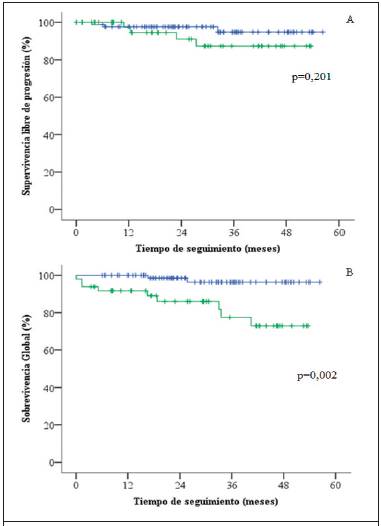
Figura 1 Curvas de Kaplan Meier referentes a supervivencia libre de progresión (A) y curva de supervivencia global (B) de pacientes buenos respondedores (azul) contra malos respondedores al tratamiento (en verde) con TKI (comparación realizada por medio de Chi-cuadrado), con una significancia del 5% (p=0,05; long rank test; 1 grado de libertad).