La albahaca (Ocium basilicum) es una laminaceae de crecimiento bajo (entre 30-130 cm), con hojas dentadas y de textura sedosa, que mide de 3 a 11 cm de largo, por 1 a 6 cm de ancho.1 Es un cultivo de importancia económica global, con una producción mundial anual de 100 tipos de aceites esenciales.2,3
Al mismo tiempo, constituye parte de los registros etnobotánicos de países como Venezuela.4,5 Ha sido objeto de estudio en consideración a sus posibles efectos curativos: la albahaca, llamada popularmente en el Caribe como basil y basilik, es muy utilizada en medicina tradicional para curar afecciones gastrointestinales (diarreas, parasitismo), respiratorias (bronquitis, tos), dolor de oídos y reumatismo. Tópicamente, es usada en baños y cataplasmas para tratar afecciones de la piel.2 Sus componentes químicos han sido estudiados en varias ocasiones y entre ellos se han encontrado las siguientes sustancias: alfa pineno, beta-pineno, 1,8- cineol, linalol, camfor, metil chavicol (estragol), metil (Z)-cinamato, eugenol, beta-elemeno, metil (E)-cinamato, beta-cariofileno, beta-cubebeno, beta-bisaboleno y alfa-muurolol.6 Se le atribuyen propiedades antisépticas, antiinflamatorias, antiespasmódicas, analgésicas,7 relajantes,8 antimicrobianas y antivirales.9,10 El objetivo general de esta investigación fue aislar mediante cromatografía y espectroscopía, algunos componentes de esta especie vegetal, y evaluar el efecto hipoglicemiante de su extracto.
Métodos
Reactivos
Los reactivos de grado analítico se adquirieron en la casa Sigma-Aldrich, y corresponden a los siguientes: hipoclorito de sodio al 0,3%, metanol, hidróxido de potasio, ácido sulfúrico, ninhidrina, ácido bórico al 10%, ácido oxálico al 10%, anisaldehído, amoniaco, n-propanol, tolueno, ácido ascórbico, cloroformo, hexano, acetona, etanodiol, etanol, tolueno, diclorometano y sulfato de magnesio. Se usó también agua desprovista de iones, agua destilada.
Material vegetal
Las hojas y tallos de albahaca fueron adquiridos durante febrero de 2011, en la Fundación Jardín Botánico de Mérida, sector la Hechicera, estado Mérida, Venezuela. La clasificación taxonómica fue realizada por esta misma fundación.
Extracto metanólico de albahaca
Las hojas y tallos fueron lavados con agua destilada y desinfectados sin agitar, con una solución de hipoclorito de sodio al 0,3% v/v. Se sometieron 15 kg de las muestras vegetales a un proceso de maceración en fresco en 20L de metanol al 70% v/v, y se colocaron en un frasco ámbar.11El macerado se concentró y se sometió al vacío, obteniéndose 139,56g de un extracto de color oscuro, el cual se empleó para los análisis cromatográficos y la administración a los animales, para evaluar su efecto hipoglicemiante.
Estudio, purificación y caracterización de compuestos
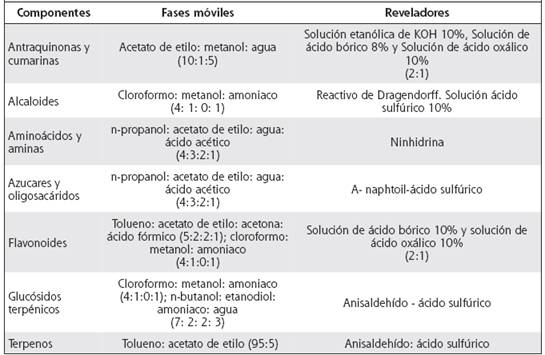
Se pesaron 20 g del extracto seco de albahaca y se disolvió en metanol; después se concentró el volumen de la solución por un rotavapor (Yamato análogo, TSRE300AW, reactivos y equipo S.A de CV, México) durante 30 min, hasta obtener 2mL, de los cuales se tomaron alícuotas de 10μL de cada muestra y se aplicaron a las placas cromatográficas (marca Merck),12, 13 con las distintas fases móviles, según el metabolito por identificar (Cuadro 1).
Cuadro 1 Distribución de fases móviles y reveladores cromatográficos, según los metabolitos estudiados
Se llevó a cabo la caracterización de los principales compuestos obtenidos en el estudio fitoquímico mediante espectrofotometría, utilizando dos espectrómetros: el Milton Roy Spectronic 1201 y el Perkin Elmer 599. Los espectros se obtuvieron mediante un equipo avance DRX Bruker 300 Mhz con software: Iris 6.5, xwinnmr 3.0. (2000). Las formas estructurales de los compuestos se verificaron empleando un programa de computación comercial ChemDraw, versión 12.0 (Addlink software científico, Madrid, 2012).
Fraccionamiento biodirigido
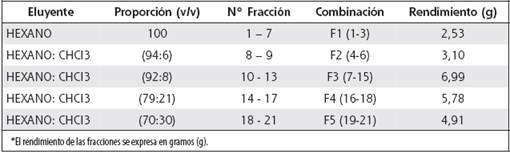
Una parte del extracto metanólico se sometió a fraccionamiento primario por cromatografía de columna abierta.7 Se obtuvo un total de 21 fracciones con un volumen de 175 ml cada una, las cuales se asociaron por similitud cromatográfica, obteniéndose 5 fracciones, que se destinaron a las pruebas de hipoglucemia en un modelo experimental de ratas hiperglicémicas. En el Cuadro 2 se muestra el número de fracciones, sus combinaciones y el rendimiento de estas, expresado en gramos.
Animales experimentales
Los protocolos aplicados se diseñaron siguiendo las buenas prácticas de manejo y empleo de animales de laboratorio.14,15
Se emplearon 44 ratas macho de la cepaC57BL/6, las cuales fueron adquiridas en el Bioterio del Instituto Venezolano de Investigaciones Científicas (IVIC). Los pesos de las ratas oscilaron entre 300 y 370 g. Previo a la realización del experimento, la ratas fueron colocadas en jaulas individuales y se les sometió a una temperatura de entre 21-22°C, en condiciones de ciclo claro/oscuro de 12 h.13,16 Se les suministró una dieta comercial granulada (Protinal®) y la ingesta de agua fuead libitum.
Inducción experimental de la diabetes y cuantificación de la glucosa “in vivo”
A las ratas se les administró, a través de la vena coccígea, una solución de aloxano monohidratado al 10% (v/v), en dosis única de 160mg/kg de peso corporal durante 5 días, diagnosticándose hiperglicemia cuando la concentración de glucosa sanguínea fuese >180mg/dL. Se evaluó la glicemia a partir de muestras seriadas tomadas de la vena lateral de la cola, y la sangre se procesó con bandas reactivas para análisis, utilizando un glucómetro (Optium Xcced, Abott).
Protocolo experimental
Se utilizaron 44 animales, los cuales fueron subdivididos en 11 grupos, a saber: Grupo I(control): cuatro ratas a las cuales se les suministró 1 mL de solución fisiológica de NaCl + dextrosa, ambas al 0,45% v/v; Grupo II: cuatro ratas: 160 mg/kg de aloxano monohidratado (AM) por kilogramo de peso corporal (PC); Grupo III: cuatro ratas: 160 mg/kg peso corporal de aloxano monohidratado + 400 μg/kg peso corporal de sitagliptina®; Grupo IV: cuatro ratas: 160 mg/kg peso corporal de aloxano monohidratado (AM) + 1,0 g/kg de PC del extracto metabólico de albahaca (EMA); Grupo V: cuatro ratas: 160mg/kg PC de AM + 1,5 g/kg PC del extracto metanólico de albahaca; Grupo VI: cuatro ratas: 160 mg/kg PC de AM + 2,0g/kg PC del extracto metanólico de albahaca; Grupo VII: cuatro ratas: 160 mg/kg PC de AM + 200 mg/kg PC de la fracción 1; Grupo VIII: cuatro ratas : 160 mg/kg PC de AM+ 200 mg/kg PC de la fracción 2 ; Grupo IX: cuatro ratas: 160 mg/kg PC de AM + 200 mg/kg PC de la fracción3; Grupo X: cuatro ratas: 160 mg/kg PC de AM + 200 mg/kg PC de la fracción 4; Grupo XI: cuatro ratas:160 mg/kg PC deAM + 200 mg/kg PC de la fracción 5. El Cuadro 3 muestra la distribución de los grupos. Todos los tratamientos fueron aplicados por vía intraperitoneal y los correspondientes a los grupos II al XI fueron disueltos en polisorbato sódico 80. (Tween 80) al 5% v/v en agua destilada. La frecuencia de administración fue cada 24 h durante 5d.
Cuadro 2 Fraccionamiento primario del extracto, proporción, número de fracciones y combinaciones y rendimiento de estas*
Análisis estadístico
Los valores obtenidos fueron expresados como la media (χ) ± el error estándar de la media (EEM). El análisis estadístico de los datos obtenidos y la interpretación de las diferencias se realizaron mediante una prueba descriptiva general de la variable concentración plasmática de glucosa por grupo (tratamiento), utilizándose para ello la prueba no paramétrica de Kruskal Wallis. Se consideró una diferencia estadísticamente significativa para aquellos valores que tuvieron una probabilidad menor o igual a 0,05 (P≤0,05). El paquete estadístico usado fue el Statistix 8.0 de ambiente Windows (2011).
Resultados
Estudio fitoquímico
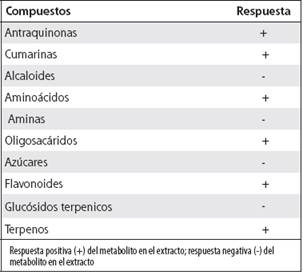
El estudio fitoquímico cualitativo realizado, permitió determinar la presencia de ciertos grupos funcionales de compuestos, los cuales se resumen en el Cuadro 4.
Caracterización de los compuestos aislados en el estudio fitoquímico
En el espectro de RMN-1H se estimaron señales para hidrógenos a dH=4,13 (1H, dd, H-1a), 4,11 (1H, dd, H-1b), 3,87 (1H, m, H-2), y 3,66 (1H, dd, H- 3a), 3,59 (1H, dd, H-3b), y carbonos a dC C =55,1 (C-1), 69,1 (C-2), y 63,3 (C-3), los cuales coinciden con las composición estructural de 1-monoglicérido, facilitando la identificación al sistema de glicerol, según la bibliografía (Kawagishi et al., 2002; Konishi et al., 2004) . La cromatografía acoplada a espectrometría de masas permitió determinar tres espectros con los iones moleculares: 312 M/Z; 354 M/Z y 410 M/Z, siendo: nandecilato de metilo, (C20O2H40), behenato de metilo (C23O2H46), y hexacosanoato de metilo (C27O2H54), respectivamente.
También se determinó la presencia de un alcaloide indólico: la didehidroibogamina (18-metoxicarbonil-3,4), un compuesto incoloro que corresponde al metil-benzeno (monoterpeno:1-isopropil-4), y el flavonoidetrimetoxiflavona (5, 7,3´-trihydroxi-3, 6, 4).
Los compuestos mencionados, exceptometil-benzeno, son reportados por primera vez para la especie vegetal Ocium basilicum. Las figuras 1, 2 y 3 muestran las respectivas estructuras químicas.
Efectos producidos por la administración del extracto metanólico de la albahaca y sus fracciones sobre la glicemia
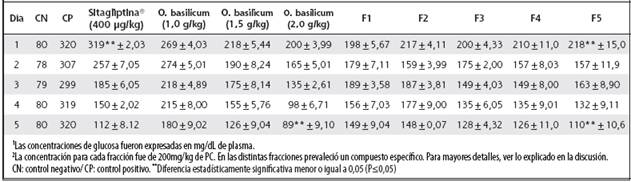
En el Cuadro 5 se muestra el efecto hipoglicemiante generado tras la administración intraperitoneal del extracto metanólico de albahaca y las cinco fracciones asociadas por similitud cromatográfica en ratas hiperglicémicas. Los valores del grupo tratado con sitagliptina® (Grupo II) como fármaco control hipoglicemiante, arrojaron diferencias estadísticamente significativas (P≤0,05) con respecto a las ratas con hiperglicemia experimental (Grupo III). Un efecto similar (P≤0,05) se evidenció en los grupos a los cuales se les administró la albahaca a dosis crecientes entre 1,0 y 2,0 g/kg (grupos IV al VI).
Discusión
Los resultados de la presente investigación permitieron identificar mediante estudios fitoquímicos, distintos metabolitos secundarios, entre los que se encuentran: fenilpropanoides, monoterpenos y sesquiterpenos, así como también metabolitos derivados de los ácidos grasos con distintas características químicas, como ésteres y aldehídos. Según investigadores,11 serían los responsables del aroma que caracteriza esta especie vegetal. No obstante, otros autores9 difieren de estas afirmaciones y señalan que estos compuestos han sido escasamente reportados en la albahaca y se sintetizan a partir de componentes en altas concentraciones, como los ácidos grasos insaturados y poliinsaturados por diferentes rutas bioquímicas.
Posiblemente, el compuesto 1-monoglicérido, aislado en este estudio, constituye un precursor de estos metabolitos.
En este ensayo, también se obtuvo un alcaloide indólico, el 18-metoxicarbonil-3,4-dehidroibogamina (Figura 1), conocido como catarantina, el cual es de interés químico, ya que se emplea en la síntesis de anhidrovinblastina, un bisindólico antitumoral. Este compuesto es un constituyente principal de la familia vegetal de las Apocynáceas que se ha investigado como alternativa en la fitoterapia del cáncer linfático,18 incluso se refiere como integrante de complejos proteicos en pro de las enterohormonas,19 lo que destaca su particular interés biomédico.
Asimismo, se aisló el monoterpeno1-isopropil-4-metil-benzeno, conocido como p-cimeno, derivado de la deshidrogenación de algunos terpenos. Este compuesto ha sido reportado 20,21como tratamiento en la hiperplasia prostática benigna sintomática (BPH) y en las infecciones de las vías urinarias. La bibliografía lo refiere como responsable de modificaciones covalentes y demás reacciones bioquímicas que inducen a disminuciones drásticas de la concentración plasmática de glucosa, incluso se ha demostrado la estimulación de los gránulos insulinógenos secretores de las células beta del páncreas, incrementando la biosíntesis de insulina,19 lo que mantiene relación con los resultados obtenidos, tras la administración de la F1 y la F2, respectivamente.
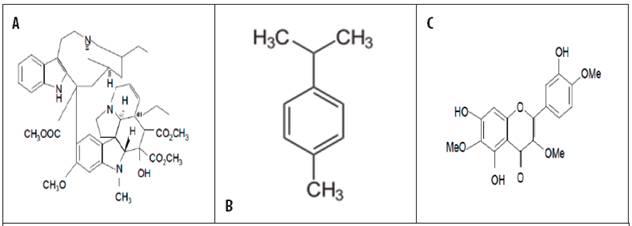
Figura 1 A. Compuesto purificado del extracto metanólico. 18-metoxicarbonil-3,4-didehidroibogamina. B. Compuesto purificado del extracto metanólico: 1-Isopropil-4-metil-benzeno. C. Compuesto purificado del extracto metanólico 5,7,3´-trihydroxi-3,6,4´-trimetoxiflavona
Cuadro 4 Evaluación fitoquímica de compuestos y metabolitos secundarios del extracto metanólico de albahaca*
Los bioensayos realizados demuestran que las fracciones 3 y 4 ejercen, de manera independiente, un efecto hipoglicemiante similar a lo reportado para el T. foenun-graceum, 23 sugiriéndose que la administración experimental combinada de los compuestos 4 y 5 obtenidos de las hojas, tallos y raíces de Ibervillea sonorae por cromatografía de columna, induce hipoglucemia.
El 18-metoxicarbonil-3,4-didehidroibogamina (catarantina) y hexacosanoato de metilo que destacan en las fracciones F1 y F5, respectivamente, pueden ser responsables del efecto hipoglucémico, atendiendo posibles asociaciones con proteasas del metabolismo de los ácidos grasos y los glúcidos, siendo un grupo bloqueador de la enzima dipeptidil peptidasa IV (cuya inhibición da por resultado incremento considerable de las concentraciones de enterohormonas capaces de incrementar la secreción insulínica de manera glucosa-dependiente) y activador de las subunidades de los receptores transmembrana de insulina.
La disminución en la concentración plasmática de glucosa, comprobada en el presente estudio, se podría explicar por la presencia del compuesto fenólico: 5, 7, 3´-trihydroxi-3, 6,4´-trimetoxiflavona (Figura 3). La bibliografía refiere que ciertos flavonoides están ligados a los receptores proliferadores de peroxisomas (PPARs), los cuales son antagonistas de los receptores de glucagón, con la realimentación positiva de los receptores de insulina.26
Fármacos como la pioglitazona y rosiglotazona actúan como sensibilizadores en el receptor PPAR-γ, el cual se relaciona con la regulación por excitación y maduración del adipocito,27,28 lo que sugiere amplia vinculación con los resultados obtenidos (Cuadro 5), tras la administración de la F5 (218 mg/dL a 110 mg/dL ± 15). 23,24,25
Cuadro 5 Concentración de la glucosa sanguínea tras la administración diaria de sitagliptina®, extracto metanólico de albahaca a dosis crecientes (1,0 g/kg, 1,5 g/kg y 2,0 g/kg) y las fracciones 1 a la 51,2
En conclusión, la albahaca es una planta medicinal opcional en el tratamiento de la diabetes mellitus y en atención a los compuestos asilados, se recomienda realizar nuevos estudios que evalúen su cinética, formalizando así la inclusión de estaespecie en el tratamiento de tal patología, al mismo tiempo que se podría disminuir los riesgos de salud pública por consumo indiscriminado de la albahaca.
Conflicto de interés: los autores cumplimos nuestra conformidad de envío para revisión y arbitraje, y declaramos no tener ningún conflicto de interés con el presente trabajo. melendezjmanuel@gmail.com