Introducción
El intestino delgado es un órgano altamente inmunogénico debido a que presenta gran cantidad de folículos linfoides que, junto con la microbiota, están encargados de la respuesta inmune innata y de la activación de mecanismos inmunológicos complejos.1-3 Los primeros trasplantes realizados en el mundo fueron de manera experimental, ya que la terapia de inmunosupresión estaba poco desarrollada y no permitía resultados óptimos a largo plazo. Fue hasta 1988 cuando se efectuó el primer trasplante de intestino exitoso en el mundo, por el Dr. Deltz, en Alemania.4,5 El éxito, en gran parte, fue por la introducción de la molécula FK-506 (tacrolimus), que a su vez marca el inicio de programas de trasplante estructurados y con adecuados resultados.6 En la década de los 90 deja de ser un procedimiento experimental y pasa a convertirse en la única opción de cura en la insuficiencia intestinal irreversible asociada a las complicaciones de la nutrición parenteral total prolongada.7
La base de datos del registro de trasplante de intestino (ITR), la cual es una base de datos mundial, reporta 2887 trasplantes hasta febrero de 2013, y existen a la fecha más de 90 centros especializados, con una supervivencia del paciente, a 1 año, del 77%; a 5 años, del 58%, y a 10 años, del 47%, y supervivencia del injerto, del 71%, 50% y 41%, respectivamente.8 El objetivo de este trabajo es reportar el primer trasplante de intestino de Costa Rica y Centroamérica.
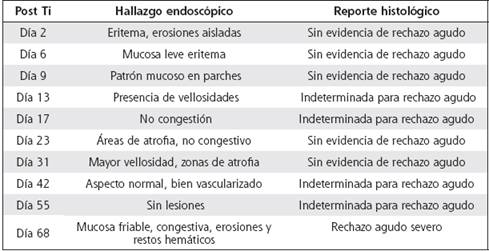
Cuadro 1. Monitoreo del injerto, ileoscopías y reportes histológicos
Presentación del caso
Masculino de 18 años previamente sano, sufrió herida por arma blanca en abdomen con lesión de la cabeza de páncreas, arteria gastroduodenal y vena cava infrarenal, el 13 de diciembre de 2013, atendido en el “Hospital San Juan de Dios”.
Se realizó cirugía de control de daños: pancreatoduodenectomía (sin anastomosis) y rafia de vena cava infrarrenal. En las siguientes 24 horas desarrolla isquemia mesentérica segmentaria de ileon distal con torsión del pedículo mesentérico superior, por lo que se le realiza resección del área comprometida y apendicectomía. 48 horas después de la segunda intervención desarrolla necrosis total del intestino delgado y necrosis de ciego; ante estos hallazgos el caso es reportado al hospital “Dr. Rafael Angel Calderón Guardia” ya que el “San Juan de Dios” no cuenta con posibilidades de trasplante intestinal.
El paciente ingresa 72 horas después del primer evento, con abdomen abierto y bolsa de Bogotá. Se le realiza resección de intestino delgado, colon derecho y mitad del colon transverso, quedando en espera de un implante de intestino. En esa misma fecha se presentó un donante cadavérico compatible con el receptor, en otro centro hospitalario. Al día siguiente se realiza con éxito el trasplante de intestino de donante cadavérico. El donador fue un masculino joven con compatibilidad de grupo, Rh, talla y peso.
Las anastomosis vasculares se efectuaron de la arteria mesentérica superior del receptor, a la arteria mesentérica superior del donante, y de la vena mesentérica superior del receptor, a la vena mesentérica superior del donante. La reperfusión fue exitosa con peristalsis inmediata, para un tiempo de isquemia total del injerto, de 6 horas. Como el receptor tenía pancreaticoduodenectomía de trauma, fue necesario realizar reconstrucción pancreático-yeyunal, colédoco-yeyunal y gastroyeyunal tipo Whipple. Se colocó sonda nasoyeyunal y se realizó ileostomía terminal para monitorizar el injerto. En este caso no se realizó anastomosis ileo-cólica, debido al gran edema de pared colónica, por su antecedente de trauma reciente y cirugías múltiples. Por último, debido al edema postreperfusión del intestino, no fue posible efectuar el cierre primario de la cavidad, por lo que se coloca terapia con presión negativa como medida alterna. En intervenciones posteriores se colocó malla dual y, finalmente, se cerró la cavidad.
La inmunosupresión utilizada fue con basiliximab y metilprednisolona como terapia de inducción, y tacrolimus, micofenolato mofetil con predinisona, como terapia de mantenimiento. Hubo cobertura antibiótica con ceftazidime y metronidazol; profilaxis antiviral con ganciclovir y, posteriormente, valganciclovir; profialxis antifúngica con fluconazol, protección gástrica con omeprazol, y aplicación de prostaglandina E (alprostadil) por 5 días. La tromboprofilaxis se hizo con enoxaparina.
Se inició nutrición enteral con fórmula elemental y glutamina. A los 7 días se cambió a nutrición parenteral por pérdida accidental de sonda nasoyeyunal. Se mantuvo por 29 días con nutrición parenteral total. Se avanzó a vía oral normal a los 40 días.
Después del trasplante se tuvo que reintervenir en 7 ocasiones, mayoritariamente por fuga de anastomosis colédoco-yeyunal y pancreático-yeyunal.
Desarrolló lesión renal secundaria al inhibidor de calcineurina (tacrolimus), por lo que se cambió a un inmunosupresor de tipo m-Tor (Sirolimus) no nefrotóxico.
El monitoreo del injerto fue mediante ileoscopías dos veces por semana durante el primer mes, y luego semanalmente, sin observarse rechazo hasta su episodio final (Cuadro 1).
Se egresó 51 días después del trasplante, en condición ambulatoria y con adecuada vía oral. El paciente reingresa tras 4 días de su egreso, por vómitos, deshidratación y trastorno hidroelectrolítico, con reagudización de la lesión renal. Durante su segunda hospitalización desarrolló leucopenia severa, trombosis venosa profunda de ambas venas iliacas comunes, sin repercusión sistémica; además, asoció intolerancia a la vía oral. Finalmente fallece el 24 de febrero de 2014, a 68 días del trasplante, por falla orgánica múltiple, secundaria a rechazo agudo severo del injerto, que no respondió a las medidas antirechazo. No se retiró el órgano para resolver su falla orgánica múltiple, por negativa familiar.
Discusión
Este es el primer caso realizado en el país; previamente solo se contaba con trabajos experimentales (no publicados) efectuados con perros en los laboratorios de fisiología de la Universidad de Costa Rica, por los doctores Clive Montalbert-Smith y Mario Sánchez Arias.
El trasplante de intestino se considera la medida terapéutica de elección para la falla intestinal irreversible cuando ya se han agotado otras posibilidades de tratamiento, como la rehabilitación intestinal o la aparición de las complicaciones de la nutrición parenteral total prolongada.4, 7 Se estima que de 2 a 3 personas por millón de habitantes, sufrirán falla intestinal por año, de los cuales el 15% será candidato para trasplante de intestino.9
La principal indicación para trasplante de intestino en cualquiera de sus modalidades es la falla intestinal irreversible secundaria a: trombosis esplácnica extensa, catástrofe abdominal, tumores benignos o malignos de bajo grado, fallo de la nutrición parenteral total a largo plazo por pérdida de 2 o más accesos venosos centrales, 2 o más episodios anuales de infección, asociados al catéter y trastorno hidroelectrolítico refractario.9-12
Actualmente el trasplante de intestino aislado es la técnica más utilizada, sin embargo, según las características del paciente se puede realizar trasplante de intestino e hígado simultáneo, o trasplante multivisceral, que incluye: estómago, páncreas, intestino e hígado con o sin bazo, según sea la afección de los diferentes órganos.9,12
El caso que aquí se reporta fue de intestino aislado y tuvo mayor dificultad técnica por el antecedente de pancreatoduodenectomía en la cirugía de control de daños, y debido a la inflamación de los tejidos por las cirugías previas, que lo convirtió en un caso urgente de trasplantar aún en esas circunstancias, ya que se requería la reconstrucción del colédoco, del conducto pancreático y del estómago con el intestino trasplantado. Debido al importante edema de las asas de intestino delgado, posterior a la reperfusión y al proceso inflamatorio del resto de los tejidos por sus antecedentes quirúrgicos, no se pudo realizar el cierre primario de la cavidad abdominal, y se utilizaron métodos alternativos de cierre que respetaran los principios de aislamiento y protección de los tejidos, como la terapia con presión negativa, malla dual y bolsa de Bogotá, lo que permitió acceso y cierre adecuado posterior a las reintervenciones.13-15
El adecuado manejo inmunosupresor es indispensable para evitar el rechazo agudo como consecuencia de la lesión de isquemia-reperfusión, infección o trauma del injerto.1 Es la complicación más relevante, y se presenta durante los primeros 90 días posteriores al trasplante, en el 92% de los casos de intestino aislado y en el 66% cuando es multivisceral.4 Otras consecuencias que se derivan de la inmunosupresión son: procesos infecciosos, enfermedad linfoproliferativa, tumores de novo, disfunción renal y mielotoxicidad, con más frecuencia que en otros tipos de trasplantes.12,16 Previo al rechazo agudo y la mielotoxicicdad, se presentó disfunción renal, y después de descartarse otra causas, fue atribuida al uso del inhibidor de calcineurina y su conocido efecto nefrotóxico, lo que llevó al cambio con el agente m-Tor.4,17 Para el monitoreo del injerto se realizaron ileoscopías con su respectivo reporte histológico, como lo dictan las normas internacionales: 2 veces por semana durante el primer mes y una vez por semana durante los próximos 2 meses, en este caso, hasta el día de fallecimiento.4,18
La mayoría de los pacientes alcanzan deshabituación de la nutrición parenteral total durante el primer mes del procedimiento, sin embargo, hay reportes de pacientes que necesitan soporte nutricional complementario prolongado después del trasplante, y algunos nunca llegan a alcanzar independencia;19 con este paciente se logró la deshabituación de la nutrición parenteral a los 40 días posteriores altrasplante.
El trasplante de intestino es un procedimiento de alta complejidad que requiere la intervención de múltiples disciplinas. La realización del primer caso en Costa Rica y Centroamérica es un paso más para ofrecer a los pacientes con falla intestinal, la posibilidad de vida normal, sin dependencia de la nutrición intravenosa (que obliga al internamiento prolongado), sobre todo en un país donde la nutrición parenteral ambulatoria todavía no se ha desarrollado adecuadamente. La consolidación de un programa de trasplante de intestino, cada vez más reafirma los alcances de un trabajo en equipo. A la fecha de esta publicación ya se han realizado 2 trasplantes de intestino.
Conflicto de interés: ninguno masanchezarias@yahoo.com
Abreviaturas: AR, artritis reumatoide; EII, enfermedad inflamatoria intestinal; PG, pioderma gangrenoso.
Trabajo realizado en Programa de Trasplantes
de órganos abdominales del Hospital “Dr. Rafael Ángel Calderón Guardia”Fuentes de apoyo: ninguna