Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Acta Médica Costarricense
On-line version ISSN 0001-6002Print version ISSN 0001-6012
Acta méd. costarric vol.51 n.2 San José Apr. 2009
Warner Alpízar-Alpízar1, 2*, Clas Une2, Rafaela Sierra2
Resumen
La infección por Helicobacter pylori produce, en algunos pacientes, inflamación crónica en el estómago, gastritis atrófica y cáncer gástrico. Los mecanismos moleculares que conducen de la infección a la inflamación crónica y al cáncer son desconocidos. La magnitud y el proceso de la inflamación dependen del tipo de cepa de H. pylori y de la respuesta del hospedero ante la infección. Esta respuesta inflamatoria está regulada por citoquinas, algunas de las cuales han sido asociadas con cambios en la secreción de ácido en el estómago y con el riesgo de desarrollar cáncer gástrico y varias lesiones gástricas precancerosas. Sin embargo, la relación entre citoquinas y cáncer gástrico no es del todo clara. Esta revisión se enfoca en los procesos inflamatorios asociados con el desarrollo del cáncer gástrico.
Descriptores: Inflamación, citoquinas, interleuquinas, Helicobacter pylori, cáncer gástrico
Abstract
Helicobacter pylori infection results, in some patients, in chronic inflammation of the stomach, atrophic gastritis and gastric cancer. The molecular mechanisms that lead from infection to chronic inflammation and gastric cancer are not understood. The degree of inflammation varies and depends on the H. pylori strain and the host response against the infection. The inflammatory response is regulated by cytokines, some of which have been associated with acid gastric secretion changes and with increased risk of stomach cancer and some precancerous lesions. Nevertheless, the relationship between cytokines and gastric cancer is not clear yet. This review focuses on the inflammatory processes associated with the development of gastric malignancies.
Key words: inflamation, cytokines, interleukins, Helicobacter pylori, gastric cancer.
A finales del siglo XIX, el patólogo Rudolf Virchow sugirió la posible asociación entre la inflamación y el desarrollo del cáncer. Sin embargo, no fue sino hasta hace pocas décadas cuando se comenzó a investigar sistemáticamente tal relación.1 Varios cánceres han sido asociados con infecciones crónicas causadas por virus o bacterias en las cuales la inflamación es uno los eventos claves.2,3
Una de las infecciones crónicas más extendidas mundialmente es la causada por Helicobacter pylori.4 Esta bacteria ha sido considerada por la Agencia Internacional para la Investigación en Cáncer (IARC/OMS), como un cancerígeno de primera clase, y es uno de los factores de riesgo más importantes de cáncer gástrico.5,6 La carcinogénesis gástrica inducida por H. pylori podría ser un paradigma para entender otros cánceres humanos asociados con agentes infecciosos.
Se presenta una revisión de las investigaciones más relevantes llevadas a cabo a la fecha sobre los procesos inflamatorios asociados con el desarrollo del cáncer gástrico.
Epidemiología del cáncer gástrico
El cáncer gástrico es la segunda causa de muerte por cáncer en el mundo, precedido por el de pulmón.5 Las tasas de incidencia de cáncer gástrico presentan variaciones muy marcadas entre los países y entre regiones de un mismo país.5,7,8 Aunque las tasas de incidencia de este tumor han venido disminuyendo en las últimas décadas, la cantidad absoluta de casos de cáncer gástrico va en aumento, debido al envejecimiento de la población.5
El cáncer gástrico se clasifica por su histología y su ubicación anatómica.9 Desde el punto de vista histológico, los subtipos intestinal y difuso son los más frecuentes. Estos tipos de cáncer presentan diferencias importantes en su etiología; el intestinal está más relacionado con factores ambientales, mientras que el de tipo difuso se asocia más con una predisposición genética.9,10 Anatómicamente, se distingue entre cáncer gástrico de la región proximal del estómago o cardias, y de la región distal de este, y entre ambos también se presentan diferencias etiológicas.11
Patogénesis de la enfermedad
El cáncer gástrico es el resultado final de una serie de eventos precancerosos iniciados por H. pylori, sustancias irritantes para la mucosa gástrica y otros factores ambientales que interactúan en diferentes etapas del proceso.10,12 Esto conduce al desarrollo de gastritis superficial y, posteriormente, gastritis crónica atrófica, que comienza en la región antral y asciende hacia el cuerpo, con la consecuente disminución en la producción de ácido (hipoclorhidria). La hipoclorhidria genera un ambiente más favorable para el crecimiento de H. pylori y facilita la colonización del estómago por parte de otras bacterias, con lo cual se produce la acumulación de compuestos carcinogénicos (productos del metabolismo de dichos microorganismos, o de los mecanismos de defensa del hospedero). Lo anterior aumenta la probabilidad de que se generen alteraciones a nivel celular y genómico, que conducen al desarrollo de cáncer gástrico.12,13
Helicobacter pylori y su participación en el desarrollo del cáncer gástrico
La mayoría de las personas infectadas por H. pylori no presentan síntomas. Sin embargo, quien porta esta bacteria posee un riesgo promedio entre dos y tres veces mayor de desarrollar cáncer gástrico, en comparación con personas no infectadas.8,13 Las personas infectadas en edades tempranas tienen un mayor riesgo de desarrollar la enfermedad.13
Algunas cepas son consideradas como más agresivas y han sido asociadas con un mayor riesgo de cáncer gástrico. Las cepas mayormente conocidas y mejor caracterizadas son aquellas que presentan los factores de virulencia VacA y CagA.4,13,14 VacA es una proteína citotóxica, codificada por el gen vacA, que induce a formación de vacuolas en células epiteliales que dañan dichas células. Todas las cepas de H. pylori producen dicha proteína, pero su expresión varía con base en polimorfismos existentes en sitios específicos de la secuencia del gen.15,16 Por su parte, las cepas CagA positivas producen una proteína codificada por el gen cagA, localizado en una región del genoma bacteriano conocida como la isla de patogenicidad Cag (PAI). Las cepas portadoras de PAI poseen un sistema de secreción tipo IV que funciona como aguja y permite "inyectar" la proteína CagA en el citoplasma de las células epiteliales del estómago. Una vez translocada al citoplasma, CagA es fosforilada y, en ese estado, desencadena una serie de eventos celulares como, por ejemplo, rearreglos del citoesqueleto celular, inducción de la expresión de citoquinas proinflamatorias, inducción de la proliferación celular y activación de oncogenes entre otros.17,18 Aunque los genes vacA y cagA no guardan relación entre sí, a menudo son coexpresados. El riesgo de desarrollar ciertas lesiones gástricas precancerosas y cáncer gástrico es aún mayor en personas infectadas con cepas que coexpresan genotipos específicos de ambos genes.19,20 Para mayor información respecto a estos y otros factores de virulencia se refiere al lector a Hakateyama17 y Kusters y cols.4
La respuesta inflamatoria y el desarrollo del cáncer gástrico
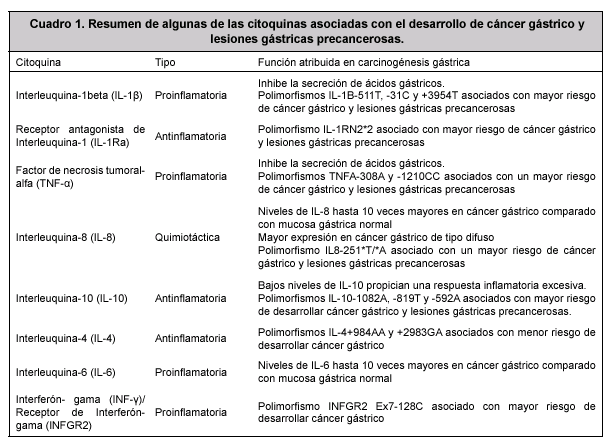
El resultado de la infección por H. pylori es una inflamación crónica caracterizada por la infiltración de varios tipos de células inflamatorias en la mucosa gástrica; entre ellas están los neutrófilos, macrófagos, células dendríticas y linfocitos T. Dicha respuesta inflamatoria está mediada por un complejo grupo de citoquinas proinflamatorias, quimiotácticas e inmunosupresoras, y moléculas reactivas derivadas de oxígeno y nitrógeno, las cuales son producidas por células inflamatorias y células epiteliales en respuesta a estímulos inducidos por la bacteria.21-23 Por ser esta una respuesta inflamatoria de tipo celular, resulta ineficaz para la eliminación de la bacteria, por lo que la infección persiste y la inflamación se prolonga durante muchos años.23 La secreción excesiva y prolongada de los mediadores de inflamación anteriormente mencionados, tiene consecuencias importantes en el contexto de la inflamación y la fisiología gástrica, las cuales podrían traducirse en un mayor riesgo de desarrollar cáncer gástrico. Algunas de las citoquinas que participan como mediadores de la respuesta inflamatoria contra H. pylori, han sido asociadas con un mayor riesgo de desarrollar lesiones gástricas precancerosas y cáncer gástrico (Cuadro 1).
Interleuquina-1.
Interleuquina-1 (IL-1) es una citoquina proinflamatoria secretada por varios tipos de células, siendo monocitos y macrófagos sus principales productores.24 IL-1 comprende tres diferentes proteínas (IL-1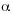 , IL-1ß e IL-1Ra), todas codificadas por genes diferentes (IL-1A, IL-1B e IL-1RN, respectivamente).25 Algunos polimorfismos de los genes IL1B e IL-1RN han sido asociados con mayor riesgo de desarrollar cáncer gástrico y lesiones gástricas precancerosas, tales como atrofia gástrica, hipoclorhidria y metaplasia intestinal.26-28 También se ha determinado que el riesgo de desarrollar cáncer gástrico, así como las lesiones mencionadas, es aún mayor para individuos portadores de ciertos genotipos en dichos polimorfismos, infectados con las cepas cagA+, vacAs1 y vacAm1 de H. pylori.29,30 Además de su papel en la respuesta inflamatoria inducida por H. pylori, IL-1ß también inhibe la secreción de ácidos gástricos.31,32 Por lo tanto, el aumento en la expresión de IL1ß, sumado a la disminución en la expresión del receptor antagonista de IL-1 (IL-1Ra), podría tener importantes consecuencias que incrementarían el riesgo de desarrollar esta neoplasia.
, IL-1ß e IL-1Ra), todas codificadas por genes diferentes (IL-1A, IL-1B e IL-1RN, respectivamente).25 Algunos polimorfismos de los genes IL1B e IL-1RN han sido asociados con mayor riesgo de desarrollar cáncer gástrico y lesiones gástricas precancerosas, tales como atrofia gástrica, hipoclorhidria y metaplasia intestinal.26-28 También se ha determinado que el riesgo de desarrollar cáncer gástrico, así como las lesiones mencionadas, es aún mayor para individuos portadores de ciertos genotipos en dichos polimorfismos, infectados con las cepas cagA+, vacAs1 y vacAm1 de H. pylori.29,30 Además de su papel en la respuesta inflamatoria inducida por H. pylori, IL-1ß también inhibe la secreción de ácidos gástricos.31,32 Por lo tanto, el aumento en la expresión de IL1ß, sumado a la disminución en la expresión del receptor antagonista de IL-1 (IL-1Ra), podría tener importantes consecuencias que incrementarían el riesgo de desarrollar esta neoplasia.
Factor de necrosis tumoral - alfa
El factor de necrosis tumoral-alfa (TNF-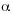 ) es una citoquina proinflamatoria que actúa como mediador central de la respuesta inmune contra muchas enfermedades infecciosas.33,34 Sin embargo, la sobreexpresión de esta proteína puede también contribuir al desarrollo de varios tipos de patologías.33,35
) es una citoquina proinflamatoria que actúa como mediador central de la respuesta inmune contra muchas enfermedades infecciosas.33,34 Sin embargo, la sobreexpresión de esta proteína puede también contribuir al desarrollo de varios tipos de patologías.33,35
Algunos polimorfismos del gen TNF-A (codifica para TNF-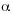 ) han sido relacionados con una mayor expresión de dicho gen y con un mayor riesgo de desarrollar cáncer gástrico y ciertas lesiones gástricas precancerosas.36-41 De igual manera, individuos infectados con H. pylori presentan mayores niveles en sangre de TNF-
) han sido relacionados con una mayor expresión de dicho gen y con un mayor riesgo de desarrollar cáncer gástrico y ciertas lesiones gástricas precancerosas.36-41 De igual manera, individuos infectados con H. pylori presentan mayores niveles en sangre de TNF- , en comparación con personas no infectadas.42 TNF-
, en comparación con personas no infectadas.42 TNF- es sobreexpresada en etapas tempranas de la infección por dicha bacteria y esta, a su vez, induce la expresión de otras citoquinas proinflamatorias y quimioquinas, amplificando de esta manera la respuesta del huésped contra la infección,43 de la misma forma que IL-1ß, TNF-
es sobreexpresada en etapas tempranas de la infección por dicha bacteria y esta, a su vez, induce la expresión de otras citoquinas proinflamatorias y quimioquinas, amplificando de esta manera la respuesta del huésped contra la infección,43 de la misma forma que IL-1ß, TNF- también actúa como un inhibidor de la secreción de ácido gástrico.31
también actúa como un inhibidor de la secreción de ácido gástrico.31
Interleuquina-8
Interleuquina-8 (IL-8) es una citoquina quimiotáctica, importante en la migración y activación de linfocitos y neutrófilos, lo que amplifica la respuesta inflamatoria.44,45 Varios estudios han atribuido a IL-8 propiedades angiogénicas, por lo que podría estar también involucrada en promover el crecimiento celular.46-48 El gen que codifica para IL-8 presenta varios polimorfismos y uno de estos ha sido asociado con un mayor riesgo de desarrollar cáncer gástrico, gastritis atrófica y úlcera gástrica.49-52 Experimentos en cáncer gástrico han determinado niveles de expresión hasta 10 veces mayores en comparación con tejido gástrico normal.22 Lo anterior podría tener repercusiones muy importantes en el contexto de la inflamación y la progresión tumoral, debido a sus propiedades proinflamatorias y proangiogénicas.2 Mediante análisis de inmunohistoquímica semicuantitativos, un estudio determinó una diferencia significativa en la expresión de IL-8, entre cáncer gástrico de tipo difuso y cáncer gástrico de tipo intestinal.46 IL-8 es secretada por las células epiteliales al inicio de la infección por H. pylori, por lo que un aumento en la expresión de IL-8 amplificaría la respuesta inflamatoria contra dicha bacteria, elevando el riesgo de desarrollar cáncer gástrico.
Interleuquina-10
Interleuquina-10 (IL-10) es una citoquina inmunoreguladora que modula la expresión de varias citoquinas proinflamatorias, entre ellas IL-1ß y TNF-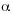 .53 Algunos polimorfismos localizados en la región 5 del gen IL-10 han sido asociados con cambios en los niveles de expresión de esta proteína.54,55 Varios estudios han vinculado algunos de estos polimorfismos con un mayor riesgo de desarrollar cáncer gástrico y lesiones gástricas precancerosas.40,56,57 De acuerdo con la función de IL-10, una menor expresión de esta proteína podría resultar un escaso control en la producción de citoquinas proinflamatorias, lo cual se traduciría en una respuesta inflamatoria excesiva y, consecuentemente, esto podría resultar en un mayor riesgo de desarrollar cáncer gástrico.
.53 Algunos polimorfismos localizados en la región 5 del gen IL-10 han sido asociados con cambios en los niveles de expresión de esta proteína.54,55 Varios estudios han vinculado algunos de estos polimorfismos con un mayor riesgo de desarrollar cáncer gástrico y lesiones gástricas precancerosas.40,56,57 De acuerdo con la función de IL-10, una menor expresión de esta proteína podría resultar un escaso control en la producción de citoquinas proinflamatorias, lo cual se traduciría en una respuesta inflamatoria excesiva y, consecuentemente, esto podría resultar en un mayor riesgo de desarrollar cáncer gástrico.
Otras citoquinas
Otras citoquinas también han sido relacionadas con aumento en el riesgo de desarrollar lesiones gástricas precancerosas y malignas, por ejemplo: IL-2, IL-4, IL-6, IL12, interferón-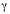 (IFN-
(IFN- ) y su receptor (INFGR2), etc. 22,38,58-61 Estas citoquinas son importantes mediadores de la respuesta inmune ante infecciones y actúan en interacción con otras de las citoquinas, por ejemplo IL-1ß o TNF-
) y su receptor (INFGR2), etc. 22,38,58-61 Estas citoquinas son importantes mediadores de la respuesta inmune ante infecciones y actúan en interacción con otras de las citoquinas, por ejemplo IL-1ß o TNF- , para inducir la respuesta inflamatoria.
, para inducir la respuesta inflamatoria.
Conclusiones y perspectivas
Aunque varios estudios señalan la participación de algunas citoquinas en el desarrollo del cáncer gástrico, existe controversia debido a los diferentes resultados obtenidos en las investigaciones.39,40,62-65 Es posible que en algunos grupos étnicos, la participación de las citoquinas en el proceso de esta enfermedad tengan más peso que en otros.65,66 Una razón que podría explicar esto es la diferencia en la prevalencia de cepas de H. pylori más o menos agresivas entre grupos étnicos.13 Así, en poblaciones con alta prevalencia de cepas más agresivas, el efecto de las citoquinas en el proceso carcinogénico sería "enmascarado" por el efecto de dichas cepas, mientras que en poblaciones con baja prevalencia de cepas virulentas, el efecto de las citoquinas sería más evidente y fácil de determinar. Por lo tanto, el antecedente étnico, el tipo de cepa de H. pylori y su prevalencia deben ser considerados al desarrollar futuros estudios.
Pocas investigaciones se han efectuado en Latinoamérica para estudiar la asociación entre citoquinas y cáncer gástrico.52,60,67-69 Recientemente, un estudio llevado a cabo por este grupo en una población de alto riesgo de Costa Rica, reportó, por primera vez, asociación significativa del polimorfismo IL-1B+3954 con el riesgo de desarrollar esta enfermedad, lo cual fue confirmado después en otras poblaciones.70,71 Debido a la compleja mezcla étnica propia de las poblaciones latinoaméricanas, los estudios en países de alto riesgo de cáncer gástrico en esta región geográfica podrían arrojar nueva luz en cuanto al papel de las citoquinas en el desarrollo del cáncer gástrico.
También son pocas las investigaciones que han estudiado la expresión, cualitativa o cuantitativa, de citoquinas en tejido gástrico.46,72,73 Con excepción de un estudio para IL-8, se desconocen otras investigaciones sobre la expresión de citoquinas y el subtipo histológico de tumor, su localización anatómica o su estadio, entre otras variables. Es necesario realizar estudios sobre la expresión de dichas proteínas en la caracinogénesis gástrica.
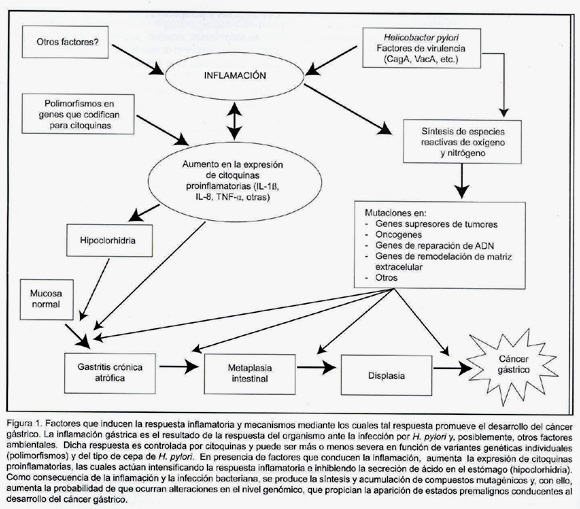
Aunque muchas investigaciones señalan la importancia de la inflamación en el desarrollo del cáncer gástrico, no están claros los mecanismos moleculares y celulares que conducen el proceso. En la Figura 1 se presenta un esquema de cómo la respuesta inflamatoria podría promover el desarrollo del cáncer gástrico.
Referencias
1. De Visser KE, Eichten A, Coussens LM. Paradoxical roles of the immune system during cancer development. Nat Rev Cancer 2006; 6:24-37. [ Links ]
2. Balkwill F, Mantovani A. Inflammation and cancer: back to Virchow?. Lancet 2001;357:539-545. [ Links ]
3. Kuper H, Adami HO, Trichopoulos D. Infections as a major preventable cause of human cancer. J Intern Med 2000. 248;171-183. [ Links ]
4. Kusters JG, van Vliet AH, Kuipers EJ. Pathogenesis of Helicobacter pylori infection. Clin Microbiol Rev. 2006; 19:449-490. [ Links ]
5. Parkin DM, Bray FI, Devesa SS. Cancer burden in the year 2000. The global picture. Eur J Cancer 2001; 37Suppl 8:S4-66. [ Links ]
6. Uemura N, Okamoto S, Yamamoto S, Matsumura N, Yamaguchi S, Yamakido M. et al. Helicobacter pylori infection and the development of gastric cancer. N Engl J Med 2001; 345:784-789. [ Links ]
7. Sierra R, Parkin DM, Leiva GM. Cancer in Costa Rica. Cancer Res 1989; 49:717-724. [ Links ]
8. Catalano V, Labianca R, Beretta GD, Gatta G, de Braud F, Van Cutsem E. Gastric cancer. Crit Rev Oncol Hematol 2005; 54:209-241. [ Links ]
9. Vauhkonen M, Vauhkonen H, Sipponen P. Pathology and molecular biology of gastric cancer. Best Pract Res Clin Gastroenterol 2006; 20:651-674. [ Links ]
10. Correa P. Human gastric carcinogenesis: a multistep and multifactorial process--First American Cancer Society Award Lecture on Cancer Epidemiology and Prevention. Cancer Res 1992; 52:6735-6740. [ Links ]
11. McColl KE. Cancer of the gastric cardia. Best Pract Res Clin Gastroenterol 2006; 20:687-696. [ Links ]
12. Stemmermann GN, Fenoglio-Preiser C. Gastric carcinoma distal to the cardia: a review of the epidemiological pathology of the precursors to a preventable cancer. Pathology 2002; 34:494-503. [ Links ]
13. Suzuki H, Hibi T, and Marshall BJ. Helicobacter pylori: present status and future prospects in Japan. J Gastroenterol 2007; 42:1-15. [ Links ]
14. Prinz C, Schwendy S, and P. Voland P. H. pylori and gastric cancer: shifting the global burden. World J Gastroenterol 2006; 12:5458-5464. [ Links ]
15. Smith MG, Hold GL, Tahara E, El-Omar E. Cellular and molecular aspects of gastric cancer. World J Gastroenterol 2006; 12:2979-2990. [ Links ]
16. Wang HT, Li ZH, Yuan JP, Zhao W, Shi XD, Tong SQ, et al. Effect of Helicobacter pylori VacA on gene expression of gastric cancer cells. World J Gastroenterol 2005; 11:109-113. [ Links ]
17. Hatakeyama M. Oncogenic mechanisms of the Helicobacter pylori CagA protein. Nat Rev Cancer 2004; 4:688-694. [ Links ]
18. Naumann M. Pathogenicity island-dependent effects of Helicobacter pylori on intracellular signal transduction in epithelial cells. Int J Med Microbiol 2005; 295:335-341. [ Links ]
19. Zambon CF, Navaglia F, Basso D, Rugge M, Plebani M. Helicobacter pylori babA2, cagA, and s1 vacA genes work synergistically in causing intestinal metaplasia. J Clin Pathol 2003; 56:287-291. [ Links ]
20. Figueiredo C, Van Doorn LJ, Nogueira C, Soares JM, Pinho C, Figueira P, et al. Helicobacter pylori genotypes are associated with clinical outcome in Portuguese patients and show a high prevalence of infections with multiple strains. Scand J Gastroenterol 2001; 36:128135. [ Links ]
21. El-Omar EM, Chow WH, Rabkin CS. Gastric cancer and H. pylori: Host genetics open the way. Gastroenterology 2001; 121:1002-1004. [ Links ]
22. Yamaoka Y, Kodama T, Kita M, Imanishi J, Kashima K, Graham DY. Relation between cytokines and Helicobacter pylori in gastric cancer. Helicobacter 2001; 6:116-124. [ Links ]
23. Wilson KT, Crabtree JE. Immunology of Helicobacter pylori: Insights into the failure of the immune response and perspectives on vaccine studies. Gastroenterolory 2007; 133:288-308. [ Links ]
24. Dinarello CA. Biologic basis for interleukin-1 in disease. Blood 1996; 87:2095-2147. [ Links ]
25. Nicklin MJ, Weith A, Duff GW. A physical map of the region encompassing the human interleukin-1 alpha, interleukin-1 beta, and interleukin-1 receptor antagonist genes. Genomics 1994; 19:382-384. [ Links ]
26. El-Omar EM, Carrington M, Chow WH, McColl KEL, Bream JH, Young HA, et al. Interleukin-1 polymorphisms associated with increased risk of gastric cancer. Nature 2000; 404:398-402. Corrección en: Nature 2001; 412:99. [ Links ]
27. Furuta T, El-Omar E, Xiao F, Shirai N, Takashima M, Sugimurra H, et al. Interleukin 1beta polymorphisms increase risk of hypochlorhydria and atrophic gastritis and reduce risk of duodenal ulcer recurrence in Japan. Gastroenterology 2002; 123:92-105. [ Links ]
28. Machado JC, Pharoah P, Sousa S, Carvalho R, Oliveira C, Figueiredo C, et al. Interleukin 1B and interleukin 1RN polymorphisms are associated with increased risk of gastric carcinoma. Gastroenterology 2001; 121:823-829. [ Links ]
29. Figueiredo C, Machado JC, Pharoah P, Seruca R, Sousa S, Carvalho R, et al. Helicobacter pylori and interleukin 1 genotyping: an opportunity to identify high-risk individuals for gastric carcinoma. J Natl Cancer Inst 2002; 94:1680-1687. [ Links ]
30. Rad R, Prinz C, Neu B, Neuhofer M, Zeitner M, Voland P, et al. Synergistic effect of Helicobacter pylori virulence factors and interleukin-1 polymorphisms for the development of severe histological changes in the gastric mucosa. J Infect Dis 2003; 188:272-281. [ Links ]
31. Beales IL, Calam J. Interleukin 1 beta and tumour necrosis factor alpha inhibit acid secretion in cultured rabbit parietal cells by multiple pathways. Gut 1998; 42:227-234. [ Links ]
32. Takashima M, Furuta T, Hanai H, Sugimura H, Kaneko E, et al. Effects of Helicobacter pylori infection on gastric acid secretion and serum gastrin levels in Mongolian gerbils. Gut 2001; 48: 765-773. [ Links ]
33. Idriss HT, Naismith JH, TNF alpha and the TNF receptor superfamily: structure-function relationship(s). Microsc Res Tech 2000; 50:184-195. [ Links ]
34. Beutler B. TNF, immunity and inflammatory disease: lessons of the past decade. J Investig Med 1995; 43:227-235. [ Links ]
35. Strieter RM, Kunkel SL, Bone RC. Role of tumor necrosis factoralpha in disease states and inflammation. Crit Care Med 1993; 21: S447-463. [ Links ]
36. Higuchi T, Seki N, Kamisono S, Yamada A, Kimura A, Kato H, et al. Polymorphism of the 5-flanking region of the human tumor necrosis factor (TNF)-alpha gene in Japanese. Tissue Antigens 1998; 51:605-612. [ Links ]
37. Skoo, T, van`t Hooft FM, Kallin B, Jovinge S, Boquist S, Nilsson J, et al. A common functional polymorphism (C-->A substitution at position -863) in the promoter region of the tumour necrosis factoralpha (TNF-alpha) gene associated with reduced circulating levels of TNF-alpha. Hum Mol Genet 1999; 8:1443-1449. [ Links ]
38. Hou L, El-Omar E, Chen J, Grillo P, Rabkin CS, Baccarelli A, et al. Polymorphisms in Th1-type cell-mediated response genes and risk of gastric cancer. Carcinogenesis 2007; 28:118-123. [ Links ]
39. Machado JC, Figueiredo C, Canedo P, Pharoah P, Carvalho R, Nabais S, et al. A proinflammatory genetic profile increases the risk for chronic atrophic gastritis and gastric carcinoma. Gastroenterology 2003; 125:364-371. [ Links ]
40. El-Omar EM, Rabkin CS, Gammon MD, Vaughan TL, Risch HA, Schoenberg JB, et al. Increased risk of noncardia gastric cancer associated with proinflammatory cytokine gene polymorphisms. Gastroenterology 2003; 124:1193-1201. [ Links ]
41. Zambon CF, Basso D, Navaglia F, Belluco C, Falda A, Fogar P, et al. Pro-and anti-inflammatory cytokines gene polymorphisms and Helicobacter pylori infection: interactions influence outcome. Cytokine 2005; 29:141-52. [ Links ]
42. Russo F, Jirillo E, Clemente C, Messa C, Chiloiro M, Riezzo G, et al. Circulating cytokines and gastrin levels in asymptomatic subjects infected by Helicobacter pylori (H. pylori). Immunopharmacol Immunotoxicol, 2001; 23:13-24. [ Links ]
43. Genta RM. The immunobiology of Helicobacter pylori gastritis. Semin Gastrointest Dis 1997; 8:2-11. [ Links ]
44. Roebuck KA. Regulation of interleukin-8 gene expression. J Interferon Cytokine Res 1999; 19:429-438. [ Links ]
45. Matsushima K, Baldwin ET, Mukaida N. Interleukin-8 and MCAF: novel leukocyte recruitment and activating cytokines. Chem Immunol 1992; 51:236-265. [ Links ]
46. Eck M, Schmaußer B, Scheller K, Brändlein S, Müller-Hermelink HK. Pleiotropic effects of CXC chemokines in gastric carcinoma: differences in CXCL8 and CXCL1 expression between diffuse and intestinal types of gastric carcinoma. Clin Exp Immunol 2003; 134:508-515. [ Links ]
47. Koch AE, Polverini PJ, Kundel SL, Harlow LA, DiPietro LA, Elner VM, et al. Interleukin-8 as a macrophage-derived mediator of angiogenesis. Science 1992; 258:1798-1801. [ Links ]
48. Strieter RM, Kundel SL, Elner VM, Matonyi CL, Koch AE, Polverini PJ, et al. Interleukin-8. Acorneal factor that induces neovascularization. Am J Pathol 1992; 141:1279-1284. [ Links ]
49. Taguchi A, Ohmiya N, Shirai K, Mabuchi N, Itoh A, Hirooka Y, et al. Interleukin-8 promoter polymorphism increases the risk of atrophic gastritis and gastric cancer in Japan. Cancer Epidemiol Biomarkers Prev 2005; 14:2487-2493. [ Links ]
50. Ohyauchi M, Imatani A, Yonechi M, Asano N, Miura A, Iijima K, et al. The polymorphism interleukin 8 -251 A/T influences the susceptibility of Helicobacter pylori related gastric diseases in the Japanese population. Gut 2005; 54:330-335. [ Links ]
51. Lee WP, Tai DI, Lan KH, Li AFY, Hsu HC, Lin EJ, et al. The -251T allele of the interleukin-8 promoter is associated with increased risk of gastric carcinoma featuring diffuse-type histopathology in Chinese population. Clin Cancer Res 2005; 11:6431-6441. [ Links ]
52. Garza-González E, Bosques-Padilla FJ, Mendoza-Ibarra SI, Flores- Gutierrez JP, Maldonado-Garza HJ, Pérez-Pérez G. Assesment of the toll-like receptor 4 Asp299Gly, Tyr399Ile and interleukin-8-251 polymorphisms in the risk for development of distal gastric cancer. BMC cancer 2007; 7:70-75. [ Links ]
53. Moore KW, de Waal Malefyt R, Coffman RL, OGarra. Interleukin-10 and the interleukin-10 receptor. Annu Rev Immunol 2001; 19:683-765. [ Links ]
54. Crawley E, Kay R, Sillibourne J, Patel P, Hutchinson I, Woo, et al. Polymorphic haplotypes of the interleukin-10 5 flanking region determine variable interleukin-10 transcription and are associated with particular phenotypes of juvenile rheumatoid arthritis. Arthritis Rheum 1999; 42:1101-1108. [ Links ]
55. Eskdale J, Kube D, Tesch H, Gallagher G, et al. Mapping of the human IL10 gene and further characterization of the 5 flanking sequence. Immunogenetics 1997; 46:120-128. [ Links ]
56. Lu W, Pan K, Zhang L, Lin D, Miao X, You W. Genetic polymorphisms of interleukin (IL)-1B, IL-1RN, IL-8, IL-10 and tumor necrosis factor {alpha} and risk of gastric cancer in a Chinese population. Carcinogenesis 2005; 26:631-636. [ Links ]
57. Wu MS, Wu CY, Chen CJ, Lin MT, Shun CT, Lin JT. Interleukin-10 genotypes associate with the risk of gastric carcinoma in Taiwanese Chinese. Int J Cancer 2003; 104:617-623. [ Links ]
58. Navaglia F, Basso D, Zambon CF, Pozano E, Caenazzo L, Gallo N, et al. Interleukin 12 gene polymorphisms enhance gastric cancer risk in H. pylori infected individuals. J Med Genet 2005; 42:503-510. [ Links ]
59. Seno H, Sato K, Tsuji S, Shiratsuchi T, Harada Y, Hamajima N, et al. Novel interleukin-4 and interleukin-1 receptor antagonist gene variations associated with non-cardia gastric cancer in Japan: comprehensive analysis of 207 polymorphisms of 11 cytokine genes. J Gastroenterol Hepatol 2007; 22:729-737. [ Links ]
60. Serrano C, Diaz MI, Valdivia A, Godoy A, Peña A, Rollan A, et al. Relationship between Helicobacter pylori virulence factors and regulatory cytokines as predictors of clinical outcome. Microbes Infect 2007; 9:428-434. [ Links ]
61. Togawa S, Joh T, Itoh M, Katsuda N, Ito H, Matsuo K, et al. Interleukin2 gene polymorphisms associated with increased risk of gastric atrophy from Helicobacter pylori infection. Helicobacter 2005; 10:172-178. [ Links ]
62. Kamangar F, Cheng C, Abnet CC, Rabkin CS. Interleukin-1B polymorphisms and gastric cancer risk--a meta-analysis. Cancer Epidemiol Biomarkers Prev 2006; 15:1920-1928. [ Links ]
63. Kato S, Onda M, Yamada S, Matsuda N, Tokunaga A, Matsukura. Association of the interleukin-1 beta genetic polymorphism and gastric cancer risk in Japanese. J Gastroenterol 2001; 36:696-699. [ Links ]
64. Wang P, Xia HHX, Zhang JY, Dai LP, Xu XQ, Wang KJ. Association of interleukin-1 gene polymorphisms with gastric cancer: a metaanalysis. Int J Cancer 2007; 120:552-562. [ Links ]
65. Camargo MC, Mera R, Correa P, Peek RM, Fontham ETH, Goodman KJ, et al. Interleukin-1beta and interleukin-1 receptor antagonist gene polymorphisms and gastric cancer: a meta-analysis. Cancer Epidemiol Biomarkers Prev 2006; 15:1674-1687. [ Links ]
66. Zeng ZR, Hu PJ, Hu S, Pang RP, Chen MH, Ng M, et al. Association of interleukin 1B gene polymorphism and gastric cancers in high and low prevalence regions in China. Gut 2003; 52:1684-1689. [ Links ]
67. Sicinschi LA, Lopez-Carrillo L, Camargo MC, Correa P, Sierra RA, Henry RR, et al. Gastric cancer risk in a Mexican population: role of Helicobacter pylori CagA positive infection and polymorphisms in interleukin-1 and -10 genes. Int J Cancer 2006; 118:649-657. [ Links ]
68. Lobo Gatti L, Rodríguez Burbano R, Pimentel de Assumpcao P, Cardoso Smith M, Marques Payao SL. Interleukin-1beta polymorphisms, Helicobacter pylori infection in individuals from Northern Brazil with gastric adenocarcinoma. Clin Exp Med 2004; 4:93-98. [ Links ]
69. Kato I, Canzian F, Franceschi S, Plummer M, van Doorn LY, Lu Y, et al. Genetic polymorphisms in anti-inflammatory cytokine signaling and the prevalence of gastric precancerous lesions in Venezuela. Cancer Causes Control 2006; 17:1183-1191. [ Links ]
70. Alpizar-Alpizar W, Pérez-Pérez GI, Une C, Cuenca P, Sierra R. Association of interleukin-1B and interleukin-1RN polymorphisms with gastric cancer in a high-risk population of Costa Rica. Clin Exp Med 2005; 5:169-176. [ Links ]
71. Zhang WH, Wang XL, Zhou J, An LZ, Xie XD. Association of interleukin-1B (IL-1B) gene polymorphisms with risk of gastric cancer in Chinese population. Cytokine 2005; 30:378-381. [ Links ]
72. Hwang IR, Kodama T, Kikuchi S, Sakai K, Peterson LE, Graham DY, et al. Effect of interleukin 1 polymorphisms on gastric mucosal interleukin 1beta production in Helicobacter pylori infection. Gastroenterology 2002; 123:1793-1803. [ Links ]
73. Rad R, Dosumbekova A, Neu B, Lang R, Bauer S, Saur D, et al. Cytokine gene polymorphisms influence mucosal cytokine expression, gastric inflammation, and host specific colonisation during Helicobacter pylori infection. Gut 2004; 53:1082-1089. [ Links ]
1 Instituto Gade, Departamento de Patología, Hospital Universitario Haukeland, Universidad de Bergen, Bergen, Noruega 2 Programa de Investigación en Cáncer, Instituto de Investigaciones en Salud (INISA), Universidad de Costa Rica, San José, Costa Rica Abreviaturas: IFN-., interferón-gama; IL-1ß, interleuquina-1 beta; IL-2, interleuquina-2; IL-4, interleuquina-4; IL-6, interleuquina-6; IL-8, interleuquina-8; IL-10, interleuquina-10; IL-12, interleuquina-12; IL-1RA, receptor antagonista de interleuquina-1; INFGR2, receptor de interferón-gama; TNF-a, factor de necrosis tumoral alfa. Correspondencia a: Warner Alpízar Alpízar. Instituto Gade, Departamento de Patología. Hospital Universitario Haukeland Bergen, Noruega. awarnercr@yahoo.com / warner.alpizar@student.uib.no














