Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Acta Médica Costarricense
On-line version ISSN 0001-6002Print version ISSN 0001-6012
Acta méd. costarric vol.50 n.4 San José Dec. 2008
Original
Evaluación de una prueba rápida para diagnóstico de dengue en el nivel local
(Evaluation of a rapid dengue test at the local level)
Elizabeth Sáenz-Bolaños1,
Jenny Lara-Araya1,
Jorge Sequeira-Soto2,
Anabelle Alfaro-Obando3
1 Centro Nacional de Referencia de Virología (CNRV) y
2 Centro Nacional de Referencia de Leptospirosis (CNRL), Inciensa.
3 Caja Costarricense de Seguro Social
Correspondencia: Elizabeth Sáenz Bolaños. Centro Nacional de Referencia de Virología. Instituto Costarricense de Investigación y Enseñanza en Nutrición y Salud, INCIENSA. Apartado 4-2250 Tres Ríos, Costa Rica. E-mail esaenz@inciensa.sa.cr
Resumen
Justificación y objetivo: Analizar concordancia entre la prueba rápida Dengue Duo IgM & IgG® de la casa comercial PanBio®, aplicada en el nivel local de diferentes áreas del país y en el Centro Nacional de Referencia de Virología (CNRV), con resultados obtenidos por MACELISA del CNRV.
Métodos: Resultados de 828 determinaciones de IgM dengue por Dengue Duo IgM & IgG® del nivel local y del CNRV se compararon por el índice kappa con los resultados del MAC-ELISA del CNRV. Para verificar el cumplimiento en procedimientos de la casa comercial, se realizó una visita de inspección a los laboratorios y se envió muestras incógnitas para evaluar el desempeño.
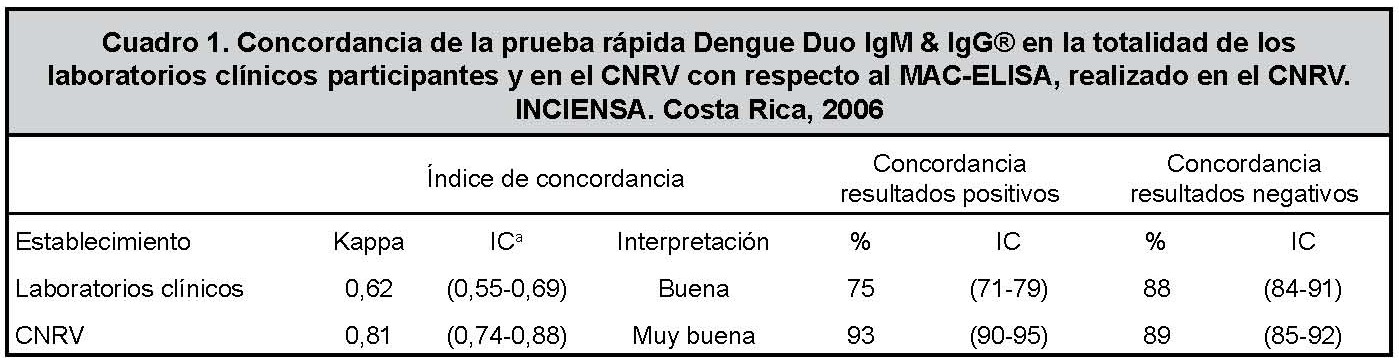
Resultados: El índice kappa de la prueba rápida en el nivel local contra el MAC-ELISA fue 0,62 (IC 95% 0,55-0,69) y la concordancia de los positivos del 75% (IC 95% 71-79). El índice kappa de la prueba rápida en el CNRV fue 0,81 (IC 95% 0,88-1,74) y la concordancia de los positivos del 93% (IC 95% 90-95). El 100% de los laboratorios mostraron condiciones adecuadas para aplicar esta prueba; su personal fue capacitado, pero la atención de otros análisis dificultó la lectura en el tiempo establecido. La concordancia de las incógnitas fue del 100%.
Conclusión: Se evidenció una diferencia significativa en el índice kappa y la concordancia de los positivos, al aplicar la prueba rápida en los laboratorios y en el CNRV, hallazgos que documentan que la descentralización de esta metodología requerirá un acompañamiento que identifique factores causales de discordancia para subsanarlos y promover la generación de resultados consistentes que orienten la toma de decisiones acertadas.
Descriptores: dengue, pruebas rápidas, diagnóstico de laboratorio, vigilancia epidemiológica, índice Kappa
Abstract
Background and aim: To analyze concordance of results obtained using the Dengue Duo IgM &IgG® rapid test (Pan Bio®) applied at the local level in different areas across the country and the MAC ELISA used at National Reference Center for Virology (CNRV)
Methodology: The results of 828 dengue tests carried out with the Duo IgM& IgG® (Pan Bio®) at local level and at the CNRV were compared by the kappa index with those obtained with a MAC ELISA test at the CNRV. An inspection visit to participating laboratories was made and unknown samples were sent to evaluate the performance of the participants and to check the fulfillment of the procedures used with the recommendations of the manufacturer.
Results: The kappa index of the results of the rapid test used at local level in comparison with the MAC ELISA was 0.62 (CI 95% 90-95); the concordance of the positive samples was 75% (CI 95% 71-79). The kappa index of the rapid test used at the CNRV was 0.81 (CI 95% 0.88- 1.74) and the concordance of the positive samples was 93% (CI 95% 90-95). All laboratories showed ideal facilities to carry out the tests and the staff got the training required; however, the attention to other analyses affected the reading within the time recommended. The concordance of the unknown samples was 100%.
Conclusion: A significant difference was demonstrated in the kappa index and the concordance of positive samples between the rapid tests carried out at the participant laboratories and at the CNRV. These results imply that decentralization of this methodology would require continuous support to identify correctable factors of disagreement and to promote the generation of consistent results to orient the decision-making process.
Key words: dengue, rapid test, lab diagnostic, concordance of results, epidemiological surveillance, kappa index.
Recibido: 18 de abril de 2008 Aceptado: 1 de Julio de 2008
El dengue es una enfermedad endémica en Costa Rica. Desde octubre de 1993 se reportaron los primeros casos de dengue, serotipo dengue 1 en la costa del Pacífico, y en los años siguientes se han presentado brotes y epidemias de distinta intensidad en diferentes regiones del país, causados por los serotipos dengue 1, 2 y 3.1
Es claro que el abordaje integral y oportuno del dengue se inicia ante la sospecha clínica del caso. De esta manera es de vital importancia que el personal de salud proceda inmediatamente con la notificación obligatoria su investigación y el manejo médico, como lo establece la normativa nacional, sin esperar el resultado serológico del laboratorio clínico del nivel local ni del Centro Nacional de Referencia. Esto significa que el aporte del laboratorio en la confirmación diagnóstica es en apoyo a la vigilancia epidemiológica de esta patología, y que, junto al análisis integral de la información clínico-epidemiológico, permite documentar la actividad del dengue con el fin de orientar las intervenciones que se realizan para su prevención y control.2,3
En la infección primaria por cualquier virus del complejo dengue, se produce una respuesta de anticuerpos de la clase IgM. Estudios sobre la cinética de la respuesta de anticuerpos demuestran un incremento de inmunoglobulinas IgM en los pacientes a los 2 días de haber disminuido la fiebre, con un pico en la respuesta aproximadamente a las dos semanas y permaneciendo en sangre hasta por 3 meses. Por este comportamiento y para su diagnóstico se requiere una sola muestra de suero obtenida al menos 6 días después de la fecha de inicio de los síntomas.
En las infecciones no primarias la respuesta de anticuerpos IgM es variable y en algunas ocasiones está ausente o es muy baja, por lo que un resultado negativo a la presencia de IgM contra dengue no excluye la posibilidad de exposición anterior a este virus, pero en estos casos existe un marcado incremento de los anticuerpos IgG que apararecen aproximadamente 2 días después de notarse los síntomas4 y aumentan con rapidez alcanzando niveles muy altos a las 2 semanas, por lo que resultan fácilmente detectables.5 Así, la bibliografía documenta que al quinto día de la enfermedad el 80% de los casos, tanto primarios como secundarios, tienen anticuerpos IgM detectables, mientras que entre el sexto y décimo día de la enfermedad, los anticuerpos IgM se detectan entre el 90% y el 99% de los pacientes.3,6 Como en los primeros 5 días de evolución de la enfermedad los anticuerpos IgM no han alcanzado niveles séricos detectables, el diagnóstico serológico no es útil para el manejo clínico de un paciente con dengue, por lo que el médico, ante un caso que evolucione como dengue hemorrágico, debe iniciar tratamiento sin esperar el resultado de la prueba rápida que se realice en el nivel local.
El método de elección para la vigilancia seroepidemiológica del dengue es el inmunoensayo enzimático sobre fase sólida de captura para IgM (MACELISA) antidengue. Este método es específico, sensible, económico, sencillo y de relativa rapidez, que determina infecciones actuales o recientes, aún cuando no permite identificar los serotipos circulantes. Sin embargo, como en el comercio existen disponibles una serie de pruebas rápidas para el diagnóstico serológico del dengue, estas resultan de fácil manejo y no requieren una infraestructura y equipo de laboratorio sofisticados,7-9 en Costa Rica su uso se ha difundido tanto en la práctica privada como en la pública. Por esta razón, como parte del sistema nacional de vigilancia de esta patología y en el contexto de la descentralización del diagnóstico serológico del dengue que contempla la Estrategia Nacional de Gestión Integrada para la Prevención y Control del Dengue en Centroamérica,10 este plan piloto aplicó la prueba rápida para detección de anticuerpos IgM e IgG anti virus Dengue de PanBio®, llamada Dengue Duo IgM & IgG® en el nivel local de diferentes áreas de nuestro país y en el Centro Nacional de Referencia de Virología (CNRV) del Instituto Costarricense de Investigación y Enseñanza en Nutrición y Salud (INCIENSA) de Costa Rica. En este sentido, el análisis comprendió el cálculo del grado de concordancia de los resultados obtenidos en cada uno de los laboratorios participantes, con respecto a los resultados obtenidos por la técnica de MAC ELISA realizada en el CNRV.
Materiales y métodos
Se analizaron los resultados de laboratorio obtenidos para la determinación de IgM contra dengue en 828 muestras de suero de pacientes sospechosos de padecer esta enfermedad y que consultaron en 13 establecimientos de salud del país, entre junio de 2005 y junio de 2006. En todo momento las muestras de suero se conservaron a 4ºC. Previa capacitación de un profesional en microbiología y siguiendo las indicaciones de la casa comercial, el laboratorio clínico del nivel local sometió cada uno de los sueros al análisis con la prueba rápida de inmunocromatografía PanBio® Dengue Duo IgM & IgG®, y el resultado obtenido se anotó en la boleta de solicitud de análisis de laboratorio que acompaña a cada muestra.
Tanto el suero analizado como la boleta con la información correspondiente al paciente y el resultado del laboratorio obtenido en el nivel local para la determinación de IgM e IgG para dengue por la prueba rápida, se refirieron, cumpliendo con la cadena de frío y las normas de bioseguridad, al INCIENSA. En el CNRV, a cada uno de los sueros se les practicó la prueba serológica ELISA de captura de anticuerpos IgM (MAC-ELISA), siguiendo los lineamientos establecidos como parte de la vigilancia de esta enfermedad, así como la misma prueba rápida de PanBio® aplicada en el nivel local.
La información brindada por el CNRV del INCIENSA al Sistema Nacional de Vigilancia del Dengue solo correspondió a las pruebas de MAC-ELISA, que son las estandarizadas y estipuladas para la vigilancia de esta enfermedad de notificación obligatoria, según lo establecen las Normas Técnicas de Dengue.2
Simultáneamente a este proceso de recepción, conservación, envío y análisis de muestras, el personal del CNRV realizó un monitoreo de la calidad diagnóstica de cada uno de los laboratorios participantes, tomando en cuenta tres aspectos: primero, una visita de inspección a los laboratorios clínicos, contemplando variables sobre el recurso humano, la planta física y el seguimiento de las instrucciones del procedimiento de la prueba rápida, información que se capturó mediante entrevista y observación en un instrumento de recolección de datos diseñado para este fin. En segundo lugar se realizó una prueba de evaluación externa del desempeño, para lo cual el CNRV envió muestras incógnitas a los laboratorios clínicos participantes. Por último, se analizó la concordancia entre los resultados obtenidos para IgM anti dengue con la prueba rápida realizada en el nivel local y en el CNRV con los resultados obtenidos por la prueba de referencia MAC-ELISA realizada en el CNRV del INCIENSA. Además, se efectúo una comparación entre los resultados obtenidos para la IgG antidengue por la prueba rápida realizada en el nivel local y en el CNRV, sin referir a una prueba estándar.
Para este plan piloto se utilizó como prueba de referencia la técnica de ELISA, de captura de anticuerpos IgM (MACELISA) descrita en el manual de técnicas de laboratorio para el diagnóstico y la caracterización del virus dengue del Instituto de Medicina Tropical Pedro Kourí,11 que utiliza, con algunas modificaciones, el CNRV. Para las distintas variantes de esta técnica, se reporta, en general, un 10% de falsos negativos y un 1,7% de falsos positivos.12 Una lectura de una densidad óptica igual o mayor a 0,200 se considera positiva para la determinación de anticuerpos IgM específicos contra el virus dengue. Ante una lectura en la densidad óptica o absorbancia mayor a 0,150, pero menor a 0,200 en presencia de síntomas clínicos compatibles con dengue, el CNRV solicitó al nivel local tomar una segunda muestra con el fin de confirmar el diagnóstico, esto porque un resultado negativo por anticuerpos IgM contra dengue en estas condiciones, no excluye la posibilidad de exposición a este virus. Un resultado inferior a 0,150 fue considerado como negativo.
Este protocolo utilizó como prueba rápida a comparar la Dengue Duo IgM & IgG® de la casa comercial PanBio®, que tiene una sensibilidad y especificidad mayor del 90%. En esta prueba inmunocromatográfica, cuando en la muestra del paciente están presentes inmunoglobulinas específicas contra virus dengue de la clase IgM o IgG, estas se unen a los anticuerpos contra IgM o IgG humanas que se encuentran inmovilizados en dos líneas a través de la membrana casete. Los complejos de oro coloidal que contienen antígenos de dengue 1, 2, 3 y 4 son capturados por las IgM o IgG del paciente, evidenciándose esta unión mediante la formación de una línea rosada visible. Este ensayo incluye una línea control que indica que el análisis ha sido desarrollado correctamente.7 El análisis de los datos se realizó en el programa Win Episcope 0,213 a un nivel de confianza del 95%. Para evaluar la proporción de concordancia se utilizó el índice de kappa,14 en el cual un valor igual a 1,0 representa una concordancia perfecta, más allá de la intervención del azar, y un valor de cero indica que no hay concordancia. Para valores mayores a 0,81 la fuerza de la concordancia se interpreta como muy buena; valores entre 0,61 y 0,80 corresponden a una buena concordancia; entre 0,41 y 0,60 a moderada; entre 0,21 y 0,40 a débil y menores de 0,20 como pobre.15
Resultados
El rango de muestras procesadas por los 13 laboratorios participantes en este plan piloto fluctuó entre un mínimo de 8 y un máximo de 131 muestras. En los 828 casos incluidos, el laboratorio clínico procedió conforme lo indica la normativa técnica nacional, pero a la vez se analizó la muestra por la prueba rápida de PanBio®. En el 80,5% (667/828) de las boletas se consignó información sobre días de evolución al momento cuando se tomó la muestra de sangre. De ellas, solo 58 (8,7%, IC 95% 6,7-11,2) correspondieron a menos de cinco días de evolución de la enfermedad, 140 (21%, IC 95% 18,0-24,3) tenían 5 ó 6 días de evolución y 469 (70,3%, IC 95% 66,7-73,7) reportaron 7 ó más días de evolución.
Con respecto a la determinación de los anticuerpos IgM contra dengue, el análisis de la concordancia entre la totalidad de las pruebas rápidas realizadas en los laboratorios clínicos participantes en este plan piloto y la técnica de MAC-ELISA realizada en el CNRV logró un índice de kappa de 0,62 correspondiente a una clasificación de buena. Además, las pruebas rápidas realizadas en el nivel local y el MAC-ELISA realizado en el CNRV concordaron en el 75% de los resultados positivos (338/450) y en el 88% de los negativos (333/378), o sea, que de un total de 383 muestras positivas por la prueba rápida, 338 también resultaron positivas por el MAC-ELISA (88%, IC 95% 85-91), y de un total de 445 muestras negativas por la prueba rápida, 333 también fueron negativas por el MAC-ELISA (75%, IC 95% 70-79).
En el análisis de la concordancia entre la prueba rápida realizada en el CNRV y la técnica de MAC-ELISA del CNRV se obtuvo un índice de concordancia kappa de 0,81 correspondiente a una clasificación de muy buena, por lo que ambas pruebas realizadas en el CNRV coincidieron en el 93% de los resultados positivos (417/450) y en el 89% de los negativos (336/378), lo que indica que de un total de 459 muestras positivas por la prueba rápida, 417 también resultaron positivas por el MAC-ELISA (90%, IC 95% 88- 93), y de un total de 369 muestras negativas por la prueba rápida, 336 también fueron negativas por el MAC-ELISA (91%, IC 95% 88-94) (Cuadro 1).
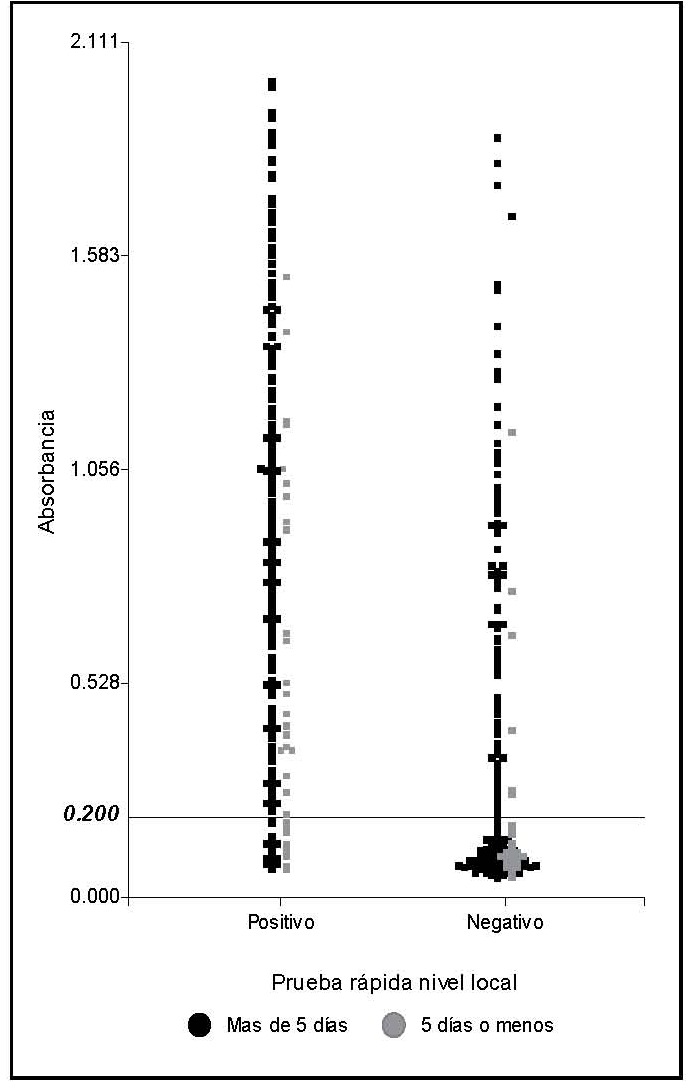
Como se observa en la Figura 1, 112 de 450 muestras (25%, IC 95% 21-29) positivas por MAC-ELISA, cuyos valores de absorbancia oscilaron desde 0,205 hasta 1,870 con una absorbancia promedio de 0,720, resultaron negativas por la prueba rápida realizada en el nivel local. De esas 112 muestras con resultados discordantes, 100 (89%) consignaban el dato sobre los días de evolución, y de ellas, 3 (3%, IC 95% 0,6-8,5) correspondieron a menos de cinco días de evolución de la enfermedad, 17 (17%, IC 95% 10-26) tenían 5 ó 6 días de evolución y 80 (80%, IC 95% 71-87) reportaron 7 ó más días de evolución; 45 de 378 muestras que resultaron negativas por MAC-ELISA (12%, IC 95% 8,9-15,7) obtuvieron resultados positivos por la prueba rápida aplicada en el nivel local. De esas 45 muestras con resultados discordantes, el 75% (IC 95% 58,8-87,3) tenían más de 5 días de evolución.
local , según las absorbancias obtenidas por MAC-ELISA en el CNRV y los días de evolución
de las muestras analizadas. INCIENSA. Costa Rica, 2006.
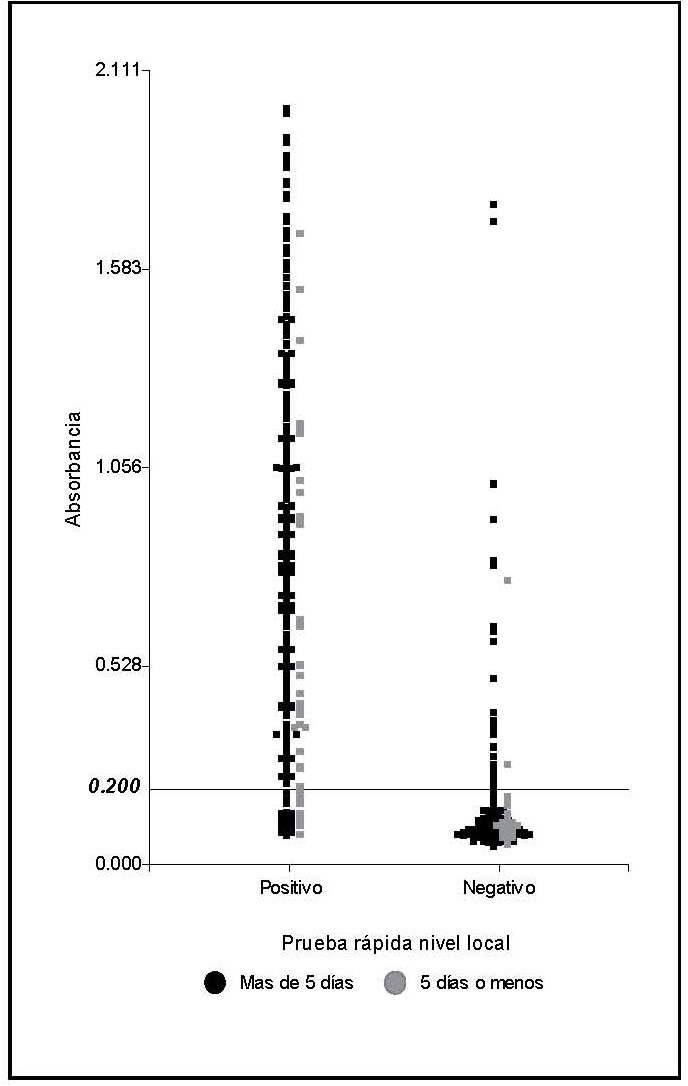
Con respecto a la prueba rápida realizada en el CNRV, la Figura 2 evidencia que de las 33 (7%) muestras negativas por esta técnica, pero con resultados positivos por MACELISA, con valores de absorbancia que fluctuaron entre 0,211 y 1,753 con una absorbancia promedio de 0,554, el 93,1% (IC 95% 77,2-99,2) refirieron tener más de 5 días de evolución al momento de la toma de la muestra. Por otra parte, de las 42 (11%) muestras que el CNRV, obtuvo como positivas por la prueba rápida y que por el MAC-ELISA se reportaron IgM contra dengue negativas, el 79,5% (IC 95% 63,5-90,7) de estos pacientes, que aportaron la información, contaban con más de 5 días de evolución de la enfermedad.
las absorbancias obtenidas por MAC ELISA en el CNRV y los días de evolución de las muestras
analizadas. INCIENSA. Costa Rica, 2006
El análisis de los resultados obtenidos para las 828 determinaciones de los anticuerpos IgM contra dengue por la prueba rápida realizada en el nivel local comparada con la misma prueba rápida realizada en el CNRV, reportó un índice de kappa de 0,72 (IC 95% 0,65-0,78), lo que indica que la prueba rápida realizada tanto en el CNRV y en el nivel local coincidió en el 78% (IC 95%=75-82) de los resultados positivos (362/459) y en el 94% (IC 95% 91-96) de los negativos (348/369), por lo que de un total de 383 muestras positivas por la prueba rápida realizada en el nivel local, 362 también resultaron positivas por la prueba rápida realizada en el CNRV (94%, IC 95% 92-96), y de un total de 445 muestras negativas por la prueba rápida aplica en el nivel local, 348 también fueron negativas por esa misma prueba rápida aplicada en el CNRV (78%, IC 95% 74-82). Con respecto a los resultados discordantes, se debe señalar que de las 97 muestras negativas por esta técnica realizada en el nivel local, pero que resultaron positivas por esa misma prueba aplicada en el CNRV, el 94,3% (IC 95% 87,1-98,1) refirieron tener más de 5 días de evolución al momento de la toma de la muestra y de las 21 muestras que el nivel local obtuvo como positivas por la prueba rápida, pero que dieron negativas para la determinación de anticuerpos IgM contra dengue, por esa misma metodología realizada en el CNRV, el 88,2% (IC 95% 63,6-98,5) de estas muestras, que contaban con la información, correspondieron a más de cinco días de evolución de la enfermedad cuando se les recolectó la muestra.
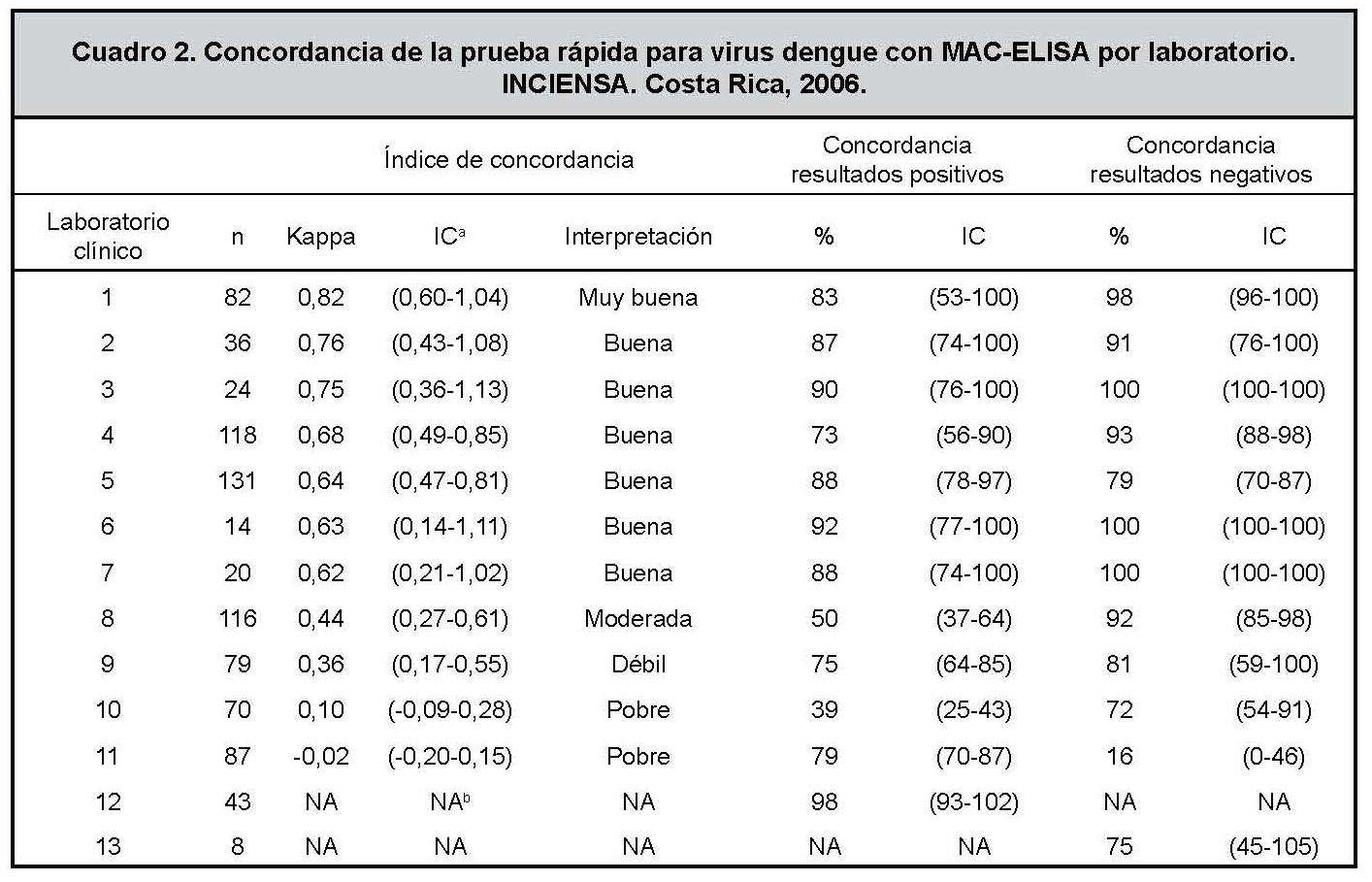
En el Cuadro 2 se observan los resultados obtenidos por laboratorio clínico participante, identificando que la diferencia que existe entre la concordancia de los resultados conseguidos por la prueba rápida realizada en el CNRV, con los obtenidos por la aplicación de esta prueba en el nivel local, está influenciad, por los resultados individuales obtenidos por los laboratorios clínicos 9, 10 y 11, que al momento de aplicar la prueba rápida en el nivel local obtuvieron una concordancia débil o pobre para un índice de kappa menor o igual a 0,40 con respecto a la técnica de MAC-ELISA del CNRV. En el caso de los resultados de las pruebas rápidas realizadas en el laboratorio participante número 12, comparadas con los resultados del MAC-ELISA realizado en el CNRV coincidieron en un 98% (42/43) de los resultados positivos y para el laboratorio 13, en un 75% (6/8) de los negativos, sin embargo, a pesar de que para ambos laboratorios los otros resultados concordaron en un 100% (0/0), los valores de cero consignados no permiten aplicar la metodología de análisis de datos utilizada.
Con respecto a la determinación de los anticuerpos IgG contra dengue, el análisis de la concordancia se realizó entre los resultados obtenidos al procesar las 828 muestras por las pruebas rápidas realizadas, tanto en los laboratorios clínicos participantes en este plan piloto, como en el CNRV, concordancia que corresponde a un índice de kappa de 0,66 (IC 95% 0,59-0,72), lo que se interpretó como bueno. Sin embargo, los resultados de IgG contra dengue obtenidos por esta prueba rápida realizada en el nivel local y el CNRV concordaron en el 64,5% (IC 95% 57-72) de los resultados positivos (111/172), y en el 96% (IC 95% 94-98) de los negativos (630/656). De un total de 137 muestras positivas por la prueba rápida realizada en el nivel local, 111 también resultaron positivas cuando la prueba rápida se aplicó en el CNRV (81%, IC 95% 74-88) y de un total de 691 muestras negativas por la prueba rápida en el nivel local, 630 también fueron negativas en el CNRV (91%, IC 95% 89-93).
Durante el desarrollo del plan piloto, personal del CNRV visitó 12 de los 13 laboratorios clínicos participantes. Mediante entrevista y observación se identificó que el 100% de los laboratorios visitados cuentan con una planta física e iluminación adecuados para realizar las pruebas rápidas. En 10 (83%) de los laboratorios la persona que realizó la prueba rápida recibió capacitación en INCIENSA, mientras que en los laboratorios 5 y 8, el profesional en microbiología capacitó al personal técnico que realizó las pruebas. Dado que el 100% del personal que realizó las pruebas rápidas también debe ejecutar entre 15 y 250 análisis de laboratorio por día, e incluso atender asuntos administrativos, solo en el 50% de los laboratorios participantes se realizó la lectura de la tira reactiva en el tiempo indicado en el procedimiento de la casa comercial. Sin embargo, el nivel de concordancia obtenido por los diferentes laboratorios no coincidió con el cumplimiento o no de los tiempos de lectura, tampoco hubo coincidencia en si la prueba rápida fue realizada por un profesional o un técnico capacitado, o la cantidad de otros análisis de laboratorio o actividades por realizar durante la jornada laboral.
Con respecto a la evaluación externa del desempeño efectuado por el CNRV a los 13 laboratorios clínicos, el 85% de los participantes (n=11) enviaron los resultados. La concordancia de estos fue de un 100% para un índice de kappa de 1,0 (IC 95% 0,66-1,03) con respecto a los resultados de las muestras incógnitas obtenidos por las técnicas diagnósticas del CNRV.
Discusión
Los resultados de IgM contra dengue obtenidos por la prueba rápida de PanBio® realizada en el nivel local y en el nivel central se compararon contra los resultados de IgM que dio la técnica de MAC ELISA lo cual, en apoyo a la vigilancia epidemiológica del dengue, se realiza de rutina en el CNRV desde octubre de 1993. En general, para estas dos situaciones, al obtener intervalos de confianza al 95% en diferente orden de magnitud, se evidenció una diferencia significativa con respecto al índice de kappa y el porcentaje de concordancia de los resultados positivos obtenidos al aplicar la prueba rápida en los laboratorios de los establecimientos de salud y en el CNRV, lo que indica que la aplicación de la prueba rápida en el nivel local, en general no detectó un 25% de las muestras positivas para IgM dengue que si detectó el MAC-ELISA, mientras que la misma prueba rápida ejecutada en el CNRV no identificó un 7% de esas muestras IgM dengue positivas por MAC-ELISA.
Sin embargo, las diferencias obtenidas al comparar los resultados individuales reportados por cada uno de los laboratorios participantes, en donde el rango del índice de concordancia varía entre -0,02 a 0,82, con un porcentaje de concordancia de los resultados positivos que oscila entre el 39% y el 98%, indica que la transferencia de esta metodología requerirá de un proceso de acompañamiento y revalidación, sobre todo en aquellos laboratorios cuyo índice de kappa resultó inferior a 0,415 y en los que este sistema no resultó efectivo porque detectó el 50% ó menos de las muestras positivas, de tal forma que se logren identificar los factores causales de esta discordancia para subsanarlos. Aún cuando los resultados de la visita a los laboratorios y la concordancia en los resultados de tres muestras incógnitas indicaron que las condiciones locales para aplicar esta prueba son adecuadas, los sesgos correspondientes a los resultados de la rutina pudieron deberse a condiciones inherentes al método en sí y al desempeño diario del personal que labora en las diferentes jornadas, realizando otras pruebas de laboratorio y atendiendo en forma simultánea múltiples tareas. Para este procedimiento es importante que siempre se garantice que el espacio físico en el cual se realiza la prueba cuente con iluminación adecuada, lo realice personal con experiencia y se cumpla con la metodología indicada por la casa comercial,16-18 de tal forma que genere resultados consistentes, confiables y oportunos para la toma de decisiones, ya que el uso de estos permitirá determinar si lo notificados son casos confirmados de dengue o si se trata de otra enfermedad clínicamente similar.3,9
Al descentralizar el diagnóstico del dengue, como se consignó en la Estrategia Nacional de Gestión Integrada para la Prevención y Control del Dengue en Centroamérica,10 el trabajo del laboratorio local no será el diagnóstico individual de cada caso, sino, apoyar el sistema de vigilancia epidemiológico, identificando mediante métodos serológicos nuevas áreas hacia donde pueda propagarse la enfermedad y orientar el diagnóstico en presentaciones atípicas de algunos casos. La función del CNRV se concentrará en identificar los serotipos del virus dengue circulantes, realizar el diagnóstico diferencial con otras enfermedades virales, a la vez que debe implementar, ejecutar y coordinar un programa de confirmación diagnóstica y evaluación externa del desempeño a los labortorios que integren la red.
Los resultados en la determinación de los anticuerpos IgM deben interpretarse con precaución y a la luz de los hallazgos clínico epidemiológicos, debido a que el nivel de anticuerpos detectables depende de los días de evolución de la enfermedad que tenga el paciente al momento cuando se le toma la muestra y de si el paciente cursa con una infección primaria o secundaria. Así, un resultado negativo temprano en el curso de la enfermedad no excluye una infección por dengue y si los síntomas clínicos persisten, se requiere repetir la prueba con una segunda muestra, mientras que un diagnóstico de laboratorio positivo por IgM en la fase aguda de la infección por el virus dengue podría definir el diagnóstico diferencial. Sin embargo, como los anticuerpos IgM pueden persistir entre 60 a 90 días, los resultados positivos deben ser provisionales porque su detección no necesariamente significa que la infección aguda es por dengue, sino que la persona sufrió la infección por dengue en el trascurso de los últimos 3 meses.
Además, en la determinación de estos anticuerpos para dengue se ha documentado reacción cruzada con otros flavivirus como Fiebre Amarilla, Virus Nilo del Oeste, Encefalitis de San Luis y también puede presentarse estimulación clonal inespecífica. Por otro lado, se debe considerar que la sintomatología en curso puede obedecer a otra patología con presentación clínica muy similar a la del dengue; es posible desarrollar un cuadro de fiebre hemorrágica por dengue (FHD) en pacientes con una infección primaria y en estos casos tampoco se debe descartar una coinfección.3,19,20
En países como el nuestro, donde el dengue es endémico y se ha documentado la circulación de tres de los cuatro serotipos de este virus,1 las infecciones secundarias resultan ser muy comunes, por lo que el personal de las regiones de salud, conocedor de este perfil epidemiológico, debe estar alerta a identificar la presentación del cuadro clínico para aplicar adecuada y efectivamente la definición de casos sospechosos que activan el sistema de vigilancia del dengue y establecen el protocolo de atención por seguir2,21,22 ya que el país cuenta con criterios de hospitalización y de monitoreo de los pacientes con dengue que han garantizado una tasa de letalidad y estancias hospitalarias bajas.23, 24
La fase crítica de los pacientes con dengue, es en los primeros días de evolución de la enfermedad, por lo que el abordaje clínico en esta fase no se beneficia con una determinación de anticuerpos IgM contra dengue, que en general alcanzan niveles detectables por la gran mayoría de las técnicas serológicas después del quinto día de evolución de la enfermedad.
Considerando los resultados obtenidos por el CNRV en este plan piloto y en concordancia con la bibliografía,25,26 una vez implementado un programa de capacitación, supervisión y evaluación externa del desempeño, al igual que el MAC ELISA, la prueba PanBio® Dengue Duo® puede ser una herramienta rápida y eficiente por usar para la detección de IgM aplicada a la vigilancia epidemiológica del dengue, sobre todo en áreas alejadas y de difícil acceso, y con limitaciones de infraestructura en el laboratorio, así como en apoyo al trabajo de campo que permita confirmar la sospecha clínica de dengue para orientar las acciones de prevención y control iniciadas.17
Sin embargo, de acuerdo con el grado de desempeño que se requiera para el sistema de vigilancia epidemiológica de esta patología, considerando las implicaciones costobeneficio de las intervenciones que se aplican, el país debe decidir el rango aceptable de sensibilidad y especificidad que está dispuesto a aceptar al seleccionar la prueba de laboratorio comercial que descentralizará.
Agradecimiento
Al personal de los laboratorios clínicos de la Caja Costarricense de Seguro Social (CCSS) participantes en este plan piloto por realizar los análisis, aportar información, facilitar el apoyo logístico local y colaborar en que se cumpliera con este proceso. Y a todo el personal del Centro Nacional de Referencia de Virología (CNRV) del INCIENSA, por el apoyo técnico que permitió enriquecer este trabajo. Este plan piloto se realizó con fondos suministrados por el Instituto Costarricense de Investigación y Enseñanza en Nutrición y Salud (INCIENSA), la Caja Costarricense de Seguro Social (CCSS) e Inmunolab Costa Rica (Investigación Biomédica).
Referencias
1. Sáenz E, González L, Víquez M, Lara J, Valverde M. Circulación del Virus Dengue 3 en Costa Rica, 1994-1997. Acta Méd Costarric 1999; 41:24-31. [ Links ]
2. Costa Rica, Ministerio de Salud, Comisión Técnica Interinstitucional de Dengue. Normas técnicas para el control del dengue y dengue hemorrágico. San José: Ministerio de Salud; 2000. [ Links ]
3. Organización Panamericana de la Salud. Dengue y dengue hemorrágico en las Américas: Guías para su prevención y control. Washington, D.C.:OPS; 1995. (publicación científica 548). [ Links ]
4. Panbio Diagnostics [homepage on the Internet] Queensland: Inverness Medical Innovations Australia Pty Ltd. En: http://www.panbio.com. Consultado 27 de marzo de 2007. [ Links ]
5. Porter KR, Widjaja S, Lohita HD, Hadiwijaya SH, Maroef CN, Suharyono WS, et al. Evaluation of a comercially available inmunoglobin m capture enzyme-linked inmunosorbent assay kit for diagnosing acute dengue infections. Clin Diagn Lab Immunol 1999; 6: 741-744. [ Links ]
6. Velez JD, Bedoya AM, editors. Papel del laboratorio en el diagnóstico del dengue [monograph on the Internet]. Cali: Fundación Clínica Valle del Lili; 2002 (cited 2006 november 29). En http://www.liliurgencias. org/index.php?option=com_content&task=view&id=282&Itemid=61. [ Links ]
7. Acosta C, Gómez I. Biología y métodos diagnósticos del dengue. Biomed 2005; 16:113-137. [ Links ]
8. Cuzzubbo AJ, Endy TP, Nisalak A, Kalayanarooj S, Vaughn DW, Ogata SA, et al. Use of recombinant envelope proteins for serological diagnosis of dengue virus infection in an inmunochromatographic assay. Clin Diagn Lab Immunol 2001; 8: 1150-1155. [ Links ]
9. Groen J, Koraka P, Velzing J, Copra C, Osterhaus A. Evaluation of six immunoassays for detection of dengue virus-specific immunoglobulin M and G antibodies. Clin Diagn Lab Immunol 2000; 7: 867-871. [ Links ]
10. Ministerio de Salud, Caja Costarricense de Seguro Social, Inciensa, OPS/OMS. Plan Nacional para la Estrategia Centroamérica de Gestión Integrada para la Prevención y Control del Dengue. Costa Rica; 2005. [ Links ]
11. Instituto de Medicina Tropical Pedro Kourí, Técnicas de laboratorio para el diagnóstico y la caracterización del virus dengue, La Habana, Cuba; Instituto de Medicina Tropical Pedro Kourí, 2001. [ Links ]
12. Guzman MG, Kourí G. Dengue diagnosis, advances and challenges. Int J Infect Dis 2004; 8:69-80 [ Links ]
13. Thrusfield M, Ortega C.; Blas I de, Noordhuizen JP, Frankena K. WIN EPISCOPE 2.0: improved epidemiological software for veterinary medicine. Vet Rec. 2001; 148:567-572. [ Links ]
14. Tarabla H. Epidemiología Diagnóstica. Santa Fe, Argentina: Universidad Nacional del Litoral, 2000. [ Links ]
15. Altman DG. Practical statistics for medical research. New York: Chapman and Hall, 1991 [ Links ]
16. Word Health Organization. The Use of rapid syphilis tests. Geneva, Switzerland, 2006. [ Links ]
17. Peeling R, Smith P, Bossuyt P. A guide for diagnostic evaluations. Nat Rev Microbiol. 2006; 4 (12 suppl): S2-S6. [ Links ]
18. World Health Organization. Special Programme for Research & Training in Tropical Diseases. Evaluation of diagnostic tests for infectious diseases: General principles. The TDR diagnostics evaluation expert panel. Nat Rev Microbiol 2006; 4 (12 suppl): S20-S32. [ Links ]
19. Biogenix [homepage on the Internet]. Bogotá: Biogenix Expanding Laboratory Technology [updated 2006 november 29]. Prueba Rápida para la detección de anticuerpos IgG e IgM en suero. [about 1 screen]. En: http://www.biogenix.com.co/internas/productos/IgGeIgMenSuero.htm. [ Links ]
20. Gutierréz J, Maroto C, editors. Serodiagnóstico de la Infección Vírica: Su Interés Clínico. [monograph on the Internet]. Madrid: Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica; 2006. [cited 2007 march 27]. En http://www.seimc.org/control/revi_Sero/Serovir.htm.
21. Sáenz E, Maranda L, Piza J, González L, Achoy R. Evaluación del sistema de vigilancia epidemiológico del dengue utilizando como indicador la aplicación de la definición de caso sospechosos, Costa Rica., 1998. Rev Costarric Cienc Med 2001; 22:117-140. [ Links ]
22. Sáenz E, Maranda L, González L. Adecuación de la definición de caso sospechoso de dengue, basado en la asociación de síntomas y signos según los registros médicos, Costa Rica, 1998. Rev Costarric Cienc Med. 2001: 22:131-140. [ Links ]
23. Alfaro A, Guardia M, Angulo C. Organización de la atención medica en la epidemia de dengue hemorrágico en el Hospital Dr. Enrique Baltodano de Liberia, 2003. Acta Med Costarric. 2006; 48 185-89. [ Links ]
24. Alfaro A, Guardia M, Wong R, Angulo D, Wong J, Pérez MT. Caracterización clínica del dengue hemorrágico en niños Hospital Dr. Enrique Baltodano de Liberia, 2003. Acta Pediátr Costarric. 2005; 19:11-16. [ Links ]
25. Palmer CJ, King SD, Cuadrado RR, Pérez E, Baum M, Ager A. Evaluation of the MRL diagnostics dengue fever virus IgM capture ELISA and the PanBio rapid inmunochromatographic test for diagnosis of dengue fever in Jamaica. J Clin Microbiol 1999; 37: 1600-1601. [ Links ]
26. Palmer CJ, Mamani E, Bonilla JA, García P, Guerra H, Gotuzzo E, et al. Aplicación de la prueba rápida Pan Bio dengue dúo para la detección de dengue en la localidad amazónica de Mazán. Rev Perú Med Exp Salud Pública. 2003; 27-30. [ Links ]
Abreviaturas: CNRV, Centro Nacional de Referencia de Virología; INCIENSA, Instituto Costarricense de Investigación y Enseñanza en Nutrición y Salud; MAC-ELISA, Inmunoensayo enzimático sobre fase sólida de captura para IgM.