En esta revisión se hace un análisis sobre el uso de los anticoagulantes directos en pacientes con FA a los que se les realizará una cardioversión ya sea eléctrica o farmacológica, un procedimiento de ablación y por último se presentan las recomendaciones para pacientes que requieren de una cirugía y están con alguno de estos fármacos.
Cardioversión
La cardioversión eléctrica y farmacológica está asociada a un riesgo inherente de ictus o embolismo sistémico en pacientes no anticoagulados, con una incidencia de tromboembolia del 5 al 7%. El tratamiento anticoagulante ha reducido de forma significativa esta complicación (<1%).1 La cardioversión es segura si la FA dura menos de 48 horas; en caso de que la duración sea superior a ésta se debe iniciar la anticoagulación al menos 3 semanas antes y continuar 4 semanas más o de forma crónica en función del riesgo moderado elevado de ictus (CHA2DS2-VASc ≥2). En esto caso, sería preferible el pretratamiento con los anticoagulantes directos con una dosis ≥4 horas previas a la cardioversión. En el caso que existan dudas sobre la adherencia al tratamiento, o en los casos en los que se prefiera una cardioversión precoz, la realización de un ecocardiograma transesofágico estaría indicado para descartar la presencia de trombos.
La seguridad y eficacia de los anticoagulantes directos se ha demostrado como alternativas al tratamiento con antagonistas de la vitamina K, permitiendo realizar una cardioversión precoz, especialmente en los pacientes tratados con Rivaroxaban y Edoxaban. Los subanálisis del ROCKET-AF sobre seguridad pericardioversión incluía a un pequeño número de pacientes. Debido a estas limitaciones se desarrolló el estudio X-Vert con más de 1 500 pacientes con fibrilación auricular que se sometían a cardioversión electiva bajo tratamiento con Rivaroxaban observándose una reducción de ictus, accidente isquémico transitorio, y embolismo periférico; sin aumentar los eventos hemorrágicos.2
En la Figura 1 se muestra el algoritmo de anticoagulación para realizar una cardioversión ya sea eléctrica o farmacológica3.
Ablación
Este procedimiento presenta un riesgo incrementado de eventos, en relación a la introducción y manipulación de catéteres, la presencia de introductores dentro de la aurícula izquierda y las lesiones endocárdicas producidas por la ablación.
Por lo que es fundamental mantener la anticoagulación durante la ablación. Sin embargo, estos procedimientos también están relacionados con complicaciones hemorrágicas.
Las tasas descritas de eventos embólicos son del 1% y de eventos hemorrágicos del 3%.
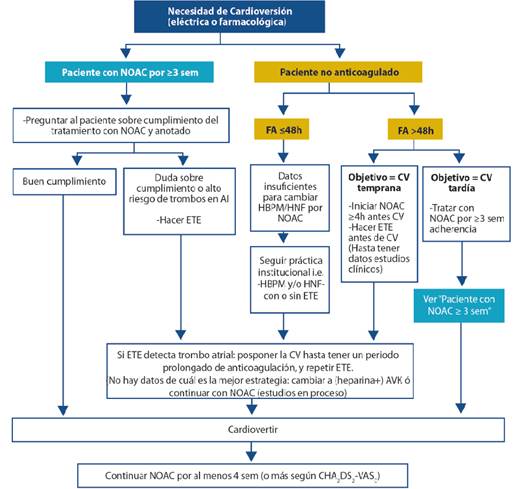
Figura 1. Algoritmo de anticoagulación en la Cardioversión Eléctrica o Farmacológica (3). AI: aurícula izquierda. AVK: Antagonistas de la Vitamina K. CV: Cardioversión. ETE: ecocardiograma transeofágico. FA: Fibrilación auricular. HBPM: Heparinas de bajo peso molecular. HNF: Heparina no fraccionada. NOAC: Nuevos anticoagulantes orales o anticoagulantes directos.
El manejo antitrombótico de la FA debe incluir desde el tratamiento previo al procedimiento, como durante y posterior al mismo. Todos los pacientes sometidos a la ablación de FA deberían recibir anticoagulación durante las 3 semanas previas, o debería realizarse un ecocardiograma transesofágico previo al procedimiento. La ablación de la FA se debe realizar con anticoagulación, ya sea con antagonistas de la vitamina K o anticoagulantes directos, ya que no se han observado problemas de seguridad en cohortes de estudios observacionales de pacientes tratados con anticoagulantes directos sometidos a ablación. En el caso del Rivaroxaban es el único del que se dispone de un estudio prospectivo en esta población observándose bajo riesgo embólico y hemorrágico.
Posteriormente a la ablación, la anticoagulación se ha de mantener durante al menos 8 semanas en pacientes de bajo riesgo, y de forma permanente en pacientes con riesgo moderado- alto (CH2DS2-VASc≥2).
Aunque los datos sobre el momento de interrupción de la anticoagulación previa a la ablación son contradictorios, parece seguro suspender los anticoagulantes directos el día previo a la misma, sin terapia puente. Recientemente estudios randomizados con rivaroxaban han demostrado que la no interrupción es segura, así como realizar la ablación bajo tratamiento con antagonistas de la vitamina K si el INR está entre 2.0 - 3.0, incluso hasta 3.54.
Manejo perioperatorio
El carácter previsible de la farmacocinética de los anticoagulantes directos hace que el manejo perioperatorio de estos esté establecido a través de consensos de expertos. La recomendación de suspensión de los mismos dependerá del tipo de fármaco, función renal y riesgo hemorrágico de la cirugía (Tabla 1). La terapia puente con heparina de bajo peso molecular no es adecuada en este contexto. Su uso se ha asociada a un incremento de la hemorragia perioperatoria.
Sin embargo, no existe consenso sobre el manejo de estos en caso de cirugía urgente. En estos casos el manejo recomendado, es el manejo del sangrado; existiendo muchas incertidumbres en pacientes con alto riesgo hemorrágico y situaciones de sangrado. Hasta hace unos años no disponíamos de antídoto, pero recientemente se han desarrollo agentes reversores de los fármacos inhibidores de la trombina, idarucizumab, ya disponible; y también de los inhibidores del X activado, andexanet alfa, que todavía está en fase de desarrollo. Por lo que en casos de cirugía urgente, en el caso de disponer antídoto, lo usaríamos y sino se usaría el algoritmo del control del sangrado.
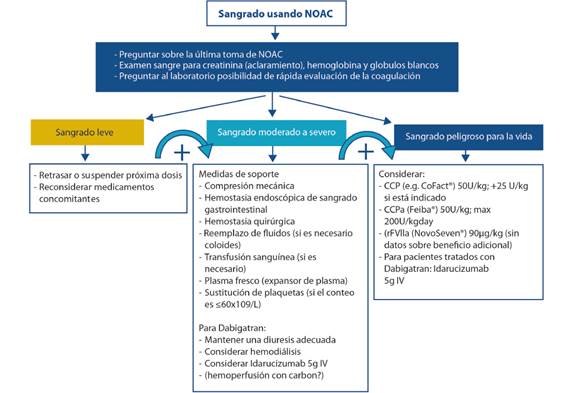
Figura 2. Algoritmo de manejo de complicaciones hemorrágicas (3). CCP: Concentrado de Complejo de protrombina. CCPa: Concentrado de Complejo de protrombina activado. NOACS: Nuevos anticoagulantes orales o anticoagulantes directos.
Tabla 1: Última dosis del fármaco antes de una intervención quirúrgica electiva en función del riesgo de sangrado de la cirugía y de la función renal del paciente 3
| DABIGATRAN | RIVAROXABAN-EDOXABAN-APIXABAN | ||||
|---|---|---|---|---|---|
| Riesgo hemorrágico no importante y/o hemostasia local posible | |||||
| Bajo Riesgo | Alto Riesgo | Bajo Riesgo | Alto Riesgo | ||
| CrCl ≥80ml/min | ≥ 24 horas | ≥ 48 horas | ≥ 24 horas | ≥ 48 horas | |
| CrCl 50-80ml/min | ≥ 36 horas | ≥ 72 horas | ≥ 24 horas | ≥ 48 horas | |
| CrCl 30-50ml/min | ≥ 48 horas | ≥ 96 horas | ≥ 24 horas | ≥ 48 horas | |
| CrCl 15-30ml/min | No indicado | No indicado | ≥ 36 horas | ≥ 48 horas | |
| CrCl< 15ml/min | No hay indicación oficial | ||||
| NO ES NECESARIO USAR TERAPIA PUENTE CON HBPM/HNF | |||||
Podría considerarse el tratamiento con concentrado de protrombina en el caso de hemorragias potencialmente mortales, y medidas generales, como reposición de volumen, transfusión de sangre y mantenimiento adecuado de diuresis.
En la figura 2 se muestra el algoritmo de manejo recomendado para pacientes que presentan hemorragia y estén en tratamiento con anticoagulantes orales directos3.














