Introducción
La producción de flores en Colombia está destinada principalmente a la exportación; el país ocupa el segundo lugar en el mercado a nivel mundial después de Holanda (Moreno & Serna, 2006; Quirós, 2012; Instituto colombiano Agropecuario, 2018a). Así mismo, se ha consolidado como el principal proveedor de flores a Estados Unidos y el segundo de la Unión Europea (Calderón, 2014; Instituto colombiano Agropecuario, 2018a). Para la temporada de San Valentín 2019, se exportaron más de 35 000 toneladas de flores para un total 600 millones de tallos (Ministerio de Comercio, Industria y Turismos, Colombia, 2019)
El número de hectáreas cultivadas con flores dentro del territorio colombiano es aproximadamente de 7 532 distribuidas principalmente en los departamentos de Cundinamarca y Antioquia (Instituto colombiano Agropecuario, 2018a). Estas zonas presentan suelos fértiles y condiciones ambientales adecuadas para el desarrollo de los cultivos de flores (Ramírez, 2014). Actualmente, el sector floricultor antioqueño tiene registradas 2 430 ha con producción de especies ornamentales. Las especies más cultivadas en el departamento son Hortensias (Hydrangea macrophylla (Thunb.) Ser.), Crisantemos (Chrysanthemum L.) y Áster (Aster L.) (Instituto colombiano Agropecuario 2018b). Para 2018, este mismo departamento registró más de 1 703 ha cultivadas con H. macrophylla (Instituto colombiano Agropecuario 2018b; Ministerio de Agricultura y Desarrollo Rural de Colombia, Agronet, 2019). Es importante resaltar que entre enero y noviembre de 2018 fueron exportadas 19 133 toneladas de H. macrophylla con un valor estimado de 70.65 mill USD (Agronegocios, 2019). Las flores H. macrophylla son un producto que se obtiene mediante un sistema de producción programado, al aire libre o bajo invernadero. Debido a sus inflorescencias grandes, coloridas y longevas, y por su abundante follaje verde, la planta es utilizada como ornamento en interiores y exteriores (Gilman, 1999). Además, se ha reportado que esta planta presenta propiedades medicinales (Seo et al., 2009; Yashaswini, Hegde & Venugopal, 2011).
El género Hydrangea L.pertenece a la familia Hydrangeaceae (APG IV, 2016) y comprende aproximadamente 220 especies (Hufford, 2004). H. macrophylla es una planta originaria del continente asiático con alta adaptabilidad a ambientes húmedos (Codarin, Galopin, & Chasseriaux, 2006; Halcomb & Reed, 2010; Hempel, Hohe, & Tränkner, 2018). Esta planta es un arbusto caducifolio que puede alcanzar hasta 1.5 m de altura, tiene inflorescencia tipo corimbo constituido por brácteas modificadas que subyacen a las flores. Presenta hojas opuestas de 7-15 cm de largo, pecioladas, de obovadas a elípticas o anchamente ovadas, gruesas, de ápice puntiagudo y margen aserrado (Simpson, 2010). La especie H. macrophylla es ampliamente cultivada por su valor ornamental, de la cual se han obtenido diferentes variedades comerciales (Cerbah et al., 2001; Dirr, 2004; Arafa, Nower, Helme, & Adb-Elaty, 2017). Se han registrado cuatro subespecies de H. macrophylla, siendo H. macrophylla ssp. macrophylla y H. macrophylla ssp. serrata las más exitosas desde el punto de vista comercial (Windham et al., 2011; Reed & Rinehart 2007).
El cultivo de H. macrophylla es afectado por patógenos que incluyen insectos (trips, pulgones), crustáceos (cochinillas) y moluscos (babosas, caracoles; Fontseré & Pahí, 1984). También se han reportado afecciones ocasionadas por nemátodos (French, John, & Williams, 1971; Basterrechea, 2005), virus (Tang, Harper, Wei, & Clover, 2010; Dória, Nozaki, Pavan, Yuki, & Sakate, 2011). Hongos (Hagan, Olive, Stephenson, & Rivas-Davila, 2004; Freire & Mosca, 2009;Windham et al., 2011; Mmbaga, Kim, Mackasmiel, & Li, 2012). Entre los hongos que ocasionan lesiones foliares en H. macropylla se encuentran Cercospora hidrangeae Ellis & Everh (Hagan et al., 2004), Rhizoctonia solani Kühn (Freire & Mosca, 2009), Erysiphe polygoni DC.(Windham et al., 2011), Alternaria alternata Fr., Colletotrichum gloeosporioides Penz, Phoma exigua Desm, Myrothecium roridum Tode (Mmbaga et al., 2012). La principal enfermedad foliar ocasionada por micopatógenos en esta planta, se conoce comúnmente como Oidiosis o ceniza (Li et al., 2018; Qiu, Braun, Li, & Li, 2019). En H. macrophylla se ha reportado que esta enfermedad puede ser ocasionada por micopatógenos del orden Erisiphales, y las especies que se reportan como agentes causantes de la Oidiosis son: Erysiphe polygoni DC., Erysiphehydrangeae (Z.X. Chen & R. X. Gao) U. Braun & S. Takam., Erysiphe schizophragmatis (Tanda & Y. Nomura) U. Braun & S. Takam., Erysipheyanshanensis T.Z. Liu & U. Braun, Golovinomyces orontii (Castagne) V.P. Heluta, Erisyphe poeltii U. Braun, Pseudoidium hortensiae (Jørst.) U. Braun & R.T.A. Cook y Oidium hortensiae Jørst (Li et al., 2009a;Li et al., 2009b; Schmidt & Scholler, 2011; Windham et al., 2011; Braun & Cook, 2012; Park, Cho, Park, Lee & Shin, 2012; Li et al., 2018; Qiu et al., 2019).
La sintomatología causada por estos micopatógenos es muy similar y se caracteriza por formar parches o manchas pulverulentas blancas a grises sobre la cara abaxial o adaxial de la lámina foliar (Kuhn et al., 2016; Li et al., 2018). Estos micopatógenos son parásitos biotrófos obligados que se desarrollan solo en las células epidérmicas y penetran a través de la cutícula por hifas especializadas llamadas apresorios. A partir de los apresorios se forman los haustorios, que le permiten al micopatógeno la absorción de agua y nutrientes (Li et al., 2009a, Li et al., 2009b; Kuhn et al., 2016; Li et al., 2018). Al utilizar los nutrientes del hospedero ocasiona un detrimento en la tasa fotosintética y aumento en tasa de respiración y transpiración, lo que implica menor eficiencia en el desarrollo de la planta que repercute negativamente en el vigor y afecta directamente la calidad y el valor comercial de las flores y por consiguiente la competitividad en los mercados (Agrios, 2005; Sinclair & Lyon, 2005; Windham et al., 2011; Li et al., 2018).
En general, la mayoría de los estudios sobre micopatógenos que originan la Oidiosis en H. macrophylla, se han enfocado en determinar cuáles son variedades resistentes al efecto del micopatógeno y evaluar estrategias de control fitosanitario (Windham et al., 2011; Li et al., 2009a, Li et al., 2009b). Por estas razones, se propuso en este trabajo realizar una descripción detallada de las alteraciones anatómicas, histológicas y citohistoquímicas ocasionadas por la Oidiosis en hojas de H. macrophylla. Referente a aspectos relevantes como la producción de polisacáridos, lípidos, pectinas, polifenoles y lignina. También posibles respuestas químicas al ataque del micopatógeno. La información obtenida se puede relacionar con la alteración de los procesos metabólicos del hospedero característicos de este pato-sistema.
Materiales y métodos
Durante la época de invierno se recolectaron hojas maduras sanas de H. macrophylla e infectadas con Oidiosis o ceniza entre abril y mayo 2015. El criterio para seleccionar las hojas infectadas se hizo sensuLi et al., (2018). El material vegetal se recolecto en el vivero El Jardín del Edén en la vereda Sajonia, Municipio de Rionegro, Antioquia a (06°09’47” N & 75°27’30” W) y 2 316 m.s.n.m. Los especímenes de H. macrophylla ssp. macrophylla fueron depositados en el herbario de la Universidad de Antioquia (HUA) con la referencia de recolección Rincón 023. Para la identificación del patógeno a nivel de género, se realizaron secciones a mano alzada de las hojas que presentaban síntomas de Oidiosis, tanto en la cara adaxial como abaxial de la lámina foliar y estas fueron teñidas con azul de Lactofenol y se observó con contraste diferencial de interferencia (CDI). Se consultaron claves taxonómicas especializadas (Schmidt & Scholler, 2011; Braun & Cook, 2012).
Para analizar las características anatómicas e histoquímicas se seccionaron 30 hojas sanas y 30 infectadas, de estas se obtuvieron fragmentos transversales de 2 cm. Estos fragmentos fueron fijados en una mezcla de formol, etanol y ácido acético (FAA) por 24 h a 6 °C. Después de la fijación se mantuvieron en solución de alcohol-glicerol por 48 hr a 6 °C, para luego deshidratarlas en una serie gradual de etanol y dos pasos de aclaramiento en Xilol. Los fragmentos se incluyeron a Paraplast plus® durante 12 hr a 55 °C (Ruzin, 1999). El material embebido fue seccionado a 5 µm de grosor en un micrótomo rotatorio LEICA RM 2125®.
Las secciones obtenidas se tiñeron con Safranina-azul de Alcian para realizar des¬cripciones de tejidos con paredes primarias y secundarias, además de resaltar de cutina y de forma no especifica, polifenoles (Ruzin, 1999; Demarco, 2017), rojo de Rutenio para determinar la presencia de pectinas (Sandoval, 2005; Soukup, 2014). Se utilizó Lacmoid y Ponceau S para calosa (Ramming, Hinrichs, & Richardson, 1973; Ulryghová, Petrü, & Pazourková, 1976; Soukup, 2014). Así mismo, Cloruro férrico para polifenoles totales (Peterson, Peterson, & Melville, 2008; Demarco, 2017) y negro de Sudán para lípidos estructurales (Demarco, 2017). Se empleó Uvitex-Hematoxilina para la detección de quitina y núcleos celulares (Sørensen, Justesen, & Hovmøller, 2012; Dugyala, Borowicz, & Acevedo, 2015), para detectar lignina se empleó Floroglucinol ácido (Soukup, 2014; Demarco, 2017) y para carbohidratos la tinción de PAS (Ruzin, 1999; Demarco, 2017).
Las observaciones se realizaron mediante un microscopio fotónico Nikon 80i eclipse® equipo con el sistema de contraste diferencial de interferencia (CDI). Las fotografías se obtuvieron con cámara digital Nikon (DS-fi 1) utilizando el programa NIS- Elements (BR 4.30.02.). Las secciones tratadas con Uvitex-Hematoxilina se examinaron mediante microscopía de epifluorescencia utilizando filtro UV- 2A (filtro de excitación 330-380 nm y filtro barrera 420 nm) (Ruzin, 1999). El término papilas (o aposiciones de la pared celular) se empleó sensuUnderwood (2007) y Voigt (2014).
Para llevar a cabo las descripciones morfológicas con microscopía electrónica de barrido (MEB), fragmentos de las hojas sanas e infectadas se fijaron y deshidrataron en metanol al 100% por 48 horas, efectuando dos cambios en este solvente (Talbot & White, 2013). Posteriormente, se desecaron a punto crítico con un desecador SAMDRI®-795. Las muestras se montaron sobre cinta conductiva de carbono de doble cara y se recubrieron con oro en una ionizadora DENTON VACUUM DESK IV durante 8 min. Las observaciones y registro fotográfico se realizaron en un microscopio electrónico de barrido JEOL JSM-6490LV.
Resultados
H. macrophylla ssp. macrophylla es un arbusto de hojas simples opuestas decusadas de color verde intenso, presentan inflorescencias terminales tipo corimbo (Fig. 1A). Las plantas observadas en el sitio de recolecta pueden presentar inflorescencias de diferentes colores, que depende principalmente del pH de los suelos y la variedad de las plantas. Los colores de las inflorescencias van desde el azul intenso al rojo, e incluso variedades de color blanco (Fig. 1A). Las plantas afectadas por la Oidiosis, por lo general presentan un micelio externo fino que forma manchas pulverulentas de color blanco o grisáceos, que se desarrollan tanto en la cara abaxial como en la adaxial de la lámina foliar. Con el progreso de la infección, estas masas de micelio cubren todo el limbo foliar y se puede apreciar lesiones de color oscuro (Fig. 1B). Los síntomas también pueden ser visibles en las brácteas florales de color blanco y se aprecian como manchas de color marrón-rojizo (Fig. 1C). Las células epidérmicas adaxiales presentan una cutícula que forma estrías epicuticulares que son más conspicuas en algunas células que en otras (Fig. 1D). Tanto en la superficie adaxial como abaxial de las hojas y brácteas florales H. macrophylla infectadas con Oidiosis se observó la presencia de un micelio externo hialino septado, ramificado y con numerosos apresorios multilobulados (Fig. 1E). Los apresorios se aprecian fuertemente adheridos a la cutícula, la cual se aprecia desgastada y con deterioro en los puntos de contacto con esta estructura fúngica (Fig. 1F). Los conidióforos son ligeramente curvados y por lo general de 2-3 células y presentan una conidia terminal elipsoide o algunas veces ovoide con numerosos gránulos refringentes en el citoplasma (Fig. 1G). Por lo general, forman un tubo de germinación corto por conidia que termina en un apresorio multilobulado (Fig. 1H). No se apreciaron estructuras de reproducción sexual de la Oidiosis en las muestras de hojas procesadas y analizadas en esta investigación”.

Fig. 1 AP: apresorio; CD: conidióforos; CN: conidias; MI: micelio; TG: tubo de germinación. Hydrangea macrophylla. Plantas sanas e infectadas por la Oidiosis o ceniza y características del hongo causante de la enfermedad. A. Planta sana. B. Planta infectada. C. Corimbos florales sanos (izquierda) e infectados (derecha). D. Superficie de la epidermis adaxial de las hojas sanas, se observan estrías cuticulares (Microscopía electrónica de barrido-MEB). E-G. Características morfológicasdel micelio externo mostrando apresorios, conidiforos y conidias.El detalle en E corresponde a una sección a mano alzada y teñida con azul de Lactofenol. En F, la cabeza de flecha roja indica el deterioro de la cutícula (Microscopía electrónica de barrido-MEB). En H detalles de las conidias y tubos de germinación teñidas con azul de lactofenol. Fig. 1 AP: appressorium; CD: conidiophores; CN: conidia; MI: mycelium; TG: germination tube. Hydrangea macrophylla . Healthy and infected plants with powdery mildew and characteristics of the disease-causing fungus. A. Healthy plant. B. Infected plant. C. Healthy (left) and infected (right) floral corymbs. D. Surface of the adaxial epidermis in healthy leaves, showing cuticular striations (scanning electron microscopy (SEM)). E-G. Morphological characteristics of the mycelium, appressorium, conidiophores, and conidia. The detail view in E depicts a freehand section stained with Lactophenol Blue. In F, the red arrowhead indicates the damage to the cuticle (scanning electron microscopy (SEM)). H. Provides a detailed view of the conidia and germination tubes, stained with Lactophenol Blue.
Observaciones anatómicas de las hojas sanas: la epidermis de las hojas es glabra, monoestratificada y está constituida por células de contorno redondeado a rectangular a ambos lados de la lámina foliar, siendo de mayor tamaño las del lado adaxial (Fig. 2A). Tanto la epidermis adaxial como la abaxial presentan una cutícula delgada y poco perceptible incluso a los máximos aumentos en las que fue observada. Las hojas de H. macrophylla son homobáricas y presentan mesófilo dorsivental. En el lado adaxial del mesófilo se encuentra el parénquima de empalizada que está constituido por un estrato de células cortas con abundantes cloroplastos (Fig. 2A). Luego se encuentra el parénquima esponjoso que por lo general forma entre 6-7 estratos de células que delimitan grandes espacios aeríferos, pero convergen alrededor de haces vasculares secundarios o terciarios (Fig. 2A).
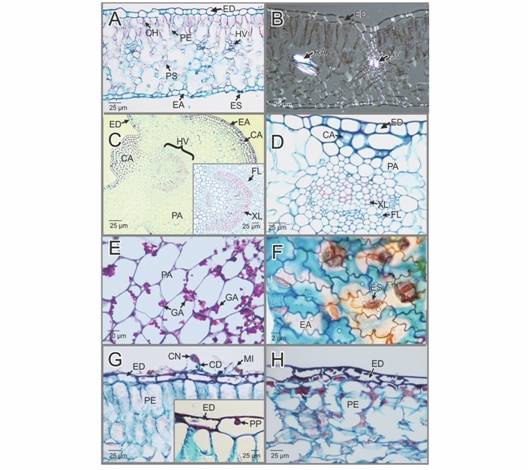
Fig. 2 CA: colénquima angular; CD: conidióforos; CH: cloroplastos; CN: conidias; EA: epidermis abaxial; ED: epidermis adaxial; ES: estoma; FL: floema; GA: gránulos de almidón; HV: haz vascular; MI: micelio; PA: parénquima fundamental o de relleno; PE: parénquima de empalizada; PP: papilas; PS: parénquima esponjoso; RA: rafidios; XL: xilema.Hydrangea macrophylla. Característica morfo-anatómicas de las hojas sanas e infectadas por la Oidiosis o ceniza. A-B. Secciones transversales de las hojas sanas, teñidas con Safranina-azul de Alcian. En campo claro y con luz polarizada, respectivamente. C-D. Secciones trasversales de las nervaduras de primer y segundo orden de las hojas sanas, respectivamente (Safranina-azul de Alcian). En C se aprecia en el recuadro, un detalle del haz vascular de primer orden. E. Detalle del parénquima de la nervadura (reacción del ácido peryódico de Schiff). F. Detalle de la epidermis abaxial (Safranina-azul de Alcian). G-H. Secciones transversales de las hojas infectadas (Safranina-azul de Alcian). G. Infección temprana. Se aprecian, el micelio externo, conidias y conidioforos sobre la pared periclinal. En el recuadro, se observa un detalle de la epidermis adaxial. H. Sección transversal de la hoja mostrando un detalle del avance de la infección. Fig. 2 CA: angular collenchyma; CD: conidiophores; CH: chloroplasts; CN: conidia; EA: abaxial epidermis; ED: adaxial epidermis; EN: stoma; FL: phloem; GA: starch granules; HV: vascular bundle; MI: mycelium; PA: fundamental parenchyma; PE: palisade parenchyma; PP: papillae; PS: spongy parenchyma; RA: raphides; XL: xylem.Hydrangea macrophylla . Morpho-anatomical characteristics of healthy leaves and leaves infected by powdery mildew. A-B. Transverse sections of the healthy leaves, stained with Alcian Blue-Safranine; under a clear field and polarized light respectively. C-D. Transverse sections of the first and second-order vascular bundles of the healthy leaves respectively (Alcian Blue-Safranine). In C, one can observe a detail view of the vascular bundle in the box. E. Detail of the parenchyma of the vascular bundle (Schiff’s periodic acid reaction). F. Detail of the abaxial epidermis. (Alcian Blue-Safranine) can be observed. G-H. Transverse sections of infected leaves (Alcian Blue-Safranine). G. Early infection.The external mycelium, conidia, and conidiophores on the outer periclinal wall of the epidermis. In the box, a detail of the adaxial epidermis is observed. H. Cross section of the leaf, showing a detail of the progress of the infection.
Las células del parénquima aerífero son cortas ramificadas y también presentan numerosos cloroplastos. Entre las células del parénquima esponjoso, se observó la presencia de idioblastos con rafidios de oxalato de calcio que se aprecian refringentes al observarlos con luz polarizada (Fig. 2B). El haz vascular de primer orden es biconvexo, forma una amplia curvatura sobre la superficie abaxial y una angosta en el lado adaxial. La epidermis en ambos lados de esta nervadura es uniestratificada y constituida por células de contorno cuadro a rectangular y cubiertas por una cutícula delgada (Fig. 2C).
En los tejidos subepidérmicos de la cara abaxial de la nervadura primaria, se aprecian entre 3-5 capas de colénquima angular en tanto que en el lado adaxial se observaron entre 7-10 capas de este mismo tejido (Fig. 2C). Los haces vasculares de la nervadura principal son colaterales cerrados que forma un único arco dispuesto hacia lado adaxial en forma cóncava-convexa, estos haces están inmersos en parénquima fundamental (Fig. 2C). El floema forma varias filas de células hacia la cara abaxial de la nervadura en tanto que el xilema se aprecia en disposición radial formando entre 25 a 30 brazos (Fig. 2C). El haz vascular de segundo orden es colateral cerrado y está soportado por columnas de parénquima y colénquima. Este haz está formado por entre cuatro a cinco brazos de xilema y varias capas de floema dirigidas hacia el lado adaxial de la nervadura (Fig. 2D). El almidón fue la principal sustancia de reserva detectada en los tejidos foliares (Fig. 2E). Las hojas de H. macrophylla son hipostomáticas y con patrón estomático paracítico, con estomas superficiales que permiten el paso a la cavidad subestomática (Fig. 2F).
Observaciones anatómicas de las hojas infectadas: sobre la pared periclinal externa de las células epidérmicas se observan estructuras fúngicas características del micopatógeno, tales como micelio y conidias (Fig. 2G). Las paredes de las células epidérmicas se aprecian con engrosamientos cuticulares, de color rojo, por la reacción a la Safranina y el citoplasma se aprecia granular (Fig. 2G). En etapas tempranas de la infección, los tejidos subepidérmicos no se ven afectados y estos se aprecian funcionales, en buen estado y con abundantes cloroplastos. En la cara interna de las paredes periclinales externas de algunas células epidérmicas tanto del lado adaxial como del abaxial, se aprecia la formación de engrosamientos en forma papilas (Fig. 2G). Posteriormente, con el avance de la infección, se observa necrosis tanto de las células epidérmicas como de los tejidos fotosintéticos yuxtapuestos (Fig. 2H). Estos tejidos se aprecian desorganizados, colapsados y con inclusiones citoplasmáticas que reaccionan con la safranina, sugiriendo la presencia de polifenoles y no se aprecian cloroplastos.
Aspectos histoquímicos de hojas sanas e infectadas: Al analizar algunas características histoquímicas en las hojas sanas, se aprecia que las células epidérmicas tienen paredes primarias delgadas que dan positivo al rojo de Rutenio, indicando la presencia de pectinas (Fig. 3A). En contraste y en respuesta a esta misma tinción, en las paredes periclinales de las células epidérmicas de las hojas infectadas, se observan engrosamientos conspicuos que indican la presencia y mayor acumulación de pectinas (Fig. 3B). Las papilas también reaccionaron de manera positiva con esta tinción. Se observó reacción cruzada del rojo de Rutenio con los cloroplastos de los tejidos tanto de hojas sanas como infectadas (Fig. 3A, Fig. 4B). Las células epidérmicas de las hojas sanas no presentan ninguna reacción con el Lacmoid (Fig. 3C); contrario a la reacción en color azul conspicua que se aprecia en algunas zonas de las células epidérmicas de las hojas infectadas, indicando la presencia de calosa (Fig. 3D). Esta reacción, también es evidente en las estructuras papilares que se aprecian en estas mismas células en la cara interna de las paredes periclinales externas (Fig. 3E). Las células epidérmicas de las hojas sanas no reaccionan con la tinción de Punceau S, excepto los cloroplastos (Fig. 3F), en tanto que las células epidérmicas infectadas reaccionan formando aglomerados de color rojo intenso que indica la presencia de calosa. Así mismo, se aprecia reacción cruzada de esta tinción con los cloroplastos de las hojas analizadas (Fig. 3G). Las células epidérmicas tanto de los tejidos sanos como infectados no reaccionan con el Floroglucinol ácido, en tanto que el xilema de los haces vasculares se tiñe de color fucsia, indicando la presencia de lignina (Fig. 3H).
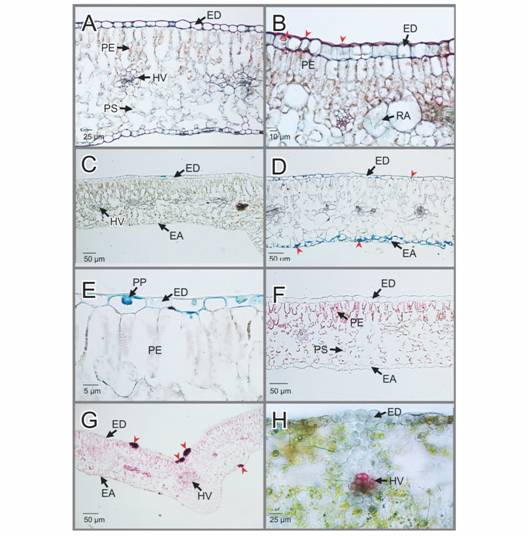
Fig. 3 EA: epidermis abaxial; ED: epidermis adaxial; HV: haces vasculares; PE: parénquima de empalizada; PP: papilas; PS: parénquima esponjoso; RA: rafidios. Hydrangea macrophylla. Pruebas histoquímicas aplicadas a las secciones de hojas sanas e infectadas por la Oidiosis o ceniza. A-B. Secciones transversales de hojas sanas e infectadas teñidas con rojo de Rutenio, respectivamente. En B Se aprecian engrosamientos de pectinas en las células epidérmicas y papilas presentes en las hojas infectadas (cabezas de flecha roja). C-D. Secciones transversales de hojas sanas e infectadas teñidas con Lacmoid, respectivamente. Se indica la calosa (cabezas de flecha roja). E. Detalle de la epidermis adaxial teñida con Lacmoid mostrando las papilas. F-G. Secciones transversales de hojas sanas e infectadas teñidas con Pounceau S, respectivamente. Se indica la calosa (cabezas de flecha roja). H. Sección trasversal de hoja infectada teñida con Floroglucinol ácido. El color fucsia en el haz vascular indica la presencia de lignina. Fig. 3 EA: abaxial epidermis; ED: adaxial epidermis; HV: vascular bundles; PE: palisade parenchyma; PP: papillae; PS: spongy parenchyma; RA: raphides. Hydrangea macrophylla.Histochemical tests applied to sections of healthy leaves and leaves infected by powdery mildew. A-B. Transverse sections of healthy leaves and infected leaves respectively, stained with Ruthenium Red. In B epidermal cells and papillae of infected leaves (red arrowheads) thickened by pectins. C-D. Transverse sections of healthy and infected leaves respectively, stained with Lacmoid. Callose is indicated (red arrowheads). E. Detail of the adaxial epidermis stained with Lacmoid, showing the papillae. F-G. Transverse sections of, respectively, healthy and infected leaves, stained with Ponceau S. Callose is indicated (red arrowheads). H. Transverse section of infected leaf stained with Phloroglucinol acid. The fuchsia color in the vascular bundle indicates the presence of lignin.
Los tejidos de las hojas sanas reaccionan de manera negativa con las tinciones de Cloruro férrico y negro de Sudan, respectivamente (Fig. 4A, Fig. 4C). Por el contrario, en las hojas infectadas con la Oidiosis, se aprecian agregados citoplasmáticos de color negro en las células epidérmicas y tejidos fotosintéticos con esta última tinción, sugiriendo la presencia de materiales lipídicos (Fig. 4B). Solo en las células epidérmicas de las hojas infectadas, se observaron agregados citoplasmaticos de color negro al aplicar Cloruro férrico (Fig. 4D). La Tinción con Uvitex 2B-Hematoxilina muestra reacción cruzada con las paredes celulares de los tejidos foliares sanos de H. macrophylla en color azul oscuro (Fig. 4E), pero presenta reacción especifica de color azul claro brillante con el material fúngico quitinoso (Fig. 4F). Las pruebas histoquímicas efectuadas y los compuestos determinados se resumen en la Tabla 1.
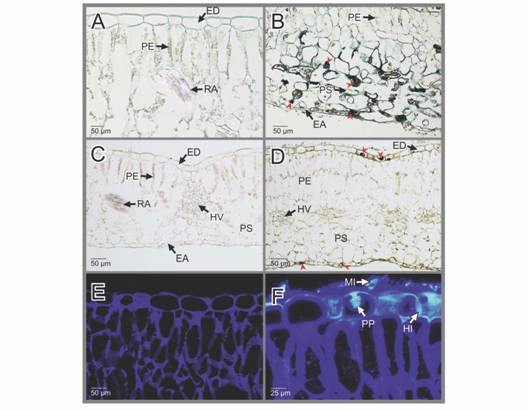
Fig. 4 EA: epidermis abaxial; ED: epidermis adaxial; HV: haces vasculares; MI: micelio; PE: parénquima de empalizada; PP: papilas; PS: parénquima esponjoso; RA: rafidios. Hydrangea macrophylla. Pruebas histoquímicas aplicadas a las secciones de hojas sanas e infectadas por la Oidiosis o ceniza. A-B. Secciones transversales de hojas sanas e infectadas respectivamente teñidas con negro de Sudan. En B, Los agregados de color negro indicarían la presencia de lípidos (cabezas de flecha roja). C-D. Secciones transversales de hojas sanas e infectadas respectivamente, teñidas con Cloruro férrico. En D, los agregados negros, indicarían la presencia de presencia de polifenoles (cabezas de flecha roja). E-F. Secciones transversales de hojas sanas e infectadas teñidas respectivamente con Uvitex 2B-Hematoxilina (microscopía de fluorescencia). Fig. 4 EA: abaxial epidermis; ED: adaxial epidermis; HV: vascular bundles; MI: mycelium; PE: palisade parenchyma; PP: papillae; PS: spongy parenchyma; RA: raphides. Hydrangea macrophylla. Histochemical tests applied to sections of healthy leaves and leaves infected by powdery mildew. A-B. Transverse sections of healthy and infected leaves respectively, stained with Sudan Black. In B, black aggregates would indicate the presence of lipids (red arrowheads). C-D. Transverse sections of healthy and infected leaves respectively, stained with ferric chloride. In D, the black aggregates would indicate the presence of polyphenols (red arrowheads). E-F. Transverse sections of healthy and infected leaves respectively, stained with Uvitex 2B- Hematoxylin (fluorescence microscopy).
TABLA 1 Pruebas histoquímicas aplicadas a hojas sanas e infectadas de Hydrangea macrophylla con Oidiosis TABLE 1 Histochemical tests applied to healthy and infected leaves of Hydrangea macrophylla with powdery milde
| Compuesto | Reactivo | Reacción de color | Sitio en el que se probó el compuesto | ||
| Muestras sanas | Muestras infectadas | ||||
| Calosa | Ponceau | Rojo | Cloroplastos (+) | Papilas (+), cloroplastos (+), paredes anticlinales y periclinales de células epidérmicas (+) | |
| Calosa | Lacmoid | Azul claro | Todos los tejidos (-) | Papilas (+), paredes anticlinales y periclinales de células epidérmicas (+) | |
| Lípidos | Negro de Sudan | Café a negro | Reacción con cloroplastos (+) | Células epidérmicas y parenquimatosas (+) | |
| Pectinas | Rojo de Rutenio | Rojo | Reacción leve con células de paredes primarias y cloroplastos (+) | Papilas (+), paredes anticlinales y periclinales de células epidérmicas (+) y cloroplastos (+) | |
| Polifenoles | Cloruro férrico | Café a negro | Todos los tejidos (-) | Células epidérmicas (+) | |
| Polisacáridos de reserva, almidón | PAS | Fucsia | Células parenquimatosas (+), los demás tejidos (-) | Células parenquimatosas (+), los demás tejidos (-) | |
| Quitina | Uvitex- Hematoxilina* (filtro UV) | Azul claro brillante | Paredes celulares vegetales (-) reacción cruzada de las paredes primarias en azul oscuro. | Paredes fúngicas y papilas (+) | |
| Lignina | Floroglucinol ácido, | Rojo | Paredes de células epidérmicas (-) En el xilema (+) | Paredes de células epidérmicas (-) En el xilema (+) | |
+ = presencia; - = ausencia; * reduce la autofluorescencia de los tejidos vegetales.
Discusion
En plantas de H. macrophylla se ha reportado que la Oidiosis es ocasionada principalmente por micopatógenos pertenecientes a los géneros Erysiphe, Golovinomyces, Pseudoidium (Li et al., 2009a, Li et al., 2009b; Braun & Cook, 2012) y en algunos casos por el género Oidium (Park et al., 2012). Las observaciones morfológicas registras en esta investigación en relación con las conidias, tubos de germinación, conidiforos, apresorios y en comparación con la literatura científica analizada, permite indicar que el agente fúngico implicado en la Oidiosis en las muestras analizadas de H. macrophylla, se relaciona con el género Erysiphe (Li et al., 2009a, Li et al., 2009b; Schmidt & Scholler, 2011; Ale-Agha et al., 2013). No obstante, en esta investigación no se encontraron estructuras de reproducción sexual, que son importantes para la determinación taxonómica de las especies dentro del género (Braun & Cook, 2012). Por lo cual, se recomienda realizar análisis filogenéticos moleculares y morfológicos que incluyan aspectos de la reproducción sexual, que permitan determinar en un esquema natural, la circunscripción exacta de la especie causante de la Oidiosis en las plantaciones de H. macropylla del nororiente antioqueño. El gran número de apresorios observados en el pato-sistema H. macropylla-Oidiosis que afectan a las células epidérmicas, estaría relacionado con las repuestas del patógeno ante los mecanismos de resistencia presentes en la planta, tales como el depósito de calosa, engrosamientos de pectina y acumulación de polifenoles; tal y como lo han indicado otros autores para Erysiphales (Li et al., 2009a, Li et al., 2009b).
Así mismos, la estrecha relación entre los apresorios y el deterioro de la cutícula observados en este pato-sistema, es congruente con los mecanismos de presión y degradación enzimática ejercidos por el apresorio, y que han sido ampliamente documentados para diferentes interacciones entre planta-micopatógeno (Dean, 1997; Zabka et al., 2008; Ryder & Talbot, 2015). Las características anatómicas de hojas de H. macrophylla observadas en esta investigación son congruentes con la estructura de hojas de simetría dorsivental y homobaricas, tal como lo indica Crang, Lyons-Sobaski y Wise (2018). Así mismo, Stern (1978) hace una descripción anatómica detallada de las hojas de H. macrophylla donde indica la posición de los estomas, tipo de patrón estomático, estructura, morfología de los tejidos del mesófilo, epidermis foliar, haces vasculares e indica la presencia de rafidios de oxalato de calcio en idioblastos. Todos estos hallazgos son coincidentes con observaciones anatómicas realizadas acá para H. macrophylla. Adicionalmente, Stern (1978) describe la presencia de tricomas e hidátodos que no se apreciaron en esta investigación.
Los engrosamientos cuticulares detectados por la tinción de Safranina-azul de Alcian en las células epidérmicas de las hojas infectadas sugieren una respuesta de reforzamiento de la pared celular con este biopolímero; lo cual ha sido indicado como uno de los mecanismos de respuesta de las plantas ante la penetración de micopatógenos (Marqués, Amorim, Spósito, & Appezzato-da-Glória, 2016; Ziv, Zhao, Gao, & Xia, 2018). La presencia de agregados granulares citoplasmáticos de color fucsia, con esta misma tinción, se relaciona con la acumulación de polifenoles; también documentados como mecanismos de defensa de las plantas (Lattanzio, Lattanzio, & Cardinali, 2006; Aoun, Rioux, Simard, & Bernier, 2009; Aoun, 2017). La detección indirecta de polifenoles por la tinción con Safranina, ha sido documentada anteriormente (Ruzin, 1999) y lo cual se contrastó en esta investigación con la tinción específica para polifenoles con Cloruro férrico. Ordeñana (2002), Lattanzio et al. (2006), Aoun et al. (2009) y Aoun (2017) han indicado, que los polifenoles pueden reforzar las paredes celulares primarias ante la presión y degradación enzimática efectuada por el micopatógeno, impidiendo la penetración de los haustorios a las células y también pueden interferir con la germinación de las esporas.
Se ha señalado, que los compuestos polifenólicos reaccionan con los grupos sulfhidrilos de algunos aminoácidos, lo que conlleva a la inhibición de procesos enzimáticos efectuados por el patógeno (Agrios, 2005; Montes-Belmont, 2009). La acumulación de compuestos polifenolicos en el citoplasma de las células infectadas podrían estar relacionados con la precipitación y coagulación del citoplasma debido a la necrosis generada por la respuesta o reacción de hipersensibilidad (RH) que han sido extensamente documentadas en plantas (Mur, Kenton, Lloyd, Ougham, & Prats, 2007; Balint-Kurti, 2019).
La RH es considerada como uno de los principales mecanismos de resistencia de las plantas al ataque por micopatógenos y se define como una muerte rápida de las células invadidas, lo cual contribuye a restringir la reproducción y desarrollo de las estructuras del patógeno (Schmelzer, 2002; Li et al., 2009a, b; Sanzón & Zavaleta, 2011; Balint-Kurti, 2019). La RH ocurre únicamente en combinaciones incompatibles entre plantas hospedantes y patógenos (Agrios, 2005; Balint-Kurti, 2019). La RH origina alteraciones anatómicas que incluyen la contracción, fragmentación y condensación del protoplasto (Sanzón & Zavaleta, 2011). Estas alteraciones de las células epidérmicas fueron verificadas en esta investigación para el pato-sistema H. macropylla-Oidium. Por el contrario, es probable que la necrosis observada en los tejidos parenquimatosos, presentes en el mesófilo de H. macrophylla a medida que avanza la infección, está relacionada con el deterioro y muerte de las células epidérmicas, que dejan desprotegidos y expuesto a los tejidos subyacentes, dado que el biotrofo solo afecta a las células epidérmicas.
En las paredes periclinales externas de las células epidérmicas de las hojas infectadas H. macrophylla, se observó el depósito de papilas o aposiciones de pared celular que son coincidentes morfológica y estructuralmente a lo registrado en otros pato-sistemas (Ordeñana, 2002; Agrios, 2005; An, Hückelhoven, Kogel, & Van Bel, 2006; Underwood, 2007; Chowdhury et al., 2014; Houston, Tucker, Chowdhury, Shirley, & Little, 2016; Kuhn et al, 2016). Li et al. (2009a), Li et al., (2009b) observaron que estas papilas están reforzadas con calosa en el pato-sistema H. macrophylla-Erysiphe polygoni, lo cual es similar a lo observado en esta investigación y que se corroboró con las tinciones específicas para este polisacárido. La formación de calosa está relacionada con mecanismo de respuesta temprana ante la penetración de fitopatógenos (Voigt, 2014; Houston et al., 2016; Kuhn et al, 2016).
En el caso específico de los hongos, estas papilas, encapsulan los haustorios bloqueando físicamente la penetración en las células epidérmicas (Camarena & de la Torre, 2007; Voigt, 2014; Chowdhury et al., 2014; Kuhn et al, 2016). Así mismo, se ha comprobado que inhiben la difusión de sustancias tóxicas secretadas en el momento de la infección (Underwood, 2007; Voigt, 2014; Kuhn et al., 2016), lo cual suprimen la nutrición del patógeno y repara el daño celular (Agrios, 2005). Adicionalmente, se ha establecido la acumulación de varios metabolitos secundarios como polifenoles, lignina y especies reactivas de oxígeno (ROS) en las papilas presentes en varios pato-sistemas (Bhuiyan, Selvaraj, Wei, & King, 2009; Clay, Adio, Denoux, Jander, & Ausubel 2009; Voigt, 2014; Malinovsky, Fangel, & Willats, 2014; Aoun, 2017; Bacete, Mélida, Miedes, & Molina, 2018). En esta investigación no se detectó la acumulación de lignina en las papilas o en las paredes de las células epidérmicas como mecanismos de respuesta de la planta al patógeno, indicado por estos mismos autores. Tampoco se evidencio la presencia de polifenoles relacionados a las papilas, es de aclarar que no se efectuaron pruebas para ROS, pero la necrosis observada también podría estar asociada a estos compuestos.
Chowdhury et al. (2014) determinó la presencia de pectinas asociadas a las papilas, además de la calosa, en hojas de cebada, afectadas por Blumeriagraminis f. sp. Hordei, resaltando su papel en el reforzamiento de la pared celular. Estas observaciones son similares a lo registrado en esta investigación para H. macrophylla. La presencia de engrosamientos de pectina en las paredes primarias de las células epidérmicas infectadas con Oidiosis en H. macrophylla aportarían reforzamiento a las paredes celulares para prevenir la entrada del patógeno. Esta situación ha sido documentada por Vogel, Raab, Somerville y Somerville (2004) y Engelsdorf et al. (2017) en sus investigaciones con mutantes de Arabidopsis Heynh. in Holl & Heynh en relación a la resistencia contra algunas especies de Erysiphe y Colletotrichum higginsianum Sacc. respectivamente.
Varios autores han documentado la activación de rutas metabólicas relacionadas con la síntesis de moléculas de naturaleza lipídica en células vegetales afectadas por patógenos, principalmente para hongos y virus e indican la importancia de estos en las rutas metabólicas asociadas a mecanismos de defensa de las plantas en especial con la biosíntesis de oxilipinas, jamonatos, glicerolípidos y ácidos grasos (Reina & Yephremov, 2009; Marqués, Kitajima, Freitas-Astúa, & Appezzato-da-Glória, 2010; Canonne, Froidure-Nicolas, & Rivas, 2011; Walley, Kliebenstein, Bostock, & Dehesh 2013; Zhang & Xiao, 2015; Laureano et al., 2018). La acumulación de lípidos en las células epidérmicas del pato-sistema H. macrophylla-Oidiosis es coincidente con estas observaciones. Dado que el patógeno causante de la Oidiosis analizado en esta investigación es un biotrofo obligado de las células epidérmicas, estos mecanismos de defensa no explicarían los agregados lipídicos observados en las células parenquimatosas del mesófilo, que probablemente estarían relacionados con el deterioro y desorganización de los sistemas de membrana de estas células.
A pesar de que el fluorocromo Uvitex 2B presentó reacción cruzada con los componentes de la pared primaria de las células epidérmicas y del mesófilo de H. macrophylla, correspondiente a la longitud de onda de emisión del azul oscuro-violeta; la emisión de la interacción con la quitina se dio en una longitud del azul claro brillante, permitiendo diferenciar sin dificultad las células del patógeno de los tejidos de la planta. Lo anterior indica que este fluorocromo es ideal para el análisis de las interacciones histológicas en este tipo de pato-sistemas, tal y como se ha indicado para la interacción entre plantas y royas (Sørensen et al., 2012; Dugyala et al., 2015)
Finalmente, la conclusión amplia de este trabajo permite establecer que las células epidérmicas de las hojas de H. macrophylla, despliegan una serie de mecanismos de defensa ante el ataque del agente causante de la Oidiosis. Estos mecanismos, incluyen el reforzamiento de las paredes celulares con la acumulación de pectinas, cutina y calosa. Además, la secreción de metabolitos secundarios, principalmente polifenoles. Es probable que la muerte de las células epidérmicas tenga relación con la RH que han sido documentada previamente para H. macrophylla por el ataque de micopatógenos del género Erysiphe. Todos estos mecanismos estas destinados a contrarrestan la penetración, propagación e inhiben el desarrollo del patógeno.
Declaración de ética: los autores declaran que todos están de acuerdo con esta publicación y que han hecho aportes que justifican su autoría; que no hay conflicto de interés de ningún tipo; y que han cumplido con todos los requisitos y procedimientos éticos y legales pertinentes. Todas las fuentes de financiamiento se detallan plena y claramente en la sección de agradecimientos. El respectivo documento legal firmado se encuentra en los archivos de la revista.












 uBio
uBio 

