Introducción
En el mes de septiembre del año 2015, se realizó el Primer Consenso Centroamericano y el Caribe de Sociedades de Cardiología para el Diagnóstico y Manejo de la Falla Cardíaca. En esa oportunidad, todas las Asociaciones de la región enviaron delegados que participaron en la redacción de este primer documento científico. Dentro de los acuerdos principales se puede mencionar:
Metodología
Como parte del seguimiento de este documento, en el mes de diciembre del año 2017, la Sociedad Panameña de Cardiología, por medio de su presidente Dr. Alfaro Marchena Noriega convocó al II Consenso Centroamericano y El Caribe de Insuficiencia Cardíaca, realizado el 7 y 8 de diciembre de 2017 en la ciudad de Panamá.
El grupo de expertos representa a las asociaciones médicas de Cardiología de Guatemala, El Salvador, Honduras, Nicaragua, Costa Rica, Panamá y República Dominicana. Para esta nueva reunión, los participantes acordaron algunos puntos generales:
Utilizar la definición de insuficiencia cardíaca (IC) en sustitución de Falla Cardíaca, debido a que es de uso más frecuente en la mayoría de los países de la región.
Influir la insuficiencia cardíaca con fracción de eyección media (ICFEm).
Utilizar como referencia para la certificación de clínicas de insuficiencia cardíaca (CIC) y adaptar a la realidad de la región, los estándares de calidad de las unidades de insuficiencia cardíacas propuestos en el Consenso científico de la Sociedad Española de Cardiología del año 2016.
Para esta reunión se acordó hacer una revisión y actualización sobre 3 puntos principales:
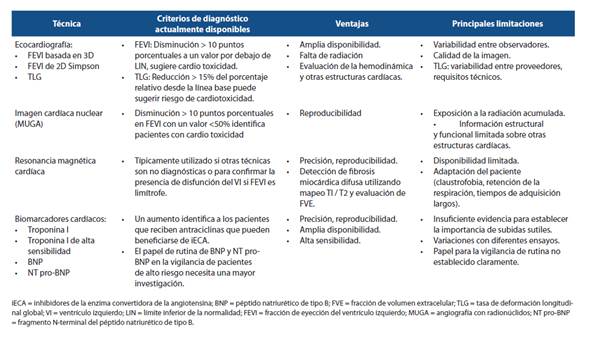
Biomarcadores en insuficiencia cardíaca.
Manejo de co-morbilidades más frecuentes.
Certificación de CIC.
Se seleccionó la información de más alto nivel de evidencia y recomendación, siguiendo la clasificación recomendada por el Colegio Americano de Cardiología y la Asociación Americana del Corazón, actualizada al mes de agosto 2015.
La búsqueda realizada en fuentes de información científica utilizó las palabras clave insuficiencia cardíaca, co-morbilidades, clínicas de insuficiencia cardíaca, certificación, consensos.
Un especial agradecimiento al Dr. Daniel Quesada, quien fungió como coordinador de las revisiones de los documentos finales.
Manejo de co-morbilidades
Introducción
El equipo de trabajo recomienda que todo aquel médico que maneje IC, debe identificar y estratificar las co-morbilidades que tiene su paciente, siguiendo las guías propias de cada patología (Nivel Evidencia Ic); sin embargo, siendo la IC una condición sistémica, muchos de sus aspectos pueden afectar las co-morbilidades del paciente y viceversa, por lo que se hace una revisión de la evidencia actual de las diferentes entidades científicas (por ejemplo: American Hearth, Sociedad Canadiense de Cardiología, etc.)CAL
Siempre se debe considerar que “las condiciones comórbidas se convierten en factores de riesgo para el deterioro futuro y pueden contribuir al deterioro clínico, complicar el tratamiento y a menudo, se asocian con un mal pronóstico”1.
Es importante considerar que los registros a nivel centro americano han identificado como principales co-morbilidades las siguientes2:
Clasificación de co-morbilidades
Cardiovasculares
Cardiopatía Isquémica
La angina/isquemia residual es un factor de descompensación muy frecuente, por lo que se recomienda de forma sistemática en todo paciente manejado con IC, realizar un estudio de imágenes no invasivo para determinar la ausencia o presencia de enfermedad arterial coronaria. En caso de presencia de enfermedad arterial coronaria se recomienda revascularización, según la disponibilidad de recursos locales. En pacientes con fracción de eyección menor de 35% in dependientemente de los síntomas, se recomienda realizar la angiografía coronaria.
Se recomienda que la angiografía coronaria sea3:
Realizada en pacientes con IC con síntomas isquémicos y que probablemente sean buenos candidatos para revascularización (Nivel Ib).
Considerada en pacientes con IC sistólica, Fracción de Eyección del Ventrículo Izquierdo (FEVI) < 35%, con riesgo de enfermedad de las arterias coronarias independientemente de angina, que podrían ser buenos candidatos para la revascularización (Nivel Ic).
Considerada en pacientes con IC sistólica y en quienes la prueba de perfusión coronaria no invasiva produce características compatibles con alto riesgo (Nivel Ib).
Para el tratamiento farmacológico óptimo y más seguro se sugiere adoptar las recomendaciones que se muestra en la tabla 1.
Hipertensión Arterial
La hipertensión arterial (HTA) se asocia con un riesgo aumentado de desarrollar IC y antecede el desarrollo de IC en un 90% de casos, en un seguimiento a 20 años.
La posibilidad de desarrollar la IC en el hipertenso vs. el normotenso es del doble en hombres y el triple en mujeres 5.
Las metas de control de presión arterial (PA) tanto en IC con fracción de eyección reducida como preservada se enfocan en una PA menor de 130/80 mmHg.
Tabla 1 Recomendaciones para el tratamiento de la angina de pecho estable con IC sintomática (NYHA II-IV) y fracción de eyección reducida 4
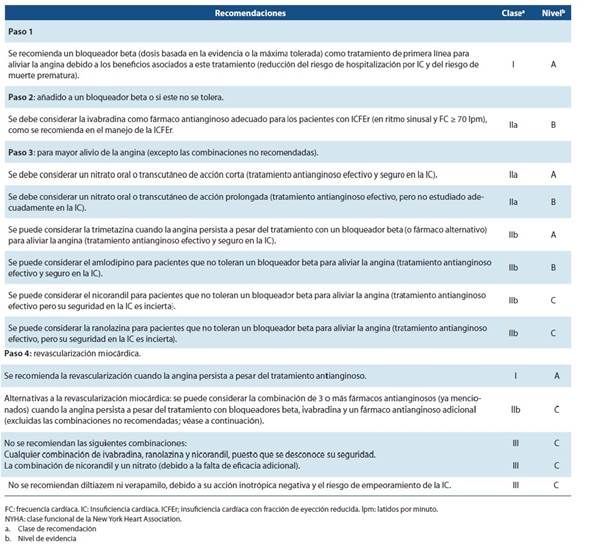
Insuficiencia cardíaca con fracción de eyección reducida (ICFEr)
Si la presión sanguínea no se controla con los iECA (ARA II-ARNI), bloqueadores beta, antagonistas de los mineralo corticoides, diuréticos; considerar agregar hidralazina y/o amlodipina como fármacos que han demostrado ser seguros en pacientes con ICFEr.
A continuación, se presentan las recomendaciones para el tratamiento de la hipertensión en pacientes con insuficiencia cardíaca sintomática (NYHA II-IV) y fracción de eyección reducida.
Tabla 3 Recomendaciones para el tratamiento de la hipertensión en pacientes con IC sintomática (NYHA II-IV) y FEr 4

Insuficiencia cardíaca con fracción de eyección preservada (ICFEp)
En este consenso se incorpora el concepto de hipertensión decapitada que describe a aquellos pacientes hipertensos que por su cardiopatía avanzada suelen ir normalizando e incluso hipotensándose a medida que la patología avanza. Son pacientes de muy difícil manejo por su incapacidad de tolerar medicamentos para IC6.
Fibrilación Auricular
La presencia de fibrilación auricular (FA) se asocia con un peor pronóstico en términos de sobrevida total, así como también en un mayor riesgo de Accidente Cerebrovascular (ACV). La FA mayor de 150 latidos/minuto es una de las causas principales de descompensación del paciente cardíaco, por lo que debe clasificarse y tratarse según las guías de la Sociedad Europea de Cardiología1.
La estrategia general para el tratamiento de la FA no varía entre los pacientes con IC, pero es conveniente tener en cuenta algunas consideraciones. El único tratamiento con valor pronóstico probado es la anticoagulación 1.
La frecuencia ventricular óptima en reposo en paciente con FA e IC no está claramente establecida, pero podría estar entre 70 y 100 lpm 4.
Los bloqueadores beta son la primera opción de tratamiento para estos pacientes pese a que no se ha encontrado una reducción en la mortalidad en los pacientes con FA de base, siendo la segunda opción la amiodarona y/o la digoxina con un efecto neutro en la mortalidad1.
En pacientes seleccionados en conjunto con el Electrofisiólogo se puede considerar la Terapia de Ablación de la FA.
Valvulopatías
Los pacientes con IC y valvulopatía concomitante constituyen un grupo de alto riesgo. Se recomienda que un equipo cardiológico multidisciplinario con experiencia en valvulo patías debe encargarse del proceso de toma de decisiones mediante una evaluación minuciosa de los riesgos y beneficios para que todos los pacientes reciban el tratamiento médico óptimo.
Para los pacientes con ICFEr, el tratamiento farmacológico debe planificarse de acuerdo con el tratamiento estándar. Es preciso tomar precauciones especiales si se administra va sodilatadores (IECA, ARA-II, BCC, hidralazina y nitratos) a los pacientes con estenosis aórtica grave, para evitar la hipotensión 4. (Nivel Ia)
El origen reumático (fiebre reumática) en nuestra región, sigue siendo una de las causas principales de deterioro valvular por lo que se recomienda el seguimiento sistemático y a largo plazo de todo paciente con evidencia de fiebre reumática con carditis7. (Nivel Ia)
No Cardiovasculares
Relacionadas con volumen
Anemia y/o deficiencia de hierro
Investigaciones recientes han contribuido a la separación definitiva entre el concepto de anemia y el de deficiencia de hierro (DH) en la IC. La DH va más allá de una mera co-morbilidad, consolidándose su rol en la fisiopatología, pronóstico y tratamiento de la IC. El estudio de la DH en la IC debería basarse en la ferritina y el Índice de saturación de la transferrina (IST). Definimos la DH como una ferritina <100g/l, o entre 100 y 300g/l junto con un IST <20%8.
La DH puede detectarse antes de que aparezca la anemia, lo que brinda una oportunidad más temprana para mejorar los resultados 3.
La anemia ha sido recientemente reconocida como un posible objetivo terapéutico en pacientes con IC. La anemia es común en pacientes con insuficiencia cardíaca congestiva, con un rango de prevalencia que varía del 4% al 55%9.
En los pacientes con deficiencia de hierro e ICFEr, el hierro oral a dosis altas aumentó mínimamente las reservas de hierro y no mejoró la capacidad de ejercicio durante 16 se manas. Estos hallazgos no apoyan el uso de suplementos orales de hierro para tratar la deficiencia de hierro en pacientes con ICFEr10.
En pacientes con IC con anemia y DH en los que se contempla la repleción de hierro, se debe considerar la administración de suplementos de hierro IV para mejorar la capacidad funcional, ya que el hierro oral no tiene eficacia conocida en este contexto; y por lo tanto el hierro IV debe administrarse, teniendo en cuenta los resultados recientemente presenta dos del estudio de efectos de la repleciónde hierro sobre la absorción de oxígeno en la IC (IRONOUT HF)3. (Nivel Ia)
Tabla 5 Dosificación de carboximaltosa de hierro para pacientes con deficiencia de hierro asociada a IC Insuficiencia Cardíaca con deficiencia de hierro2. Determinación de la dosis total de hierro requerida: (si el paciente tiene ferritina <100 ng/mL o si ferritina 100-300 ng/mL y TSAT < 20%)
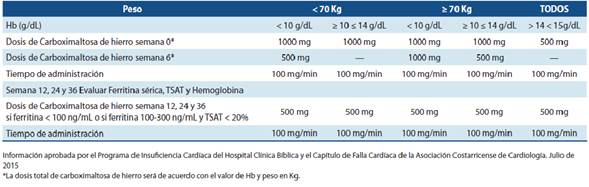
En diferentes estudios realizados los pacientes que recibieron hierro IV experimentaron mejoras limitadas, pero estadísticamente significativas en la capacidad funcional y la FEVI, pero no redujeron la tasa de mortalidad con evidencia favorable para el uso del hierro carboximaltosa 11.’
Carboximaltosa de hierro debe administrarse únicamente por vía intravenosa y no debe administrarse por vía subcutánea o intramuscular.
Una dosis única de carboximaltosa de hierro no debe superar los 1000 mg de hierro (20 ml) al día. Máximo de 20 mg de hierro/Kg de peso corporal.
No administrar más de 1000 mg de hierro (20ml) por semana.
Para corregir depósito de ferritina: dosis única de 500 mg de carboximaltosa de hierro.
La anemia (definida como una concentración de hemoglobina < 13,0 g/dl en los varones y < 12,0 g/dl en las mujeres) es común en la IC, especialmente en pacientes hospitalizados.
Ante cualquier hallazgo de anemia, está indicado seguir un proceso diagnóstico para encontrar la causa (p. ej., pérdida oculta de sangre, déficit de hierro, déficit de B12/folato, discrasias sanguíneas), aunque en muchos pacientes no se encuentra ninguna causa específica. Los agentes estimuladores de la eritropoyetina no mejoraron los resultados clínicos en pacientes con ICFEr y anemia leve o moderada y se asoció a un exceso de complicaciones tromboembólicas, por lo que no están recomendados 4.
Disfunción renal
La disfunción cardíaca y renal a menudo ocurre junto con consecuencias hemodinámicas, neuro hormonales, vasculares y hematológicas.
Anteriormente, se pensaba que la disfunción renal repre sentaba simplemente una co-morbilidad en pacientes con IC avanzada.
Cada vez se reconoce más que la interacción cardíaca y renal es compleja. El síndrome cardiorrenal (SCR) se refiere a interacciones en las que la disfunción renal y la IC interactúan y se refuerzan mutuamente.
En los pacientes con insuficiencia cardíaca e insuficiencia renal crónica estable, leve a moderada, con Tasa de Filtración Glomerular (TFG) > 30, se recomienda que reciban una terapia estándar con un iECA o ARA II y un Antagonistas del Receptor Mineralocorticoide (ARM)3. (Nivel Ia)
Se ha excluido sistemáticamente a los pacientes con insuficiencia renal grave, con tasa estimada de filtración glomerular (TeFG) < 30 ml/min/1,73 m2, de los estudios aleatorizados, por lo cual no existen tratamientos basados en la evidencia para estos pacientes4.
Como regla general, el nivel de creatinina sérica puede aumentar o el nivel de TeFG puede disminuir hasta en un 30% desde el inicio, antes de que sea necesario detener o reducir la dosis de iECA, ARA II o ARM.
Recomendamos que se evite la digoxina en pacientes con lesión renal aguda y en pacientes con insuficiencia renal crónica grave (TFG <30). En la insuficiencia renal estable de leve a moderada, la digoxina debe usarse con prudencia, a dosis bajas. A medida que disminuye la función renal, se debe volver a evaluar el uso de digoxina para evitar el desarrollo de toxicidad por digoxina.
Se recomienda que en todos los casos se descarten las posibles causas reversibles de disminución de la función renal y debe considerarse la derivación a un nefrólogo 3. (Nivel Ia)
El grupo del Consenso recomienda realizar control de la boratorio, cada dos a cuatro semanas.(Nivel Ic)
Metabólicos
Diabetes
La diabetes es muy común entre los pacientes con Insuficiencia Cardíaca Crónica (ICC) y se asocia con un peor resultado cardiovascular en estos pacientes 9.
En pacientes con diabetes mellitus e IC, se debe implementar el control glucémico gradual y moderadamente, dando preferencia a los fármacos como la metformina, que han demostrado ser seguros y efectivos.
Recientemente, la empagliflozina, un inhibidor del co-transportador de sodio y glucosa 2, mostró una reducción de las hospitalizaciones por IC y la mortalidad, pero no del infarto de miocardio e ictus, en pacientes con diabetes mellitus y riesgo cardiovascular alto, de los que algunos tenían IC. Debido a la falta de otros estudios con fármacos de este grupo, no se puede considerar los resultados obtenidos con empagliflozina como prueba de un efecto de clase.
Los inhibidores de la dipeptidil peptidasa 4 (DPP4; gliptinas) y los agonistas del receptor del péptido de tipo glucagón 1 (GLP-1) de acción lenta mejoran los índices glicémicos. Su impacto en IC es variable y deben considerarse las diferencias entre drogas.
Las tiazolidinedionas (glitazonas) causan retención de sodio y agua, aumentan el riesgo de empeoramiento de la IC y hospitalización, por lo cual no se recomiendan para pacientes con IC 4.
La metformina puede ser considerada como agente de primera línea para el tratamiento de la diabetes tipo 2 (Nivel IIb-b). Es efectiva, tiene un perfil de seguridad conocido y es bien tolerado en pacientes con IC3.
Obesidad
Los pacientes que presentaban IC y obesidad (31 ± 4 kg/ m2), lo que, junto a la posible coexistencia de alteraciones respiratorias, puede justificar sus síntomas. Los pacientes con ICFEp presentaron Índice de Masa Corporal (IMC) más elevados, próximos a la obesidad (29,8 ± 5,1 kg) frente a los ICFEr. Se ha descrito la relación entre obesidad y alteraciones cardíacas como hipertrofia VI, dilatación de cavidades, disfunción diastólica y semiología de IC. La obesidad y su tratamiento pueden reducir los valores de péptidos natriuréticos (PN) o considerar que no existen consideraciones especiales fuera del manejo tradicional de la obesidad en los pacientes con enfermedad cardiovascular 2.
Dislipidemia
No hay pruebas para recomendar la instauración de tra tamiento con estatinas para la mayoría de los pacientes por su IC. Sin embargo, para los pacientes que ya están en tratamiento con una estatina para la enfermedad arterial coronaria (EAC), se puede considerar continuarlo (Nivel Ia) 4.
Hiperuricemia/gota
Los pacientes con IC son propensos a la hiperuricemia como resultado del tratamiento con diuréticos de ASA y la disfunción renal. En la IC, la hiperuricemia se asocia a un mal pronóstico.
En los ataques agudos de gota, se considera la administración de un ciclo corto de colchicina para aliviar el dolor y la inflamación.
Siempre que sea posible se debe evitar el uso de anti inflamatorios no esteroideos (AINES) y esteroides sistémicos en pacientes sintomáticos. Se recomienda el tratamiento profiláctico con un inhibidor de la xantina oxidasa (alopurinol) para prevenir recurrencias, a pesar de que su seguridad en IC con fracción de eyección reducida es incierta (Nivel Ia)2.
Pulmonares
Enfermedad pulmonar, incluidos asma y enfermedad pulmonar obstructiva crónica(EPOC)2
No existen datos de nuestra área, pero en un estudio de registro de pacientes con IC y co-morbilidades, reportó que un 17% de los pacientes censados tenían Asma y EPOC.
La EPOC es una co-morbilidad frecuente en la IC y su prevalencia alcanza un 20-30%. Las anomalías pulmonares restrictivas y obstructivas son comunes.
Los pacientes con EPOC tienen un riesgo muy elevado de IC y la EPOC es un poderoso factor de riesgo independiente para la morbilidad y la mortalidad cardiovascular. La EPOC empeora el pronóstico de los pacientes con IC.
En la práctica clínica, la evaluación diagnóstica de la IC en presencia de EPOC es un desafío. Hay una importante su perposición de los signos y síntomas, con una sensibilidad relativamente baja de las pruebas diagnósticas como radiografía de tórax, electrocardiograma (ECG), ecocardiografía y espirometría.
En estos pacientes, la determinación del PN tipo B (BNP) y el pro-BNP aminoterminal (NT pro-BNP) puede ser útil, aun que los resultados se suelen situar en valores intermedios. El valor predictivo negativo puede ser de más utilidad.
La mayoría de los pacientes con IC y EPOC pueden tolerar sin riesgos el tratamiento con bloqueadores beta. Se recomienda la instauración del tratamiento a dosis bajas y aumentarlas gradualmente. El deterioro leve de la función pulmonar y de los síntomas no requiere la interrupción inmediata del tratamiento.
En caso de empeoramiento de los síntomas, podría ser necesario reducir la dosis o interrumpir el tratamiento. Se administrarán nebulizaciones con agonistas beta como se requiere en pacientes con EPOC.
La concomitancia de EPOC e IC puede reducir drásticamente la tolerancia al ejercicio. Puede ser aconsejable la realización de programas de rehabilitación supervisados para mejorar la función del músculo esquelético y la fatiga (Nivel IIc-c).
Los bloqueadores beta tienen una contraindicación relativa en el asma, pero no en la EPOC, aunque se prefiere el uso de un antagonista selectivo del receptor adrenérgico beta-1 (bisoprolol, succinato de metoprolol o nebivolol).
La hipertensión pulmonar puede complicar la EPOC grave de larga duración y aumentar la probabilidad de IC derecha y congestión4.
Apnea del sueño
Los tipos más comunes son: la apnea del sueño central (ASC), similar a la respiración de Cheyne Stokes, la apnea obstructiva del sueño (AOS) y un patrón mixto de ambas 4.
Los trastornos del sueño son comunes en pacientes con insuficiencia cardíaca. Un estudio de adultos con IC crónica tratados con terapias basadas en evidencia, encontró que el 61% tenía ya sea apnea del sueño central u obstructiva. Es clínicamente importante distinguir la apnea obstructiva del sueño de la apnea central del sueño, dadas las diferentes respuestas al tratamiento. La servo-ventilación adaptativa para la apnea central del sueño está asociada con daño. La presión positiva continua en la vía aérea (PPCVA) para la apnea obstructiva del sueño mejora la calidad del sueño, reduce el índice de apnea-hipopnea y mejora la oxigenación nocturna11.
Se recomienda, que los médicos que tratan a pacientes con insuficiencia cardíaca fomenten una mayor participación en los programas de médicos del sueño experimentados y la boratorios de sueño con capacidad demostrada, para discriminar entre AOS y ASC utilizando estándares de diagnóstico contemporáneos (Nivel IIb-b)3.
Otras
Cáncer
Algunos agentes quimioterápicos pueden causar disfunción sistólica del ventrículo Izquierdo (VI) e IC o empeorarla. Los tratamientos de este tipo más reconocidos son las antraciclinas (como doxorubicina), el trastuzumab y los inhibidores de la tirosincinasa 4.
La insuficiencia cardíaca como resultado de la terapia del cáncer se ha relacionado con un riesgo de mortalidad 3,5 veces mayor en comparación con la miocardiopatía idiopática 12.
La FEVI debe determinarse antes y de forma periódica, durante el tratamiento para la detección temprana de la disfunción cardíaca en pacientes que reciben quimioterapia potencialmente cardiotóxica, con un método que proporcione una suficiente calidad de imagen y preferiblemente, utilizan do el mismo método durante el seguimiento.
Este grupo recomienda considerar el límite inferior de la FEVI normal en ecocardiografía como 50%, de acuerdo con la definición de cardiotoxicidad comúnmente utilizado en registros y ensayos en pacientes con cáncer.
Un paciente con una disminución significativa de la FEVI (por ejemplo, una disminución de 10%), a un valor que no cae por debajo del límite inferior del normal, debería someterse a una evaluación repetida de la FEVI inmediatamente después y durante el tratamiento del cáncer.
Si la FEVI disminuye un 10% a un valor inferior al límite inferior del normal (considerado como una FEVI, 50%), los inhibidores ECA (o ARA II) en combinación con bloqueadores beta se recomiendan para prevenir más allá la disfunción del VI o el desarrollo de IC sintomática, a menos que esté contraindicado, ya que estos pacientes tienen un alto riesgo de desarrollar insuficiencia cardíaca Los inhibidores de la ECA (o ARA II) y los bloqueadores beta se recomiendan en pacientes con insuficiencia cardíaca sintomática o disfunción cardíaca asintomática a menos que esté contraindicado (Nivel Ia)13.
Chagas
La enfermedad de Chagas es la mayor causa de discapacidad secundaria a enfermedades tropicales en adultos jóvenes de Latinoamérica (LA) y es una causa común de IC en muchos países de la región. Esta enfermedad es causada por el Trypanosoma cruzi, endémico en América Central y del Sur, donde se estima que 18 millones de personas están infectadas y 100-120 millones están en riesgo de contraerla.
La cardiomiopatía crónica es la manifestación más importante y grave de la enfermedad, que afecta a aproximadamente un 20-30 % de los sujetos en la fase crónica y causa IC, arritmias, bloqueos cardíacos, tromboembolia y muerte súbita. Se estima que cada año ocurren 21 000 muertes relacionadas con Chagas solo en la región del cono sur de LA.
La historia natural de la enfermedad de Chagas, debida a la presencia del Trypanosoma cruzi en los corazones de los pacientes afectados, se caracteriza por una fase aguda, seguida de un período indeterminado o de transición y una etapa terminal arrítmico-congestiva. Es una enfermedad de evolución tes afectados puede llegar a tener síntomas y signos de ICc.
La supervivencia de los pacientes chagásicos es apenas del 25% a los 60 meses de haber aparecido los síntomas de IC. Por el contrario, la supervivencia de pacientes no chagásicos, en el mismo lapso de seguimiento, es cercana al 50%. Estas marcadas diferencias serían debidas a que la enfermedad de Chagas, como causa subyacente de IC, implica un mayor riesgo de muerte. Sin embargo, estos mismos estudios destacan que el tratamiento de los pacientes chagásicos no es homogéneo.
En efecto, por ser una enfermedad de origen infeccioso y por tener aparentemente alteraciones primarias de los mecanismos de control de la PA y de los líquidos corporales, estos pacientes no recibían, hasta ahora, tratamiento para contrarrestar la activación neuro hormonal.
Investigaciones más recientes, con énfasis en el diagnóstico y tratamiento moderno del síndrome de IC, demuestran:
El factor predictivo de muerte más importante en pacientes con IC de etiología chagásica, es la no administración de bloqueadores beta adrenérgicos 2.
La mortalidad del paciente chagásico, que recibe estos fármacos es semejante a la del síndrome de IC de pacientes con otras enfermedades cardíacas 2.
NT pro-BNP y los niveles de la troponina T cardíaca de alta sensibilidad (Hs-cTnT) tienen el mismo valor diagnóstico para distinguir la gravedad de la miocardiopatía de chagas (MCC)14.
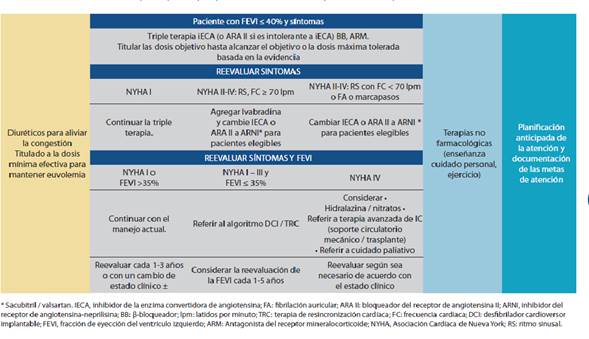
Algoritmo de manejo farmacológico de ic
De los algoritmos de manejo farmacológico surgidos a partir del año 2016, consideramos que el canadiense responde mejor a las características de nuestra región, ya que es una zona con poco personal especializado en donde se aprove charía una terapia triple desde el inicio en los pacientes de origen isquémico (etiología más frecuente documentada en los registros locales), esto permite un beneficio más rápido y una titulación más efectiva.
Conflicto de intereses
Dr. Mario Speranza Sánchez es consultor de Novartis, Servier, Medtronic y Vifor Pharma. Es investigador para Novartis y Presentador de Novartis, Servier, Vifor Pharma y Roche.
Dra. Gabriela Castillo Chaves, es consultora de Novartis y Pfizer y presentadora de Novartis.
Dr. Daniel Quesada Chaves es Consultor de Novartis y Pfizer y Presentador para Novartis y Servier.
Dr. Julio A Effio es Consultor de Grupo Médico Panamá y presentador de Pfizer y Sanofi.
Dr. Gabriel Frago es investigador para Novartis.
Dr. Fredis Molina es Presentador para Merck, Serono y Novartis.
Dr. Emilio Peralta López es presentador para Abbott, Menarini y Servier.
Dr. Carlos Ramos Midence es presentador para Novartis.
Dr. Jaime Ventura Umanzor ha sido presentador para Novartis, Merck, Serono y Boehringer.