Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.13 n.2 San José Dec. 2011
Trabajo Original
El Aislamiento de las Venas Pulmonares como Tratamiento de la Fibrilación Auricular Refractaria
Fernando Scazzuso, Santiago Rivera, Luis A. Gómez, Victoria Sammartino, Albina Gastón, Rubén Laiño, Alberto Giniger
*Dirección para correspondencia
Resumen
Introducción. La fibrilación auricular (FA) es la arritmia sostenida más común. En pacientes seleccionados, se realiza ablación por catéter a nivel de las venas pulmonares, en donde se genera actividad ectópica que la produce. Se presenta la experiencia en el tratamiento de
Materiales y métodos. La población estuvo constituida por 152 pacientes (122 hombres), edad promedio de 55.58 años. El 81.9% de la población no presentaba cardiopatía estructural. La forma de presentación fue paroxística en el 65.95% de los casos, con una historia de arritmia de 7 años en promedio, habiendo cumplido tratamiento con 3 fármacos antiarrítmicos diferentes. Se realizó mapeo no fluoroscópico y ablación de la porción antral de cada vena pulmonar, en forma secuencial.
Resultados. La tasa de éxito durante el procedimiento fue del 97.87%. Se presentaron 12 complicaciones, 4 de ellas derrame pericárdico; ninguno requirió cirugía correctiva. El seguimiento promedio fue de 18±6 meses. En 24 pacientes se presentó recurrencia de
Conclusión. El aislamiento de las venas pulmonares es una modalidad de tratamiento con una aceptable tasa de éxito primario en casos seleccionados.
Palabras clave: Fibrilación auricular, ablación, venas pulmonares, arritmias.
Abstract
Introduction. Atrial fibrillation (AF) is the most common sustained cardiac arrhythmia. In selected patients, catheter ablation was performed at the sites of the pulmonary veins where ectopic activity triggers AF. Our experience with AF treatment by pulmonary vein isolation in 152 consecutive cases is presented and discussed.
Methods. Our population consisted mainly of men (122 of 152 patients), with an average age of 55.6 years. Paroxysmal AF was present in 65.9% of the cases and 81.9% of the population had a structurally normal heart. AF had been present for an average of 7 years. All of the patients fulfilled a treatment period protocol in which three different antiarrhythmic drugs were used first. Nonfluoroscopic mapping and antral pulmonary vein isolation were performed sequentially
Results. The procedural success rate was 97.9%. There were 12 complications, including 4 pericardial effusions but none required surgical repair. The mean follow-up period was 18±6 months. AF recurred in 24 patients after the third month of follow-up. There was an 84.04% success rate at 12 months: 88.3% for the group with a normal heart and 64.1% for the group with a cardiomyopathy.
Conclusion. Isolation of the pulmonary veins can be achieved in appropriately selected cases with AF and has an acceptable rate of success.
Key-words: atrial fibrillation, ablation, pulmonary vein, arrhythmias.
Introducción
La fibrilación auricular (FA) es la arritmia sostenida más común1.
En algunos casos, causa un deterioro considerable en la calidad de vida, conlleva un alto porcentaje de comorbilidad y es de difícil tratamiento2-4. En pacientes seleccionados, se realiza ablación por catéter, con el fin de crear una barrera anatómica que impida que la actividad ectópica que se genera en las venas pulmonares produzca FA5. En el presente trabajo se presenta la experiencia inicial en el tratamiento de
Métodos
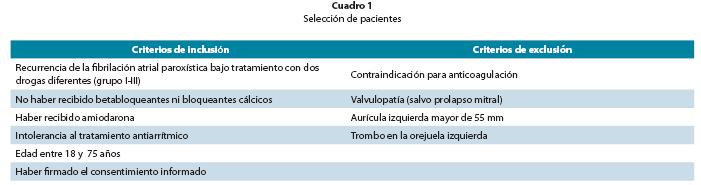
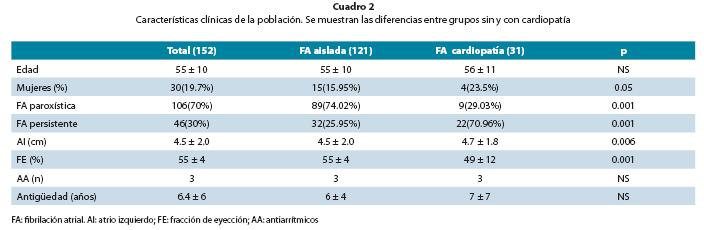
Pacientes. Cada uno de los pacientes referido por su médico de cabecera fue valorado en nuestra clínica antes de su inclusión en el estudio, para determinar si cumplían con los criterios de inclusión o presentaban criterios de exclusión, mostrados en el cuadro 1. La población estudiada (152 pacientes, cuadro 2) estuvo constituida mayoritariamente por hombres (n=122), con una edad promedio de 55.58±10.53 años. El 71.9% de la población no presentaba antecedentes de enfermedad cardiovascular y el 28.1% presentaba historia de hipertensión arterial, diabetes, dislipidemia o cardiopatía isquémica. De estos, solo el 4.25% presentaba disfunción ventricular izquierda severa y el 10.63% presentaba una valvulopatía (distinta de prolapso de la válvula mitral) o antecedente de cirugía de revascularización miocárdica. Dependiendo de la existencia o no de cardiopatía, se dividió a la población en dos grupos: un grupo con FA aislada sin cardiopatía estructural y un grupo con FA y cardiopatía subyacente. A su vez, de acuerdo a la forma de presentación, se clasificó la arritmia en paroxística (episodios autolimitados de arritmia) y persistente (pacientes con episodios sostenidos a los que se les debía practicar alguna forma de cardioversión para que retornen a ritmo sinusal). Si los pacientes presentaban episodios de ambas características se los clasificaba acorde al tipo de episodio más frecuente.
La forma de presentación era paroxística en el 65.3% de los casos, con una historia de arritmia de 7 años en promedio, habiendo cumplido tratamiento con tres fármacos antiarrítmicos diferentes; no se incluían betabloqueantes ni bloqueantes cálcicos, ya que su efecto antiarrítmico es muy limitado y solo se utilizan para el control de la frecuencia ventricular durante los episodios recurrentes de FA; es decir, se utilizó un criterio de recurrencia arrítmica bien específico.
Cabe destacar que el 84,5% de la población estaba en tratamiento con amiodarona. El número de episodios de FA fue en promedio, 6 por año. Destaca la mayor presencia de FA paroxística en el grupo sin cardiopatía, en comparación al grupo con cardiopatía, en el que la forma de presentación más frecuente fue la persistente; este grupo también presentó mayor porcentaje de sexo femenino, mayor tamaño de la aurícula izquierda y menor fracción de eyección.
En la evaluación preoperatoria, se realizaron 3 estimaciones de
En todos los casos se realizó una ecocardiografía transesofágica al momento de la admisión, para verificar la ausencia de trombos y 48 horas previas al procedimiento, una tomografía computada de alta resolución (“multi-slice-
Procedimiento. Los procedimientos fueron realizados bajo anestesia general, con monitoreo permanente mediante una línea arterial invasiva. Luego de antisepsia cutánea, mediante técnica de Seldinger modificada, se realizaron las punciones de ambas venas femorales. Se posicionό un catéter decapolar en el seno coronario y un catéter cuadripolar en la región tricuspídea para el registro del electrograma del haz de His. Asimismo, se realizaron dos punciones transeptales bajo control radioscópico, en proyección oblicua anterior izquierda; mediante control continuo de la presión intracavitaria a través de la aguja de Brokenbrough, se posicionaron dos introductores largos preformados SL1 y SL2 (St. Jude Medical). A través de ellos se avanzó respectivamente un catéter Lasso® (Biosense Webster) para la adquisición de múltiples puntos de manera simultánea y un catéter irrigado de ablación Thermo-cool® (Biosense Webster) para determinar el ostium y la porción antral de las venas pulmonares y para la aplicación de la radiofrecuencia. En todos los casos se utilizó un sistema de mapeo no fluoroscópico EnSite® (St. Jude Medical) modelo NaVx, versión 7.0 para la reconstrucción anatómica y realización de la cartografía.
Con un catéter circular duo-decapolar Optima (St. Jude Medical) se obtuvo el registro de la actividad eléctrica de cada vena pulmonar.
Si se identificaban potenciales en más de una de ellas, el tratamiento se comenzó por la vena pulmonar superior izquierda, luego la inferior izquierda y finalmente se realizaba la misma secuencia del lado derecho. Se aplicó energía por radiofrecuencia con una potencia de 35-40 W en el aspecto anterior y 30 W en la vertiente posterior de cada vena. Las lesiones se aplicaron en el aspecto antral y no ostial de las venas. En cada caso se analizó la morfología del electrograma registrado por el catéter de ablación antes y durante la lesión (electrograma de alta frecuencia y fraccionado). Se utilizó como criterio de lesión exitosa la disminución en la amplitud del electrograma en al menos 75% o su desaparición. Se monitorizó de manera continua la impedancia durante la lesión, para asegurar la posición del catéter en su aspecto antral y evitar lesiones dentro de la vena pulmonar.
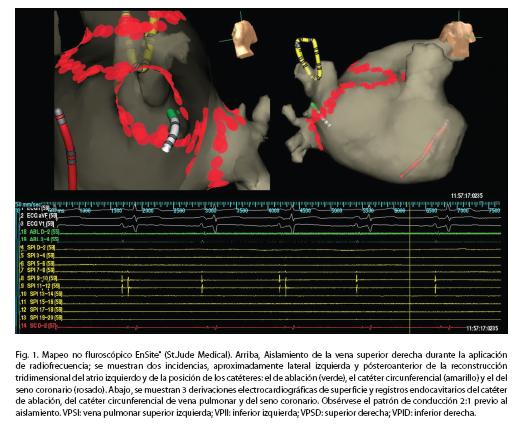
Se verificó la secuencia de activación en el ostium de la vena pulmonar para determinar su patrón de activación antes de iniciar el aislamiento (Fig. 1). Si durante la aplicación de la radiofrecuencia el patrón de conducción se modificaba, se comenzaba una nueva aplicación en la región de mayor precocidad registrada en el catéter Lasso. Una vez finalizado el proceso de aislamiento de las venas, se controló por 30 minutos la persistencia del bloqueo en cada vena y si era necesario, se completó el aislamiento con lesiones de consolidación hasta alcanzar una línea de bloqueo en su vertiente antral, discriminando la activación eléctrica local o lejana. Al finalizar cada procedimiento se realizó una evaluación neurológica en el laboratorio de electrofisiología, luego del despertar de la anestesia y a las 24 Hs. El mismo día del procedimiento se reinició el tratamiento con warfarina hasta alcanzar una RIN entre 2 y 3. El paciente era dado de alta al día siguiente, luego de realizarse un ecocardiograma para verificar la ausencia de derrame pericárdico y se continuó con el mismo tratamiento antiarrítmico durante tres meses, si no mediaba ninguna contraindicación.
Seguimiento. Consistió en una entrevista a los 3, 6, 9, 12 meses con registro Holter de 24 hs. A partir del tercer mes, se suspendiό el tratamiento anticoagulante y antiarrítmico. Si el paciente refería palpitaciones durante el seguimiento, concurría a la sala de urgencias; si se confirmaba una recurrencia después del tercer mes, se realizó un segundo procedimiento para todos los casos, sea para el tratamiento de
Resultados
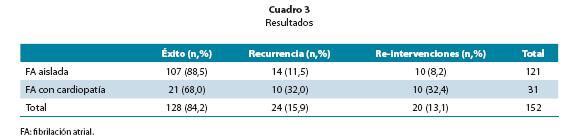
En cuadro 3 se observan los resultados obtenidos en los 152 pacientes, con un seguimiento de 18±6 meses. Se obtuvo el aislamiento de las venas pulmonares en el 97.87% de los casos, encontrándose la mayor dificultad técnica en el aislamiento de la vena pulmonar inferior derecha. El tiempo medio para el aislamiento de cada vena fue 20 minutos en promedio. El tiempo total de fluoroscopía fue 23±10 minutos y la duración total promedio del procedimiento de 3.2±0.5 horas. Las complicaciones se muestran en el cuadro 4. De los 4 casos con taponamiento cardiaco, ninguno requirió tratamiento quirúrgico y todos fueron tratados con drenaje pericárdico y control de la hemostasia (reversión intraoperatoria con protamina), lo que permitió continuar el procedimiento sin dificultad; en todos se determinó que las perforaciones fueron consecuencia de la punción transeptal y ocurrieron en pacientes con un tamaño de aurícula izquierda más pequeña. Los 2 casos de isquemia cerebral aguda transitoria fueron evaluados y tratados por el servicio de neurología y en ninguno se observó secuelas. No se registraron complicaciones mayores como muerte, fístula atrio-esofágica o estenosis de la vena pulmonar; esta última se evaluó clínicamente.
El 15.95% (n=24) de los pacientes presentaron recurrencia de
A un año de seguimiento, la tasa de éxito primario fue del 84.04% (88.32% para el grupo sin cardiopatía y del 64.8% para el grupo con cardiopatía).
Discusión
La ablación de
Otra diferencia significativa de nuestro procedimiento con la técnica del aislamiento circunferencial de las venas pulmonares (desarrollada por el Dr. Pappone en Milán) es que se evita la superposición de líneas, causa principal de dicha complicación, como fuera reportado por estos autores19.
Recientemente la comunidad europea modificó sus guías de tratamiento de
Conclusión
En nuestra experiencia, el aislamiento de las venas pulmonares es una modalidad de tratamiento para
Rerefencias
1. Camm AJ, Obel OA. Epidemiology and mechanism of atrial fibrillation and atrial flutter. Am J Cardiol 1996; 78: 3-11
2.- Benjamin EJ, Wolf PA, D’Agostino RB et al. Impact of atrial fibrillation on the risk of death: the Framingham Heart Study. Circulation 1998; 98: 946-52. [ Links ]
3. Connolly SJ. Preventing stroke in atrial fibrillation: why are so many eligible patients not receiving anticoagulant therapy? Canadian Medical Association Journal 1999; 161: 533-4. [ Links ]
4. Wolf PA, Mitchell JB, Baker CS, et al. Impact of atrial fibrillation on morality, stroke, and medical costs. Arch Intern Med 1998; 158: 229-34. [ Links ]
5. Oral H, Knight BP, Tada H et al. Pulmonary vein isolation for paroxysmal and persistent atrial fibrillation. Circulation 2002; 105: 1077-81. [ Links ]
6. Natale A, Raviele A, Arentz T, et al.
7. Haїsaguerre M, Jais P,
8. Haїsaguerre M, Jais P, Shah DC et al. Electrophysiological end point for catheter ablation of atrial fibrillation initiated from multiple pulmonary venous foci. Circulation 2000; 101: 1409-17. [ Links ]
9. Haїsaguerre M, Jais P, Shah DC et al. Electrophysiological breakthroughs from the left atrium to the pulmonary veins. Circulation 2000; 102: 2463-5. [ Links ]
10. Gerstenfeld EP, Guerra P, Sparks PB, et al. Clinical outcome after radiofrecuency catheter ablation of focal atrial fibrillation triggers. J Cardiovascular Electrophysiology 2001; 12: 900-8. [ Links ]
11. Saliba W, Martin DO, Schweiker R et al. Early atrial fibrillation recurrence post pulmonary vein isolation: Should we intervene? Circulation 2002;106: 541. [ Links ]
12. - Haїsaguerre M, Jais P, Dipen C et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. N Engl J med 1998; 339: 659-666. [ Links ]
13. Matiello M, Lennon VA, Jacob A et al. Cooled-tip vs. 8 mm-tip catheter for circumferential pulmonary vein ablation: comparison of efficacy, safety, and lesion extension. Europace 2008; 10: 955-960. [ Links ]
14. Kalman JM, Fitzpatrick AP, Olgin JE et al. Biophysical characteristics of radiofrecuency lesion formation in vivo: dynamics of catheter tip-tissue contact evaluated by intracardiac echocardiography. Am Heart J 1997; 133: 8-18. [ Links ]
15. Natale A, Pisano E, Shewchik J et al. First human experience with pulmonary vein isolation using a through the ballon circumferential ultrasound ablation system for recurrent atrial fibrillation. Circulation 2000; 102: 1879-82. [ Links ]
16. Pappone C, Oreto G, Santinelli V et al. Catheter ablation of paroxysmal atrial fibrillation using a 3D mapping system. Circulation 1999; 100: 1203-1208. [ Links ]
17. Piorkowski C, Kircher S, Arya A et al. Computed tomography model-based treatment of atrial fibrillation and atrial macro-re-entrant tachycardia Europace, 2008;10: 939-948. [ Links ]
18. Cappato R, Calkins H, Shih-Ann Chen, et al. Worldwide Survey on the Methods, efficacy, and Safety on Catheter Ablation for Human Atrial Fibrillation. Circulation: Arrhythmia and Electrophysiology. 2010; 3: 32-38. [ Links ]
19. Pappone C, Oral K, Santinelli V, et al. Atrio-esophageal fistula as complication of percutaneous transcatheter ablation of atrial fibrillation. Circulation 2004;109: 2724-2726. [ Links ]
20. Camm AJ, Kirchhof P, Lip GYH et al. Guidelines for the management of atrial fibrillation of the European society of cardiology. The Task force for the Management of Atrial Fibrillation of the European Society of Cardiology. Eur Heart J 2010; 31(19): 2369-2429. [ Links ]
21. Piccini J, Hasselblad V, Peterson E et al. Comparative Efficacy of Dronedarone and Amiodarone for the Maintenance of Sinus Rhythm in Patients With Atrial Fibrillation. J Am Coll Cardiol 2009;54: 1089-1095. [ Links ]
*Correspondencia a: Servicio de Cardiología, Instituto Cardiovascular de Buenos Aires (ICBA).