Acerca de este trabajo
Este trabajo presenta información general acerca del fenómeno de corrosión a modo de introducción.
El fenómeno de corrosión
La Corrosión es un término que se utiliza para describir el proceso de deterioro de materiales metálicos (incluyendo tanto metales puros, como aleaciones de estos), mediante reacciones químicas y electroquímicas (Revie y Uhlig, 2008). Para el caso del deterioro relacionado con otros tipos de materiales, como los polímeros y cerámicos, se utiliza el término degradación.
Estos materiales metálicos son obtenidos a través del procesamiento de minerales y menas, que constituyen su estado natural, induciéndolos a un estado de mayor energía. El fenómeno de la corrosión ocurre debido a que, con el tiempo, dichos materiales tratan de alcanzar su estado natural, el cual constituye un estado energético de menor potencial, lo que les permite estabilizarse termodinámicamente (Javaherdashti, 2008).
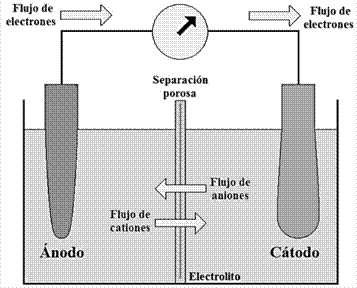
La mayoría de procesos de corrosión involucran reacciones de reducción-oxidación (reacciones electroquímicas), donde para que se desarrollen estos procesos, es necesaria la existencia de tres constituyentes: (1) unos electrodos (un ánodo y un cátodo), (2) un electrolito, como medio conductor, que en la mayoría de casos corresponde de una solución acuosa, y (3) una conexión eléctrica entre los electrodos (ECCA, 2011). La Figura 1 muestra de forma representativa un esquema de estos elementos, formando lo que se conoce como una celda electroquímica. Las ecuaciones de las reacciones que ocurren en los electrodos son las siguientes:
En el ánodo:
M0 → Mn + ne¯ (Oxidación)
En el cátodo:
Mn + ne¯ → M0 (Reducción)
Ambas reacciones ocurren de forma simultánea (ECCA, 2011). Como se observa en las ecuaciones, el ánodo cede electrones al sistema cuando reacciona, aumentando su número de oxidación, cambiando de su estado metálico base a cationes que se disuelven en el electrolito, siendo este el material que se sufre el fenómeno de corrosión; mientras que, en el cátodo, los aniones metálicos absorben electrones, disminuyendo su número de oxidación, por lo que cambian a su estado base.
El potencial electroquímico define la susceptibilidad o la resistencia de un material metálico a la corrosión, cuyo valor varia en dependencia de la composición del electrolito. Cuanto más positivo sea el valor de dicho potencial, más noble (resistente) es el material. Mientras que en el caso contrario, cuanto más negativo sea este, más reactivo es el material a la corrosión. La serie galvánica consiste es una tabla donde se ubican diferentes tipos de materiales respecto al potencial electroquímico de estos. La Figura 2 muestra representativamente una tabla de serie galvánica para algunos metales y aleaciones comunes.
Los productos que se forman a partir del proceso de corrosión, sobre la superficie del material, pueden afectar de manera negativa o positiva, las propiedades del material, dependiendo de su naturaleza y las condiciones que lo rodean. Para el caso del hierro (y otros metales), el producto que se forma se conoce como herrumbre, y tiene una menor densidad que el metal base, lo que provoca que este se desprenda de la superficie, facilitando que la corrosión continúe ocurriendo, consumiendo el material. Por otro lado, para otros tipos de metales, como el aluminio, el níquel o el cromo, los productos de la corrosión tienen una mayor densidad que el material base, formando un capa sólida y estable sobre la superficie de este, evitando que la corrosión se extienda, protegiendo al material. Este proceso se conoce como pasivación, fenómeno que brinda la denominación de inoxidable a un material como, por ejemplo, los aceros inoxidables (Revie, 2011; Schweitzer, 2010).
A continuación, se presentarán algunos tipos de corrosión, siendo los que se pueden observar con mayor frecuencia. También se mencionarán los factores que mayor efecto tienen sobre la incidencia y la velocidad de este fenómeno. Y, finalmente, se presentarán algunos aspectos a tomar en cuenta respecto al control de la corrosión y la protección de materiales.
Tipos de corrosión
Existen muchos tipos de procesos de corrosión diferentes que se caracterizan dependiendo tanto de la naturaleza del material y de las condiciones del medioambiente, donde se desarrollen. Una forma común de clasificar los tipos de corrosión, es mediante las siguientes cuatro categorías: corrosión generalizada, corrosión localizada, corrosión combinada con un fenómeno físico, y otros tipos.
Corrosión generalizada (uniforme)
La corrosión generalizada, también nombrada como corrosión uniforme, ocurre sobre toda la superficie del material de forma homogénea, deteriorándolo completamente. Este tipo de corrosión es el que mayor pérdida de material provoca, pero es relativamente fácil de predecir y controlar, por lo que un accidente producido por este es de rara ocurrencia (Revie, 2011). Se puede observar comúnmente en materiales, sobre todo en la industria de la construcción, a base de hierro no aleado con metales inoxidables, como el níquel y el cromo.
La velocidad de corrosión para estos casos, es altamente influenciada por la existencia de impurezas y fases distintas en el material, ya que estas inducen a una variación en la energía potencial, formando electrodos a pequeña escala, propiciando el proceso de corrosión.
Corrosión localizada
La corrosión localizada, al contrario de la corrosión uniforme, representa un mayor riesgo potencial, debido a su difícil detectabilidad ya que se manifiesta en zonas específicas en el material, determinadas tanto por la naturaleza del material, la geometría de este, y las condiciones del medio al que se somete. Los procesos de corrosión localizada de mayor ocurrencia son galvánica, por fisura, por picaduras, por cavitación y microbiológica.
Corrosión galvánica
La corrosión galvánica ocurre cuando existe una unión, física o eléctrica, entre metales de diferente naturaleza, lo cuales, en la presencia de un electrolito, forman una celda electroquímica, donde el material de menor potencial electroquímico es el que se corroe (Revie, 2011). La Figura 3 muestra un ejemplo de este tipo de corrosión.
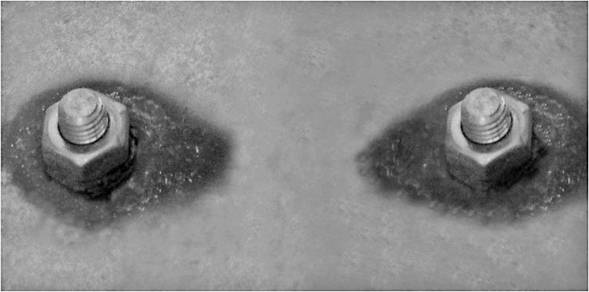
Figura 3: Corrosión galvánica sobre una placa de acero (ánodo) en contacto con unos tornillos y tuercas de acero inoxidables. Tomada de http://commons.wikimedia.org/wiki/File:Galvanic_corrosion-1b.jpg
Un factor de importante consideración es la relación de área de la zona de contacto entre los material. Entre mayor sea la relación del ánodo respecto al cátodo, el proceso de corrosión ocurre con mayor velocidad (Javaherdashti, 2008).
Corrosión por fisuras
Este tipo de corrosión es similar a la corrosión galvánica, que se produce en zonas estrechas donde la concentración de oxígeno es mucho menor que en el resto del sistema, y cuyo efecto induce a que estas zonas de menor concentración de oxígeno actúen como un ánodo, propiciando el proceso de corrosión, en las fisuras.
Corrosión por picaduras (pitting)
La corrosión por picadura, conocida también como pitting se presenta en materiales pasivados, debido a las características geométricas del sistema, existe una acumulación de agentes oxidantes y un incremento del pH del medio, lo que propicia el deterioro de la capa pasivada, permitiendo que la corrosión se desarrolle en éstas zonas puntuales.
Corrosión por cavitación
La corrosión por cavitación ocurre en sistemas de transporte de líquidos, hechos de materiales pasivados, donde por cambios de presión en el sistema, se producen flujos turbulentos que forman burbujas de aire, las cuales implosionan contra el material del sistema, deteriorando la capa de pasivación, facilitando el desarrollo del proceso de corrosión, de forma similar a la corrosión por picaduras, cuya diferencia se observa, en que el efecto de la cavitación es de mayor tamaño (Revie, 2011).
Corrosión microbiológica
La corrosión microbiológica, en realidad no es un tipo de corrosión en sí, sino que más bien es un fenómeno que facilita el desarrollo de otros procesos de corrosión. Las bacterias son los microorganismos más influyentes en este caso, por lo que también es conocida como corrosión bacteriana y se produce en sistemas de transporte de líquido, facilitando la corrosión por picaduras.
La naturaleza del líquido que se transporta en estos sistemas, propicia la acumulación y reproducción de bacterias, las cuales se aglomeran, y propician las condiciones, como variación en la concentración de sales y oxígeno, para que se desarrollen otros proceso de corrosión como el pitting.
Corrosión combinada con un fenómeno físico
Este tipo de corrosión también se puede incluir dentro de la clasificación de corrosión localizada, pero la diferencia con estos es que se encuentran condicionados por la presencia de un fenómeno físico, que funciona como iniciador del proceso de corrosión.
Corrosión - erosión
Este tipo de corrosión se observa en sistema de transportes de fluidos hechos con materiales pasivados, donde existen partículas de mayor dureza que la capa de pasivación. Estas partículas al estar en movimiento, erosionan la capa pasivada, permitiendo que el proceso de corrosión se desarrolle (Javaherdashti, 2008).
Corrosión - tensión
Ocurre cuando en un material, sometido a esfuerzo de tensión, ya sea de forma interna o externa, se forman pequeñas fisuras, que dan inicio al proceso de corrosión (Revie, 2011). El material que permanece en ambos fenómenos, se deteriora con mayor rapidez, que si estuviese bajo el efecto individual de cada uno, ya que la corrosión debilita el material, lo cual permite que la tensión tenga mayor impacto, fracturando en mayor medida el material, lo cual a su vez incita a que la corrosión se propague en un área mayor, y así, sucesivamente.
Corrosión - fatiga
Este proceso se desarrolla en materiales, sujetos a esfuerzos externos, similar al de tensión, con la diferencia de que estos esfuerzos son cíclicos o fluctuantes. De igual forma que con el proceso de tensión, el material se deteriora en mayor medida mediante la combinación de los dos fenómenos, comparado a cada uno por separado (Revie, 2011).
Otros tipos de corrosión
También existen muchos tipos de corrosión que no caen dentro de las categorías anteriores. Algunos de estos son, la desaleación, la corrosión filiforme y la oxidación.
Desaleación
La desaleación es un proceso de corrosión que actúa sobre aleaciones metálicas, en donde uno de los elementos, de mayor afinidad con el oxígeno, se separa de la aleación y dejan una estructura porosa de pobres propiedades conformada por el resto de constituyentes. El proceso se nombra alternativamente respecto al elemento que se separa de la aleación como, por ejemplo, la descincificación para el latón, aleación que sufre comúnmente de este tipo de corrosión, en la cual se separa el zinc de la matriz cobre (Revie, 2011).
Filiforme
La corrosión filiforme se presenta en ambientes de alta humedad sobre materiales con recubrimientos orgánicos (pinturas), los cuales al ser rayados, se induce el desarrollo de la corrosión, que se propaga como filamentos delgados (Revie y Uhlig, 2008).
Oxidación
La oxidación es un tipo de corrosión que se desarrolla en procesos de alta temperatura, en la presencia de algún gas oxidante, como el oxígeno, azufre y elementos halógenos. Las reacciones relacionadas son meramente química al no existir un electrolito de por medio, por lo que también se conoce como corrosión seca. Las moléculas del gas oxidante reaccionan con el material involucrado, donde, por efecto de la temperatura, el compuesto formado se difunde al interior del material, permitiendo que el proceso continúe, fragilizando el material.
Factores que influyen el proceso de corrosión
Existen muchos factores que influyen el proceso de corrosión, donde se debe de tomar en cuenta tanto las características del material sobre el que incide y el medio que rodea a este. A continuación, se mencionan algunos factores, considerados como los de mayor efecto sobre el proceso corrosivo.
Acidez de la solución
El pH de una solución es una propiedad que define la cantidad de iones de hidrógeno libres en dicha solución. Si el pH es menor a 7 (pH<7) se dice que la solución es ácida. Esto significa que existe una concentración relativamente alta de iones hidrógeno libres en la solución, los cuales son capaces de recibir electrones para poder estabilizarse.
Debido a la capacidad de aceptar electrones, las soluciones ácidas son más corrosivas que las soluciones tanto neutrales (pH = 7) como alcalinas (pH > 7) [6], ya que permiten que la zona anódica reaccione en mayor proporción, ya que se liberan electrones de tales reacciones.
Sales disueltas
Las sales ácidas, al diluirse en la solución electrolítica, disminuyen su pH, acelerando el proceso de corrosión por el efecto de acidez. Algunos ejemplos de sales ácidas son, el cloruro de aluminio, el cloruro de hierro y el cloruro de amonio (Charng y Lansing, 1982).
Por otro lado, las sales alcalinas, incrementan el pH de la solución electrolítica, por lo que en algunos casos funcionan como inhibidores del proceso de corrosión. Ejemplos de estas sales son el fosfato trisódico, tetraborato de sodio, silicato de sodio y el carbonato de sodio (Charng y Lansing, 1982).
Capas protectoras
La tendencia a la corrosión de un material se puede reducir con la existencia de capas que protejan su superficie. Estas capas pueden ser aplicadas artificialmente, en forma de recubrimientos; o pueden aparecer a través del fenómeno de pasividad, formándose capas de óxidos metálicos que impiden el avance del proceso corrosivo (Charng y Lansing, 1982).
Concentración de oxígeno
La concentración de oxígeno en el medio electrolítico puede acelerar o retardar el proceso de corrosión, dependiendo de la naturaleza del material (Charng y Lansing, 1982) . Para el caso de materiales ferrosos, al aumentar la concentración de O2, aumenta la velocidad de corrosión pues el producto corrosivo no protege al material. Mientras que para materiales pasivables, cuan mayor sea la concentración de O2, mayor capacidad tendrá el material de formar la capa protectora que lo caracteriza.
Temperatura
La velocidad de corrosión tiende a aumentar al incrementar la temperatura, debido a que se acelera la difusión del oxígeno del medio hacia el material afectado, inclusive a través de capas de pasivación, fragilizando a este. Experimentalmente se ha demostrado que un aumento en la temperatura de 2° C, incrementa al doble la tasa de corrosión, aproximadamente (Charng y Lansing, 1982). La temperatura, representa el factor más importante para el desarrollo del proceso de corrosión por oxidación, como se mencionó con anterioridad.
Velocidad de flujo
En sistemas de transporte de fluidos, al aumentar la velocidad de flujo del medio, por lo general, aumenta la tasa de corrosión, debido a que: (1) permite a las sustancias corrosivas alcanzar y atacar zonas aún no afectadas, y (2) evita en cierta medida la formación y/o acumulación de capas resistentes a la corrosión que protejan al material por efecto erosivo (Charng y Lansing, 1982).
Control de la corrosión y protección de materiales
Debido a las implicaciones económicas, de seguridad y de conservación de materiales, que envuelven los efectos negativos de los procesos de corrosión (Schweitzer, 2010), actualmente se ha investigado y desarrollado diferentes tipos de métodos para el control de este fenómeno, permitiendo proteger los materiales expuestos a este.
La selección de un material resistente a la corrosión, siempre es el primer tipo de control que se debe considerar. Esto en muchas ocasiones no es posible, ya que este es limitado por (1) las condiciones del medio circundante; (2) las condiciones dimensionales y geométricas necesarias en el material en función de la aplicación requerida; y (3) un costo económico elevado. Lo cual hace que la selección de un material resistente no sea factible y/o posible, por lo que se deben considerar otros tipos de métodos para esto.
A continuación, se presentan algunos métodos de control de la corrosión, para la protección de los materiales afectados. Estos son los que más se emplean a nivel comercial.
Inhibidores
Un inhibidor es una sustancia química que, al añadirse al medio corrosivo, disminuye la velocidad de corrosión (Revie y Uhlig, 2008). Existen varios tipos de estas sustancias; los más conocidos son los anódicos y catódicos.
Inhibidores anódicos (pasivadores)
Los inhibidores anódicos, también llamados pasivadores son sustancias oxidantes, por lo general, inorgánicas, que aumentan el potencial electroquímico del material por proteger, volviéndolo más noble (Revie, 2011).
Inhibidores catódicos
Los inhibidores catódicos controlan el pH del medio corrosivo, que impide que las reacciones de reducción ocurran, Estos evitan la reducción ya sea, de iones de hidrógeno en (1) moléculas de hidrógeno, en medios ácidos, o (2) de oxígeno, en medios alcalinos (Revie, 2011).
Recubrimientos orgánicos
Los recubrimientos orgánicos son de sustancias a base de polímeros (pinturas), resistentes a la degradación, que se emplean para recubrir el material por proteger. Estos actúan mediante ya sea, (1) la formación de una barrera, que impide en gran medida la penetración de oxígeno y agua, o (2) la inhibición del proceso de corrosión, al incrementar tanto la resistividad eléctrica como la iónica, cortando el ciclo de corrosión (Schweitzer, 2006).
Recubrimientos metálicos
Consiste en recubrir el material a proteger con algún metal que tenga mayor resistencia a la corrosión. Existen diferentes métodos para efectuar estos recubrimientos, y los más utilizados son el electroplating y el galvanizado (Revie y Uhlig, 2008).
Electroplating
Es un proceso de protección en el que se utiliza una corriente eléctrica externa para depositar un material con mayor resistencia a la corrosión sobre su superficie.
Galvanizado
El material por proteger se sumerge sobre un baño del metal de recubrimiento, el cual tienen un mayor potencial electroquímico.
Recubrimientos no metálicos
Trata sobre recubrir el material a proteger con el uso de un material no metálico, que impida el proceso de corrosión. Existen diferentes métodos para efectuar estos recubrimientos. El más utilizado es el anodisado (Revie y Uhlig, 2008). Este método se emplea en materiales pasivables, y consiste en el uso de una corriente eléctrica sobre el material por proteger, de modo que el potencial electroquímico del sistema induzca a un comportamiento anódico a dicho material, generando el desarrollo de una capa de pasivación.
Protección catódica
Radica en modificar relativamente el valor del potencial electroquímico del material por proteger, haciendo que este material se comporte como un cátodo. Se emplea mayormente en sistemas enterrados o inmersos en agua de mar. Existen 2 formas de realizar esto, mediante (1) una corriente impresa o (2) un ánodo de sacrificio (Revie y Uhlig, 2008).
Ánodo de sacrificio
Se conecta eléctricamente un material con menor potencial electroquímico, el cual se comporta como el ánodo del sistema. Este ánodo protege al material, al ser degradado por la corrosión en lugar de dicho material, por lo cual se conoce como un ánodo de sacrificio.
Corriente impresa
Es un proceso similar al de ánodo de sacrificio, cuya diferencia consiste en inyectar una corriente externa al sistema debido a que, por sí solo, este sistema no generaría suficiente corriente para poder formar la celda electroquímica, siendo ineficaz contra la corrosión. La corriente impresa hace posible la protección del material en cuestión, al promover las reacciones electroquímicas, empleando el ánodo de sacrificio.
Protección anódica
Mucho menos conocida que el método de protección catódica, la protección anódica consiste en disminuir el potencial electroquímico del material a proteger, a través de la inyección de una corriente externa, volviéndolo más anódico, lo cual induce al material hacia un estado de pasivación, formándose la capa pasivada que protege al material. Al mantener la corriente externa, la capa de pasivación continúa en constante regeneración, evitando que se deteriore el material. Solo puede ser empleado en algunos tipos de materiales, sobre todo los metales de transición.
Comentario final
Se han presentado, a modo de introducción, información sobre, (1) algunos tipos de corrosión que se pueden observar comúnmente, (2) algunos factores que influencia al proceso de corrosión y su velocidad, y (3) algunos tipos de métodos para el control de la corrosión y la protección de material ante este fenómeno.