Introducción
La papaya (Carica papayaL.) es la tercera fruta tropical más producida y consumida en el mundo después del mango y la piña. Es originaria de Centroamérica y el sur de México, donde ya era cultivada antes del descubrimiento de América. Este fruto, es uno de los más importantes desde el punto de vista económico y social, ya que es fuente de ingresos para miles de familias y se posiciona como una fuente de ingreso de divisas para muchos países gracias a su demanda internacional (Valenciaet al.2017).
Esta fruta se produce en más de 60 países principalmente tropicales y subtropicales en donde se propaga rápidamente, debido a la abundancia y viabilidad de sus semillas; además de los requerimientos de suelos fértiles y abundantes lluvias (De La Cruzet al.2003). También, es reconocida por sus cualidades médico-gastrointestinales, así como insumo para la industria de los jugos (SAGARPA 2017).
Actualmente se cultivan alrededor de 440 000 ha en todo el mundo, con una producción de casi 12,5 millones de toneladas. La India y Brasil son los principales productores de papaya; sin embargo, también destacan países como México, Nigeria e Indonesia. El mercado internacional está dominado por México que exporta más de 130 000 toneladas al principal consumidor de papaya en el mundo que es Estados Unidos. Anualmente, la Unión Europea, el Reino Unido, Holanda y Alemania importan alrededor de 8000 toneladas anuales cada uno, mientras que España supera las 5000 toneladas anuales (Huesoet al.2017).
En Costa Rica existen 3264 fincas dedicadas a la producción de papaya, las cuales representan un total 1393,5 ha. Las principales zonas productoras se encuentran en las provincias de Limón con 514,8 ha, seguido de Alajuela y Puntarenas respectivamente (INEC 2014). De acuerdo con la Promotora de Comercio Exterior (PROCOMER 2017), en 2016, la exportación de esta fruta alcanzó los $3 millones y 3889 toneladas, donde Canadá es el principal país importador con un 52%, seguido de España (14%) y finalmente, Holanda (5%).
La variabilidad de papayas en Costa Rica representa un potencial para el desarrollo de nuevas variedades o híbridos. Actualmente se produce la variedad Pococí, conocida como''papaya perfecta'' que destaca por sus altos rendimientos, calidad de la fruta, uniformidad de las plantaciones, sabor y aroma. Este híbrido es protegido y desarrollado por el Instituto de Innovación y Transferencia de Tecnología Agropecuaria (INTA), adscrito al Ministerio de Agricultura y Ganadería, y la Universidad de Costa Rica (Boganteset al.2011).
El cultivo de papaya puede ver afectada su producción debido a la interacción de patógenos como hongos, bacterias, virus y nematodos. De estos últimos microorganismos, soloMeloidogynespp. yRotylenchulusspp. parecen tener importancia económica y se identifican mundialmente en ese cultivo (Inserra y Cartia 1976, Lambertiet al.1980 y 1993, McSorley 1983 y 1992, Cohn y Duncan 1990, Lucet al.2005). El daño que provocan las especiesM. hapla,M. incognita y M. javanicaen este cultivo, fue previamente reportada en Brasil (Chaful y De'Arc 1994).
En Colombia, Espinosaet al.(2004) y Jarabaet al.(2007), encontraron las especiesM. arenaria,M. javanicayM. incognita, esta última, la especie más frecuente. Asimismo, en México, Cid del Pradoet al.(2011) reportaron en los estados de Michoacán y Morelos aM. incognitaraza 1 yM. arenariaen el estado de Morelos. En Pakistán, Khanet al.(2007, 2008) reportaron la presencia deM. incognita; y en Hawái Hineet al.(1965) identificaron la misma especie asociada a plantaciones de papaya. Además, Koenninget al.(1999), hallaron pérdidas del 15 al 20% en el rendimiento de esta fruta en Hawái causadas porMeloidogynesp. yRotylenchulussp. Finalmente, en España Castillo y Gómez-Barcina (1993), indicaron la presencia deM. javanicaen este cultivo.
Los géneros y especies mencionadas anteriormente afectan el sistema radical de la planta, donde ocasionan daños mecánicos y la formación de agallas (Chaful y De'Arc 1994). Cohn y Duncan (1990) mencionan queMeloidogynespp. es capaz de ocasionar pudrición de la raíz lo cual disminuye la vida útil de las plantas de papaya, así como la reducción drástica de su productividad. Estos patógenos limitan el rendimiento y la producción de la fruta, pero en Costa Rica no existen datos sobre las pérdidas ocasionadas por nematodos en este cultivo.
Estudios realizados por Ramakrishnan y Rajendran (1998) en India, estimaron una disminución en el rendimiento del 15,9 al 36,6% en el número y peso promedio de frutos de papaya, es decir, por cada aumento de nematodos en 5 g de raíz hallaron una pérdida de 0,35% en el rendimiento de la fruta (0,811 g por árbol) debido aM. incognita. Además, determinaron que el nivel de agresividad deM. incognitafue un juvenil por g de suelo, suficiente para reducir los parámetros de crecimiento de las plantas y para alterar la fisiología del fruto.
En Costa Rica, el géneroMeloidogynespp. está asociado a una gran variedad de cultivos de importancia agrícola de hortalizas como brócoli, coliflor, culantro, chile, tomate, zanahoria, raíces y tubérculos como papa, ñampí, ñame, yuca, frutales entre ellos mango, durazno, papaya, guanábana y otros (Esquivel y Peraza 2010). No existe información que relacione el daño de las plantas con la presencia de esta plaga, o la caracterización a nivel de especie. La correcta identificación de este nematodo facilitaría la implementación de técnicas de combate, como el uso de cultivares resistentes y la ejecución de medidas cuarentenarias (Vovlaset al.2005). Los procedimientos de identificación a nivel de género o especie basados en la observación de caracteres morfológicos y morfométricos son lentos, requieren de tiempo, un amplio conocimiento sobre taxonomía de nematodos y en algunos casos no son concluyentes (Taylor y Sasser 1978, Britoet al.2004).
Actualmente, los procedimientos tradicionales de identificación se combinan con técnicas moleculares de análisis del genoma que permiten una caracterización más precisa. Dentro de los análisis moleculares se utiliza la reacción en cadena de la polimerasa (PCR por sus siglas en inglés) (Mulliset al.1986), la técnica RFLP (Polimorfismo en la Longitud de los Fragmentos de Restricción) y la secuenciación con las cuales se obtiene un patrón de digestión único para cada especie. Luego mediante el uso de primers/indicadores, amplifican una región conservada y polimórfica en su longitud que son de diferente tamaño para cada especie (Monteroet al. 2007).
En la presente investigación, se integraron métodos morfológicos y moleculares para determinar la especie deMeloidogyneresponsable de producir agallas en el sistema radical de plantas de papaya, provenientes de una plantación comercial en Pococí, Limón, Costa Rica.
Materiales y métodos
Sitio de muestreo. Se llevó a cabo en abril de 2015 en una parcela de aproximadamente 0,5 ha con una densidad de siembra de 900 plantas.ha-1. La parcela pertenece al Instituto Nacional de Tecnología Agropecuaria (INTA) en Pococí, Guápiles, Limón (10°15'28.56''N y 83°46'14.62''O), se encuentra a una altura de 150 msnm con una precipitación anual de 3500 a 5000 mm anuales y una temperatura promedio de 17 a 23°C, lo que la ubica en bosque muy húmedo tropical (bmh-T) (Holdridge 1982).
Se tomaron 20 submuestras de suelo de 100 g y diez submuestras de 5 g al azar, las cuales se llevaron al Laboratorio de Nematología de la Escuela de Ciencias Agrarias (ECA) de la Universidad Nacional para su análisis.
Extracción de nematodos e identificación morfométrica. Se extrajeron hembras, juveniles y masas de huevos deMeloidogynesp. a partir de raíces con agallas por medio de una aguja de disección y un estereoscopio a 45X. Luego, varias hembras se colocaron en portaobjetos para observar e identificar la especie de acuerdo con el método descrito por Franklin (1962). Se comparó la morfología de los diseños perineales con descripciones e ilustraciones elaboradas por Esseret al.(1976), López y Dickson (1977), Taylor y Sasser (1978), Whitehead (1968). Un total de 25 juveniles y diez hembras se identificaron con base en sus características morfológicas mediante las claves taxonómicas de Lucet al.(1990) y Maiet al.(1964). Se midió en los juveniles, la longitud del cuerpo, ancho del cuerpo, ancho del cuerpo a nivel del ano, longitud del estilete, ancho de la región labial, desembocadura de la glándula faríngea, distancia de la cabeza hasta el poro excretor, longitud del esófago, longitud de la cola, porción de la región hialina. Asimismo, se tomaron otras medidas para relacionar la proporción de los juveniles con respecto al largo del nematodo versus ancho del cuerpo, longitud del esófago, longitud de la cola y finalmente, ancho del cuerpo a nivel del ano. En el caso de los machos únicamente se realizaron mediciones de la longitud del estilete y de la desembocadura de la glándula faríngea dorsal desde la base del estilete (DGO). Se tomaron imágenes de hembras, huevos y juveniles con una cámara digital integrada y adaptada a un microscopio con contraste de interferencia diferencial (DIC). Cada fotografía se editó con el programa Photoshop CS6®.
Análisis molecular
Extracción de ADN. Se utilizaron 10 juveniles que individualmente se transfirieron a un tubo de PCR de 0,2 ml con 47 µl de Tris-HCl 0,2 M (pH 8,0) y 5 µl de proteinasa K (20 mg.ml-1). Los tubos con los nematodos se colocaron en un baño maría ultrasónico (Bransonic 2510, Branson Ultrasonidos™) durante 10 min a 60°C y posteriormente se incubaron durante 30 min a 60°C en un termociclador termociclador. Después se mezclaron con ayuda de un agitador tipo vórtex, se incubaron a -20ºC durante 15 min y a 90°C durante 10 min. Posteriormente, la mezcla se volvió a agitar y se repitió nuevamente el ciclo de congelación/descongelación anterior. Por último, las muestras se agitaron en el vórtex durante 30 s y se centrifugaron durante 2 min a 2000 rpm (Solano-Gonzálezet al.2015). Las suspensiones con el ADN se almacenaron a -20°C para su posterior uso en PCR.
Amplificación del ADN mitocondrialy análisis RFLP.Por medio de PCR se amplificó la región entre la subunidad II del citocromo oxidasa (COII) y la subunidad grande (16S) del ADN mitocondrial (ADNmt) con los primers C2F3 (5'-GGTCAATGTTCAGAAATTTGTGG-3') y 1108 (5'-TACCTTTGACCAATCACGCT-3'-) (Powers y Harris 1993). Se prepararon reacciones de PCR en tubos de 0,2 mL con un volumen final de 25 µl que contenían la siguiente mezcla de reacción: buffer de la Taq polimerasa 1X, dNTPs 0,08 mM, MgCl21,0 mM, imprimadores a 0,8 µM cada uno, 0,8 U de Taq polimerasa y 15 µL de ADN. La amplificación del ADN se llevó a cabo en un termociclador (Veriti 96-Well, Thermo Scientific®) de 96 pozos bajo las siguientes condiciones de temperatura: una fase de desnaturalización inicial a 94°C durante 2 min, seguida de 35 ciclos de 10 seg de desnaturalización a 94°C, 30 seg de alineamiento a 48°C y 2 min de extensión a 68°C y una fase final de extensión a 72°C durante 2 min.
Los productos de PCR se trataron posteriormente con las enzimas de restricciónAluI yDraI en forma independiente, según las indicaciones por la casa fabricante. Para ello se prepararon reacciones de 15 µL (5 µL de producto de PCR, 1 µL de enzima, 1,5 µL del buffer de reacción de la enzima a 1X, 7,5 µL de agua ultrapura) y se incubaron durante 1 h a 37°C en el termociclador.
Los fragmentos de PCR y RFLP se separaron por medio de electroforesis en geles de agarosa de 1,5 y 2% respectivamente, preparados con TBE 1X. Los geles se corrieron dentro de una cámara de electroforesis a 90V durante 1 h y 30 min. Los fragmentos de ADN se visualizaron y se digitalizaron en un fotodocumentador con un transiluminador de luz UV después de teñir los geles con Gel Red a 3X.
Resultados y discusión
Las raíces recolectadas mostraron síntomas severos de agallamiento (Figura 1). Se extrajeron un total de 200 J2/100 cc de suelo y 3952 J2/10 g en raíz deMeloidogyne javanica. En el campo no se observaron síntomas de clorosis, enanismo, escaso desarrollo vegetativo o poca producción lo que podría estar relacionado a un buen manejo de la plantación. De acuerdo con Rojas (2010), la salud general observada en una parcela o finca se relacionada a prácticas de manejo en el uso de fertilización y materia orgánica.

Figura 1 A y B. Agallamiento inducido porM. javanicaen raíces de papaya (C. papayaL.). Cultivada en Pococí, Limón, Costa Rica. 2015.
Actualmente en Costa Rica no existen referencias acerca de límites de tolerancia y umbrales económicos; sin embargo, los resultados de estudio muestran altas densidades poblacionales principalmente en raíz que se presume podrían afectar la producción de este cultivo. En ocasiones se observaron en lotes o fincas, algunos árboles con poco crecimiento con respecto a los demás, también clorosis, marchitez y hasta una disminución en fructificación. Según Khan y Husain (1991), se debe considerar no solo las condiciones experimentales y ambientales, sino también la virulencia de la población de nematodos. En algunas ocasiones la infestación con otros patógenos puede formar un complejoplaga-hospedantedifícil de controlar como es el caso de este nematodo que causa un daño severo a la raíz y posibilita la entrada dePhytophthorasp (Diaz 2002).
Identificación morfológica y morfométrica. El patrón perineal de las 25 hembras mostró un arco dorsal alto e incisiones laterales (estrías transversales) marcadas que separan las regiones dorsal y ventral y que a su vez se extienden a ambos lados del extremo de la cola y que son únicas para la especieM. javanica(Figura 2). Además, se observó que las crestas recorren todo el ancho del patrón, pero desaparecen gradualmente cerca del extremo de la cola. Las estrías son lisas o ligeramente onduladas y algunas pueden doblarse hacia los bordes vulvares (Figura 2). Estos resultados coinciden con los reportados porChaful y De'Arc (1994) en Brasil, Espinosaet al.(2004), Jarabaet al.(2007) en Colombia y Cid del Pradoet al.(2011) en México.
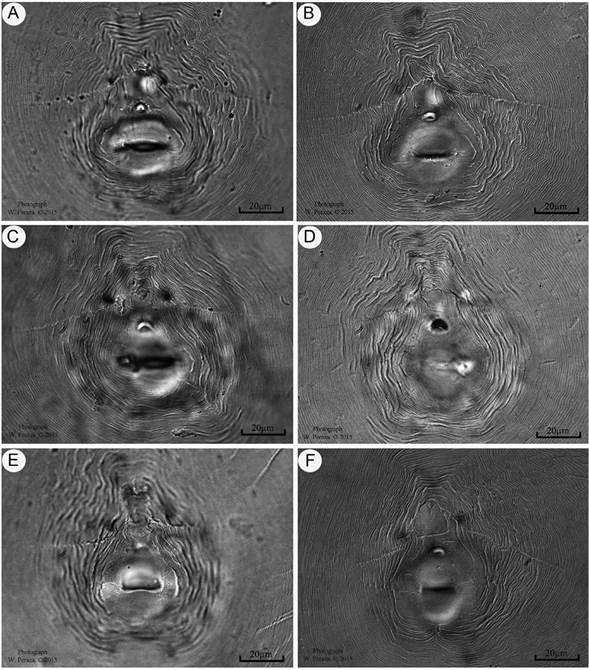
Figura 2 A-F. Fotomicrografías a escala = 20µm del patrón perineal de hembras deM. javanicaprovenientes de una plantación de papaya (C. papayaL.). Cultivada en Pococí, Limón, Costa Rica. 2015
El patrón perineal es una característica valiosa y utilizada en la identificación de especies del géneroMeloidogyne(Chitwood 1949, Eisenbacket al.1980, Hirschmann 1985). No obstante, debido a la variabilidad intraespecífica y similitudes morfológicas dificulta en muchas ocasiones una correcta identificación (Pamjavet al. 1999). En el presente estudio, no hubo dificultad en la identificación de los diseños, ya que todos ellos presentaron características similares para la especie. En el casoM. arenaria, presenta un diseño perineal con un arco dorsal bajo, redondeado, pero a diferencia deM. javanica, sin líneas laterales evidentes marcadas por estrías cortas, irregulares y bifurcadas (Eisenback 1985).
Asimismo, el patrón perineal deM. incognita, presenta un arco dorsal alto y cuadrado sin líneas laterales y la presencia de bifurcaciones en las estrías a diferencia de M. javanica (Eisenback 1985). Sin embargo, es importante mencionar que en estudios realizados por Britoet al.2004, observaron variaciones morfológicas en un patrón perineal para una especie en específico, las cuales podrían coincidir o ser similares para otra especie.
En la medición de las 10 hembras, se determinó que el largo fue de 608,0±42,1 (547,7-643,2 µm), el ancho de 392,2±17,2 (355,3-432,8 µm), la longitud del cuello de 219,4±10,8 (194,2-254,7 µm). Con respecto al estilete, presentó una longitud de 16,0±0,72 (14,8-16,9 µm) mientras que la distancia del orificio de la glándula dorsal esofágica (DGO) fue de una longitud de 4,2±0,16 (4,0-4,5) (Figura 3). En investigaciones realizadas, Jepson (1987) determinó que en promedio el largo de hembras de hembras deM. javanicafue de 672,5 μm con un rango entre 545 a 800μm, mientras que el ancho del cuerpo 422,5 con un rango entre 300 a 545μm. Finalmente, el largo del estilete tuvo un promedio de 16μmcon un rango entre 14 a 18μm. Por su parte, en estudios taxonómicos realizados por Kauret al.(2016) para esta misma especie, encontró qué, las hembras presentaban en promedio un largo de 654,5μmcon un rango entre 519 a 790μm; el ancho fue de 402μmcon un rango de 287 a 517μmy por último, la longitud del cuello con un promedio de 214,5μmy un rango entre 129 a 300μm. En el caso del estilete un promedio de 16 μm con un rango entre 14 a 18μmy el DGO un promedio de 3,8 μm con un rango entre 2,9 a 4,8μm. Asimismo, Espinosaet al.(2004), determinaron los parámetros morfométricos de la longitud del estilete de 15,4 µm ± 0,7 µm (14-16 µm) y del DGO 3,2 µm±0,6 µm (2-4 µm) los cuales junto con las otras investigaciones se encuentran dentro del rango para la descripción original de la especie y coinciden con la población deM. javanicade este estudio.
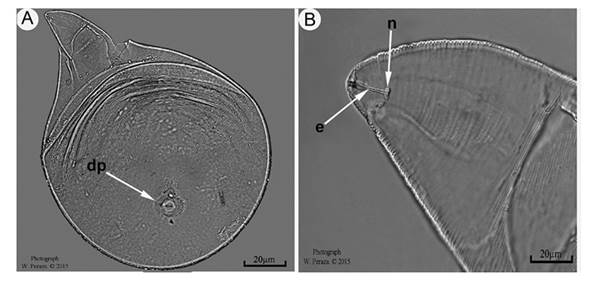
Figura 3. Fotomicrografías a escala = 20 µm que permiten observar hembras deM. javanica. A. Hembra completa que muestra el patrón del diseño perineal (dp). B. Parte anterior de la hembra en la posición del poro excretor (pe), estilete (e) y nódulos (n). Plantación de papaya (C. papayaL.). Pococí, Limón, Costa Rica. 2015.
Con respecto a los machos, estos presentaron en su parte anterior, un disco labial grande y plano, con labios medios fusionados en una región cefálica alta. También al medir tanto el estilete como el DGO, presentaron rangos de longitud de entre 15,3 a 16,8 µm y de 2,2 a 3,8 µm respectivamente; ambos dentro del rango para la especieM. javanicareportado por Eisenback (1985) y Espinosaet al.(2004).
El análisis morfométrico de 25 juveniles del segundo estadio (J2) (Tabla 1, Figura 4) mostró que el valor promedio de la longitud del cuerpo de los estadios juveniles medidos fue de 419,2 µm, con un ancho del cuerpo de 13,1 (12,5-13,7) µm. La longitud del estilete fue de 11,8 µm, mientras que el ancho del cuerpo a nivel del ano fue de 9,8 µm y el ancho de la región labial de 4,7 µm. La distancia de la glándula esofágica dorsal desde la base del estilete fue de 3,5 µm. Finalmente, longitud de la cola fue de 49,3 µm y la porción hialina de 12,1 µm.
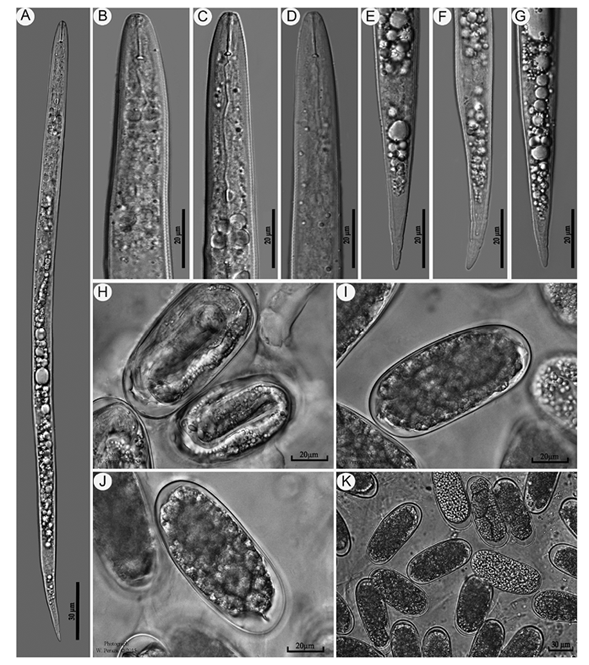
Figura 4 Fotomicrografías de segundos estados juveniles y huevos deM. javanicade una plantación de papaya (C. papayaL.).
A. Segundo estado juvenil (J2). B, C y D. Región anterior de J2 en la posición del estilete (e), nódulos (n), glándula dorsal esofágica (gde), y metacorpus (m). E, F y G. Región posterior de J2donde se muestra el ano (a) y la región hialina de la cola (rh). H, I, J (Huevos (h) de hembras deM. javanica) y K. Escala: A= 30 µm, B-J = 20 µm, K= 30 µm.
Cultivo en Pococí, Limón, Costa Rica. 2015.
Todos los caracteres morfológicos de importancia diagnóstica (Tabla 1) y referentes a la población deM. javanicaen estudio, presentaron valores que se encuentran dentro del rango para dicha especie (Whitehead 1968, Jepson 1987, Kauret al.2016). Asimismo, al comparar las mediciones de la población deM. javanicatambién presentó similitud con estudios llevados a cabo por Williams (1972), Özarslandan y Elekçioğlu (2010) yÖztürk et al.(2020). No obstante, un estudio realizado por Rusinqueet al.(2018), sauna población deM. javanicade Portugal, mostró similitudes con la población en estudio en el largo del nematodo y el DGO, no así en las medidas de la región hialina (14,0 (10,0-18,0) versus 12,1 (11,0-13,9)), largo del estile (55,3 (49,9-60,8) versus 49,3 (45,8-55,5)) y la cola (55,3 (49,9-60,8) versus 49,3 (45,8-55,5)), las cuales fueron inferiores en la población en estudio; sin embargo, estos valores se encuentran dentro del rango para la descripción de la especie.
Tabla 1 Comparación morfométrica de juveniles de segundo estadio (J2) en una plantación de papaya (C. papayaL.). Pococí, Limón, Costa Rica, 2015.
| Medidas y relaciones (µm) | M. javanica (n=20) Papaya (presente estudio) | M. javanica (Jepson 1987) |
|---|---|---|
| Longitud del cuerpo (L) | a419,2±14,4 (398,1-448,2) | 387-459 |
| Ancho máximo del cuerpo (MBW) | 13,1±0,4 (12,5-13,7) | 11-13,6* |
| Ancho del cuerpo a nivel del ano (ABW) | 9,8±0,5 (9,3-10,7) | - |
| Longitud del estilete (E) | 11,8±1,2 (10,4-14,6) | 9,4-11,4 |
| Ancho de región labial (LRW) | 4,7±0,1 (4,5-5,0) | - |
| Desembocadura de la glándula faríngea dorsal desde la base del estilete (DGO) | 3,5±0,3 (3,2-4,0) | 2-3,2* |
| Distancia desde la cabeza hasta el poro excretor | 84,0±3,6 (76,4-89,1) | 62,9-85,0* |
| Longitud del esófago (Le) | 115,3±1,3 (113,8-118,3) | - |
| Longitud de la cola (Lc) | 49,3±3,3 (45,8-55,5) | 46,8-59,8* |
| Porción hialina | 12,1±0,9 (11,0-13,9) | 9-18 |
| a (L/MBW) | 30,7±1,6 (27,8-33,0) | 27,1-35,9** |
| b (L/Le) | 3,6±0,1 (3,4-3,9) | - |
| c (L/Lc) | 8,3±0,3 (7,9-9,2) | 7,3-8,1** |
| c' (Lc/ABW) | 5,0±0,4 (4,4-5,6) | - |
aPromedio ± desviación estándar (rango); n= número de especímenes analizados.
*Medidas tomadas de Kaur et al. (2016).
**Medidas tomadas de Whithead (1968).
De acuerdo con Hirschmann (1985), las medidas entre especies son en muchas ocasiones estrechas, por lo que es común encontrar que algunas de ellas se superponen entre sí. En el caso de la longitud de la cola, es una de las características más útiles porque varía considerablemente entre especies y tiene poca variación intraespecífica lo que ayuda a distinguir con mayor facilidad entre ellas (Karssen y Moens 2006).
Análisis molecular. La amplificación del ADN de la región mitocondrial COII/16S a partir de los imprimadores C2F3/1108 generó un fragmento de aproximadamente 1,7 kb para cada uno de los individuos analizados (Figura 5). El peso molecular de 1,7 kb obtenido paraM. javanica,concuerda con el reportado en investigaciones previas por Powers y Harris (1993), Williamsonet al.(1994); Orui (1998), Hanet al.(2004); Britoet al.(2004), Flores (2008) y Ohet al.(2009). No obstante, en estudios realizados por Powers y Harris (1993), Orui, (1998), Ohet al.(2009) paraM. incognitay Orui (1998), Ohet al.(2009) paraM. arenariatambién reportaron un peso molecular de 1,7 kb para las especies mencionadas. Sin embargo, en este estudio al utilizar diferentes enzimas de restricción se pudo discriminar entre las 3 especies (M. arenaria, M. incognita y M. javanica).
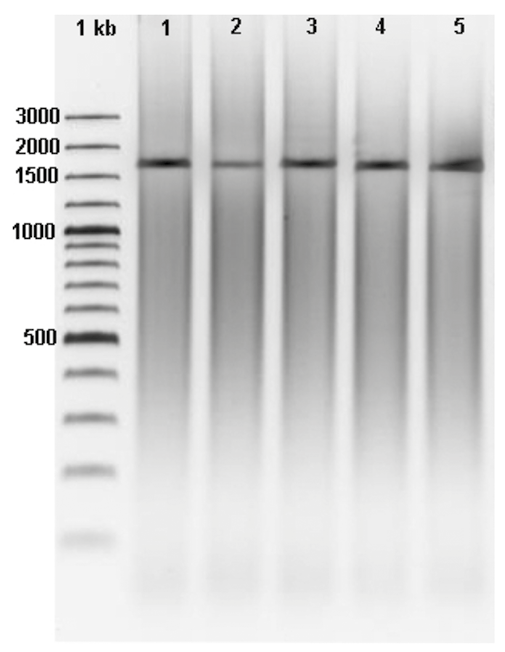
Figura 5. Electroforesis en gel de agarosa al 1% de los productos de la amplificación (PCR) de la región de mitocondrial COII/16S con los imprimadores C2F3/1108 (Powers y Harris 1993). Marcadores de peso molecular de 1 kb. Carriles 1-5: juveniles deM. javanica. Pococí, Limón, Costa Rica. 2015.
Al cortar el fragmento de 1,7 kb obtenido paraM. javanicageneró con la endonucleasaAluI tres fragmentos, uno de 250, 460 y 1000 pb (Figura 6, carriles 2 y 6) mientras que con la enzimaDraI cuatro, uno de 85, 105, 150, 600 y 600 pb (Figura 6, carriles 3 y 7) (Orui 1998). En el caso de la endonucleasaHinfI, no hubo corte de la enzima, es decir, generó un fragmento similar al del producto no cortado de 1,7 kb (Figura 6, carriles 4 y 8) y coincidió con resultados obtenidos por Orui (1998), Flores (2008) y Ohet al.(2009).
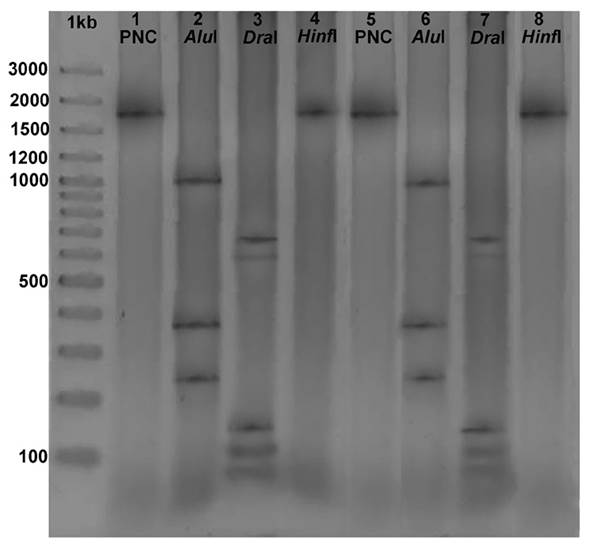
Figura 6 Patrones generados con las enzimas de restricciónAluI,DraI yHinfI mediante electroforesis en un gel de agarosa al 1,5%. Carriles 1 y 5: Productos de PCR sin cortar con enzimas de restricción; Carriles 2 y 6: fragmentos generados con la enzimaAluI; Carriles 3 y 7: fragmentos generados con la enzimaDraI, Carriles 4 y 8: fragmentos generados con la enzimaHinfI. Marcador de peso molecular 1 kb. Pococí, Limón, Costa Rica. 2015.
Sin embargo, estudios de Powers y Harris (1993), Flores (2008), reportaron un producto de PCR paraM. javanicatratado con la enzima de restricciónAluI que generó 3 fragmentos, uno de 150, 400 y 1000 pb. Asimismo, al comparar los fragmentos obtenidos con esta misma enzima para la especieM. incognita, investigaciones realizadas por Powers y Harris (1993), Flores (2008), indicaron la presencia de 3 fragmentos cuyo peso molecular fue de 230, 400 y 900 pb. Por su parte, Orui (1998) obtuvo fragmentos con pesos moleculares de 150, 250, 460 y 820 pb para esta misma especie lo que afirma la presencia de fragmentos diferentes.
En el caso de la enzimaHinfI existen también el reporte de diferentes fragmentos. Por ejemplo, Orui (1998), Williamsonet al.(1994) y Ohet al.(2009) reportaron paraM. incognita2 fragmentos, uno de 400 y otro de 1300 kb. Asimismo, Powers y Harris (1993) determinó 3 fragmentos, uno de 300, 400 y 100 pb para esta misma especie con esta enzima.
De acuerdo con Perazaet al.(2013) aunque los juveniles de la población en estudio presentaron una morfología y taxonomía similar a poblaciones de esta especie en otras latitudes, las variaciones en el tamaño de los fragmentos que se generan con las enzimas de restricción pueden estar ligadas a variantes genéticas o polimorfismos dentro de una misma especie o población que se puede deber a mutaciones en el sitio de corte de las enzimas. Adicionalmente indica que otra razón por la cual existen distintos tamaños se podría obedecer a diferencias en el tiempo de corrida que hacen la visualización o ausencia de las diferentes bandas en un mismo gel.
Es importante aumentar el conocimiento e identificación de las principales especies de nematodos asociados a cultivos de importancia agrícola, ya que de esta manera no solo se podrá conocer su distribución y propagación, sino que también se logrará un diagnóstico preciso de cuáles especies podrían generar algún daño a un cultivo en particular. Además, al identificar y conocer una determinada especie, se pueden implementar algunas estrategias de combate, como la rotación de cultivos, el uso de cultivares resistentes y el establecimiento de regulaciones cuarentenarias con respecto al traslado de material vegetal y suelo de un sitio a otro para evitar la diseminación.
Para la correcta identificación de nematodos es necesario el uso de diferentes técnicas. Gracias a la utilización de algunas de ellas, se logró la caracterización deM. javanicaasociada a una plantación de papaya.















