Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Ciencias Médicas
Print version ISSN 0253-2948
Rev. costarric. cienc. méd vol.25 n.1-2 San José Jan. 2004
Hospital de las Mujeres Dr Adolfo Carit Eva
Eugenia Delgado-Picado 1 , Carmen Sáenz-Sánchez 1, Alberto Calderón-Zúñiga 2 *
Resumen
A partir del año 1970, Streptococcus agalactiae (SGB), se sumó a la lista de gérmenes importantes por su capacidad para producir sepsis neonatal, infecciones en gestantes y en adultos inmunocomprometidos. En nuestro medio no existen datos sobre su incidencia; su detección en mujeres embarazadas antes del parto es fundamental para prevenir la transmisión vertical al neonato. Esta investigación tiene como objetivos: calcular las tasas de colonización en diferentes sitios anatómicos en gestantes y neonatos y concientizar a médicos y microbiólogos de su aislamiento e importancia clínica.
Del 16 de junio 2002 al 15 de marzo 2004, en el Hospital de las Mujeres, se analizaron 2952 urocultivos, 667 hemocultivos, 383 cultivos vaginales en distintas edades gestacionales, 53 cultivos de heridas quirúrgicas y 7 cultivos de líquido amniótico. Se utilizaron medios convencionales para el aislamiento de bacterias aerobias y anaerobias facultativas, la identificación y antibiograma se llevó a cabo por método automatizado Microscan®.
Se aisló EGB en 43 ocasiones, el 95,3% (41 casos) en Obstetricia y 4,7% en Neonatología. Un 5,4% (22 casos) en tracto urinario, 3,7% (14 casos) en tracto vaginal, 5,7% (3 casos) en piel y tejidos blandos, 28,5% (2 casos) en líquido amniótico y 0,3% (2 casos) en sangre (1,7 neonatos/10,000 nacidos vivos).
La incidencia baja en cultivos vaginales se debió a la no utilización de medios de cultivo adicionales que detectan el microorganismo en pequeñas cantidades, los cultivos de tamizaje no se efectuaron a las 35-37 semanas de gestación, ni se tomaron sin espéculo de la entrada de la vagina y/o zona ano-rectal. La incidencia en urocultivos aumentaría si se reporta EGB en cantidades > 10,000 UFC/ml en Agar Sangre, su presencia en orina implica alta colonización vaginal. La tasa de infección neonatal implicó la presencia de cepas poco virulentas.
Palabras clave: Streptococcus agalactiae, Streptococcus grupo B, infecciones perinatales, sepsis neonatal.
Abstract
Since 1970, Streptococcus agalactiae or Group B Streptococcus (EGB), was added to the list of important germs due to its capacity to produce neonatal sepsis, infections in pregnants and inmunocompromised adults. In our environment do not exist data about their incidence. Its detection in pregnant women before the delivery is fundamental in order to prevent the vertical transmission to the newborns. This investigation has as objectives: estimate the rates of colonization in newborn and pregnants in different anatomical sites, and also urge Doctors and Microbiologists to take consciousness of its isolation and clinical importance.
Since June 16th 2002 until March 15th 2004, in the Hospital de Las Mujeres, 2952 urine cultures, 667 blood cultures, 383 vaginal cultures in different gestacional ages, 53 cultures of surgical wounds and 7 cultures of amniotic fluid were analyzed. Conventional methods for the isolation of facultative aerobic and anaerobic bacteria were used; the identification and antimicrobial susceptibility test were carried out by Microscan automatized method.
EGB was isolated in 43 occasions, 95.3% (41 cases) in Obstetrics and 4.7% in Neonatology, 5.4% (22 cases) in urinary tract, 3.7% (14 cases) in vaginal tract, 5.7% (3 cases) in skin and soft tissues, 28.5% (2 cases) in amniotic fluid, and 0.3% (2 cases) in blood (1.7 newborns/10.000 live births).
The low incidence in vaginal cultures was due to the non use of additional culture media that can detect the microorganism in small amounts. The screening cultures were not taking on to 35-37 weeks of gestation; neither was it taken without especulum from the entrance from the vagina and/or anorectum zone. The incidence in urine tract would increase if EGB were reported > 10.000 UFC/ml in blood media. This is important because its presence in urine implies high density of vaginal tract colonization. The so low incidence of neonatal infection implied the presence of few virulent germs.
Key words: Streptococcus agalactiae, Group B Streptococcus, perinatal infection, neonatal sepsis.
Introducción
Para los servicios de Obstetricia y Neonatología de cualquier hospital, Streptococcus agalactiae o Streptococcus del Grupo B (SGB) se convierte en un importante agente etiológico; hoy en día, está clara su asociación directa con infecciones perinatales, infecciones en gestantes y en adultos inmunocomprometidos (1, 3, 5, 15, 18, 19) Desde la década de los años setentas se ha estudiado la epidemiología del microorganismo, métodos de aislamiento y manifestaciones clínicas entre otros, que confirman lo anteriormente expuesto. SGB es un comensal propio del tracto gastrointestinal y coloniza la vagina y el tracto urinario en forma intermitente. También, puede colonizar con menor frecuencia la faringe del feto (9, 17, 19, 21) Una de cada 4 o 5 mujeres portan el germen en el tracto vaginal sin manifestar síntomas (4-6, 14, 21); no obstante, la cifra de colonización en el tracto genital y gastrointestinal de gestantes varía del 5% al 35% (1, 5, 9, 16)
Este agente es capaz de ocasionar sepsis neonatal temprana o tardía, con una incidencia de 1 a 3 neonatos/1000 nacidos vivos y una mortalidad próxima al 10% (14,20) Se manifiesta como sepsis, neumonía, meningitis, artritis séptica, osteomielitis, celulitis, endocarditis y epiglotitis (1, 5, 8, 14, 17). En gestantes y puerpéreas puede causar infecciones urinarias, bacteriurias asintomáticas, bacteremias, leucorreas, fiebre > 38°C intraparto o posparto, endometritis, muerte intrauterina, aborto expontáneo, ruptura prematura de membranas > 18 hrs, parto pretérmino e infecciones en piel y tejidos blandos postcirugía (3, 9, 10, 14, 15, 19)
S. agalactiae es un coco Gram positivo, se describe como de menos de 2 micras de diámetro, crece bien en agar sangre y expresa mejor su crecimiento en atmósfera capnofílica, formando colonias blancuzcas y lisas. El 98% de las cepas son beta hemolíticas en agar sangre, también, son catalasa negativa y prueba de CAMP positiva, tienen el antígeno capsular específico que los clasifica en el grupo B de Lancefield, SGB poseé polisacáridos específicos que permiten su clasificación en 9 serotipos: Ia, Ib, Ic, III, IV, VI, VII, VIII y IX (1, 2, 14, 16). El cultivo sigue siendo el método de referencia, aunque el plateo directo de los cultivos vaginales en agar sangre, detecta solo las capas con colonización intensa; por consiguiente, para aumentar la sensibilidad del aislamiento se utilizan técnicas de cultivo adicionales que permiten recobrar el germen hasta en un 50% de las muestras vaginales de mujeres portadoras a pesar de la flora normal concomitante (14,16). Entre los medios de cultivo selectivos que se encuentran disponibles están: agar Granada, caldo Todd Hewitt suplementado con gentamicina (8 ug/ml), ácido nalidíxico (15 ug/ml), o colistina (10 ug/ml), conocidos comercialmente como caldo LIM o SBM (7, 8, 14, 16, 18). También existen pruebas inmunológicas rápidas, muy específicos, pero poco sensibles, útiles en mujeres gestantes con una alta densidad del germen en vagina (21). La prueba de la reacción en cadena de la polimeraza (PCR) tiene una sensibilidad del 97%; pero, es poco accesible por su alto costo (4-6, 8,17).
Entre las estrategias para reducir la infección perinatal por SGB, establecida por el Centro de Prevención y Control de Enfermedades, el Colegio Americano de Obstetricia y Ginecología y la Academia Americana de Pediatría, figuran los cultivos de muestras tomadas sin espéculo, de la parte inferior de la vagina y del exudado anorectal de rutina entre las 35 y 37 semanas de gestación. Esto ofrece un mejor valor predictivo de la presencia del germen en vagina en el período próximo al nacimiento del niño (3, 16, 18, 20). Las bacteriurias por SGB son importantes a cualquier edad gestacional y requieren ser tratadas; además, su presencia en tracto urinario implica una alta densidad microbiana en tracto vaginal. Una madre con SGB en tracto urinario o tracto vaginal es candidata a recibir profilaxis antibiótica intraparto para prevenir la sepsis neonatal (14,15).
Siendo el Hospital de Las Mujeres un Centro Materno – Infantil que no cuenta con un estudio al respecto, se hizo necesario realizar un análisis microbiológico retrospectivo, que tiene como objetivos conocer las tasas de incidencia en gestantes y neonatos en sitios anatómicos como tractos vaginal, urinario, sangre, líquido amniótico, piel y tejidos blandos. Además es importante llamar la atención de médicos y microbiólogos con relación a las técnicas de cultivo complementarias para el aislamiento de este agente y las modificaciones en el conteo de colonias en agar sangre de los urocultivos de gestantes (15), así como las tomas de muestra adecuadas en tracto vaginal y anorectal y los cultivos tamizaje de rutina entre las semanas 35-37 de la gestación. Todas estas disposiciones convergen en un oportuno diagnóstico para bien del binomio madre-neonato.
Materiales y métodos:
El estudio se realizó en el Hospital de Las Mujeres entre el 16 de junio de 2002 y el 15 de marzo de 2004 y abarcó 3 servicios: Obstetricia, Neonatología y Laboratorio Clínico. El protocolo de estudio cumplió con los requerimientos del Comité de Ética del Hospital. Para el estudio retrospectivo se recolectaron los datos de los cultivos microbiológicos de Streptococcus agalactiae o Streptococcus Grupo B, obtenidas a partir de 2952 urocultivos, 667 hemocultivos de neonatos, 383 cultivos vaginales de madres a distinta edad gestacional, 53 cultivos de piel y tejidos blandos postcirugía y 7 cultivos de líquido amniótico.
Procesamiento de muestras
Todas las muestras para cultivo fueron tomadas por métodos estandarizados (11). Los urocultivos se inocularon con asa plástica estéril calibrada a 0,01 ml en agar sangre y agar Mac Conkey. Las placas de agar sangre se incubaron bajo condiciones capnofílicas por 18-24 horas a 37°C, se tomaron como válidos aquellos cultivos que presentaron conteos > a 100.000 unidades formadoras de colonias/ mililitro.
Para los hemocultivos de neonatos, las tomas de muestras se hicieron en frascos con los caldos nutritivos estériles, los cuales se incubaron por un lapso de 5 días a 37°C, con reportes previos a las 24 y 48 horas y 5 días; aquellos cultivos que presentaron crecimiento mostrado por hemólisis, turbidez del caldo y producción de gas, se sometieron a tinción de Gram, identificación y antibiograma.
Los cultivos vaginales se tomaron en 2 tubos, cada uno con una torunda estéril, una en seco y otra con un mililitro de solución salina estéril, la primera torunda fue inoculada en placas de agar sangre, agar chocolate, agar MacConkey, agar manitol sal, agar Tayer-Martín. Además se hizo un frotis para tinción de Gram. Las dos primeras placas y el Tayer-Martín se incubaron en condiciones capnofílicas por 24-48 horas a 37°C, los otros medios de cultivo se incubaron en aerobiosis por 18 a 24 horas a 37°C. La torunda con salina se utilizó para la observación a fresco en búsqueda de otros agentes infecciosos agregados.
Los cultivos de líquido amniótico se tomaron en tubos estériles o directamente con una jeringa se tomó aproximadamente de 5 a 10 mililitros; una parte se inoculó en placas de agar sangre, agar chocolate, agar MacConkey, agar manitol sal y agar Tayer-Martín. Las placas de agar sangre, agar chocolate y Tayer y Martin se incubaron bajo condiciones capnofílicas por 24 a 48 horas a 37°C; otra parte se inoculó en un tubo con caldo Tioglicolato como cultivo de respaldo y de una tercera muestra se preparó un frotis para tinción de Gram.
Para los cultivos de piel y tejidos blandos, se recolectaron dos torundas de la lesión supurativa, la primera se cultivó en agar sangre, agar MacConkey, agar manitol sal y se hizo un frotis para tinción de Gram. La segunda torunda se inoculó en tubo con caldo tioglicolato. Las placas de agar sangre se incubaron bajo condiciones capnofílicas por 18 a 24 horas a 37°C y los otros medios de cultivo se incubaron en aerobiosis por 18 a 24 horas a 37°C.
Todos los cultivos que presentaron crecimiento fueron identificados y sometidos al antibiograma respectivo utilizando placas, las cuales contienen la bioquímica en miniatura necesaria para la identificación del germen y los antibióticos incorporados en diluciones, las placas después de 18-24 horas de incubación a 37°C se leyeron en un equipo automatizado Microscan (12,13).
Resultados
Se aisló Streptococcus agalactiae en 43 ocasiones, el 83,7% (36 casos) solo y el 16,3% (7 casos) asociado a otro u otros gérmenes como Trichomonas vaginalis, Gardnerella vaginalis, Candida albicans, Staphylococcus aureus y Streptococcus pyogenes. El 95,3% (41 casos) provenían de Obstetricia y 4,7% (2 casos) de Neonatología.
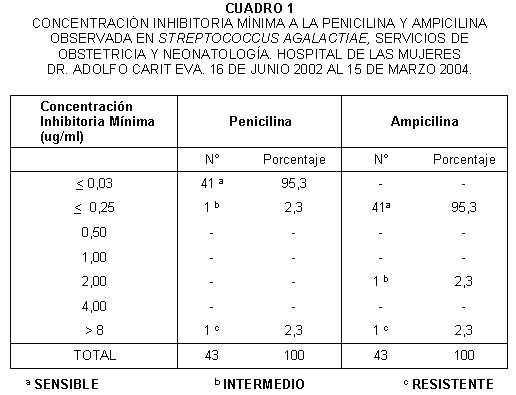
El antibiograma respectivo mostró que el 95,3% (41 casos) fueron sensibles a la penicilina y ampicilina a una concentración inhibitoria mínima (CIM) de 0,03 ug/ml y 0,25 ug/ml respectivamente (Cuadro 1).
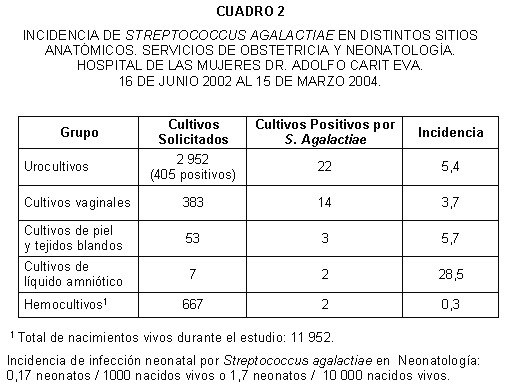
Las tasas de incidencia respectivas en los distintos sitios anatómicos fueron las siguientes: 5,4% (22 casos) en urocultivos, 3,7% (14 casos) en cultivos vaginales, 5,7% (3 casos) en piel y tejidos blandos, 28,5% (2 casos) en cultivos de líquido amniótico y 0,3% (2 casos) en sangre. Hubo un total de 11952 nacidos vivos durante el período en estudio, por lo tanto la tasa de incidencia neonatal fue de 0,17 neonatos / 1000 nacidos vivos o 1,7 neonatos/ 10.000 nacidos vivos (Cuadro 2).
El cuadro 3 es una comparación de 2 tasas de incidencia halladas en diferentes estudios a nivel mundial y las encontradas en el Hospital de las Mujeres, del tracto vaginal y de la tasa de infección neonatal (1, 5,12, 19, 21, 25).
Discusión
En tracto vaginal se obtuvo una incidencia de un 3,7%, un poco más baja que los datos publicados por otros autores de 5% a 35%, esto posiblemente debido a 3 razones: primero, el aislamiento del germen se hizo en agar sangre solamente, este medio permite el crecimiento de SGB en altas concentraciones en tracto vaginal, sin embargo, para los casos de poca densidad microbiana es necesario utilizar medios de cultivo selectivos adicionales como agar Granada o caldos LIM o SBM. (7, 8,14). La segunda razón fue que la toma de muestra vaginal en búsqueda de Streptococcus agalactiae, recomendada sin espéculo a la entrada de la vagina y en la zona anorectal, sitios anatómicos de más alta colonización por la proximidad con el tracto gastrointestinal (16, 21), tampoco fueron cumplidos. En tercer lugar, los cultivos vaginales se hicieron a cualquier edad gestacional, todos motivados por ruptura prematura de membranas, amenaza de parto prematuro o leucorrea; pero, en ningún caso se hizo como examen de rutina; lo cual es recomendado por el Centro de Prevención y Control de Enfermedades, el Colegio Americano de Obstetricia y Ginecología y la Academia Americana de Pediatría, en búsqueda de madres portadoras asintomáticas por SGB entre las 35 a 37 semanas de gestación próximo al nacimiento del niño, importante todo esto, para el tratamiento profiláctico intraparto y la consiguiente prevención de sepsis neonatal temprana entre en un 70% - 90% (3,6,7,15,21).
Con respecto a los urocultivos en gestantes, el hecho de que Streptococcus agalactiae se encuentre en tracto urinario, supone una alta densidad microbiana en tracto vaginal, por consiguiente existe riesgo de infección al neonato, por esa razón es que los organismos antes mencionados recomiendan su detección en agar sangre a partir de conteos > a 10,000 UFC/ml. (14,). En este estudio se tomaron como válidos sólo los cultivos con conteos > 100,000 Unidades Formadoras de Colonias/mililitro (UFC/ml).
Los microorganismos aislados en nuestro medio fueron sensibles en un 95,3% a la Penicilina y Ampicilina. La tasa de incidencia tan baja de infección neonatal temprana (2 casos), fue de 0,17 neonatos/1000 nacidos vivos o 1,7 neonatos/10.000 nacidos vivos, sin embargo no debemos confiarnos de esta conclusión, en este estudio hubo también 2 cepas que ocasionaron muerte neonatal, de hecho el 2,7% (una cepa intermedia en cultivo vaginal) y otro 2,7% (una cepa resistente en líquido amniótico, cuadro 1), se correlacionaron con 2 muertes intrauterinas en el lapso de un año y 9 meses de estudio.
Se recomienda replantear nuevamente este estudio a futuro, una vez que se corrijan las debilidades actuales.
Referencias
1. Crespo M, Vélez J. Importancia clínica del Streptococcus agalactiae como agente causal de infecciones. Col Médica. 1996; 27: 53-58. [ Links ]
2. American Academy of Pediatrics, Revised guidelines for prevención of early onset group B streptococcal (GBS) infección. Pediatrics. 1997; 99: 489-496. [ Links ]
3. Nizet V, Rubens C. Pathogenic mechanisms and virulence factors of group B streptococci. En: Fischetti C, Novick RP, Ferrett JJ, Portnoy DA, Rood JI, eds. The Gram positives pathogens.Washington DC, ASM. 2000. pp. 125-136. [ Links ]
4. Bergeron M, KE D, Menard C, et al. Rapid detection of group B streptococci in preganant women at delivery. New Engl J of Med. 2000; 343: 175-179. [ Links ]
5. Schuchat A. Neonatal group B streptococcal disease. New Engl J of Med 2000; 343: 209-210. [ Links ]
6. De Cueto M, De La Rosa M. Prevención de la infección neonatal por Streptococcus agalactiae. Un tema consolidado. Enf infecc Microb Clín. 2003; 21: 171-173. [ Links ]
7. De La Rosa M, Villarreal R, Vega D, Miranda C, Martínezzbrocal A. Granada medium for detección and identification of group B streptococci. Journal of Clin Microb. 1983; 18: 779-785. [ Links ]
8. Miranda J, Sánchez I, Mattar S. Detección de Streptococcus agalactiae en mujeres embarazadas del hospital San Jerónimo de Montería. Ins Nal Salud. 2000; 7: 193-197. [ Links ]
9. Corazza R, Janer M, Rotmen T, et al. Infecciones perinatales bacterianas. Cons Infec Perinatal. 1999; 97: 151-153. [ Links ]
10. Ovalle A, Gómez R, Martínez M, Aspillaga C, Dolz S. Infección vaginal y tratamiento de Streptococcus grupo B en embarazadas con factores universales de riesgo de infección. Resultados neonatales y factores de riesgo de infección neonatal. Rev Chil Obstet Ginecol. 2002; 67: 467-475. [ Links ]
11. Miller M, Holmes H. Specimen, collection, transport and storage. En: Murray Pr. Manual of clinical microbiology. 6th ed. Washington, D.C.: ASM Press; 1995. pp. 19-33. [ Links ]
12. Kiehn T, Capitolo Ch, Amstrong D. Comparison of direct and standar microtiter broth dilution susceptibility testing of blood culture isolates. Journ of Clin Microb.1983; 18: 645-651. [ Links ]
13. Barry A, Badal R, Hawkinson R. Influence of inoculum grouth phase on microdilution susceptibility test. Journ of Clin Microb.1983; 18: 645-651. [ Links ]
14. Schuchat A. Epidemiology of group B streptococcal disease in United States: Shifting paradigms. Clin Microb Rev. 1998; 11: 497-513. [ Links ]
15. Hernáis C, Antón N, Alós J, et al. Significado clínico del aislamiento de Streptococcus agalactiae en orina de pacientes de centros de salud. Enf Infecc Microb Clín. 2004; 22:89-91. [ Links ]
16. Mc Duffie R. Sreening techniques or group B streptococcal infection. En: Gabbe S, Simpson N. Obstetrics. 4th ed. Churchill Livingstone of Harcourt: Health Sciences Company, USA; 2002. pp. 23-30. [ Links ]
17. Larsen J, Groeup B streptococcal infeccions in pregnancy. En: Gabble S, Simpson N. Obstetrics. 4th ed. Churchill Livingstone of Harcourt: Health Sciences Company, USA; 2002. pp. 31-35. [ Links ]
18. Arbazúa F, Zajer Cl, Guzman A, et al. Deteminación de la portación de Streptococcus agalactiae (grupo B) en embarazadas durantes el tercer trimestre mediante inmunoensayo. Rev Chil Obstet Ginecol. 2002; 67: 293-295. [ Links ]
19. Schuchat A. Group B Streptococcus. The Lancet. 1999; 353: 51-56. [ Links ]
20. Juncosa T, Muñoz C, Gene A, Fortea J, Latorre C. Infecciones neonatales por Streptococcus agalactiae. An Esp Pediatr. 1996; 45: 153-156. [ Links ]
21. Centres for Disease Control and Prevention. Prevention of perinatal proup B streptococcal disease: a public health perspective. MMWR. 1996; 45: 1-24. [ Links ]
1 Servicio Laboratorio Clínico
2 Servicio Ginecología y abstetricia
Hospital de las Mujeres Dr. Adolfo Carit Eva, C.C.S.S.