Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.60 n.2 San José Jun. 2012
Biología reproductiva de Anisotremus interruptus (Perciformes: Haemulidae) en el Pacífico central mexicano
Salvador Ruiz-Ramírez1*, Gabriela Lucano-Ramírez1, Gaspar González-Sansón1, J.A. Rojo-Vázquez1 & Marcial Arellano-Martínez2*
*Dirección de correspondencia:
Abstract
Anisotremus interruptus is a widely distributed and commercially important species in the Eastern Pacific. A multi-year research on the reproduction of this species was carried out in coastal waters of Jalisco, Mexico. For this purpose, monthly samples were gathered with gillnets of different mesh sizes from 1998-2008. A total of 1 090 individuals were collected with a total length range between 15.6-61.0cm. Significant differences from expected 1:1 ratio were found for sex ratios in the total sample and for each size class, but not when comparisons among months and years were done. Temporal variations of the gonadosomatic index and proportions of maturation stages suggest that the main reproductive period is from February to May, although some less intensive spawning events were observed in other months. Seven stages of oocytes development were identified. Oocytes in different stages of development were identified in ovaries classified as mature, suggesting an asynchronic type of gonad development. Mean maturation length (L50) was 31.0 for females and 29.7cm for males. The internal organization of testes is of lobular type. Rev. Biol. Trop. 60 (2): 709-720. Epub 2012 June 01.
Key words: Haemulidae, reproduction, gonadosomatic index, maturity size, mexican central Pacific.
Resumen
Anisotremus interruptus es una especie de importancia económica que se distribuye ampliamente en el Pacífico oriental. Para investigar las características de la reproducción de esta especie, se realizó un estudio a lo largo de varios años en la costa de Jalisco, México. Para este fin, se tomaron muestras entre 1998 y 2008 con redes de enmalle de diferente luz de malla. Asimismo, se recolectaron en total 1 090 organismos que presentaron un intervalo de longitud total de 15.6-61.0cm. Además, se observó una diferencia significativa con respecto al valor esperado de 1:1 en la proporción de hembras y machos para todos los organismos recolectados y por clase de talla, pero no se encontró diferencia en dicha proporción en los análisis entre meses y entre años. La distribución temporal del índice gonadosomático y de la proporción de estadios de maduración gonadal sugieren que el periodo de reproducción en A. interruptus se concentra principalmente entre febrero-mayo, aunque se registraron desoves de menor intensidad en otros meses. También, se identificaron siete fases de desarrollo de los ovocitos. En ovarios de estadio maduro, se observaron ovocitos en diferente fase de desarrollo, lo cual sugiere que el desarrollo ovárico es de tipo asincrónico. La organización interna del testículo es del tipo lobular. La longitud de maduración sexual (L50) para las hembras fue de 31.0cm y para los machos de 29.7cm.
Palabras clave: Haemulidae, reproducción, índice gonadosomático, talla de maduración, Pacífico central mexicano.
Los peces de la familia Haemulidae son especies principalmente marinas, algunas de estuario y pocas de agua dulce. Asimismo, se distribuyen en los océanos Atlántico, Índico y Pacífico. Además, se conoce que representantes de esta familia tienen importancia económica en el Caribe (Palazón-Fernández 2007), Kuwait (Al-Husaini et al. 2001), Pakistán (Moazzam et al. 2006) y zonas del Mediterráneo (Chakroun-Marzouk & Mohamed-Hédi 2006). En el Pacífico oriental tropical se han reportado 29 especies de esta familia agrupadas en nueve géneros. Anisotremus interruptus (Gill, 1862) se distribuye en el océano Pacífico oriental desde el Golfo de California hasta Perú, incluidas las Islas Galápagos (Allen & Robertson 1998). Detalles sobre esta especie se pueden encontrar en diferentes trabajos: listas de especies para Jalisco y Colima, México (Rodríguez-Ibarra 1995, Aguilar-Palomino et al. 2001, Lucano-Ramírez et al. 2001a), estudios de la relación longitud-peso (Rojo-Vázquez et al. 2009), como parte de la captura comercial (Amezcua-Linares 1996, Rojo-Vázquez 1997, Rojo-Vázquez & Ramírez-Rodríguez 1997, Aldaco-González 2007, León-Arriola 2010), composición de la pesquería en relación con el efecto de El Niño (Godínez-Domínguez et al. 2000, Rojo-Vázquez et al. 2001, 2008, 2010), estudios sobre la edad, el crecimiento y la mortalidad (Cruz-Romero et al. 1993, Gallardo-Cabello et al. 2003, Espino-Barr et al. 2004a) y en otros que proporcionan información biológica y de la captura que proviene de la pesca en los estados de Colima (Espino-Barr et al 2003) y Jalisco (Espino-Barr et al. 2004b).
A. interruptus es una de las especies más importantes en la pesquería con redes de enmalle en la costa de Jalisco (Rojo-Vázquez 1997, Rojo-Vázquez & Ramírez-Rodríguez 1997, Godínez-Domínguez et al. 2000, Rojo-Vázquez et al. 2001, Aldaco-González 2007, Rojo-Vázquez et al. 2008, León-Arriola 2010, Rojo-Vázquez et al. 2010) y Colima (Cruz-Romero et al. 1993, Gallardo-Cabello et al. 2003), México. Aunque, A. interruptus es una especie que tiene amplia distribución en el Pacífico oriental y tiene gran importancia para la región, ningún estudio ha abordado la biología reproductiva. El conocimiento de los aspectos reproductivos es útil como una referencia para la implementación del manejo de su pesquería y en otras investigaciones biológicas. El objetivo de este trabajo fue investigar las características de las gónadas, el periodo reproductivo, la talla promedio de maduración y la proporción sexual en organismos de A. interruptus capturados por la pesquería artesanal costera en el Pacífico central mexicano.
Materiales y métodos
Área de estudio y recolecta de muestras: Los individuos analizados fueron recolectados en la Bahía de Navidad, que se localiza en la costa sur del estado de Jalisco (19º10’30’’-19º12’50’’N y104º42’45’’-104º41’30’’ W), en el Pacífico central mexicano. Ahora bien, se realizaron muestreos nocturnos entre enero de 1998 y diciembre de 2008, con redes de enmalle de 7.62, 8.89, 10.16 y 11.43cm de luz de malla. De cada individuo de Anisotremus interruptus se registraron la longitud total (LT; medida al milímetro más cercano), el peso total (PT; con precisión de 0.1g) y el peso de las gónadas (PG; con precisión de 0.01g) y se identificó el sexo. El desarrollo gonádico se evaluó mediante observación directa con base en los criterios de Palazón-Fernández (2007), con los cuales establece una escala morfocromática de cuatro fases de desarrollo gonádico para Haemulon plumieri: inmaduro, en desarrollo, maduro y desovado. Las gónadas se fijaron y preservaron en formol neutro al 10%. Entonces, para investigar las características citológicas de las gónadas, algunas de ellas fueron procesadas histológicamente mediante el siguiente procedimiento: deshidratación en una serie de alcoholes de concentración creciente, inclusión en paraplast, cortes de 5-8μm de grosor y tinción con hematoxilina-eosina. La determinación de los estadios de desarrollo de los ovocitos se basó en las características que describen Yamamoto & Yamazaki (1961), Cerisola (1984) y Lucano-Ramírez et al. (2001b). En el caso del testículo las características se basaron en lo descrito por Hyder (1969).
Además, se calculó la proporción de sexos para la captura total, por año y mes de estudio, y por clase de longitud (intervalos de 4.0cm). La significación estadística de la diferencia con respecto a la proporción 1:1 se determinó mediante la prueba chi-cuadrada (X2) con corrección para continuidad de Yates (Zar 1999).
Para establecer la estacionalidad de la reproducción se graficó la variación mensual de la frecuencia de las fases de desarrollo gonádico por sexo. De cada individuo se calcularon el índice gonadosomático (IGS) y el factor de condición (FC) mediante las expresiones:
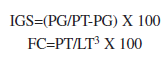
Para el análisis de la tendencia temporal (mensual), tanto de las frecuencias mensuales de desarrollo gonádico como del IGS y del FC se combinaron los datos de los meses iguales de los diferentes años de estudio (año tipo). También, se analizó la variación temporal del IGS y del FC mediante el análisis de varianza (ANDEVA) de una vía y efectos fijos, previa transformación de los datos a logaritmos; cuando fue necesario se aplicó la prueba de comparaciones múltiples de Newman-Keuls (Zar 1999). La variación conjunta del IGS y del FC se analizó mediante la prueba de correlación por rangos de Spearman (rs) (Zar 1999).
Para estimar la longitud de maduración sexual se calculó la longitud en donde 50% de los individuos se encontraron maduros sexualmente (L50), mediante un ajuste no-lineal de la ecuación logística a la fracción de peces maduros (Echeverría 1987) mediante:
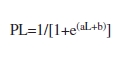
Este modelo se ajustó mediante un método basado en el algoritmo de Levenberg-Maquard (Palazón-Fernández 2007). En los casos donde fue necesario se calculó la media±error estándar (EE). Además, se utilizó un nivel de significación de 0.05. El manejo de datos y algunos cálculos se efectuaron en el programa Excel V. 2007 (Microsoft) y las pruebas estadísticas se realizaron en el programa STATISTICA V. 7.1 (Stat Soft Inc. 2006).
Resultados
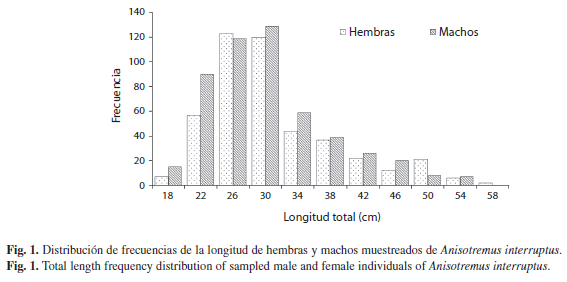
Composición por tallas y proporción sexual: De 1998-2008 se recolectaron en total 1 090 individuos de Anisotremus interruptus. Para esta muestra las longitudes promedio, mínima y máxima fueron de 31.2, 15.6 y 61.0cm, respectivamente; estos mismos valores para hembras y machos fueron 33.0, 18.0, 61.0cm y 32.0, 18.3 y 56.2cm, respectivamente. Mientras que los percentiles de 50% y 90% para las hembras y machos estuvieron entre 27.8-36.7cm y 26.6-35.6cm y entre 25.0-45.2cm y 24.0-43.2cm, respectivamente. Las clases de talla de 22.0-34.0cm presentaron las mayores frecuencias en los dos sexos, en tanto que las menores frecuencias ocurrieron en las clases de 18.0, 54.0 y 58.0cm. Asimismo, se aprecia una clara tendencia de disminución en las frecuencias en las clases de talla 34.0-58.0cm. En la mayoría de las clases de longitud, la frecuencia de machos fue ligeramente mayor que las hembras (Fig. 1).
Ahora bien, se identificó el sexo a 965 organismos de los 1 090 recolectados, de los cuales 452 fueron hembras y 513 fueron machos. En el total de la muestra se presentaron significativamente más machos que hembras (x21=3.86, p=0.049). Sin embargo, en el análisis de la proporción de sexos por año y mes no se encontró diferencia significativa (x210=15.66, p=0.109 y x211=5.10, p=0.073, respectivamente). Por otro lado, con el análisis de la proporción de sexos por clase de talla se encontró que hubo significativamente más machos que hembras (x211,=23.18, p=0.016) en las clases de tallas de 22.0-25.9 y 50.0-53.9cm.
Variación mensual de los estadios de desarrollo gonádico (Fig. 2):
Inmaduro: Fue el estadio más frecuente y se presentó durante todos los meses con una frecuencia superior al 25%. Tanto en las hembras como en los machos, las menores frecuencias se observaron en febrero y mayo, mientras que las mayores frecuencias se registraron durante enero, junio-septiembre y noviembre.
En desarrollo: Este estadio también se presentó en prácticamente todos los meses pero con frecuencias bajas; en las hembras los porcentajes de este estadio fueron menores que en los machos.
Maduro: Al igual que el estadio anterior, también se presentó en prácticamente todos los meses; las mayores frecuencias ocurrieron de febrero-mayo en los dos sexos.
Desovado: Se presentó en todos los meses, aunque en mayor frecuencia en las hembras que en los machos. La tendencia que se observa en ambos sexos es que la mayor actividad reproductiva (suma acumulada de los estadios En desarrollo, Maduro y Desovado), se concentra de febrero-mayo (40-50%), periodo que coincide con las menores frecuencias de individuos inmaduros.
Índice gonadosomático: La tendencia temporal del IGS promedio mostró un patrón muy similar entre sexos (Fig. 3, superior), aunque el promedio general del IGS de las hembras (1.09) fue mayor que el de los machos (0.87) (F1,883=4.14, p=0.042). El IGS mostró diferencias estadísticas entre los meses del año, tanto en las hembras (F11,398=7.45, p=0.0001) como en los machos (F11,463=4.23, p=0.001). Los menores valores del IGS ocurrieron en enero y de junio a diciembre (<1%). En ambos sexos se observaron dos incrementos significativos en el IGS (ANDEVA, p<0.05), uno en febrero y otro en mayo. Las pruebas de comparaciones múltiples de Newman-Keuls del IGS de cada sexo identificaron varios grupos con superposición entre algunos. En las hembras, el promedio del IGS entre febrero y mayo no fue diferente, este último fue diferente al resto de los meses; también el IGS en febrero fue mayor que en julio. En los machos, el IGS en mayo fue mayor al de la mayoría de los meses con excepción de febrero y abril.
Factor de condición: No se presentó diferencia significativa entre los valores promedio de FC de hembras y machos (F1,887=0.393, p=0.530). La tendencia temporal del FC siguió un patrón parecido entre sexos (Fig. 3, inferior). Sin embargo, esta tendencia mensual del FC fue diferente en hembras (F1,11=7.46, p=0.019) y machos (F1,11=5.21, p=0.043). Los valores más altos del FC se observaron entre abril y septiembre, y los más bajos de diciembre a marzo. En los dos sexos los valores del FC presentaron una variación relativamente estrecha con valores promedio, mínimo y máximo de 1.91, 1.26 y 3.4, respectivamente. Las pruebas de comparaciones múltiples de Newman-Keuls del FC de cada sexo identificaron varios grupos con superposición entre algunos. En las hembras, septiembre presentó el FC más alto y difiere de la mayoría de meses a excepción de los meses de mayo a agosto; marzo donde se presentó el menor valor del FC y difiere con la mayoría de meses a excepción de octubre, diciembre a febrero. Abril, mayo, octubre hasta diciembre, ocupan una posición intermedia. En los machos, julio presentó el mayor valor del FC y difiere sólo de los meses de noviembre a marzo, pero no de enero y del resto de los meses; marzo registró el menor valor y difiere de la mayoría de meses excepto de octubre a febrero; varios meses tienen una posición intermedia, de tal forma que no presentaron diferencias con ningún otro mes.
Las tendencias temporales del IGS y el FC mostraron clara diferencia. Los valores más altos del IGS se presentaron en febrero y mayo, entretanto que los mayores valores del FC ocurrieron en julio o septiembre (hembras), lo cual contrasta con la caída en el IGS para estos mismos meses. Es decir, se presentó un desfase o corrimiento en los valores más altos de estos índices (IGS y FC). Se encontró una correlación negativa significativa entre el IGS y FC, tanto en hembras (n=409, rs=-0.246, p<0.05) como en machos (n=474, rs =-0.18, p<0.01). De tal manera que se observó correlación positiva entre el FC de hembras y machos (n=409, rs=0.11, p<0.01). Sin embargo, no se apreció correlación entre el IGS de hembras y machos (n=409, rs=0.013, p=0.782).
Descripción microscópica de las gónadas: Los ovarios están recubiertos externamente por la túnica, a partir de ella se extienden al interior las lamelas ovígeras, en donde penden los ovocitos. En el proceso de desarrollo de los ovocitos de A. interruptus se identificaron las siguientes siete fases de desarrollo: 1) ovocitos cromatina nucléolo: Se caracterizan por presentar poco citoplasma y un núcleo relativamente grande con pocos nucléolos; 2) ovocitos en perinucléolo: Varios nucléolos se localizan en la periferia del núcleo; 3) ovocitos con vesículas vitelinas: En el citoplasma se observan estructuras esféricas como gotas de aceite, lo cual señala el inicio de la formación de vitelo; 4) ovocitos en vitelogénesis primaria: Se observan glóbulos de vitelo en el citoplasma; 5) ovocitos en vitelogénesis secundaria: Glóbulos de vitelo ocupan gran parte del citoplasma; 6) ovocitos en vitelogénesis terciaria: Los glóbulos de vitelo se empiezan a fusionar y el núcleo se encuentra en proceso de migración hacia el polo animal y 7) ovocitos maduros: El vitelo parcial o completamente fusionado, puede ser difícil observar el núcleo en posición excéntrica. Se observaron pocos ovocitos maduros, así como cuerpos atrésicos y folículos postovulatorios. En el ovario se contemplaron ovocitos en diferentes grados de desarrollo, lo que sugiere que A. interruptus presenta un desarrollo ovárico de tipo asincrónico (Fig. 4).
En el ovario en estadio Inmaduro (Fig. 4A), se observaron ovocitos en cromatina nucléolo y en perinucleólo. Ahora bien, en el estadio En desarrollo (Fig. 4B), se presentan ovocitos en varias fases: en cromatina nucléolo, en perinucléolo, con vesículas vitelinas, en vitelogénesis primaria y pocos en vitelogénesis secundaria. En el estadio Maduro (Fig. 4C), se distinguen principalmente ovocitos en vitelogénesis secundaria, aunque, también se pueden presentar otras fases (cromatina nucléolo, perinucléolo, vesículas vitelinas y vitelogénesis primaria). Por último en el estadio Desovado (Fig. 4D), se distinguen ovocitos en diferente fase desarrollo desde cromatina nucléolo a vitelogénesis secundaria, aunque en baja frecuencia.
El testículo se encuentra organizado por lóbulos y su interior está conformado por cistos, dentro de los cuales ocurre todo el proceso de espermatogénesis. Adentro del compartimento lobular, cada cisto tiene un grado de desarrollo diferente de maduración. Una vez formados los espermatozoides son liberados al interior del lóbulo y posteriormente se agrupan en el conducto eferente para ser liberados al exterior. Esta organización celular del testículo indica desarrollo de tipo lobular. En el testículo en estadio Inmaduro (Fig. 5A) se distinguieron cistos con escaso desarrollo celular y en el centro del mismo no se aprecian espermatozoides. Luego, en estadio En desarrollo (Fig. 5B), se presenta mayor crecimiento celular en los cistos y se observan algunos espermatozoides en el centro del testículo. En estadio Maduro (Fig. 5C) se aprecian muchos espermatozoides en el centro de la gónada y en cistos cercanos al mismo. Y en estadio Eyaculado (Fig. 5D), aparecen cistos con área reducida y algunos vacíos (Ci*), así como remanentes de espermatozoides en la parte central del testículo.
Longitud de maduración sexual (L50): Los organismos más pequeños que tuvieron gónadas en estadio de desarrollo midieron 22.5cm LT, por lo tanto, todas las hembras y machos con longitud menor a ésta fueron inmaduros. Organismos de 30.0cm LT presentaron porcentajes de maduración entre 40-50% en hembras y machos, respectivamente. El 100% de hembras y machos maduros se mostraron en aquellos mayores a 36.0cm LT. El modelo logístico ajustado, permitió estimar que el 50% de las hembras de A. interruptus alcanzan la madurez sexual a los 31.0cm LT, mientras que, los machos lo hacen a los 29.7cm LT. Los porcentajes de maduración observados en hembras y machos presentaron una distribución muy similar; de igual forma los valores calculados con el modelo logístico presentaron un buen ajuste (r2=0.99) a los valores observados en los dos sexos (Fig. 6).
Discusión
En este trabajo, la talla máxima de A. interruptus fue de 61.0cm. Los estudios sobre esta especie han encontrado valores muy cercanos (60.5cm, Espino-Barr et al. 2003; 62.1cm, Espino-Barr et al. 2004b). En contraste, otros estudios señalan valores relativamente menores (46.0cm, McKay & Schneider 1995; 46.0cm, Allen & Robertson 1998; 46.0cm, Thomson et al. 2000; 51.0cm, Jiménez-Prado & Béarez 2004) o mayores (90.0cm, Amezcua-Linares 1996). En este estudio la talla promedio de A. interruptus fue de 31.7cm, la cual no está muy alejada de las reportadas en otros trabajos (30.0cm, McKay & Schneider 1995; 34.7cm Espino-Barr et al. 2003; 35.1cm, Espino-Barr et al. 2004b). Las discrepancias en las tallas encontradas podrían deberse a diferencias en el tamaño de muestra, el sitio de recolecta y el arte de pesca escogidos.
La proporción de sexos en A. interruptus presentó diferencias en dos de las cuatro variantes analizadas. En el análisis de toda la muestra el valor de chi-cuadrado calculado (3.85) es muy cercano del valor crítico (3.84) el cual permite decidir si se acepta o rechaza la hipótesis de la proporción 1:1. A su vez, en el análisis de la proporción de sexos por clase de longitud, el valor de chi-cuadrado alto, proviene principalmente de los valores parciales de sólo dos de las 12 clases de talla analizadas. Con base en lo anterior, se considera que no hay una clara tendencia en la proporción de sexos en A. interruptus. Otros estudios han encontrado que la proporción de sexos puede variar de un año a otro en una misma población, pero en la mayoría de las especies de peces la proporción es muy cercana a uno (Nikolsky 1963). Cuando la proporción de sexos está sesgada se le relaciona a diferencias por crecimiento, mortalidad, costos energéticos de la reproducción y migración diferencial o segregación espacial por sexo (Sadovy & Shapiro 1987, Stergiou et al. 1996).
Este es el primer trabajo que aborda la reproducción de A. interruptus, a pesar de que esta especie tiene amplia distribución en el Pacífico y es de gran importancia en la región de estudio. Varios autores han señalado en diferentes especies de peces que el IGS puede ser un indicador confiable del periodo reproductivo (Arellano-Martínez & Ceballos-Vázquez 2001, González & Oyarzún 2002, Palomera-Sánchez 2004, Lucano-Ramírez et al. 2001c, 2005, 2006, Sánchez-Cárdenas et al. 2007, Piñón et al. 2009). En este caso, el IGS es un indicador aceptable del principal periodo de reproducción en A. interruptus, (febrero-mayo). La presencia de organismos desovados en todos los meses, así como de individuos con gónadas maduras en varios meses, sugiere que ocurren desoves aislados en gran parte del año y no está restringido a un solo periodo reproductivo al año. Esta última característica también se ha observado en Haemulon plumieri (Haemulidae; Palazón-Fernández 2007) en la Isla Margarita, Venezuela.
En un estudio sobre Schizodon fasciatus, Fabre & Saint-Paul (1998) encontraron que el periodo de menor crecimiento ocurrió en enero y febrero, justo cuando las gónadas estaban en proceso de maduración. En este mismo sentido, Gallardo-Cabello et al. (2003), encontraron que el menor incremento marginal en el crecimiento de las escamas de A. interruptus ocurrió en el mes de abril, esto coincide temporalmente con el principal periodo reproductivo encontrado en este estudio.
También, se registraron valores bajos del FC antes del pico reproductivo lo que puede estar relacionado con la movilización de reservas de energía somáticas, las cuales son necesarias para la actividad reproductiva, y/o con una reducción en la actividad de alimentación durante el periodo de desove (Maddock & Burton 1999, Palazón-Fernández 2007). García-Cagide (1986) encontró marcadas diferencias en el FC de Haemulon sciurus y propone que estos cambios estuvieron relacionados a la temperatura del agua, el suministro de alimento, el crecimiento y la actividad reproductiva. En este trabajo el FC y el IGS se correlacionan de forma negativa tanto en hembras como en machos. Un resultado similar fue reportado para H. aurolineatum entre los índices de las hembras, pero no con los machos (Kossowski 1985). Correlación negativa entre estos índices también se encontró en Holocanthus passer en el Golfo de California (Arellano-Martínez & Ceballos-Vázquez 2001). En peces tropicales, el FC puede disminuir durante la temporada de desove debido a una pérdida en el peso corporal de aproximadamente 10% (García-Cagide et al. 1983).
La edad-talla de primera reproducción en peces puede variar ampliamente tanto intra como interespecíficamente. Esta variación está moldeada principalmente por el ambiente en el que habitan (Berg & Finstad 2008). Espino-Barr et al (2004a) mencionan que en A. interruptus la edad de primera madurez es de tres años con una longitud patrón o estándar de 22.0cm (que corresponde a 29.2cm de LT). Este valor está próximo a las tallas de maduración promedio encontradas en este estudio (hembras L50=31.0cm y machos L50=29.7cm). En A. interruptus al parecer la edad-talla de primera maduración ha presentado poca variación temporal.
Al comparar la talla promedio de maduración (L50) en hembras (31.0cm) y machos (30.7cm) con la talla promedio de toda la muestra (31.7cm) se concluye que aproximadamente 58% de los organismos capturados fueron inmaduros, lo cual coincide con los resultados de estadios de madurez. Resultados similares encontraron Espino-Barr et al. (2004a) en cuyo trabajo 66% de la captura incluyó individuos pre adultos, lo que implica que la mayoría de la población no alcanza la edad (y talla) para la primera reproducción y pudiera darse a mediano o largo plazo una situación de sobrepesca que comprometa la explotación.
Agradecimientos
A Manuel Díaz, Daniel y Gerardo Kosonoy, por su ayuda en las actividades de pesca. A las cooperativas pesqueras “Melaque” y “Punta Farallón” por facilitar sus instalaciones. A la Universidad de Guadalajara por el financiamiento y a los estudiantes del Departamento de Estudios para el Desarrollo Sustentable de Zonas Costeras, que colaboraron en la obtención de datos biológicos y el trabajo de laboratorio.
Referencias
Aguilar-Palomino, B., C. Pérez-Reyes, F. Galván-Magaña & L.A. Abítia-Cárdenas. 2001. Ictiofauna de la Bahía de Navidad, Jalisco, México. Rev. Biol. Trop. 49: 173 190 (también disponible en línea: ww.biologiatropical.ucr.ac.cr/attachments/volumes/vol49-1/19-Aguilar-Ictiofauna-171-188.pdf). [ Links ]
Al-Husaini, M., A. Al-Baz, S. Al-Ayoub, S. Safar, Z. Alwazan & S. Al-Jazzaf. 2001. Age, growth, mortality, and yield-per-recruit for nagroor, Pomadasys kaakan, in Kuwait’s waters. Fish. Res. 59: 101-115. [ Links ]
Aldaco-González, C.L. 2007. Caracterización de la pesquería artesanal de redes de enmalle en Bahía de Navidad, Jalisco. Tesis de licenciatura, Universidad de Guadalajara, Autlán de Navarro, Jalisco, México. [ Links ]
Allen, G.R. & D.R. Robertson. 1998. Peces del pacífico oriental tropical. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad y Agrupación Sierra Madre, Ciudad de México, México. [ Links ]
Amezcua-Linares, F. 1996. Peces demersales de la plataforma continental del pacífico central de México. Instituto de Ciencias del Mar y Limnología, UNAM, Ciudad de México, México. [ Links ]
Arellano-Martínez, M. & B.P. Ceballos-Vázquez. 2001. Reproductive activity and condition index of Holacanthus passer (Teleostei: Pomacanthidae) in the Gulf of California, México. Rev. Biol. Trop. 49: 939-943 (también disponible en línea: www.biologiatropical.ucr.ac.cr/attachments/volumes/vol49-34/13_Arellano_Reproductive.pdf). [ Links ]
Berg, O.K. & A.G. Finstad. 2008. Energetic trade-off in reproduction: cost benefit considerations and plasticity, p. 351-375. In M.J. Rocha, A. Arukwe & B.C. Kapoor (eds.). Fish reproduction. Science, Edenbridge Ltd., New Hampshire, EEUU. [ Links ]
Cerisola, H. 1984. Cambios estructurales del folículo ovárico durante su maduración en el pejesapo Sicyases sanguineus, Muller y Troschel 1843. (Gobiescocidae: Teleostei). Rev. Biol. Mar. 20: 1-21. [ Links ]
Chakroun-Marzouk, N. & K. Mohamed-Hédi. 2006. Caractésitiques de la reproducton et de la croissance pondérale relative de Pomadasys incisus (Haemulidae) du Golfe de Tunis. Cybium 30: 333-342. [ Links ]
Cruz-Romero, M., E. Espino-Barr & A. García-Boa. 1993. Aspectos poblacionales de cinco especies de la familia Haemulidae (Pisces) en la costa de Colima, México. Cienc. Pesq. 10: 43-54. [ Links ]
Echeverría, T.W. 1987.Thirty-four species of California rockfishes: maturity and seasonality of reproduction. Fish. Bull. 85: 229-250. [ Links ]
Espino-Barr, E., M. Gallardo-Cabello & M. Cruz-Romero. 2003. Peces marinos con valor comercial de la costa de Colima, México. CONABIO, INP, CRIP, Manzanillo, México. [ Links ]
Espino-Barr, E., M. Gallardo-Cabello, F. González-Orozco & A. García-Boa. 2004a. Análisis del crecimiento y la mortalidad de Anisotremus interruptus (Gill) (Perciformes: Haemulidae) en la costa de Colima, México. Bol. Invest. Mar. Cost. 33: 69-77. [ Links ]
Espino-Barr, E., E.G. Cabral-Solís, A. García-Boa & M. Puente-Gómez. 2004b. Especies marinas con valor comercial de la costa de Jalisco, México. SAGARPA, INP, CRIP, Manzanillo, México. [ Links ]
Fabre, N.N. & U. Saint-Paul. 1998. Annulus formation on scales and seasonal growth of the central Amazonian anostomid Schizodon fasciatus J. Fish Biol. 53: 1-11. [ Links ]
Gallardo-Cabello, M., E. Espino-Barr, F. González-Orozco & A. García-Boa. 2003. Age determination of Anisotremus interruptus (Perciformes: Haemulidae) by scale reading, in the coast of Colima, Mexico. Rev. Biol. Trop. 51: 519-528 (también disponible en línea: www.biologiatropical.ucr.ac.cr/attachments/volumes/ vol51-2/23-GALLARDO-AGE.pdf). [ Links ]
García-Cagide, A. 1986. Características de la reproducción del ronco amarillo, Haemulon sciurus, en la región oriental del Golfo de Batabanó, Cuba. Rep. Invest. Inst. Oceanol. Acad. Cienc. Cuba 48: 1-28. [ Links ]
García-Cagide, A., R. Claro & B.V. Koshelev.1983. Peculiaridades de los ciclos reproductivos de los peces de diferentes latitudes. Rep. Invest. Inst. Oceanol. Acad.
Cienc. Cuba 21: 1-14. [ Links ]
Godínez-Domínguez, E., J. Rojo-Vázquez, V. Galván-Piña & B. Aguilar-Palomino. 2000. Changes in the structure of a coastal fish assemblage exploited by a small scale gillnet fishery during an El Niño-La Niña event. Estuarine, Coastal Shelf Sci. 51: 773-787. [ Links ]
González, P. & C. Oyarzún. 2002. Variabilidad de índices biológicos en Pinguipes chilensis Valenciennes 1833 (Perciformes, Pinguipedidae): ¿Están realmente correlacionados? Gayana 66: 249-253. [ Links ]
Hyder, M. 1969. Histological studies on the testis of tilapia leucosticta and other species of the genus Tilapia (Pisces:Teleostei). Trans. Am. Microsc. Soc. 88: 211-231. [ Links ]
Jiménez-Prado, P. & P. Béarez. 2004. Peces marinos del Ecuador continental. Tomo 2: Guía de especies. Quito, Ecuador. [ Links ]
Kossowski, A. 1985. Reproducción del cují, Haemulon aurolineatum (Cuvier, 1829) (Pisces: Haemulidae) de la isla de Margarita, Venezuela. Tesis de Licenciatura, Universidad de Oriente, Cumaná, Venezuela. [ Links ]
León-Arriola, A.M. 2010. Análisis de la captura obtenida por la pesquería de redes de enmalle en la Bahía de Chamela, Jalisco. Tesis de Licenciatura, Universidad de Guadalajara, Autlán de Navarro, Jalisco, México. [ Links ]
Lucano-Ramírez, G., S. Ruiz-Ramírez, B. Aguilar-Palomino & J.A. Rojo-Vázquez. 2001a. Listado de especies de peces de la región costera de Jalisco y Colima, México. Ciencia y Mar 15: 13-20. [ Links ]
Lucano-Ramírez, G., M. Villagrán-Santa Cruz, S. Ruiz-Ramírez & M.T. López-Trujillo. 2001b. Histología de los ovocitos de Lutjanus peru (Nichols y Murphy, 1922) (Pisces: Lutjanidae). Cienc. Mar. 3: 335-349. [ Links ]
Lucano-Ramírez, G., M. Villagrán-Santa Cruz & S. Ruiz-Ramírez. 2001c. Cambios estructurales en las gónadas de Lutjanus peru (Pisces:Lutjanidae), en la Costa sur de Jalisco, México. Bol. Centro Invest. Biol. 35: 295-316. [ Links ]
Lucano-Ramírez, G., S. Ruiz-Ramírez & J.A. Rojo-Vázquez. 2005. Biología reproductiva de Prionotus ruscarius (Pisces:Triglidae) en las costas de Jalisco y Colima, México. Revista Digital Universitaria 6: 13 (también disponible en línea: www.revista.unam.mx/ vol.6/num8/art75/int75.htm). [ Links ]
Lucano-Ramírez, G., S. Ruiz-Ramírez & J.A. Rojo-Vázquez. 2006. Composición por tallas y ciclo reproductivo de Pseudopeneus grandisquamis (Pisces:Mullidae) en el Pacífico central mexicano. Rev. Biol. Trop. 54: 195-207 (también disponible en línea: www.biologiatropical.ucr.ac.cr/attachments/volumes/vol54-1/20-LUCANO-Composici.pdf). [ Links ]
McKay, R.J. & M. Schneider. 1995. Haemulidae. Burros, corocoros, chulas, gallinazos, roncos, p. 1136-1173. In W. Fischer, F. Krupp, W. Schneider, C. Sommer, K.E. Carpenter & V. Niem (eds.). Guía FAO para identificación de especies para los fines de la pesca. Pacifico Centro-Oriental, Vol. 2, FAO, Roma, Italia. [ Links ]
Maddock, D.M. & M.P. Burton. 1999. Gross and histological observations of ovarian development and related condition changes in American Plaice. J. Fish Biol. 53: 928-944. [ Links ]
Moazzam, M., H.B. Osmany, K. Zohra & H. Manzoor. 2006. Review of family Haemulidae occurring in Pakistan. Rec. Zool. Surv. 17: 41-64. [ Links ]
Nikolsky, G. 1963. The ecology of fishes. Academic, Londres, Inglaterra. [ Links ]
Palazón-Fernández, J.L. 2007. Reproduction of the White grunt, Haemulon plumieri (Lacépede, 1802) (Pisces: Haemulidae) from Margarita Island, Venezuela. Sci. Mar. 71: 429-440. [ Links ]
Palomera-Sánchez, F.I. 2004. Características reproductivas de Scomberomorus sierra Jordan y Starks 1895 (PISCES: SCOMBRIDAE) en Bahía Navidad, Jalisco, México. Tesis de Licenciatura, Universidad de Guadalajara, Autlán de Navarro, Jalisco, México. [ Links ]
Piñón, A., F. Amezcua & N. Duncan. 2009. Reproductive cycle of female yellow snapper Lutjanus argentiventris (Pisces, Actinopterygii, Lutjanidae) in the SW Gulf of California: gonadic stages, spawning seasonality and length at sexual maturity. J. Appl. Ichthyol. 25: 18-25. [ Links ]
Rodríguez-Ibarra, L.E. 1995. Ictiofauna de la región de la Bahía de Navidad, Jalisco, México. Tesis de Licenciatura, Universidad de Guadalajara, Autlán de Navarro, Jalisco, México. [ Links ]
Rojo-Vázquez, J.A. 1997. Selectividad y eficiencia de redes de enmalle en Bahía de Navidad, Jalisco, México. Tesis de Maestría, Centro Interdisciplinario de Ciencias Marinas Instituto Politécnico Nacional (CICIMAR- IPN), México. [ Links ]
Rojo-Vázquez, J.A. & M. Ramírez-Rodríguez. 1997. Composición específica de la captura con redes de enmalle en Bahía de Navidad, Jalisco, México. Oceánides 12: 121-126. [ Links ]
Rojo-Vázquez, J.A., B. Aguilar-Palomino, V.H. Galván-Piña, E. Godínez-Domínguez, S. Hernández-Vázquez, S. Ruiz-Ramírez & G. Lucano-Ramírez. 2001. Ictiofauna de la pesquería en Bahía de Navidad, Jalisco, México, asociada al evento de El Niño 1997-1998. Rev. Biol. Trop. 49: 915-929 (también disponible en línea: www.biologiatropical.ucr.ac.cr/attachments/volumes/vol49-3-4/11_Rojo_Ictiofauna.pdf). [ Links ]
Rojo-Vázquez, J.A., C. Quiñonez-Velázquez, H.A. Echavarría-Heras, G. Lucano-Ramírez, E. Godínez-Domínguez, S. Ruiz-Ramírez, V.H. Galván-Piña & O. Sosa-Nishizaki. 2008. The fish species composition and variation of catch from the small-scale gillnet fishery before, during and after the 1997-1998 ENSO event, central Mexican Pacific. Rev. Biol. Trop. 56: 133-152 (también disponible en línea: ww.latindex.ucr.ac.cr/rbt-56-1/09-Rojo-Fish.pdf). [ Links ]
Rojo-Vázquez, J.A., G. Lucano-Ramírez & S. Ruiz-Ramírez. 2009. Length-weight relationships for coastal fish species from the gillnet artisanal fishery in the central Mexican Pacific. J. Appl. Ichthyol. 25: 497-498. [ Links ]
Rojo-Vázquez, J.A., E. Godínez-Domínguez, V.H. Galván-Piña, S. Hernández-Vázquez, M.C. Franco-Gordo & G. González-Sansón. 2010. Diversidad de peces de la plataforma continental de Jalisco y Colima, México, p. 127-1153. In E. Godínez-Domínguez, M.C. Franco-Gordo, J.A. Rojo-Vázquez, F.A. Silva-Bátiz & G. González-Sansón (eds.). Ecosistemas marinos de la costa sur de Jalisco y Colima. Universidad de Guadalajara, Autlán de Navarro, Jalisco, México. [ Links ]
Sadovy, Y. & D. Shapiro. 1987. Criteria for the diagnosis of hermaphroditism in fishes. Copeia 1987: 136-156. [ Links ]
Sánchez-Cárdenas, R., B.P. Ceballos-Vázquez, M. Arellano-Martínez, M.C. Valdez-Pineda & R.E. Morán-Angulo. 2007. Reproductive aspects of Sphoeroides annulatus (Jenyns, 1842) (Tetraodontiformes, Tetraodontidae) inhabiting the Mazatlan coast, Sinaloa, Mexico. Rev. Biol. Mar. Oceanog. 42: 385-392 (también disponible en línea: www.revbiolmar.cl/resumenes/v423/423-385.pdf). [ Links ]
Stergiou, K.I., P. Economidis & A. Sinis. 1996. Sex ratio, spawning season and size at maturity of red brand fish in the western Aegean Sea. J. Fish Biol. 49: 561-572. [ Links ]
Thomson, D.A., L.T. Findley & A.N. Kerstitch. 2000. Reef fishes of the Sea of Cortez. The rocky-shore fishes of the Gulf of California. The University of Arizona, Tucson, Arizona, EEUU. [ Links ]
Yamamoto, K. & M. Yamazaki. 1961. Rhythm of development in the oocyte of the gold-fish, Carassius Auratus. Bull. Fac. Fish. Hokkaido Univ. 12: 93-114. [ Links ]
Zar, J.H. 1999. Bioestatistical analysis. Prentice Hall, Nueva Jersey, EEUU. [ Links ]
*Correspondencia a: Salvador Ruiz-Ramírez, Gabriela Lucano-Ramírez, Gaspar González-Sansón & J.A. Rojo-Vázquez: Departamento de Estudios para el Desarrollo Sustentable de Zonas Costeras Universidad de Guadalajara, V. Gómez Farías 82, San Patricio-Melaque, Jalisco, México. 48980; sruizram@costera.melaque.udg.mx, lucanorg@costera.melaque.udg.mx, gaspargonzalez2001@yahoo.es
Marcial Arellano-Martínez: Laboratorio de Invertebrados Marinos, Centro Interdisciplinario de Ciencias Marinas, Instituto Politécnico Nacional, Apartado Postal 592, 23000, La Paz, Baja California Sur, México; marellam@ipn.mx
1. Departamento de Estudios para el Desarrollo Sustentable de Zonas Costeras Universidad de Guadalajara, V. Gómez Farías 82, San Patricio-Melaque, Jalisco, México. 48980; sruizram@costera.melaque.udg.mx, lucanorg@costera.melaque.udg.mx, gaspargonzalez2001@yahoo.es
2. Laboratorio de Invertebrados Marinos, Centro Interdisciplinario de Ciencias Marinas, Instituto Politécnico Nacional, Apartado Postal 592, 23000, La Paz, Baja California Sur, México; marellam@ipn.mx
Recibido 22-III-2011. Corregido 29-VIII-2011. Aceptado 27-IX-2011.