1.Introducción
Desde la publicación del concepto de síndromes coronarios crónicos (SCC) en las guías europeas de 2019 -que presentan la enfermedad coronaria como un continuo dinámico-, diversas guías y sociedades internacionales han ampliado su enfoque diagnóstico y terapéutico. En este nuevo marco, la angina estable ha dejado de considerarse una entidad patológica aislada para entenderse como uno de los múltiples escenarios clínicos de la compleja y heterogénea enfermedad isquémica cardiaca. Si bien la aterosclerosis se reconoce como uno de los principales mecanismos subyacentes, no es el único implicado en su etiología.
Esto también ha dado pie a una revisión continua de las terapéuticas y la evidencia alrededor de las recomendaciones, ya que cada vez es más claro que no existe un abordaje único, no existe una terapéutica estándar, pero, sobre todo, no existen estudios suficientes para responder a este heterogéneo grupo de pacientes.
Es imperioso enfatizar que se trata de una enfermedad que se manifiesta dentro de un continuo entre síndromes coronarios agudos y síndromes coronarios crónicos; puede permanecer estable durante periodos largos, pero también puede desestabilizarse en cualquier momento, generalmente como resultado de un evento aterotrombótico agudo provocado por la rotura o la erosión de la placa (1).
Fisiopatológicamente, es un proceso dinámico donde la acumulación de placas ateroescleróticas y las alteraciones funcionales de la circulación (vasoespasmo o enfermedad de la microcirculación) pueden llegar a ser modificadas por cambios en el estilo de vida, terapias farmacológicas o la revascularización. Esto repercute en la estabilización e, incluso, en la regresión de la enfermedad. Es importante señalar que, aun en las fases clínicamente latentes de este continuo isquémico, rara vez es una condición silente y requiere de esfuerzos conscientes y constantes entre el paciente y el médico para prevenir la progresión de la enfermedad.
El grupo de médicos que participó en la elaboración de estas recomendaciones fue encabezado por la Dra. Castillo, con la participación de al menos un médico de cada país Centroamericano, con la intención de obtener la experiencia de primera mano de médicos tratantes de SCC, que además conocen los sistemas de salud de cada uno de sus países. De esta forma se garantiza que las recomendaciones seleccionadas puedan aplicarse en las condiciones actuales de los sistemas de salud en la región Centroamericana.
2.Métodos
Ha sido este interés en los SCC, el que agrupó a un conjunto de cardiólogos de las diferentes sociedades centroamericanas para discutir y discernir sobre la última evidencia escrita y reunir en un solo documento los principales lineamientos y posturas. Durante las reuniones, realizadas de enero a mayo de 2024, se analizaron las guías de práctica clínica más recientemente publicadas que incluyen la guía de la Sociedad Europea de Cardiología (ESC) de 2019 - 2024, y la Guía de la American Heart Association/American College of Cardiology (AHA/ACC) de 2023.
Esta recopilación de recomendaciones fue una iniciativa de médicos de los países Centroamericanos (Costa Rica, El Salvador, Guatemala, Honduras, Nicaragua, Panamá y República Dominicana), encabezados por la Dra. Castillo, quién invitó a expertos en SCC de cada país para participar en el equipo de trabajo. Los participantes se dividieron en grupos para analizar la evidencia. Las reuniones se realizaron de forma virtual, con el fin de analizar cada una de las secciones incluidas en este documento, tomando en cuenta las condiciones de los servicios de cardiología de esta región. Por ello, solo se han incluido las recomendaciones que se consideraron adecuadas y aplicables, con base en el acceso a equipamiento, instalaciones y servicios disponibles en nuestros países. Las principales discrepancias que se observaron fueron en la aplicabilidad de las recomendaciones, según las características de cada sistema de salud, por lo que algunas recomendaciones son múltiples para abarcar la heterogeneidad de la región.
Se debe tener en cuenta que estas recomendaciones brindan un marco general para el cuidado del paciente, pero en última instancia, el médico debe tomar la decisión final, en consulta con el paciente y, si es necesario, con la persona responsable del cuidado del paciente.
Para el desarrollo de este documento, se empleó la clasificación de niveles de evidencia y grado de recomendación presentadas en la guía ESC 2024 (2).
A lo largo de este documento se utilizarán las siguientes abreviaturas:
3. Escenarios clínicos
Este documento se reconoce e identifica cinco escenarios clínicos (2):
El paciente sintomático con angina o isquemia demostrada en estudios de estrés con enfermedad obstructiva de la circulación epicárdica.
El paciente con angina o isquemia causada por anormalidades vasomotoras o alteraciones estructurales de la microcirculación epicárdica en ausencia de enfermedad obstructiva de la circulación (ANOCA/INOCA).
El paciente en el contexto no agudo post-síndrome coronario agudo o después de la revascularización.
El paciente con falla cardiaca en el contexto no agudo.
Son los individuos asintomáticos en los que se detecta una enfermedad coronaria aguda epicárdica durante una prueba de imagen para afinar la evaluación del riesgo cardiovascular
3.1 Conceptos clave
Reconocer que la angina no es la única manifestación de la patología coronaria y cada vez más se fomenta la interrogación e inclusión de la disnea como equivalente anginoso.
Abandonar el término de angina estable, ya que lleva a confusiones y simplificaciones que pueden desencadenar un abordaje erróneo o incompleto del paciente; el término “estable” no puede estar más alejado del comportamiento real de la circulación, además de que puede condicionar a una etiología exclusiva de placa y subestimando el comportamiento de la microcirculación y vasoespasmo.
3.2 Abordaje clínico y diagnóstico
A pesar de que la angina de pecho es el síntoma descrito más característico asociado a los SCC, la disnea debe ser reconocida como un equivalente anginoso, o bien, el paciente puede cursar libre de síntomas. En el caso de angina y disnea se recomienda utilizar algún tipo de clasificación que permita caracterizar gatillantes y limitantes dentro de la condición física del paciente; se identifican la clasificación Diamond y la de la Asociación Canadiense Cardiovascular, las más frecuentemente utilizadas en la región (2).
Antes de considerar la realización de pruebas diagnósticas, confirmatorias o pronósticos, se recomienda que la historia clínica de los SCC explore tres condiciones que pueden optimizar los recursos:
El estado general de salud (funcionalidad, dependencia y fragilidad como determinantes pronósticos)
Las comorbilidades (interacciones, estabilidad y complicaciones) y la reversibilidad de sus consecuencias.
La calidad de vida del paciente.
Basándose en estos tres factores, existen primicias que nos permiten guiar el abordaje del SCC:
No se recomienda estudiar a ningún paciente con SCC que no presente cambios clínicos o que mantengan una buena capacidad funcional (3).
Ofrecer el mejor tratamiento médico según guías, incluso antes de sugerir algún tipo de estudio de tamizaje o estratificación (3).
Si la revascularización no es una opción viable o aceptable, se limitan las pruebas diagnósticas a lo mínimo clínicamente indicado y se inicia un tratamiento farmacológico adecuado, que puede incluir fármacos antianginosos, incluso, si no se tiene el diagnóstico definitivo de enfermedad coronaria (1).
Se recomienda una evaluación pretest de la enfermedad coronaria para determinar los estudios diagnósticos.
Realizar los estudios básicos de gabinete y laboratorio: Electrocardiograma (ECG) en reposo, bioquímica sanguínea, radiografía de tórax (RT) a pacientes seleccionados y una ecocardiografía en reposo (pese a no ser una herramienta diagnóstica por sí sola, conocer la contractilidad basal es un factor determinante para la selección terapéutica a posteriori).
En el anexo A (sección 8.1) se presenta la probabilidad pretest de enfermedad coronaria obstructiva recomendada por la ESC y un esquema que presenta los factores determinantes de la probabilidad clínica de enfermedad coronaria obstructiva.
3.3 Herramientas diagnósticas recomendadas
Los múltiples escenarios clínicos descritos comprenden poblaciones muy heterogéneas y en diversos momentos de la enfermedad con diferentes pronósticos; por lo tanto, el estudio diagnóstico tampoco es único para su identificación y/o estratificación.
Existe una gama amplia de estudios diagnósticos (Ecocardiograma de estrés, angiotomografía coronaria (angioTC), angiografía invasiva diagnóstica, resonancia magnética cardiaca (RMC), tomografía por emisión de positrones / tomografía por emisión de fotón simple (PET/SPECT)) con diferentes fortalezas, costos, aprendizajes y reproducibilidad; por lo antes de definir cuál utilizar y a fin de dar un uso más apropiado de los recursos, se recomienda:
Ofrecer pruebas diagnósticas según la probabilidad pretest clínica, las características y preferencias del paciente y la disponibilidad y la experiencia del centro.
Como primera línea se recomienda el uso de imágenes funcionales no invasivas para detectar isquemia, tipo ecocardiograma de estrés ejercicio o farmacológico (por su amplia disponibilidad en la región, capacitación y costo) y complementar en casos específicos con imágenes anatómicas mediante angioTC, cuando existe necesidad de profundizar o definir con mayor precisión la patología coronaria (1).
Es importante tener en cuenta, que, si bien el estudio funcional puede ser negativo para inducción de isquemia, no descarta la presencia de ateroesclerosis coronaria, por lo tanto, se debe insistir en corregir los factores de riesgo y prescribir tratamiento con base en guías de prevención primaria (1).
En el anexo A (sección 8.2) se presenta un esquema con las estrategias diagnósticas para pacientes con sospecha de EC obstructiva.
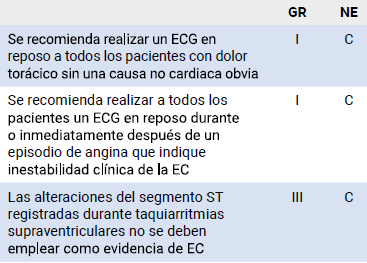
Electrocardiograma
El diagnóstico de angina Prinzmetal y vasoespástica se basa en la detección de una elevación o depresión transitoria del segmento ST durante el ataque anginoso (usualmente en reposo). Condición clínica en donde el electrocardiograma se vuelve una herramienta primordial (4,5).
Monitoreo electrocardiográfico ambulatorio (Holter cardiaco)
El ECG ambulatorio permite identificar episodios de isquemia miocárdica asintomática, es decir, isquemia silente, que de otra manera podrían pasar desapercibidos (6,7). Esto es especialmente importante en pacientes con diabetes u otras condiciones que pueden enmascarar los síntomas de angina (8).
Sin embargo, es importante señalar que las estrategias terapéuticas dirigidas a la isquemia silente detectada en la monitorización ambulatoria no han mostrado beneficios claros en supervivencia.
3.6 Prueba de esfuerzo
Aunque el ECG de esfuerzo es una herramienta valiosa, tiene limitaciones en la detección de isquemia, especialmente en pacientes con enfermedad coronaria crónica que pueden presentar isquemia silente o cambios electrocardiográficos atípicos que no se reflejan adecuadamente durante la prueba de esfuerzo (12).
Pese a tener un rendimiento diagnóstico menor para considerar o descartar la presencia de EC obstructiva sigue siendo una herramienta de alta difusión y uso en la región Centroamericana; este documento insta a aumentar el rendimiento con la combinación de imágenes e identificar aquellas condiciones basales donde se pierde el valor diagnóstico, por ejemplo: bloqueo de rama izquierda del Haz de Hiz, ritmo de marcapaso, síndrome de Wolff-Parkinson-White con depresión del ST mayor de 0.1 mm en reposo o pacientes tratados con digital (1).
3.7 AngioTC coronario
* Pruebas funcionales invasivas (iFR: índice diastólico instantáneo sin ondas; RFF: reserva fraccional de flujo).
En la región Centroamericana, la tomografía computarizada es una de las técnicas diagnósticas más accesibles y presenta beneficios significativos. Una angioTC tiene un alto valor predictivo negativo para descartar una enfermedad coronaria significativa en pacientes con dolor torácico (13).
La interpretación debe ser realizada por un médico radiólogo o cardiólogo entrenado formalmente en estas técnicas de imagen.
3.8 Angiografía Coronaria Invasiva
La angiografía coronaria invasiva se considera el estándar de oro en el estudio de pacientes con enfermedad coronaria, permitiendo una visualización directa y detallada de las arterias coronarias, lo que facilita la detección de estenosis y obstrucciones significativas (14). En nuestra región es un recurso limitado y de difícil acceso para la población general, se hace énfasis en que no se recomienda para diagnóstico de primera línea, estratificación de los pacientes, y/o guiar terapéutica; teniendo opciones de menor costo, acceso y alto rendimiento.
3.9 Criterios de alto riesgo para la angiografía coronaria invasiva
Aunque múltiples estudios aleatorizados (COURAGE, ISCHEMIA y BARI 2D) han demostrado que la revascularización de rutina no reduce los eventos adversos cardiovasculares mayores (EACM), una evaluación integral que contemple la sintomatología, el perfil de riesgo individual y las condiciones clínicas específicas -como la angina persistente o la insuficiencia cardiaca con fracción de eyección reducida- resulta fundamental para identificar a aquellos pacientes con síndrome coronario crónico que sí podrían beneficiarse significativamente de la revascularización (24).
3.10 Criterios de alto riesgo para las distintas pruebas diagnósticas
Definición de alto riesgo de eventos para distintos tipos de pruebas en pacientes con síndrome coronario crónico establecido (18,25,26).
ACI: angiografía coronaria invasiva; AngioTC: angiografía por tomografía computarizada; ECG: electrocardiograma; iFR: índice diastólico instantáneo sin ondas; PET: tomografía por emisión de positrones; RFF: reserva fraccional de flujo; RMC: resonancia magnética coronaria; SPECT: tomografía por emisión de fotón único; TCI: tronco común izquierdo. Fuente: guía ESC 2019
Tratamiento SCC
El objetivo principal del tratamiento farmacológico en pacientes con síndrome coronario crónico es el control de los síntomas, la prevención de eventos ad- versos cardiovasculares y el manejo integral de las comorbilidades, todo ello de manera individualizada y optimizada para cada paciente (27). A través del control de los factores de riesgo, la disminución de la carga isquémica y la prevención de complicaciones trombóticas (27).
4.1. Conductas terapéuticas
En los pacientes con SCC, los resultados de los estudios no invasivos e invasivos por sí solos no son suficientes para estratificar de forma correcta el riesgo cardiovascular individual anual, ni el riesgo futuro de muerte cardiovascular (CV) o IAM no fatal.
Es importante destacar que estas puntuaciones de riesgo deben utilizarse de manera integrada con la evaluación clínica, antecedentes y pruebas diagnósticas del paciente para realizar una estratificación de riesgo cardiovascular precisa y guiar el manejo terapéutico en pacientes con síndrome coronario crónico (32).
4.2. Determinantes sociales de la salud
Identificar los determinantes sociales de la salud (DSS) en pacientes con SCC implica evaluar las condiciones de vida, el nivel educativo, el ingreso eco- nómico, la red de apoyo social, el acceso a recursos y servicios de salud, y los factores ambientales que pueden influir en la salud y el manejo de la enferme- dad cardiovascular en estos pacientes. Estos deter- minantes subrayan la importancia de abordar los factores sociales en la atención de los pacientes con síndrome coronario crónico para mejorar los resulta- dos sanitarios y reducir las disparidades en la salud cardiovascular (33).
En pacientes con enfermedades crónicas, existe evidencia empírica que apoya el uso de herramientas de evaluación de los determinantes sociales de la salud en el escenario clínico, facilitando el abordaje individualizado y a la medida de los planes de atención y mejorando la calidad de vida y el pronóstico (37,42-47).
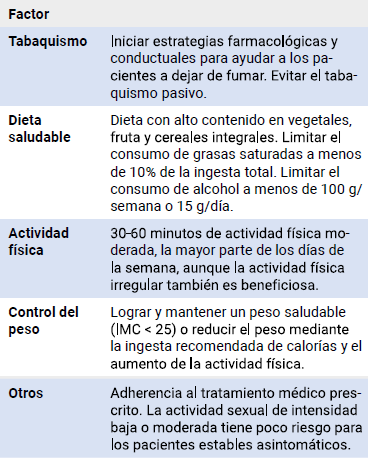
Medidas no farmacológicas
Las medidas no farmacológicas en el tratamiento del síndrome coronario crónico se enfocan en la modificación del estilo de vida, la educación y el apoyo al paciente, la rehabilitación cardiaca y el manejo integral de las comorbilidades, con el objetivo de mejorar los resultados clínicos y la calidad de vida de estos pacientes (48).
Tratamiento farmacológico
El tratamiento farmacológico del síndrome coronario crónico tiene dos objetivos:
Reducción de eventos cardiovasculares mayores (infarto, muerte de origen cardiovascular) a través de tratamiento que no necesariamente alivia síntomas anginosos, pero que tiene la evidencia suficiente para mejorar el pronóstico cardiovascular del paciente.
Controlar los síntomas anginosos y mejorar la calidad de vida del paciente. Tratamiento que no cuenta con evidencia suficiente para repercutir en el pronóstico cardiovascular del paciente.
4.4.1. Reducción de eventos cardiovasculares mayores
4.4.1.1. Recomendaciones para manejo de lípidos
Recomendaciones para el manejo de la presión arterial
Recomendaciones de uso de iSGLT2 o arGLP-1 para diabetes mellitus
Agentes antiinflamatorios
Terapia antiplaquetaria
En pacientes anticoagulados que requieren antiplaquetarios ver diagrama en la sección 8.3.
Betabloqueadores
Antes de prescribir betabloqueadores en pacientes con síndrome coronario crónico, es fundamental verificar la presencia de angina de pecho, la frecuencia cardiaca, la presencia de arritmias, la función ventricular izquierda y descartar la presencia de broncoespasmo. Esto permitirá garantizar una prescripción segura y efectiva de estos fármacos, maximizando sus beneficios terapéuticos (140).
4.4.3. Terapia antianginosa
El dolor anginoso es una condición cuya etiología es compleja y su calidad, percepción y asociación con isquemia puede llegar a ser retadora. En el corazón, existen numerosos ganglios alfa, principalmente en la grasa epicárdica, y son irrigados por las arterias coronarias proximales. Este sistema neuronal está integrado no solo con los ganglios a nivel cardiaco, sino también con ganglios a nivel mediastinal, cervical, dorsal y ganglio estrellado; lo que explica las múltiples presentaciones de dolor (e incluso la ausencia de este como los casos de isquemia silenciosa) en diferentes partes del cuerpo, siendo siempre la más frecuente en el pecho o brazo izquierdo.
La angina y sus equivalentes pueden ser originadas por diferentes mecanismos (ateroesclerosis, vasoespasmo, microcirculación), puede tener múltiples desencadenantes (inflamación, arritmia) y su comportamiento no va a ser el mismo según las comorbilidades y condiciones propias del paciente (silenciosa, refractaria, umbrales).
La terapia médica antianginosa para pacientes con el SCC actúa a través de dos mecanismos generales:
Al reducir la demanda de oxígeno miocárdica (disminuyendo contractilidad, FC o ambos)
Al disminuir el abastecimiento sanguíneo arterial miocardio (vasodilatación)
El objetivo principal de este abordaje antianginoso es el alivio de los síntomas, identificando el tratamiento que no exacerbará las comorbilidades y que no tendrá interacciones importantes con medicaciones concomitantes y que sea bien tolerado.
De forma reciente, revisiones sistemáticas de más de 50 años de tratamiento médico han demostrado la increíble escasez de información y evidencia validada; es claro que no existe superioridad de un antianginoso sobre otro, ni de un abordaje en específico sobre el resto.
A nivel mundial se han publicado dos tipos de estrategias:
La incorporación gradual y bajo recomendaciones de primera y segunda línea según fallo terapéutico
La selección del antianginoso individualizando según las distintas comorbilidades del paciente y las diferentes presentaciones etiológicas de la angina.
A continuación, se enumerarán de forma breve los principales antianginosos recomendados y sus características principales:
Nitratos: entrega alivio inmediato en el caso de angina de esfuerzo (nitratos de corta acción); las formulaciones de larga acción suelen generar tolerancia (taquifilaxia) por lo que se recomiendan periodos libres de medicamento de 10-14 horas. Puede generar hipotensión, cefaleas o flushing. Se contraindican en la cardiomiopatía hipertrófica obstructiva, estenosis aórtica severa y la coadministración con inhibidores de la fosfodiesterasa (sildenafil, tadalafil) o riociguat.
Betabloqueadores: a pesar de ser considerados como medicamentos de primera línea en muchas guías, existe muy poca evidencia que sustente esta priorización. Deben usarse con precaución en combinación con calcioantagonistas con efecto bradicardizante.
Calcioantagonistas: verapamilo y diltiazem deben utilizarse con precaución junto a betabloqueadores, se contraindica su uso en disfunción sistólica severa. Nifedipino y amlodipino han demostrado beneficios sintomáticos en el contexto de vasoespasmo.
Ivabradina: actúa a través de canales regulares del nodo sinusal, su acción es más efectiva a frecuencias cardiacas más altas. Preserva la contractilidad e incrementa el tiempo diastólico, potenciando la perfusión microvascular (por cada 1% de aumento del tiempo diastólico, se incrementa la circulación subendocárdica entre 2.6 y 6%).
Ranolazina: demostró reducir los episodios anginosos y el requerimiento de nitritos.
Trimetazidina: modulador metabólico sin efectos hemodinámicos, provoca un cambio en el perfil energético celular logrando una mayor producción de energía con menos oxígeno (“efecto ahorrador de energía”). Un metaanálisis Cochrane que reunió 23 ensayos clínicos, comprobó una reducción de 44% en los episodios de angina semanales, un 47% de reducción en el consumo de nitritos, así como un retraso significativo en el tiempo hasta la aparición del infradesnivel del segmento ST en las ergometrías (SIAC).
Nicoradil: nitrito con un efecto adicional: apertura de canales de potasio vasculares, lo que provoca vasodilatación adicional. No se observa taquifilaxia.
Nota: referencia a la sección 8.4
4.4.4. Revascularización coronaria
Los criterios para decidir revascularizar a un paciente con síndrome coronario incluyen varios aspectos clave. Estos criterios se basan en la evaluación de la severidad de la enfermedad coronaria, la presencia de síntomas persistentes, el impacto en la función ventricular y la extensión de la isquemia, y son fundamentales para determinar la necesidad de revascularización en pacientes con síndrome coronario severo (149,150). Algunos de los criterios que predominan en la toma de decisiones son:
Persistencia de síntomas a pesar del tratamiento médico óptimo
Extensión y gravedad de la enfermedad coronaria
Impacto en la calidad de vida y pronóstico
Función ventricular izquierda: La presencia de disfunción ventricular izquierda puede influir en la decisión de revascularizar, en particular si la función ventricular está significativamente comprometida.
Evaluación funcional de la presencia de isquemia a través de prueba de esfuerzo o resonancia magnética cardiaca, puede ser un factor determinante para optar por la revascularización.
Estos criterios, junto con la evaluación individualizada de cada paciente, guían la decisión entre medicar y revascularizar a pacientes con síndrome coronario crónico, buscando mejorar los síntomas, la calidad de vida y el pronóstico a largo plazo.
Rehabilitación cardiaca
La rehabilitación cardiaca tiene un lugar fundamental en el tratamiento del SCC y la prevención de eventos, al mejorar la capacidad funcional, reducir el riesgo cardiovascular, brindar un manejo integral y ofrecer apoyo psicosocial a los pacientes (151).
5.1. Recomendaciones generales:
Determinar el umbral isquémico. Es un parámetro clave que permite prescribir de forma segura y efectiva el ejercicio en pacientes con cardiopatía isquémica, adaptando la intensidad y supervisión según el riesgo individual de cada paciente (154).
Diseñar un programa personalizado y efectivo para el manejo del SCC y la prevención de eventos adversos cardiovasculares.
A los pacientes con historia de enfermedad coronaria de alto riesgo o isquemia resistente se deberá prohibir los deportes de competición, sin embargo, una vez determinado el umbral isquémico se podrán insertar en programas de ejercicio que no sobrepasen este límite (155).
Los pacientes con síndromes coronarios crónicos establecidos, sin anomalías en la ergometría máxima o pruebas funcionales por imagen sin disfunción del ventrículo izquierdo, pueden considerarse de bajo riesgo y podrían participar en todos los deportes de competición individual (156).
6. Discusión
La enfermedad coronaria, entendida como un continuo a lo largo de la vida del paciente, genera retos constantes diagnósticos y terapéuticos en el médico tratante. Los avances tecnológicos nos acercan más a la precisión diagnóstica y la individualización terapéutica. Sin embargo, los determinantes socioeconómicos de la región obstaculizan en muchos casos el acceso a dichos beneficios.
Puntos clave del documento:
Desligar los SCC del término angina estable que permita extender el beneficio de la atención a un grupo más amplio de pacientes.
Hacer un uso apropiado de los recursos exclusivamente en aquellos pacientes sintomáticos, con baja capacidad funcional o alto riesgo cardiovascular.
Priorizar las herramientas diagnósticas con mayor rendimiento y promover capacitaciones locales que permitan su adopción generalizada.
Enfocar recursos terapéuticos en dos ejes: mejorar el pronóstico cardiovascular y aliviar los síntomas anginosos del paciente.
7. Conclusiones
Este documento busca reunir de la forma más clara y precisa las principales recomendaciones mundiales en torno a los síndromes coronarios crónicos, pero bajo una premisa centroamericana. La aportación de las Sociedades Cardiológicas de la región es priorizar aquellos lineamientos que nos acerquen a un diagnóstico y una terapéutica cada vez más precisas; pero también teniendo en cuenta las limitantes económicas, humanas y científicas.
En una región donde la atención al paciente es la prioridad, bajo un contexto de escasez de recursos y donde la investigación ha sido relegada a un segundo plano, se recopilaron aquellas recomendaciones aplicables que puedan mejorar la atención de los SCC.
Agradecimientos
A las Asociaciones de Cardiología y a los colegas participantes.
Conflictos de interés
Los autores declaran no tener conflictos de interés.
Financiación
Servier Centro América y Caribe S.A. patrocinó los servicios de asistencia y redacción médica del presente Consenso. El contenido de esta publicación refleja única y exclusivamente las opiniones de los autores. Los autores declaran que el patrocinador no tuvo ninguna intervención directa o indirecta en los análisis de la información, calificación de la evidencia, recomendaciones, ni en la interpretación de los datos.