Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.6 n.3 San José Sep. 2004
electrocardiografía. Utilidad de los nuevos criterios.
* Dr. Vivencio Barrios Alonso, Dr. Alberto Calderón Montero
Introducción
La hipertrofia del ventrículo izquierdo (HVI) es la lesión de órgano diana más frecuente en hipertensión arterial (HTA) y es, después de la edad, el principal factor predictivo de complicaciones cardíacas y cerebro vasculares1. Como fue demostrado a finales de los noventa, la regresión de la HVI como consecuencia del tratamiento, disminuye la morbilidad y mortalidad cardiovascular en comparación con los pacientes sin regresión ó con aumento de masa ventricular izquierda (MVI) 2.
El diagnóstico de la HVI debe ser por tanto uno de los objetivos prioritarios en el correcto manejo del paciente hipertenso. Clásicamente, el método diagnóstico de mayor validez ha sido la Ecocardiografía-Doppler, que sin embargo presenta algunas limitaciones tanto técnicas como de validez 3. Por ello, en el momento actual, la ecocardiografía ha sido desplazada por la resonancia magnética nuclear (RMN)como patrón oro de HVI 4.
Sin embargo ambos métodos no pueden aplicarse de manera rutinaria para el diagnóstico de HVI, y además no son fácilmente accesibles desde la Atención Primaria (AP). El ECG en cambio, es una técnica sencilla, económica y plenamente disponible en AP. La mayor limitación del ECG es su baja sensibilidad, tanto si se utilizan los criterios diagnósticos de voltaje como criterios mixtos. Sin embargo, recientemente se ha descrito un nuevo criterio que mejora mucho la sensibilidad del ECG sin pérdida de especificidad, aumentando por lo tanto la detección de pacientes con HVI. Otros criterios basados en alteraciones de la repolarización pueden complementar y mejorar el diagnóstico de la HVI 5.
El objetivo del presente artículo, es revisar y actualizar el diagnóstico electrocardiográfico de la HVI, partiendo de un repaso de los conceptos fisiopatológicos básicos y haciendo especial hincapié en aquellos criterios que aumentan la eficiencia del ECG, y permiten un mejor manejo y estratificación del paciente hipertenso desde AP, sin recurrir a técnicas diagnósticas más complejas propias de la atención especializada.
Fisiopatología
Mecanismos fisiopatológicos
El crecimiento del ventrículo izquierdo (VI)en respuesta a la HTA se desarrolla en función de un doble mecanismo:
a. Hemodinámico: el incremento de la PA determina un aumento de la presión intraventricular y del estrés de la pared del ventrículo, factores ambos que estimulan la síntesis proteica y la síntesis local de sustancias tróficas.
b. No hemodinámicos: fundamentalmente hormonales, como la noradrenalina a través del estímulo de receptores adrenérgicos, la angiotensina II mediante la estimulación de los receptores AT1 o la aldosterona, que parece intervenir en los mecanismos de fibrosis miocárdica.
Tipos de HVI
En función de la medición ecocardiográfica de la MVI y del grosor parietal relativo (GPR), existen cuatro grupos de geometría del VI en los hipertensos como se refleja en la tabla 1.
Las implicaciones pronósticas de los diferentes tipos de geometría del VI, no han sido definitivamente aclaradas hasta el momento actual. En general, la hipertrofia excéntrica y sobre todo la concéntrica se asocia con un peor pronóstico 6. La hipertrofia concéntrica tendría un mayor riesgo relativo para el desarrollo de insuficiencia cardíaca crónica (ICC), mientras que la hipertrofia excéntrica lo tendría para el desarrollo de cardiopatía isquémica 7. Recientemente, se ha demostrado como la hipertrofia concéntrica se asocia con un riesgo mayor de ACV que la hipertrofia excéntrica 8. Otros estudios sin embargo, no ha podido confirmar la existencia de mayor riesgo entre los diferentes tipos de HVI 9.
Implicaciones clínicas de la HVI
Las complicaciones de la HVI se pueden resumir en:
a. Cardiopatía isquémica, mediada no sólo por el desarrollo de lesiones coronarias ateroscleróticas obstructivas, sino también por otros mecanismos. Entre ellos, el aumento de la masa ventricular que incrementa las necesidades de O2 del miocardio, la disminución de la capacidad de vasodilatación coronaria y el deterioro de la autorregulación del flujo coronario. La presión arterial sistólica parece ser el principal determinante de la CI, mientras que la diastólica deja de ser un factor de riesgo por encima de los 60 años 10.
b. Insuficiencia cardíaca derivada de la disfunción diastólica primero y de la disfunción sistólica en fases avanzadas. Además, el propio efecto de la HVI sobre la isquemia miocárdica predispone aún más a la ICC 11.
c. Arritmias, cuya relación con la HVI es lineal, de modo que tanto las arritmias auriculares como las ventriculares son más frecuentes a medida que aumenta la MVI 12,13.
d. Muerte súbita, normalmente asociada a arritmias ventriculares complejas desencadenadas por la propia HVI o por la isquemia asociada 14.
Diagnóstico de la HVI
Fundamentos electrofisiológicos del crecimiento ventricular izquierdo.
El aumento de la MVI en el contexto de la HTA, prolonga la despolarización, lo que conlleva un predominio de las fuerzas vectoriales del VI dirigidas hacia la izquierda y hacia atrás. Simultáneamente se altera la repolarización, de modo que invierte su curso normal de epicardio a endocardio. La repolarización comienza en el endocardio cuando aún no ha finalizado la despolarización, lo que hace que el signo de la onda T se oponga al complejo QRS.
Como consecuencia, las alteraciones que podemos encontrar en el ECG son :
- Complejo QRS: El aumento de la MVI condiciona un desplazamiento de las fuerzas vectoriales hacia la izquierda y atrás, lo que se manifiesta en un aumento de la negatividad de S en V1-V2 y un aumento de la positividad de R en V5-V6. Asimismo, al existir mayor masa muscular, se produce un alargamiento de la despolarización del VI que se traduce en una prolongación del QRS (100-120 mseg).
- Segmento ST y onda T: Las modificaciones van a depender de la duración y del grado de HVI. En fases iniciales, no aparecen alteraciones ó estas son muy leves con una onda T de menor voltaje y simétrica. A medida que evoluciona la HVI, se produce una infradesnivelación del segmento ST convexa respecto de la línea isoeléctrica y un aplanamiento y posterior inversión de la onda T.
Conviene recordar que en la sobrecarga sistólica encontraremos aumento de voltaje y aplanamiento ó inversión de T en precordiales izquierdas, mientras que en la sobrecarga diastólica aparecerán trastornos de voltaje y onda T alta y picuda en la cara lateral del VI.
Criterios "clásicos" para el diagnóstico de HVI
1. Criterios de voltaje
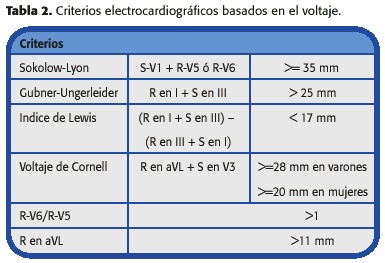
Clásicamente la valoración electrocardiográfica de la HVI ha venido realizándose de acuerdo a los criterios de voltaje, en función de los fundamentos fisiopatológicos previamente explicados. Múltiples criterios diagnósticos han sido elaborados basados en la amplitud del complejo QRS (tabla 2), y entre ellos probablemente los más utilizados en la práctica clínica por su sencillez sean el criterio de Sokolow 15 y el criterio de Cornell ajustado por sexo 16. La especificidad de ambos criterios se ha demostrado superior al 90% , siendo tal vez algo mayor para el criterio de Sokolow (98-99% ).
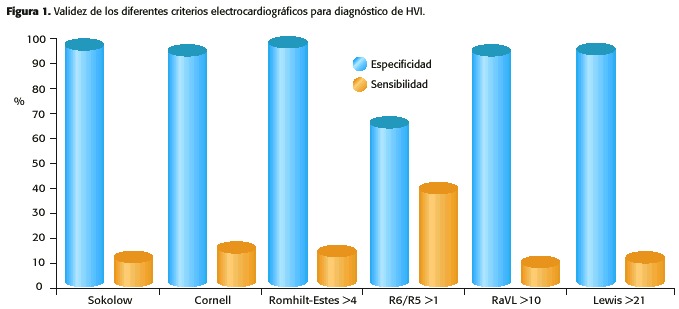
El principal problema de la mayoría de los criterios de voltaje es su baja sensibilidad, es decir la existencia de muchos falsos negativos. Si bien inicialmente se describieron sensibilidades próximas al 25-30% , la realidad es que en la población hipertensa, la sensibilidad no supera el 15%. Esta discrepancia se debe a que en los estudios originales las poblaciones seleccionadas correspondían a pacientes con HTA muy evolucionada, presiones arteriales elevadas y por ende HVI de grado severo. En la práctica clínica diaria de Atención Primaria, dónde la HVI es mayoritariamente de grado ligero, la sensibilidad del criterio de Cornell oscila en torno al 12-15% y la del criterio de Sokolow alrededor del 10-12%. La sensibilidad del criterio de Sokolow aumenta algo en los casos de HTA de larga evolución con HVI de grado moderado ó severo y en los varones. Del mismo modo, el resto de criterios de voltaje no presentan sensibilidades superiores (Figura 1).
Para intentar salvar esta limitación, se describieron otros criterios de voltaje como el cociente R-V6/R-V5. Inicialmente una relación R-V6/R-V5 >1 17 diagnostica HVI y sin embargo su sensibilidad no supera los criterios de Cornell y Sokolow. Posteriormente se propuso reducir el punto de corte del cociente a 0.65 18, lo que permite obtener una sensibilidad próxima al 40-45%. Sin embargo, la especificidad se reduce mucho, incluso hasta menos del 40% , con lo que el número de falsos positivos es muy elevado y obligaría a confirmar por medio de técnicas de imagen un elevado número de casos.
Una alternativa propuesta para mejorar la sensibilidad de los criterios de voltaje ha sido la combinación de uno ó más criterios. Algunos autores han propuesto la combinación de criterios de voltaje en paralelo, lo que mejora la sensibilidad, de modo que es suficiente con que uno sea positivo para el diagnóstico de HVI.
Uno de estos métodos, denominado puntuación de Perugia 19, muestra una sensibilidad superior al 20-25% para una especificidad del 93%. Según sus autores, la prevalencia de HVI por el método de Perugia supera a los criterios clásicos de voltaje, lo que probablemente condiciona su mayor valor predictivo de eventos cardiovasculares.
En resumen, los criterios de voltaje en general, y en particular los de Cornell y Sokolow, tienen la ventaja de ser muy específicos y sencillos de aplicar, pero el inconveniente de ser poco sensibles.
2. Criterios mixtos
Para intentar mejorar el rendimiento del ECG en el diagnóstico de HVI, se han descrito otros criterios que además del voltaje, combinan diferentes alteraciones del ECG ó bien modelos matemáticos que incluyen variables tanto electrocardiográficas como demográficas y clínicas 20, 21.
Tal vez el criterio combinado más conocido sea el de Romhilt-Estes 22 , basado en un sistema de puntuación que engloba el complejo QRS, alteraciones en el segmento ST y onda T y modificaciones de la onda P. La sensibilidad del estudio original para los hipertensos era del 40-45% , si bien la población seleccionada se correspondía con HVI severa definida por autopsia. En estudios posteriores en la práctica clínica esta sensibilidad no ha podido ser demostrada, y en cualquier caso, no mejora apreciablemente la de los criterios de voltaje. Además, la complejidad de la puntuación, dificulta su aplicación rápida en la práctica clínica.
Se ha propuesto la utilización de modelos matemáticos de regresión logística para aumentar la sensibilidad del ECG. Su descripción detallada escapa de los objetivos de este artículo, si bien se puede resaltar que algunos modelos, en particular los que incluyen la edad y el IMC además de las variables electrocardiográficas, obtienen una sensibilidad superior al 40% y una correlación ecocardiográfica muy aceptable (0.70) 23. Sin embargo, son complejos de utilizar, se corresponden con estudios observacionales y con poblaciones muy seleccionadas en la mayoría de los casos, por lo que son de escasa aplicación en atención primaria.
Factores implicados en la sensibilidad del ECG
A partir de los datos aportados por el seguimiento de las cohortes de Framingham, se pudo comprobar cómo la sensibilidad de los diferentes criterios electrocardiográficos de HVI era función de una serie de variables (Tabla 3)que revisamos a continuación.
A. Sexo: La amplitud del complejo QRS es una manifestación por lo menos parcial del IMVI, y en la mujer es un 20-25% menor que en el varón. Además el fenotipo femenino, al interponer mayor volumen de grasa entre los electrodos y el corazón, también disminuye el voltaje en aquellas derivaciones afectadas.
B. Edad: Con el avance de los años, se produce una esviación del eje hacia la izquierda en la mujeres y además una disminución en el voltaje del QRS en los varones. Sin embargo, la sensibilidad del ECG aumenta en los mayores, y esta paradoja se debe a una mayor prevalencia de HVI. En la población mayor de 75-80 años, la sensibilidad del ECG disminuye debido a la reducción del volumen intracavitario, la mayor prevalencia de insuficiencia cardíaca por lo menos latente y la frecuente deshidratación de la población anciana. Por ello en este segmento de población, la utilización combinada de criterios de voltaje y alteraciones del ST-T parece una alternativa aceptable.
C. Obesidad: La grasa en la pared torácica atenúa el voltaje de QRS, lo que disminuye la sensibilidad. Por ello el voltaje de Cornell y la duración del QRS son los que menos se afectan por este factor 24.
D. Tabaco: En los fumadores, disminuye la sensibilidad del ECG probablemente por las alteraciones pulmonares secundarias.
E. Grado de HVI: Como ya se ha comentado, la sensibilidad aumenta a medida que aumenta la MVI, lo cual se observa para ambos sexos.
F. Otros factores: Cabe mencionar la raza (mayor sensibilidad del ECG en negros que en blancos), grasa pericárdica, volumen cardíaco, masa muscular torácica y alteraciones del parénquima pulmonar.
Criterio del Producto Duración por Voltaje (PDV)
1. Introducción.
El criterio del PDV fue inicialmente descrito en el año 1992 26 cuando se analizó su validez utilizando como patrón de referencia la masa ventricular izquierda obtenida por necropsia. Se comprobó como la sensibilidad (S)del PDV superaba el 50% para una especificidad (E)del 96% , siendo clínicamente superior a los criterios de voltaje de Cornell, de Sokolow y de la duración del QRS. Tres años después, los mismos autores utilizando la ecocardiografía como patrón oro, describieron como la aplicación del PDV al criterio de voltaje de Cornell, Sokolow y suma del QRS en las doce derivaciones, alcanza una sensibilidad claramente superior a la de los criterios de voltaje aislados 27. En concreto, para el PDV de Cornell se obtenía una sensibilidad del 37% para una E= 96% , superior y clínicamente relevante comparada con el criterio de voltaje de Cornell (S= 27% ). A la hora de comprender la elevada sensibilidad del criterio de voltaje de Cornell, es muy importante destacar que la HVI de la población en el estudio referido era mayoritariamente (>60% ), de origen valvular, lo que implica valores de MVI más elevados y consecuentemente una mayor prevalencia.
Más recientemente, el PDV ha sido el principal criterio de inclusión en el estudio LIFE 28, donde más del 70% de los pacientes con HVI por ECG cumplían el PDV para el criterio de Cornell, 15% tenían criterios de HVI por el PDV-Cornell y el criterio de voltaje de Sokolow y sólo un 15% entraron cumpliendo aisladamente este último criterio. De hecho, en las guías de la SEH-SEC publicadas en el año 2003, se incluye el criterio del PDV de Cornell junto con el voltaje de Sokolow como los criterios principales para el diagnóstico de HVI por ECG 29.
La aplicación del PDV, tiene la gran ventaja de incorporar dentro de un mismo criterio dos fenómenos fisiopatológicos complementarios como son:
a. el aumento de la masa del VI, implica un desplazamiento del vector electrocardiográfico hacia la izquierda y atrás, y por tanto un aumento del voltaje en las derivaciones izquierdas (onda R)y un aumento consecuente de la onda S (negativa)en las derivaciones derechas.
b. la despolarización del ventrículo (onda QRS)se relaciona también con la masa ventricular izquierda, de modo que cuando aumenta, la despolarización se prolonga lo que se manifiesta en una mayor duración del QRS.
2. Cálculo del PDV.
Como se ha comentado en las líneas anteriores, el PDV se fundamenta en el voltaje de las diferentes ondas según el criterio elegido y la duración del QRS. De forma genérica, se podría definir como:
PDV =(criterio de voltaje en mV) x (duración de QRS en mseg)
El PDV por lo tanto, se puede aplicar a cualquiera de los criterios de voltaje "clásicos", es decir al criterio de Cornell, Sokolow o a la suma del QRS en las 12 derivaciones. La forma de aplicar el PDV a cada criterio queda reflejada en la tabla 4.
Conviene resaltar que para el caso de la aplicación del PDV al criterio de Cornell ajustado por sexo, es necesario sumar 6 al resultado del voltaje en el caso de las mujeres. Por medio de esta corrección se obtiene un valor uniforme para ambos sexos y un punto de corte único, a diferencia del criterio de voltaje de Cornell donde existe uno para cada sexo (20 mm en mujeres y 28 mm en varones)
3. Límites para el PDV.
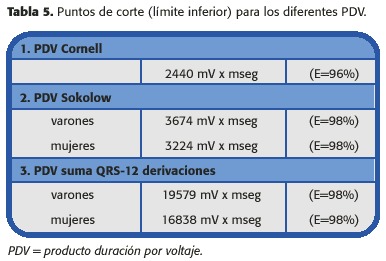
Los puntos de corte para considerar o no HVI, fueron calculados en el estudio original 27 sobre los resultados obtenidos en la población control sin HVI. Utilizando el criterio de la media + 2 DE, que no precisa de asumir criterios de normalidad en la población, se estimaron los límites inferiores para HVI que se reflejan en la tabla 5.
Las características muestrales del estudio original, llevaron a nuestro grupo a verificar los puntos de corte para el PDV-Cornell en la población hipertensa. Sobre una muestra de más de 120 pacientes, con un porcentaje de no HVI por ecocardiografía del 43% , encontramos que si establecíamos el límite en 2190 mV x mseg, la S se elevaba hasta el 40% sin apenas pérdida de especificidad (92% ) (30). Y si utilizábamos el criterio de la media +2DE, el límite inferior para HVI se establecía en 2235 mV x mseg.
En consecuencia, podemos optimizar el rendimiento del PDV-Cornell en la detección de HVI bajando el punto de corte a las cifras referidas, lo que nos permitirá detectar un mayor porcentaje de pacientes con HVI.
4. Validez del PDV
Por ser el criterio de Cornell y el criterio de Sokolow los habitualmente utilizados en AP, nos vamos a referir casi en exclusiva al PDV aplicado a ambos.
En el estudio original 27, la S del PDV-Sokolow comparada con el criterio de voltaje aislado no mostró diferencias sustanciales (45% vs 43% ), mientras que en el caso del PDV-Cornell si fueron clínicamente importantes (37% vs 28% ). Ello puede explicarse en función de la mayor sensibilidad del criterio de Sokolow ante hipertrofias más severas como son las que se producen en las valvulopatías y que sumaban un porcentaje mayoritario de la muestra.
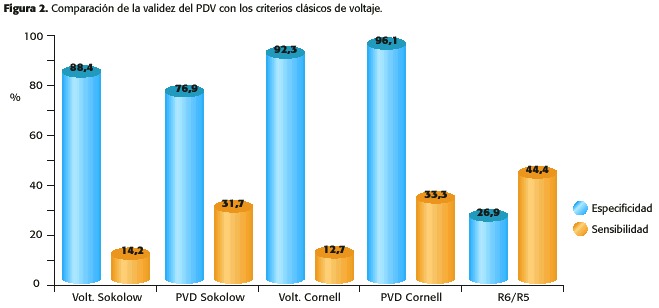
Para resolver esta discrepancia, pusimos en marcha un estudio transversal para analizar la validez del PDV aplicado al criterio de Cornell y de Sokolow en una población de hipertensos esenciales atendidos en las consultas de AP 31. Se excluyeron los pacientes con complicaciones cardiovasculares y con lesiones valvulares. Comparamos cada criterio de voltaje y su correspondiente PDV e incluimos el cociente R6/R5 por ser sencillo de aplicar, conocido en nuestro medio y tener una aceptable sensibilidad cuando el punto de corte se baja hasta 0. 65. Los resultados quedan reflejados en la figura 2. El PDV-Cornell muestra una sensibilidad del 33, 3% , ligeramente superior al PDV de Sokolow y que casi triplica al criterio de voltaje de Cornell (12. 6% ). La especificidad no se ve afectada (96% para el PDV-Cornell y 92. 3% para el voltaje de Cornell). La S obtenida en nuestro estudio, ligeramente inferior a la del estudio original, puede explicarse, como ya ha sido esbozado previamente, por las características de ambas muestras. La S del cociente R6/R5 para un nivel de corte del 0. 65 fue del 44%, y sin embargo la especificidad bajó hasta el 26% , lo que en la práctica clínica daría lugar a muchos falsos positivos, lo que obligaría a realizar una ecocardiografía a la mayoría de ellos para poder discriminarlos.
En cualquier caso, la utilización en la práctica clínica en AP del PDV-Cornell (ó en su caso el PDV-Sokolow)nos puede permitir detectar casi el triple de casos de HVI que si utilizamos los criterios de voltaje aislados, con las implicaciones en la estratificación del riesgo y el tratamiento que puede tener para nuestros pacientes.
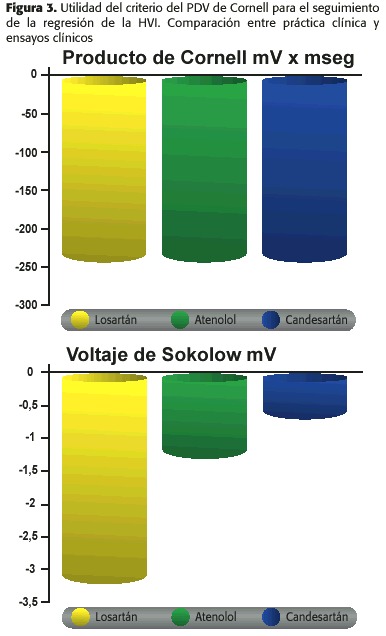
5. Utilidad del PDV en el seguimiento y regresión de la HVI. Un aspecto de gran interés que incorpora el PDV es su utilidad para el seguimiento y cuantificación de la regresión de la HVI por ECG. Ya en el estudio LIFE se pudo comprobar como tanto la reducción del PDV-Cornell como del voltaje de Sokolow, se correlacionaban con una reducción en la incidencia de eventos cardiovasculares según la variable combinada principal 32. Y también se observó como la mayor parte de la reducción se produjo al finalizar el primer año de tratamiento (-200 mV x mseg para el PDV-Cornell)pudiéndose detectar descensos significativos ya a partir del 6º mes 33. Ello es de gran trascendencia, en tanto en cuanto no había sido verificado previamente. De hecho, en el estudio de Framingham y teniendo en cuenta la variabilidad de los criterios electrocardiográficos, no se detectaron cambios sustanciales en tiempos inferiores a dos años.
La utilidad del PDV-Cornell fuera del escenario restringido de los ensayos clínicos, ha sido verificada por nuestro grupo en un estudio abierto con candesartán durante 12 meses 34. Al finalizar el período de tratamiento, la reducción media fue de 102 mV x mseg. Si comparamos con los resultados del estudio LIFE, la reducción es menor a la obtenida con un fármaco de la misma familia como losartán, pero hay que considerar que las condiciones de práctica clínica son diferentes a la de los ensayos (figura 3).
Muy recientemente y por primera vez, la utilización del PDV-Cornell ha permitido cuantificar los beneficios de la reducción de la HVI por ECG. Datos procedentes también del estudio LIFE 35, ponen de manifiesto como cada 1.050 mV x mseg de reducción en el PDV-Cornell, se asocian con una disminución del 14% en la variable combinada principal y de un 10% en la incidencia de IAM y ACVA. Y ello ocurre independientemente del grupo de tratamiento asignado, de los niveles basales de presión arterial y del nivel basal de riesgo según las tablas de Framingham. Desde el punto de vista de la práctica clínica, la utilización seriada del producto duración voltaje de Cornell, permite evaluar el efecto del tratamiento sobre la HVI, así como la correcta monitorización de la estratificación del riesgo cardiovascular.
Alteraciones de la repolarización
Desde hace más de 40 años, se sabe como las alteraciones de la repolarización que acompañan a la HVI, se asocian a un mal pronóstico 36. De hecho, las alteraciones mayores de la repolarización (tabla 6) predicen la mortalidad cardiovascular total, la muerte súbita y la enfermedad coronaria en la población general 37.
Sin embargo, sólo recientemente se ha analizado el valor predictivo de las alteraciones inespecíficas de la repolarización.
Se entienden como tales, aquellas que no cumplen los criterios de alteraciones mayores referidos en la tabla 2. En el estudio de Schillacci y cols 38, se compara de forma prospectiva la incidencia de eventos cardiovasculares en tres grupos de pacientes clasificados según la existencia en el ECG de repolarización normal (grupo control), alteraciones menores de la repolarización y alteraciones mayores. Si bien el riesgo fue mayor para los pacientes con alteraciones típicas, el grupo de alteraciones menores presentó un RR de 2,07 (1.23-2.47) con respecto al grupo control. Y estos resultados se mantenían independientemente de que se asociara o no HVI por el criterio de voltaje de Cornell.
Las aplicaciones prácticas son claras: las alteraciones inespecíficas de la repolarización deben ser valoradas de manera sistemática al evaluar el riesgo del paciente hipertenso, ya que confieren un mayor riesgo cardiovascular. En consecuencia, el tratamiento deberá ser lo más vigoroso e intensivo posible en este grupo de pacientes.
En resumen , sabemos que la HVI es el principal factor de riesgo modificable en la HTA y su diagnóstico debe ser una estrategia prioritaria en el manejo del paciente hipertenso. La detección de HVI por ECG es un método sencillo y económico al alcance de todos los médicos de AP. Si bien los criterios clásicos de voltaje no alcanzan a detectar 1 de cada 9 pacientes con HVI, el nuevo criterio del producto duración por voltaje de Cornell mejora ampliamente la sensibilidad sin pérdida de especificidad. Además permite un seguimiento y una cuantificación del efecto del tratamiento sobre la HVI, que se correlaciona muy bien con el desarrollo de complicaciones mortales y no mortales entre los pacientes hipertensos. Por ello consideramos que la utilización del PDV-Cornell (y en su caso para el criterio de Sokolow)debe implantarse de rutina en el manejo del paciente hipertenso en la práctica clínica de AP, tal y como recomiendan las guías de la SEH-SEC del año 2003 y como muestran los resultados de los diferentes ensayos tanto controlados como en diseño abierto. Además como información complementaria, se deben valorar no solo las alteraciones típicas de la repolarización, sino también las alteraciones menores, ya que confieren un mayor riesgo cardiovascular y exigen un tratamiento mas intensivo.
Bibliografía:
1. The Seventh Report of Joint National Committee on prevention, detection, evaluation and treatment of high blood pressure: The JNC 7 report. JAMA 2003; 289: 2560-72. [ Links ]
2. Verdecchia P, Schillacci G, Borgioni C, Ciucci A, Gattobigio R, Zampi I et al. Prognostic significance of serial changes in left ventricular mass in essential hypertension. Circulation 1998; 97: 48-54. [ Links ]
3. Germain P, Roul G, Kastler B, Mossard JM, Bareiss P, Sacrez A. Inter-study variability in left ventricular mass measurement. Comparision between M-mode echography and MRI. Eur Heart J 1992; 13: 1011-9. [ Links ]
4. Bottini PB, Carr AA, Prisant LM, Flickinger FW, Allison JD, Gottdiener JS. Magnetic resonance imaging compared to echocardiography to asses left ventricular mass in the hypertensive patient. Am J Hypertens 1995; 8: 221-8. [ Links ]
5. Okin PM, Devereux RB, Nieminen MS, Jern S, Oikarinen L, Viitasalo M et al. Electrocardiographic strain pattern and prediction of cardiovascular morbidity and mortality in hypertensive patients. Hipertensión 2004; 44: 48-54. [ Links ]
6. Koren MJ, Devereaux RB, Casale PN. Relation of left ventricular mass and geometry to morbidity and mortality in uncomplicated essential hypertension. Ann Intern Med 1991; 114: 335-52. [ Links ]
7. Gardin JM, McClelland R, Kitzman D, Lima JA, Bommer W, Klopfenstein HS et al. M-mode echocardiography predictors of six-to-seven year incidence of coronary heart disease, stroke, congestive heart failure an mortality in an elderly cohort (the Cardiovascular Health Study). Am J Cardiol 2001; 87: 1051-7. [ Links ]
8. Di Tullio MR, Zwas DR, Secco RL, Sciacca RR, Homma S. Left ventricular mass and geometry and the risk of ischemic stroke. Stroke 2003; 34: 2380-4. [ Links ]
9. Verdecchia P, Schillacci G, Borgioni C, Ciucci A, Gattobigio R, Zampi I et al. Prognostic value of left ventricular mass and geometry in systemic hypertension with left ventricular hypertrophy. Am J Cardiol 1996; 78: 197-202. [ Links ]
10. Franklin SS, Khan SA, Wong ND, Larson MG, Levy D. Is pulse pressure useful in predicting risk for coronary heart disease?The Framingham Heart Study. Circulation 1999; 100: 354-401. [ Links ]
11. Barrios V, Campuzano R. Utilidad de los antagonistas de los receptores de angotensina II en la insuficiencia cardiaca. Rev Clin Esp 2003; 203: 28-32. [ Links ]
12. Ciaroni S, Cuenoud L, Bloch A. Clinical study to investigate the predictive parameters for the onset of atrial fibrillation in patients with essential hypertension. Am Heart J 2000; 139: 814-19. [ Links ]
13. Haider AW, Larson MG, Benjamin EJ, Levy D. Increased left ventricular mass and hypertrophy are associated with increased risk for sudden death. J Am Coll Cardiol 1998; 32: 1454-9. [ Links ]
14. Saadeh AM, Evans SJ, James MA, Jones JV. QTs dispersion and complex ventricular arrhythmias in untreated newly presenting hypertensive patients. J Hum Hypertens 1999; 13: 665-69. [ Links ]
15. Sokolow M Lyon TP. The ventricular complex in left ventricular hypertrophy as obtained by unipolar precordial and limb leads. Am Heart J 1949; 37: 161-186. [ Links ]
16. Casale PN, Devereaux RB, Alonso DR, Campo E, Kliegfield P. Improved sex-specific criteria of left ventricular hypertrophy for clinical and computer interpretation of electrocardiograms: validation with autopsy findings. Circulation 1987; 75: 565-72. [ Links ]
17. Koiti H, Spodick DH. Accuracy of the R6: R5 voltage ratio for increased left ventricular mass. Am J Cardiol 1988; 62: 986- 7. [ Links ]
18. Rodríguez Radial L, Navarro A, Sanchez J. R6: R5 voltage ratio in systemic hypertension. Am J Cardiol 1990; 66: 869-71. [ Links ]
19. Verdecchia P, Schillacci G, Borgioni C. Prognostic value of a new electrocardiographic method for diagnosis left ventricular hypertrophy in essential hypertension. Am J Cardiol 1998; 31: 383-90. [ Links ]
20. Wolf HK, Burgraff GW, Cuddy E. Prediction of left ventricular mass from the electrocardiogram. J Electrocardiol 1991; 24: 121-27. [ Links ]
21. De Vries SO, Essen WF, Beltman FW. Prediction of left ventricular mass from the electrocardiogram in systemic hypertension. Am J Cardiol 1996; 77: 974-78. [ Links ]
22. Romhilt DW, Estes EH. A point-score system for the ECG diagnosis of left ventricular hypertrophy. Am Heart J 1968; 75: 752-59. [ Links ]
23. Norman JE, Levy D. Adjustament of ECG left ventricular hypertrophy criteria for body mass index and age improves classification accuracy. J of Electrocardiol 1991; 29(suppl): 241- 47. [ Links ]
24. Okin PM, Roman MJ, Devereaux RB. ECG identification of left ventricular hypertrophy. Relationship of test performance to body habitus. J of Electrocardiol 1996; 29(suppl): 256-61. [ Links ]
25. Levy D, Labib SB, Anderson KM. Determinants of sensivity and specificity of electrocardiographic criteria for left ventricular hypertrophy. Circulation 1990; 81: 815. [ Links ]
26. Molloy TJ, Okin PM, Devereaux RB, Kligfield P. Electrocardiographic detection of left ventricular hypertrophy by the simple QRS voltage-duration product. J Am Coll Cardiol 1992; 20: 1180-6. [ Links ]
27. Okin PM, Roman MJ, Devereaux RB, Kligfield P. Electrocardiographic identification of increased left ventricular mass by simple voltage-duration products. J Am Coll Cardiol 1995; 25: 417-23. [ Links ]
28. Dahlof B, Devereaux RB, Julius J, Kjeldsen SE, Beevers G, de Fraire U et al. Characteristics of 9194 patients with left ventricular hypertrophy. The LIFE Study. Hypertension 1998; 32: 989-97. [ Links ]
29. Guidelines Committee. 2003 European Society of Hypertensión-European Society of Cardiology guidelines for the management of arterial hypertension. J Hypertens 2003; 21: 1011-53. [ Links ]
30. Calderón A, Barrios V. The optimization of voltage-duration product criteria may improve the electrocardiographic diagnosis of left ventricular hypertrophy in hypertension. J Hypertens 2004; 22(suppl 2): 276. [ Links ]
31. Calderón A, Barrios V. Detección de hipertrofia ventricular izquierda por ECG mediante el producto duración por voltaje. Validación por eco cardiografía. Hipertensión, 2003: 20: 381- 88. [ Links ]
32. Dahlof B, Devereaux RB, Julius J, Kjeldsen SE, Beepers G, de Fraire U et al. Cardiovascular morbidity and mortality in the Losartan Intervention for Endpoint reduction in hypertensión study (LIFE): a randomised trial against atenolol. Lancet 2002; 359: 995-1003. [ Links ]
33. Okin PM, Devereaux RB, Julius J, Kjeldsen SE, Beepers G, de Fraire U et al. Regression of electrocardiographic left ventricular hypertrophy by losartan versus atenolol. The LIFE Study. Circulation 2003; 108: 684-90. [ Links ]
34. Estudio VIPE. Datos pendientes de publicación. [ Links ]
35. Okin PM, Devereaux RB, Julius J, Kjeldsen SE, Beepers G, de Fraire U et al. Regressión of electrocardiographic left ventricular hypertrophy during antihypertensive treatment and the prediction of mayor cardiovascular events. JAMA 2004; 92: 2343-49. [ Links ]
36. Tervahauta M, Pekkanen J, Punsar S, Nissinen A. Resting electrocardiographic abnormalities as predictor of coronary events and total mortality among elderly men. Am J Cardiol 1996; 100; 641-45. [ Links ]
37. Larsen CT, Dahlin J, Blackburn H, Scharling H, Appleyard M, Sigurd B et al. Prevalence and prognosis of electrocardiographic left ventricular hypertrophy, ST segment depressión and negative T-wave: The Copenhagen City Heart Study. Eur Heart J 2002; 23: 315-23. [ Links ]
38. Schillacci G, Pirro M, Pasqualini L, Vaudo G, Ronti T, Gemelli F et al. Prognostic significance of isolated, non-specific left ventricular repolaritation abnormalities in hypertension. J Hypertens 2004; 22: 407-14. [ Links ]
Dirección para correspondencia: Vivencio Barrios Alonso Ecocardiografía (3ª izda. ). Servicio de Cardiología, Hospital Ramón y Cajal. Ctra. Colmenar km. 9.100 28034 Madrid e-mail: vbarriosa@meditex.es vbarrios.hrc@salud.madrid.org