Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Ciencias Médicas
Print version ISSN 0253-2948
Rev. costarric. cienc. méd vol.23 n.3-4 San José Dec. 2002
La introducción de nuevas metodología moleculares ha permitido la diferenciación de Entamoeba histomica de la ameba comensal Entamoeba dispar, morfológicamente idéntica a E. histolytica. Entre los mecanismos de patogenicidad en Entamoeba histolytica se encuentra la presencia de la lecitina de galactosa-galactosamina en la superficie de los trofozoito, responsables de la adhesión a las células intestinales. También se han identificado polipéptidos solubles denominados ameboporos, los que se insertan en la membrana de fa célula blanco e inducen la lisis celular. Además se han caracterizado proteasas de cisteína, capaces de degradar distintos componentes de la matriz extracelular. Las proteasas de cisteína están también involucradas en la evasión de la respuesta inmune por cuanto degradan inmunoglobulinas IgA e IgG, y las anafilotoxinas C3a y C5a. En E. dispar se ha demostrado la presencia de ameboporos y proteasas de cisteína en menor concentración y con menor actividad biológica lo que se cree tiene un impacto en la carencia de patogenicidad de esta especie.
Se revisan los nuevos hallazgos en cuanto la epidemiología en distintos países del mundo, utilizando las técnicas moleculares de diferenciación para E. histolytica. En Costa Rica la seroprevalencia por E. histolytica en pacientes con heces positivas por quistes de E. histolyticale / E. dispar fue de 7,3%, por lo que se considera que la mayoría de los pacientes en cuyo examen al fresco se observan quistes se trata verdaderamente de E. dispar, por cuanto la presencia de anticuerpos se utiliza para diferenciar una infección por E. histolytica de una causada por E. Dispar.
El referencia al diagnóstico el hallazgo de trofozoitos con eritrocitos fagocitados en heces frescas o biopsias se correlaciona con la presencia de E. histolytica. Por el contrario los quistes de ambos protozoarios son indistinguibles. En la actualidad se dispone de variadas técnicas inmunológicas, algunos comercialmente disponibles, para la detección de antígenos en heces y anticuerpos en suero, para ambos casos la técnica más utilizada es el ELISA.
Palabras clave
Entamoeba histolytica, Entamoeba dispar, patogénesis, epidemiología, diagnóstico diferencial.
Abstract
The introduction of molecular techniques allowed the differentiation of Entamoeba histomica from E. dispar, a comensal ameba morphologically indistinguisable from E. histolytica. Pathogenic mechanisms of E. histolytica inciudes the presence of a galactosa binding lectin that attachs trophozoites to intestinal epithelial cells. Also pore-forming peptides termed amebopores have been demonstrated, this peptides oligomerize after insertion in the cell membrane and form waterfilled channels through which ions and other molecules can pass, causing cell lysis. Cysteine proteasas have also been characterized as a viruience factor responsable of the degradation of the extracellular matrix and the evasion of the immune response by degradation of IgA, disruption of IgG, and degradation of anaphylotoxins C3a and C5a.
The new epidemiological findings around the worid by the use of molecular technics are also discussed. In Costa Rica seroprevalence of 7,3% in E.histoyica / E.dispar cysts positive patients is taken an indication that the majority of the infections are caused by E. dispar. Antibody are present only in E. histoyica infection.
As far as diagnosis, the finding of trofozoites with enguifed eritrocytes in fresh fecal samples or biopses correlates with E. histoyica. On the other hand, cysts of both protozoa are indistinguisable. Several immunological technics are available for the determination of antigen in stool samples or antibodies in sera.
Key words
Entamoeba histolytica, Entamoeba dispar, pathogenesis, epidemiology, diferencial diagnosis.
Introducción
En el año 1875 el médico ruso Fedor Lösch describe el caso de un granjero que había sido admitido a su clínica en St. Petersburgo. Este joven presentaba un cuadro de disenteria crónica y al observar las heces Lösch encontró gran cantidad de amebas a las que denominó con el nombre de Amoeba coli y cuya descripción concordaba con la morfología típica de Entamoeba histomica (1 ). Sin embargo, Lösch no consideró que las amebas fueran causantes de la diarrea, sino que ayudaban a mantener el proceso inflamatorio (1 ).
Durante los años siguientes se presentó una serie de discrepancias entre los distintos investigadores, principalmente en cuanto a los aspectos taxonómicos, lo cual se refleja en la gran cantidad de nombres que este parásito recibió (Amoeba coli, Amoeba dysenteriae, etc) (2 ). El 1903 el zoólogo alemán Fritz Schaudinn, diferenció Entamoeba coli ameba comensal del intestino, de la ameba patógena capaz de destruir tejido, característica por lo que la llamó por primera vez Entamoeba histolytica (3 ). Schaudin murió en el año 1906 a la edad de 35 años de complicaciones secundarias a una amibiasis adquirida de manera experimental (3 ).
En el año 1925 Emil Brumpt parasitólogo francés describió una especie de Entamoeba similar morfológicamente Entamoeba histolytica, con cuatro núcleos en su forma quística, y la denomina Entamoeba dispar , considerándola no patógena. Sus conclusiones se fundamentaron en tres argumentos: primero, el seguimiento por un período de ocho años de individuos infectados que nunca desarrollaron síntomas; segundo la infección de gatos, un método muy sensible para la producción experimental de amibiasis intestinal, que con E . dispar nunca llevó a la producción de síntomas y por último estudios epidemiológicos que demostraban altas tasas de infección por E. histomica en países en los que no se reportaban casos de amibiasis. Brumpt concluye con estos datos que las infecciones en países de zonas templadas eran debidas a una especie distinta aunque morfológicamente idéntica a E. histolytica y la denominó E. dispar ( 4 ,5 ). Todos estos argumentos fueron rechazados por la comunidad científica internacional principalmente por considerarse en ese momento que el concepto de especie representaba una idea morfológica y no debería basarse en aspectos patológicos (6 ).
La resurrección de E. dispar como una especie diferente a E. histolytica ocurrió muy lentamente. En 1978 Sargeunt y Williams utilizando los patrones de migración electroforética de tres isoenzimas (glucosa fosfato isomerasa, fosfoglucomutasa y malato oxidoreductasa) lograron establecer cuatro diferentes zimodemas, uno de los cuales es relacionado con la forma invasora y los otros con la forma no invasora o comensal (7 ). Con la inclusión de la hexokinasa y su respectivo patrón electroforético, se demostró que aislamientos derivados de casos sintomáticos presentan una banda de hexokinasa de rápida migración (banda á) y por el contrario, los aislamientos de pacientes asintomáticos bandas de lenta migración ( 8 ,9 ). Finalmente, se establece la presencia de veintiún zimodemas, de los cuales nueve corresponden a zimodemas no patogénicos, actualmente identificados para E. dispar y los restantes doce a zimodemas patogénicos que corresponden a E. histolytica ( 10 ).
En los años posteriores además de las diferencias en los patrones de migración electroforética, se desarrollaron anticuerpos monocionales contra varios antígenos que permiten diferenciar las cepas invasoras de las no invasoras. Dentro de estos se encuentran: la lectina de adherencia Gal/GalNac (GIAP) ( 11 ), un antígeno de superficie de 96 kDa (12 ,13 ), un antígeno proteínico interno de 81-84 kDa ( 14 ), una proteína hidrofílica de membrana de 29 kDA/30 kDa ( 15 ,16 ), así como el antígeno aislado de los gránulos electrodensos (EDG) producidos al interactuar trofozoitos del parásito con colágeno "in vitro" (17 ).
Con el advenimiento de mejores técnicas para el análisis del ADN, los procesos de hibridación y la reacción en cadena de la polimerasa (PCR), se establecieron diferencias no sólo a nivel bioquímico y antigénico sino también desde el punto de vista genético principalmente en secuencias altamente repetitivas de¡ ADN circular extracromosomal (18 ,19 ), así como diferencias en genes codificantes para la actina ( 20 ), la cisteina proteinasa (21 ), la superóxido dismutasa (22 ).
De acuerdo a esta evidencia inmunológica, bioquímica y genética, en 1993 Diamond y Clark ( 23 ) confirman la validez de Entamoeba dispar Brumpt, 1925 como una especie diferente a la E. histolytica, Schaudinn 1903. La Organización Mundial de la Salud en 1997 reconoce que la diferenciación ha sido universalmente aceptada y recomienda el reportar el hallazgo de quistes y trofozoitos de la forma comensal como E. histoyica / E. dispar (24 ,25 )
Patogénesis
El principal factor de virulencia presente en E. histolytica es su capacidad de citotoxicidad, proceso que está mediado por una serie de factores y sustancias producidas por la ameba dentro de las cuales destacan los ameboporos y las proteasas de cisteína ( 33 ).
La familia de los ameboporos comprende tres isomorf os, el ameboporo A, B y C, que se encuentran en una proporción aproximadamente de 35:10:1 respectivamente y presentan un 35-57% de identidad en sus secuencias de aminoácidos. (34 ,35 ) Los ameboporos son polipéptidos solubles que se insertan en la membrana de la célula blanco por la unión con fosfolípidos aniónicos a bajo pH, oligomerizan, proceso mediado por la interacción péptido-péptido, difunden en la membrana y forman un canal a través de¡ cual se produce la salida de iones y otras moléculas pequeñas. En consecuencia el medio interno celular cambia y esto resulta en muerte por lisis ( 35 ). Se ha demostrado que los ameboporos presentan homología con el polipéptido de las células NK y de los linfocitos citotóxicos de cerdos, con la saponina y con el surfactante de la proteína B ( 34 ,36 ), todas estas sustancias producen un efecto lítico similar a los ameboporos.
Se ha postulado que los trofozoitos de E. histolytica son resistente a la actividad del ameboporo por cuanto su membrana celular posee fosfolípidos neutros que impiden la unión de los polipéptidos (37 ,38 ). La principal función de los ameboporos es la eliminación de las bacterias fagocitadas principal fuente de alimento de los trofozoitos (39 ,40 ).
En E. dispar se ha demostrado la presencia de ameboporo A y B, en menor concentración y con menor actividad biológica lo que se cree tiene un impacto en la carencia de patogenicidad de esta especie (41 ).
Epidemiología
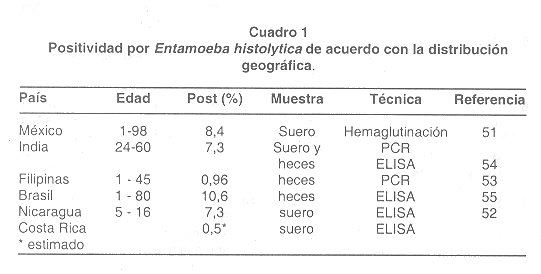
Áreas altamente endémicas por E. histolytica incluyen la India, el oeste y surdeafrica, así como ciertas regiones de Sur y Centro América en donde más del 50% de las poblaciones de alto riesgo pueden estar infectadas ( 25 ). Uno de los países latinoamericanos más afectados es México en donde, de acuerdo a un estudio del año 1 994, la prevalencia de anticuerpos contra E. histolytica en una muestra de 67 668 personas y representativa de la población general, fue de 8,4% ( 51 ). Por otro lado en Nicaragua se ha informado una seropositividad en personas asintomáticas excretoras de quistes de aproximadamente de 7,3% con el uso de un ELISA para la detección de IgG, encontrándose además un pico de prevalencia en el grupo de edad de los 5 a 16 años ( 52 ). Estudios en la región norte de las Filipinas, utilizando PCR, muestran una prevalencia del 0,96% de infección por E. histolytica y del 7,16 % por E. dispar en la población general ( 53 ). En Bangladesh se ha informado una prevalencia de 4,2% por E. histomica y de 6,5% por E. disparen niños del área urbana con diarrea y una prevalencia de 1 % por E. histolytica y 7% por E. dispar en niños asintomáticos del área rural (54 ). En Brasil, Braga et al (55 ) reporta un 24,7% de positividad en 335 individuos con un promedio de edad de 14 años (Cuadro l ).
En nuestro país Reyes et al informan una prevalencia de 16% de E. histolytica / E. dispar en niños de guarderías del Cantón Central de San José utilizando examen directo, concentración y tinción con hematoxilina férrica ( 56 ). Otro estudio realizado por Morales et al (57 ) encuentran una prevalencia del 2,9% en el año de 1989 y del 1,08% en 1994, en ambos casos en la comunidad de Torremolinos en Desamparados. En la provincia de Limón se ha demostrado una prevalencia por E. histolytica / E. dispar en la zona central y alrededores es del 7,5 % (58 ). En pacientes HIV seropositivos se ha demostrado 9,3% de positividad por E. histolytica / E. dispar en heces por método directo (59).
En referencia a la prevalencia de anticuerpos contra E. histolytica, León y Reyes (60 ) realizaron un estudio en 41 pacientes positivos por quistes de E.histolytica / E dispar en heces. Se demostró la presencia de anticuerpos utilizando la técnica de ELISA (Sigma Chemical Company, St. Louis, MO) en 3 de las 41 muestras de suero analizadas (7,3%). La mayoría de los pacientes fueron asintomático (n 29), dentro de los cuales se encontró un único caso serológicamente positivo (3,4%). De los pacientes con algún tipo de sintomatología asociada con amibiasis (n 12) se demostró seropositividad en 2 casos (1 6%) (59). En conclusión, este estudio demostró que la gran mayoría de los pacientes del área metropolitana de San José, en cuyo examen al fresco se observan quistes de E. histolytica / E. dispar, se tratan de E. dispar, esto por cuanto la presencia de anticuerpos se utiliza para diferenciar una infección por E. histoyica de una provocada por E. dispar (59 ).
Si estimáramos en promedio en nuestro país una prevalencia de E. histolytica / E. dispar de aproximadamente 7% y si consideramos que un 7% de estos pacientes a su vez presentan anticuerpos, se podría extrapolar una prevalencia de E. histolytica en la población general cercana al 0,5%. Estas estimaciones parecen corresponder con el bajo número de casos clínicos observados en nuestro país.
Diagnóstico
El diagnóstico parasitológico de la amibiasis intestinal está basado en la demostración de trofozoitos de E. histomica en las heces por medio del análisis directo en solución salina, lugol o tinción (hematoxilina férrica o tinción tricrómica), o su demostración en biopsias de la mucosa intestinal o hepáticas. El examen microscópico de una única muestra de heces lleva a una sensibilidad del 50 al 70%, por lo que se requiere de al menos el análisis de tres muestras diferentes para lograr una sensibilidad del 90% (10 ).La eficacia de muchas de estas técnicas diagnosticas, básicamente la observación directa de las heces así como las tinciones, está determinada por la habilidad y experiencia del microbiólogo para detectar y diferenciar a los trofozoitos de E. histolytica de otras amebas comensales, de leucocitos, etc. Además como ya se indicó la observación directa de los quistes no permite diferenciar entre E. histolytica y E. dispar. El hallazgo de trofozoitos con eritrocitos fagocitados en heces frescas u otros especimenes y trofozoitos en biopsia tisular están en ambos casos fuertemente correlacionados con la presencia de E. histolytica y enfermedad invasiva (4 ,10 ).
Acuña-Soto et al ( 61 ) informan que no hay diferencias estadísticas significativas en cuanto al diámetro de los quistes entre las dos especies, demostrando un promedio para E. histomica de 12,27 ± 1,29 u y de 1 1,63 ± 0,81 para E. dispar, por lo anterior es imposible hacer la diferenciación con la simple observación de quistes al microscopio.
Por estas razones en los últimos años se han realizado considerables esfuerzos en desarrollar técnicas inmunológicas para una fácil detección de E. histolytica. De esta forma existen en la actualidad métodos inmunológicos, algunos comercialmente disponibles, que pueden detectar tanto antígenos en heces como anticuerpos en suero y para ambos casos la técnica más utilizada es el ELISA (62 ).
Entre estas tenemos: el empleo de antígenos solubles de una cepa patógena (63 ,64 ), principalmente la denominada HM1:IMSS, los cuales se obtienen a partir de un cultivo de la ameba y un proceso de sonicación. Con este tipo de antígeno podría esperarse que la especificidad nos sea la apropiada, sin embargo partiendo deshecho de que únicamente la infección por E. histolytica va a generar una respuesta inmune humoral detectable (10 ), este aparente inconveniente no representa un gran problema.
Otros métodos más específicos que utilizan la lectina denominada GIAP. Esta lectina de 260 kDa presenta dos subunidades: una pesada de 170 kDa unida por puentes disulfuro con otra subunidad liviana de 35 kDa. La subunidad de 170 kDa es antigénicamente conservada y además es inmunogénica, por el contrario la de 35 kDa no desarrolla una respuesta inmune (62 ). Por lo anterior, el antígeno de 179 kDa ha sido utilizado tanto para la detección de anticuerpos (64 ,65 ), como para el desarrollo de anticuerpos monocionales que permiten su identificación directamente en las heces (66-68 ). Se ha desarrollado anticuerpos monoclonales contra esta subunidad y establecido la presencia de al menos 6 epitopos importantes como posibles herramientas para la diferenciación de E. Histolytica / E. dispar. Dos de estos anticuerpos monoclonales reconocen dos epitopos presentes en ambas especies y los cuatro restantes reconocen epitopos que se encuentran sólo en la especie patógena (62 ,68 ).
El empleo de antígenos recombinantes (69 ,70-72 ) como es el caso de la subunidad de 170 kDa (69 ,71 ,72 ) o del antígenos denominado proteína de E. histomica rica en residuos de serina (SREHP) (69 ), ofrecen una serie de ventajas: pueden ser producidos en grandes cantidades con relativa facilidad, se evita la necesidad de mantener cultivos de E. histolytica y además el uso de un antígeno recombinante puede ayudar al desarrollo de un ensayo bien estandarizado ( 69 ,71 ). Otro posible beneficio es la aparente capacidad que tienen los ELISA basados en este tipo de antígenos, para diferenciar un cuadro agudo de crónicos (69 ,70 ). Esto sería muy útil principalmente en zonas altamente endémicas en donde el número de individuos seropositivos por infección anterior es muy elevado (69 ). Estos estudios han establecido que pacientes con absceso hepático amibiano se tornan seronegativos a estos antígenos a partir de los 120 días posteriores a la aparición de los síntomas ( 69 ).
Recientemente se han desarrollado anticuerpos monocionales que reconocen específicamente los quiste en muestras no fijadas (73 ) y trofozoitos en muestras preservadas (74 ). Estos hallazgos podría constituir una importante herramienta ya que eventualmente acoplados a un ELISA, permitirían diferenciar directamente en las heces los quistes y/o trofozoitos de E. histomica de los de E. dispar. En la actualidad la diferenciación de los quistes de E. histolytica y E. dispar directamente de las heces y sin recurrir al cultivo, únicamente se puede realizar empleando PCR ( 16 ,51 ,52 ).Las pruebas serológicas son de gran importancia principalmente en áreas no endémicas ya que en estos sitios un 90% de los individuos con amibiasis invasiva poseen anticuerpos anti-E. histolytica (25 ). En estas áreas la serología es una prueba diagnóstico sensible debido a la predominancia de individuos seronegativos. Otra técnica que se ha venido desarrollando desde los inicios de los años 90, es la reacción en cadena de la polimerasa (PCR), la cual ha demostrado ser muy eficaz para la diferenciación de ambas especies pero cuyo empleo se haya limitado a estudios epidemiológicos o experimentales pero no a nivel diagnóstico rutinario (18 ,19 ,53 ).

Referencia
2. Quincke, H I. On amoebic enteritis En: Kean B H, Mott KE, Russell AJ, eds. Tropical Medicine and Parasitology Classic lnvestigations volumen 1 London, U K: Cornell University Press; 1978. Pp 103-109. [ Links ]
3. Schaudinn, F. On the development of some Rhizopoda ( Preliminary Report) En: Kean B H, Mott KE, Russell AJ, eds. Tropical Medicine and Parasitology Classic lnvestigations volumen 1 London, U K: Cornell University Press; 1978. pp 110-118. [ Links ]
4. Petithory JC, Ardoin-Guidon F y Chaumeil C. Amibes et fiagellés intestinaux. Amibes oculaires Leur diagnostic microscopique. Cahier de Formation Biologie médicale No. 11. Bioforma, 1998; 61-93.
5. Clark CG. Entamoeba dispar , an organism reborn. Trans Roy Soc Trop Med Hyg 1998; 92: 361-364. [ Links ]
6. Wenyon, C.M. Protozoology A manual for medical men, veterinarians ans zoologists, Great Britan: William Good and Company, 1926:184-210. [ Links ]
7. Sargeunt PG, Williams JE, Grene JD. The differentiation of invasive and non-invasive Entamoeba histolytica by isoenzyme electrophoresis.Trans Roy Soc Trop Med Hyg 1978; 72:519-521. [ Links ]
8. Sargeunt PG, Williams JE, Kumate J, Jiménez E. The epidemiology of Entamoeba histolytica in Mexico City. A pilot survey I. Trans Roy Soc Trop Med Hyg 1980; 74: 653-656. [ Links ]
9. Sargeunt PG, Williams JE, Rhojnani R, Campos JE, Gomez A. The epidemiology of Entamoeba histolytica in a rural and an urban area of Mexico. A pilot survey Il. Trans Roy Soc Trop Med Hyg 1982; 76:208-210. [ Links ]
10. Bruckner DA. Amebiasis. Clin Microbiol Rev 1992; 356-369. [ Links ]
11. Petri WA, Jackson TF, Gathiramm V, et al Pathogenic and nonpathogenic strains of Entamoeba histolytica can be differentiated by monocional antibodies to the galactose-specific adherence lectin. Infect lmmun 1990; 58:1802-1806. [ Links ]
12. Torian BE, Lukehart SA, Stamm WE. Use of monocional antibodies to identify, characterize, and purify a 96,000 dalton surface antigen of pathogenic Entamoeba histolytica. J Infect Dis 1987; 156: 334-343. [ Links ]
13. Torian BE, Reed SL, Creely CM, Coward JE, Vial K, Stamm WE. The 96-Kiiodalton antigen as an integral membrane protein in pathogenic Entamoeba histolytica: potencial differences in pathogenic and nonpathogenic isolates. Infect. lmmun 1990; 58:753- [ Links ]
14. González-Ruiz AR, Haque R, Rehman T, et al A monocional antibody for distinction of invasive and noninvasive clinical isolates of Entamoeba histolytica. J Clin Microbiol 1992:30:2807-2813. [ Links ]
15. Reed SL, Flores BM, Batzer MA, et al Molecular and cellular characterization of the 29 kilodalton peripheral membrane protein of Entamoeba histolytica: differentiation between pathogenic and nonpathogenic isolates. Infect Immun 1992; 60:542-549. [ Links ]
16. Tachibana H, Kobayashi S, Kato Y, Nagakura K, Kaneda Y, Takeuchi ldentification of pathogenic isolate-specific 30,000-M, antigen ofentamoeba histolytica by using a monocional antibody. Infect Immun 1990; 58:955-960. [ Links ]
17. Muñoz ML, Lamoyi E, León G, et al Antigens in electron-dense granules from Entamoeba histolytica as posible markers for pathogenicity. J Clin Microbiol 1990; 28:2418-2424. [ Links ]
18. Acuña-Soto RS, Samuelson J, de Girolami P, et al Appgcation of the polymerase chain reaction to the epidemiology of pathogenic and nonpathogenic Entamoeba histolytica. Amer J Trop Med Hyg 1993; 48:58-70. [ Links ]
19. Bracha R, Diamond LS, Ackers JP, Burchard GD, Mirelman D. Differentiation of clinical isolates of Entamoeba histoyica by using specific DNA probes. J Clin Microbiol 1990; 28:680-684. [ Links ]
20. Tannich E, Horstmann RD, Knobloch J, Arnold HH. Genomic DNA differences between pathogenic and nonpathogenic Entamoeba histolytica. Proc. Natl Acad Sci 1989;86:5118-5122. [ Links ]
21. Tannich E, Schoize H, Nicke R y Horstmann RD. Homologous cysteine proteinases of pathogenic and nonpathogenic Entamoeba histolytica. J Biol Chem 1991; 266: 4798-4803. [ Links ]
22. Tannich E, Bruchaus I Walter RD, Horstmann RD. Pathogenic and nonpathogenic Entamoeba histolytica: identification and molecular cloning of an iron.containing superoxide dismutase. Mol Biochem Parasitol 1991; 49: 61-72 [ Links ]
23. Diamond LS, Clark CG. A redescription of Entamoeba histolytica Schaudinn, 1903 (Emended Walder, 1911) Separating it from Entamoeba dispar Brumpt, 1925. J Euk Microbiol 1993;40:340-344 . [ Links ]
24. World Health Organization Report of a xonsultation of experts on amoebiasis Weekly Epidemiot Rep 1997; 72:97-99 [ Links ]
25. Aucott JN, Ravdin Jl. Amebiasis and "nonpathogenic" intestinal protozoa. Infectious Disease Clinics of North America 1993; 7: 467-485. [ Links ]
26. Espinoza-Cantellano ME, Martínez-Palomo AM. Pathogenesis of intestinal amebiasis: from molecules to disease. Clin Microbiol Rev 2000; 318-331. [ Links ]
27. Chadee K, Petri WA, Innes DJ, Ravdin Ji. Rat and human colonic mucins bind to and inhibit the adherence lectin of Entamoeba histolytica J Clin Invest 1987; 80: 1245-1254. [ Links ]
28. Petri WA, Chapman MD, Snodgrass T, Mann BJ, Broman J, Ravdin J l. Subunits structure of the galactose and N acetyl galactosamine inhabitable adherente lectin of Entamoeba histomica. J Biol Chem 1989; 262: 3007-3012. [ Links ]
29. Reed SL, Flores BM, Batzer MA, Stein MA, et al. Molecular and cellular characterization of the 29-kilodalton peripheral membrane protein of Entamoeba histolytica: differentiation between pathogenic and nopathogenic isolates. Infect lmmun 1992; 60:542-549. [ Links ]
30. Braga L, lnhibition of the complement membrana attack complex by the galactose-specific adhesin of Entamoeba histolytica J Clin Investig 1992; 90:1131-1137. [ Links ]
31. Meza I. Extracellular matrizinduced signaling in Entamoeba histolytica: its role in invasiveness. Parasitol Today 2000; 16:23-28. [ Links ]
32. Talamás-Rohana P, Meza I. lnteraction between pathogenic amebas and fibronectin: susbstrate degradation and changes in cytoskeleton organization. J Cell Biol 1998; 106:1787-1794. [ Links ]
33. Tannich E. Amoebic disease Entamoeba histolytica and E. dispar. Comparison of molecules considered important for host tissue destruction. Trans Roy Soc Trop Med Hyg 1998; 92:593-596. [ Links ]
34. Leippe M, Andra J, Nickel R, Tannich E, Muller-Eberhard HJ. Amebopores, a family of membranolytic peptides from cytoplasmic granules of Entamoeba histomica: isolation, primary structure, and pore formation in bacterial cytoplasmic membranas. Mol Microbiol 1997; 14: 895-904. [ Links ]
35. Leippe M. Amoebapores. Parasitol Today 1997; 13:178-183. [ Links ]
36. Leippe M. Acient weapons: NK lysin is a mammalian homolog to pore-forming pepetides of a protozoan parasite. Cell 1995; 83: 17-18. [ Links ]
37. Aley SB, Scout WA, Cohn ZA. Plasma membrana of Entamoeba histomíca. J Exp Med 1980; 152: 391-404. [ Links ]
38. Leippe M. The pore forming peptide of Entamoeba histolytica, the protozoan parasite causing human amoebiasis Toxicology 1994; 87: 5-18. [ Links ]
39. Leippe M, Andra J, Muller-Eberhard HJ. Cytolytic and antibacterial activity of synthetic peptides derived from amoebapore, the pore-forming pepptide of Entamoeba histomica. Proc Natl Acad Sci USA 1994; 91: 26022606. [ Links ]
40. Bracha R, Kobiler D, Mirelman D. Attachment and ingestion of bacteria by trophozoites of Entamoeba histolytica. Infect lmmun 1982; 36:396-406. [ Links ]
41. Nickel R, Ott C, Dankekar T, Leippe Pore-forming peptides of Entamoeba dispar. Similarity and divergence to amoebapores in structure, expression and activity. Eur J Biochem 1999; 265: 10021007. [ Links ]
42. Reed SL, Keene WE, McKerrow JH. Thiol proteinase expresión and pathogenicity of Entamoeba histolytica. J Clin Microbiol 1989; 27:2772-2777. [ Links ]
43. Que X, Reed S.L. Cysteine proteinases and the pathogenesis of amebiasis. Clin Microbiol Rev 2000; 13:196-206. [ Links ]
44. Kensali BL, Ravdin Jl Degradation of human inmunogiobulin A by Entamoeba histolytica. J Infect Dis 1993; 168:1319-1322. [ Links ]
45. Tran VQ, Herdman DS, Torian BE, Reed SL. The neutral cysteine proteinase of Entamoeba histolytica degrades IgG and prevents its binding J Infect Dis 1998; 177: 508-511. [ Links ]
46. Reed S, Keene WE, McKerrow JH, Gigli I. Cleavage of C3 by a neutral cysteine proteinase of Entamoeba histolytica. J Ammunol 1989; 143: 189-195. [ Links ]
47. Reed SL, Ember JA, Herdman DS, DiScipio RG, Hugli TE, Gigli I.. The extracellular neutral cysteine proteinase of Entamoeba histolytica degrades anaphy-lotoxins C3a and C5a. J Immunol 1995; 266-274. [ Links ]
48. Petri WA, Haque R, Lyerly D, Vines RR. Estimating the impact of amebiasis on Health. Parasitol Today2000; 16:320-321. [ Links ]
49. World Health Organization. The World Health Report 2000. [ Links ]
50. World Health Organization. The World Health Report 1998- Life in the 21 st century: a vision for all. [ Links ]
51. Caballero-Salcedo A, Viveros Rogel M, Salvatierra B, et al Seroepidemiology of amebiasis in México. Am J Trop Med Hyg 1994; 50:412-419. [ Links ]
52. Tellez AS, Cortez LR, Aust AK et al. Amebiasis in Nicaragua: Class specific antibody response. Archives Medical Research. 1992; 23:261-264. [ Links ]
53. Rivera WL, Tachinaba H, Kanbara Fiel study on the distribution of Entamoeba histolytica and Entamoeba dispar in the northern Philippines as detected by the polymerase chain reaction. Am J Trop Med Hyg 1 998; 59: 916-921. [ Links ]
54. Haque R, Ali IM, Petri WA. Prevalence and immune response to Entamoeba histomica infection in preschool children in Bangladesh. Am J Trop Med Hyg 1999; 60:1031-1034. [ Links ]
55. Braga LL, Mendonca Y, Paiva CA, Sales A, Calvacante ALM, Mann BJ. Seropositivity for and intestinal colinization with Entamoeba histomica and Entamoeba dispar in individuas in northeastern Brazil. J Clin Mícrobiol 1998; 36: 3044-3045. [ Links ]
56. Reyes L, Marín R, Catarinella G, et al Parasitosis intestinales en niños en guarderías de San José, Costa Rica. Rev Costarric Cienc Med 1987; 486:23-26. [ Links ]
57. Morales M, Esquivel M, Sancho Y, Murillo A. Estudio comparativo sobre parasitismo intestinal en niños de la comunidad de Torremolinos, Cantón de Desamparados en los años 1989 y 1994. Acta Ped Costarric 1995; 9: 109-111. [ Links ]
58. Kenton R, Rojas O. Parasitosis intestinal en la provincia de Limón. Rev Méd Costa Rica 1982; 47:71-74 [ Links ]
59. Gutiérrez G., Reyes L, Chinchilla M, Herrera G, Rodríguez M, Frajman M. Presencia de parásitosintestinales en pacientes HIV seropositivos. Primer informe de microsporosis humana en Costa Rica. Parasitol al Día 1997; 21: 3-4
60. León R, Reyes L. Serología de la amibiasis en Costa Rica. Tesis. Universidad de Costa Rica, Ciudad Universitaria Rodrigo Facio: San Pedro de Montes de Oca, 1999. [ Links ]
61. Acuña-Soto R, Samuelson J, De Girolami P, et al Application of the polymerase chain reaction to the epidemiology of pathogenic and nonpathogenic Entamoeba histolytica. Am J Trop Med Hyg 1993; 48: 58-70. [ Links ]
62. Jackson TFHG, Ravdin JI. Differentiation of Entamoeba dispar infections. Parasitol Today 1996; 12: 406-409. [ Links ]
63. Gandhi BM, Irshad M, Chawla TC, Tandon BN. Enzyme linked protein A: an ELISA for detection of amoebic antibody. Trans R Soc Trop Med Hyg 1987; 81: 183-185. [ Links ]
64. Abd-Alla MD, El-Hawey AM, Ravdin JI. Use of enzyme linked immunosorbent assay to detect anti-adherence protein with invasive amebiasis in Cairo, Egypt. Am J Trp Med Hyg 1992; 47:800-804. [ Links ]
65. Abd-Alla, MD, Jackson TFHG, Gathiram V, El-Hawey AM, Ravdin JI. Differentiation of pathogenic Entamoeba histolytica infections from nonpathoñgenic infections by detection of galactose inhabitable adherente protein antigen in sera and feces. J Clin Microbiol 1993; 31: 2845-2850. [ Links ]
66. Haque R, Kress K, Wood S, et al Diagnosis of pathogenic Entamoeba histolytica infection using a stoll ELISA base on monoclonal antibodies to the galctose-specific adhesin. J Infectious Dis 1993; 167:247-249 [ Links ]
67. Haque R, Neville LM, Wood S, Petri W. Short report: detection of Entamoeba histolytica and E. dispar directly in stool. Am J Trop Med Hyg 1994; 50: 595-596 [ Links ]
68. Haque R, Neville LM, Hahn P, Petri W A. Rapid diagnosis of entamoeba and Entamoeba histolytica stool antigen detection kits. J Clin Microbiol 1995; 33:2558-2561. [ Links ]
69. Stanley Sl, Jackson TFHG, Foster L, Singh S. Longitudinal study of the antibody response to recombinant Entamoeba histolytica antigens in patients with amebic liver abscess. Am J Trop Med Hyg 1998; 58:414-416 [ Links ]
70. Lotter H, Jackson TFHG, Tannich E. Evaluation of three serological test for the detection of antiamebic antibodies applied to sera of patients from an area endemic for amebiasis Trop Med Parasitol 1995; 46:180-182 [ Links ]
71. Shenai BR, Komalam BL, Arvind AS, Krishnaswamy PR, Subba Rao PV. Recombinant antigen-based avidin- biotin microtitire enzyme linked immunosorbent assay for serodiagnosis of invasive amebiasis. J Clin Microbiol 1996; 34: 828-833 [ Links ]
72. Kraql L, Adjmi H, Lavarde V, Pays JF, Tourte-Schaefer C, Hennequin C. Evaluation of rapid enzyme immunoassay for diagnosis of hepatic amoebiasis. J Clin Microbiol 1997; 35: 1530-1533. [ Links ]
73. Walderich B, Burchard G, Knobloch J, Müller L. Development of monoclonal antibodies sepecifically recognizing the cyst stage of Entamoeba histolytica. Am J Trop Med Hyg 1998; 59:347-351. [ Links ]
74. Yau Y C W, Crandall I, Kain K C. Development of monoclonal antibodies which specifically recognize Entamoeba histolytica in preserved stool samples. J Clin Microbiol 2001; 39:716-719. [ Links ]
1 Centro de Investigación en Enfermedades Tropicales
2 Facultad de Microbiología, Universidad de Costa Rica.













