Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.58 n.3 San José Sep. 2010
Biomasa fúngica y bacteriana como indicadoras del secuestro de C en suelos de sabanas sustituidos por pinares en Uverito, Venezuela
1. Departamento de Ciencias, Laboratorio de Investigaciones Biológicas, Universidad de Oriente, Estado Anzoátegui, Venezuela; irmagomez52@hotmail.com
Abstract: Fungal and bacterial biomass as indicators of soil C sequestration in savannas soils substituted by pine plantations. A transformation of any natural ecosystem to an agricultural or forest system leads to an important soil modification, not only in the total carbon pool, but also in the carbon associated to the microbial biomass. This way, carbon quantification on soil quality is important for the determination of impacts of agricultural practices and land use changes. The aim of this study was to the determine, through the selective inhibition technique, the fungal and bacterial biomass, and fungal-to-bacterial ratio (F:B) in pine plantations (Pinus caribaea var. hondurensis), to establish if these parameters are sensible indicators of changes in the carbon content in Uverito soils (Venezuela). Furthermore, the inhibitor additivity ratio (IAR) and total combined inhibition (TCI) were carried out to determine if the antibiotics caused non-target inhibition. The quantification of fungal and bacterial biomass was carried out by using of cyloheximide as fungal inhibitor, and streptomycin and chloranphenicol as specific bacterial inhibitors. This research evidences that this land use change exerted a significant effect on soil microbial biomass, and shows that in pine plantations there is a dominance of the fungal component, in contrast to the native savanna, in which the bacterial biomass dominates. The substitution of native savanna by pine plantation in Uverito promotes a major soil carbon sequestration. The values of the inhibitor additivity ratio (IAR) as for native savanna as pine system, were both>1.0. The total combined inhibition (TCI) was smaller in the pine systems, from which it is possible to infer that a high proportion of microbial biomass was affected by the combination of the inhibitors. Rev. Biol. Trop. 58 (3): 977-989. Epub 2010 September 01.
Key words: bacterial biomass, C sequestration, fungal biomass, pine, savanna.
En Venezuela la superficie ocupada por las sabanas se estima en 260 000km2, de las cuales 189 000km2 se localizan en los llanos orientales. Éstas son usadas en gran medida para la ganadería extensiva, aunque cada vez se extiende más su conversión a sistema de producción agrícola y forestal (López-Hernández & Ojeda 1996). Actualmente unas 615 000 has han sido sustituidas por plantaciones de pino caribe (Pinus caribaea var. hondurensis Barr. & Golf.), lo cual representa la mayor área del trópico con una plantación forestal monoespecífica (Cedeño et al. 2001). El estudio de este cambio de uso de la tierra reviste interés, ya que puede conducir a una modificación importante en la cantidad de carbono total en el suelo (Blair et al. 1997). De éste total, el carbono asociado a la biomasa microbiana ha sido considerado como el principal indicador de la tasa de recambio de carbono en el suelo (Cuevas & Medina 1998) por su papel como fuente y reservorio de nutrientes (Lodge et al. 1994, Leita et al. 1999); además de ser considerada como un indicador ecológico (Alef & Nannipieri 1995) por su capacidad de responder a corto plazo a los cambios en la calidad del suelo (Jenkinson & Ladd 1981). Por otro lado, la biomasa microbiana a través de su interacción con otros componentes biológicos, juega un papel preponderante en la regulación de las emisiones de algunos gases de efecto invernadero tales como el CO2 y en el secuestro de carbono; contribuyendo así, a mitigar los efectos negativos sobre el cambio climático.
Ya que el suelo forestal constituye una fuente de secuestro de carbono, es importante cuantificar la masa de carbono que se incorpora o se pierde en el suelo cuando un sistema de vegetación es sustituido por otro. La cuantificación de la proporción de la biomasa fúngica y bacteriana del total de la biomasa microbiana, puede llevarse a cabo a través de la respiración inducida por sustrato (RIS) (Anderson & Domsh 1978), mediante la utilización combinada de inhibidores selectivos (Nakamoto & Wakahara 2004). Su cuantificación, en términos de distinción de ambos componente microbianos es importante, ya que estos grupos de microorganismos juegan diferentes papeles en el reciclaje de nutrientes, y difieren en su capacidad para secuestrar el carbono dentro de su biomasa. Así, es posible establecer la contribución de cada componente al carbono total almacenado en el suelo y su longevidad; así como el destino del sustrato añadido al mismo (Bailey et al. 2002, 2003).
Si las bacterias tienen una eficiencia menor en la asimilación del C con respecto a los hongos, y por lo tanto almacenan menos carbono que el que metabolizan (Adu & Oades 1978), entonces es de esperar, que el carbono secuestrado en la biomasa microbiana sea más persistente cuando está mediado por la biomasa fúngica, y más lábil cuando esta mediado por la biomasa bacteriana (Biley et al. 2002). Evidentemente, aquel manejo del suelo que promueva una mayor abundancia de la flora micótica, promoverá un mayor secuestro del carbono en el suelo.
La técnica de la inhibición selectiva de la respiración permite el cálculo de la proporción relativa de hongos y bacterias del total de la biomasa microbiana (Parkinson 1994), así como la determinación de la relación biomasa fúngica:biomasa bacteriana (H:B), la cual no sólo expresa la estructura cambiante de las poblaciones microbianas del suelo (Beare et al. 1990, Wardle & Parkinson 1990, Frey et al.1999), sino también los cambios en su contenido de carbono. Una relación H:B=1 indica que los hongos y las bacterias contribuyen por igual a la actividad microbiológica del suelo (Biley et al. 2002).
Ya que el cambio de uso de la tierra puede afectar la composición de la biomasa microbiana y sus actividades (Carter et al. 1999), nosotros formulamos, que la sustitución de la sabana nativa por pinares en Uverito, acarrea consigo cambios en el contenido de carbono del suelo; por lo que los objetivos de esta investigación fueron: determinar, a través del método de la inhibición selectiva, la biomasa fúngica y bacteriana y la relación (H:B) en suelos de sabana nativa sustituidos por pinares, para establecer si estos parámetros son indicadores sensibles del secuestro de carbono en el suelo. Por otro lado, para complementar la información sobre la acción de los antibióticos empleados, se determinó la relación de aditividad del inhibidor (RAI) con el objeto de establecer, si los inhibidores microbianos (bactericidas y fungicidas), tuvieron actividad sobre otros organismos para los cuales éstos no estaban destinados; mientras que la inhibición total por efecto combinado del inhibidor (ITC) se llevó a cabo para determinar el porcentaje de la biomasa microbiana inhibido por la combinación de estos.
Materiales y métodos
Área de estudio: El área de estudio está localizada en Uverito, Venezuela, a una altitud entre 50-60 m por encima del nivel del mar. Es parte de una antigua altiplanicie del Pleistoceno conocida como Mesa de Guanipa (Brito et al. 1975). La sabana nativa de esta área está dominada por una vegetación herbácea (Trachypogon spp.) con aislados parches de árboles de bosques de vegetación semidecidua (Curatella americana, Bowdichia virgiloides y Byrsonimia crassifolia).
La zona está caracterizada por suelos altamente meteorizados y de baja fertilidad (Brito et al. 1975), lo cual se explica por su origen e historia erosiva. Éstos han sido clasificados como Arenic Haplustox, Psamentic Haplustox y Oxic Haplustults (Márquez et al. 1994). Las características físicas y químicas predominantes en los suelos de Uverito se muestran en el Cuadro 1.
El muestreo fue llevado a cabo durante el período de lluvias (valores promedio mensuales: precipitación 188.3mm, evaporación 154.46mm). La media anual de la temperatura del aire durante este período fue de 22.4°C, y la temperatura del suelo registrada en los primeros 10cm de profundidad fue de 28.1ºC (Vizáes 2004). El muestreo del suelo se realizó durante el período de lluvias, ya que en éste se ha registrado una mayor biomasa microbiana (Gómez 2004).
En el área objeto de estudio se seleccionaron tres sitios: la sabana nativa (8°31’ N, 62°38’ W), considerada como control, una plantación de P. caribaea var. hondurensis de 20 años (8°38’ N, 62°45’ W) y 29 años de edad (8°39’ N, 62°38’ W). En cada una se demarcaron 3 transectos, a lo largo de los cuales se establecieron cinco puntos de muestreo. En cada punto de muestreo se tomaron muestras por triplicado. Las muestras se homogenizaron para formar tres muestras compuestas por transecto, para un total de nueve muestras compuestas por parcela. Las muestras de suelo fueron recolectadas con un barreno a una profundidad de 0-10cm. La hojarasca del piso del bosque fue removida previamente al muestreo. Las muestras fueron colocadas en bolsas plásticas, transferidas al laboratorio, tamizadas (2mm) y almacenadas a 4ºC hasta su análisis.
Análisis físico y químico del suelo: El contenido de humedad fue determinado mediante un analizador de humedad, y el pH del suelo se estimó en agua (1:5). El carbono orgánico total se llevó a cabo por el método de oxidación del dicromato de Walkey-Black (Anderson & Ingram 1993), el N total por el método de Kjeldal (Bremner 1965) y la concentración de P total por el método colorimétrico del azul de molibdeno (Murphy & Riley 1962).
Biomasa microbiana: La biomasa microbiana (activa) se determinó mediante la técnica de la respiración inducida por sustrato (RIS) descrita por Stotzky (1965). Para ello, 50g de suelo a humedad de campo, previamente cernidos y estabilizados por 5 días a temperatura ambiente, se colocaron en recipientes de vidrio, de 500ml de capacidad, y se mezclaron con 400mg de glucosa disueltos en la cantidad de agua destilada necesaria para ajustar las muestras al 80 % de su capacidad de retención hídrica (CRH). El CO2 liberado durante el período de incubación (4 horas a 22ºC), fue atrapado en una solución de NaOH (0.1M) y titulado con HCl (0.1M). La biomasa microbiana fue calculada tomando en consideración: que 1 mlHCl (0.1M), equivale a 2.2mg de CO2, y que para un coeficiente de respiración igual a 1, se cumple que: 1mg de CO2/100 g.h=20.6 mg C-biomasa/100 g.
Inhibición selectiva de hongos y bacterias: La determinación de la biomasa fúngica y bacteriana se llevó a cabo según la metodología descrita por West (1986). La inhibición selectiva de los hongos y bacterias se realizó mediante el empleo de estreptomicina y cloranfenicol como inhibidores bacterianos, y cicloheximida como inhibidor fúngico. En esta investigación la razón del empleo de la estreptomicina y el cloranfenicol como inhibidores bacterianos se fundamentó, en que a pesar de que ambos antibióticos poseen actividad contra estos microorganismos (Malgor & Valsecia 1999), existen discrepancias sobre la efectividad de los mismos en la inhibición bacteriana. Los informes de Nakamoto & Wakahara (2004) sugieren que el cloranfenicol tiene una actividad antimicrobiana más efectiva sobre las bacterias; mientras que se ha señalado que la estreptomicina puede tener un efecto estimulante sobre la respiración microbiana (West 1986, Jonson et al. 1996, Lin & Brookes 1999).
La selección de la concentración de los inhibidores: estreptomicina, cloranfenicol y cicloheximida se realizó según los informes de Lin & Brookes (1999) y Nakamoto & Wakahara (2004). Al igual que la glucosa, los antibióticos seleccionados fueron disueltos en la cantidad de agua destilada necesaria para ajustar las muestras al 80% de su capacidad de retención hídrica. El CO2 determinado representó la respuesta de la inhibición de la respiración causada por el fungicida y el bactericida, y fue expresado en mg de Cmic/kg.
Para la determinación de la biomasa fúngica (BF), bacteriana (BB) y residual (BR), las muestras de suelo recibieron el siguiente tratamiento:
1. Suelo tratado con Glucosa (400mg/g).
2. Suelo tratado con Glucosa (400mg/g)+estreptomicina (4mg/g) o cloranfenicol (4 mg/g).
3. Suelo tratado con Glucosa (400 mg/g) +cicloheximida (8mg/g).
4. Suelo tratado con Glucosa (400mg/g)+estreptomicina (4mg/g) ó cloranfenicol (4mg/g)+cicloheximida (8mg/g).
De acuerdo a los basamentos de West (1986), la BF, BB y la BR se calculó considerando los siguientes aspectos:
A=biomasa microbiana activa
(A-B)=biomasa fúngica
(A-C)=biomasa bacteriana
D=biomasa residual
A-B/A-C=relación hongo:bacteria
El porcentaje de inhibición de la biomasa microbiana causado por el empleo de los antibióticos en forma individual y combinada se determinó así:
- IBB=[(A-C)/A]100=porcentaje de inhibición causado por la estreptomicina o cloranfenicol.
- IBF=[(A-B)/A]100=porcentaje de inhibición causado por la cicloheximida.
- IBR=[(A-D)/A]100=porcentaje de inhibición causado por la combinación de ambos antibióticos.
- La proporción de la biomasa fúngica y bacteriana se calculó así:
- 100[{(A-B)+(C-D)}/2]/(A-D)=proporción de hongos
- 100[{(A-C)+(B-D)}/2]/(A-D)=proporción de bacterias
Relación de aditividad del inhibidor (RAI): Se ha señalado que un problema de la técnica de inhibición selectiva de la biomasa microbiana, es la posibilidad de que los inhibidores tengan actividad sobre organismos para los cuales éstos no fueron destinados (ejemplo bactericidas que actúan sobre los hongos y fungicidas que actúan sobre bacterias) (Scheu & Parkinson 1994, Johnson et al. 1996, Velvis 1997, Lin & Brookes 1999).
En esta investigación la RAI fue calculada a partir de la respuesta de la respiración inducida por el sustrato (RIS), expresada como biomasa microbiana, de un suelo intacto y de un suelo tratado con estreptomicina o cloranfenicol como inhibidores bacterianos, y de cicloheximida como inhibidor fúngico; así como mediante el uso simultáneo de los inhibidores de ambos grupos de microorganismos (Beare et al. 1990). Ésta fue determinada de la siguiente forma:
RAI=[(A-B)+(A-C)]/(A-D).
Se ha establecido, que la relación de aditividad del inhibidor (RAI) sería igual 1.0 si no ocurre efecto inhibitorio sobre otros organismos para los cuales el antibiótico no fue elaborado. Una relación de aditividad >1.0, indica que el antibiótico tiene un efecto inhibitorio sobre otros organismos para los cuales éste no fue destinado (West 1986, Alphei et al. 1995, Velvis 1997, Nakamoto & Wakahara 2004), y una relación de aditividad <1.0 indica que éste tiene un efecto de estimulación sobre los microorganismos (Beare et al. 1990, Nakamoto & Wakahara 2004).
Inhibición total por efecto combinado del inhibidor (ITC): Expresa el porcentaje de la biomasa microbiana inhibida por la combinación de los inhibidores estreptomicinacicloheximida o cloranfenicol-cicloheximida (Lin & Brookes 1999) y fue calculada mediante la expresión:
ITC=((A-D)/(A))x100
Los resultados fueron analizados mediante ANOVA de dos vías, para determinar las diferencias entre las medias provocadas por el efecto de los antibióticos empleados, en forma individual o conjunta, sobre la biomasa microbiana activa; así como para determinar del impacto del cambio de uso de la tierra sobre la biomasa fúngica, bacteriana y residual, y la interacción de ambos factores. Los análisis estadísticos se realizaron a través del programa SPSS para Windows.
Resultados
Inhibición selectiva: El porcentaje de inhibición microbiana por efecto de la estreptomicina, el cloranfenicol y la cicloheximida, usados individualmente o en combinación, en suelos de la sabana nativa y las plantaciones de 20 y 29 años, no mostró variación significativa (Cuadro 2). Sin embargo, se puede apreciar que el empleo por separado de los mismos ejerció un mayor porcentaje de inhibición con respecto a su empleo en combinación.
Los valores de la BM (activa), BF, BB y BR obtenidos en suelos de la sabana nativa y las plantaciones de 20 y 29 años (Cuadro 3) variaron ente si (F=408.43, p<0.001; F= 177.05, p<0.001; F=9.331, p<0.001; y F=243.32, p<0.001, respectivamente). La plantación de 29 años presentó el mayor contenido de BM (99.06mg/kg) y BR (42.81mg Cmic/kg). En los pinares de 20 y 29 años dominó el componente fúngico (52.17-55.98mg/kg, respectivamente); mientras que en el sistema de sabana se observó una dominancia del componente bacteriano (34.77mg/kg) y una menor biomasa residual (12.25mg/kg).
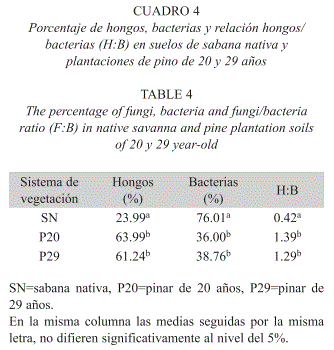
La determinación de las proporciones de hongos y bacterias presentes en los sistemas de sabanas y pinares (Cuadro 4), confirma que en el suelo de las plantaciones de 20 y 29 años existe una mayor proporción de hongos (63.99- 61.24%, respectivamente), en contraste con la sabana nativa, donde la mayor proporción de la biomasa microbiana está representada por las bacterias (76.01%). La relación hongos/ bacterias (H:B) determinada en los pinares de 20 y 29 años (1.39 y 1.29, respectivamente) no mostró variación significativa; sin embargo, ésta fue mayor (p<0.01) con respecto a la sabana nativa (0.42) (Cuadro 4).
Relación de aditividad del inhibidor (RAI): Los valores de la relación de aditividad del inhibidor (RAI) determinados por efecto de la combinación de los inhibidores: estreptomicina- cicloheximida y cloranfenicol-cicloheximida, variaron estadísticamente (p<0.05) entre si (Cuadro 5). Bajo ambas combinaciones de los inhibidores, el valor del RAI fue >1.0 en todos los sistemas estudiados; aunque éste fue menor en la sabana nativa (1.26 y 1.39, respectivamente) con respecto a los pinares de 20 (1.70 y 1.64, respectivamente) y 29 años (1.77 y 1.69, respectivamente).
Inhibición total por efecto combinado de los inhibidores (ITC): La inhibición total de los microorganismos causada por la combinación de los inhibidores: estreptomicinacicloheximida y cloranfenicol-cicloheximida en la sabana nativa fue de 76.09 y 61.18%, respectivamente. Estos valores variaron significativamente (p<0.001) con respecto a los de los pinares de 20 (57.39-58.26%, respectivamente) y 29 años (56.78-58.38%, respectivamente), en los cuales este índice resultó menor (Cuadro 5).
Discusión
A pesar de las controversias surgidas sobre la efectividad del uso de la estreptomicina y el cloranfenicol como inhibidores bacterianos (Nakamoto & Wakahara 2004), en esta investigación estos antibióticos, empleados individualmente y en combinación con la cicloheximida, no mostraron diferencias en el porcentaje de inhibición sobre la biomasa microbiana (Cuadro 2), por lo que ambos pueden ser usados indistintamente para esta determinación en suelos. La acción combinada de los inhibidores (estreptomicina-cicloexhimida y cloranfenicol- cicloheximida) fue menos eficiente que la individual; ya que la suma de los efectos antibióticos individuales, superaron los de la aplicación combinada.
Las diferencias en los valores de la BM (activa), BF y BB presentes en la sabana y los pinares (Cuadro 3), podrían relacionarse en parte con la calidad de los residuos y el contenido de carbono de estos sistemas. Otros factores que pueden estar relacionados con estas diferencias son las mejores condiciones microclimáticas presentes en los pinares y la eficiencia en la utilización del carbono (qCO2) de las poblaciones en estos sistemas, la cual se ha determinado que es mayor en las plantaciones de pinos de Uverito (Gómez 2004).
Los mayores valores de la biomasa fúngica (BF) observados en las plantaciones de pino de 20 y 29 años (Cuadro 3), soportan los informes de Anderson & Domsch (1975) y Scheu & Parkinson (1994), sobre una mayor abundancia de la proporción de hongos activos que de bacterias en estos sistemas, lo cual se asocia con grupos de organismos que descomponen más eficientemente los sustratos de baja calidad, que se caracterizan por poseer una alta relación C:N, altos contenidos de polifenoles recalcitrantes a base de lignina y taninos, así como los subproductos de su descomposición (Paul & Clark 1989).
La escasez de estudios dirigidos a determinar el efecto de la edad de las plantaciones sobre la biomasa microbiana, tanto en zonas tropicales como templadas, dificulta la comparación de los resultados obtenidos en esta investigación, en los cuales se observó un incremento de la biomasa microbiana con la edad de la plantación (Cuadro 3). Esto contrasta con los informes de Bauhus et al. (1998) quienes señalaron, que en plantaciones de coníferas, la biomasa microbiana disminuye con la edad de la plantación; efecto que los autores atribuyeron al bajo contenido de P presente en estas parcelas. Sin embargo, en suelos de Uverito, el pinar de 29 años presentó la mayor biomasa microbiana (Cuadro 3), a pesar de poseer el mayor contenido de P y C (Cuadro 1).
Los valores de la biomasa microbiana residual (BR) (Cuadro 3) reflejan que en el sistema de pinares existe un elevado contenido de biomasa microbiana para la cual los antibióticos empleados (estreptomicina, cloranfenicol y cicloheximida) no cumplieron una función inhibitoria total. En este sentido se han señalado varios factores que pueden reducir la efectividad de los antibióticos: (1) el tiempo de incubación de las muestras con los antibióticos (Badalucco et al. 1994, Landi et al. 1993), (2) su utilización como sustratos por otros organismos para los cuales no son específicos (Landi et al. 1993, Scheu & Parkinson 1994, Badalucco et al. 1994, Alphei et al. 1995), (3) la resistencia a los antibióticos por ciertos microorganismos (Heilmann et al. 1995, Imberger & Chiu 2001), (4) la ausencia o poco contacto de algunos microorganismos con los antibióticos en su paso a través del suelo (Alef & Sparling 1995) y (6) la textura y el pH del suelo (Coleman & Crossley 1996). Por consiguiente, rara vez hay una absoluta especificidad por un antibiótico, y esto va a depender del suelo y de la concentración de los antibióticos (Alef & Sparling 1995).
Con respecto al cambio de uso de la tierra en Uverito, la presencia de pinares en estos suelos ha traído consigo una serie de cambios en el microclima y en muchas propiedades físicas y químicas del suelo; factores que han afectado sus comunidades microbianas nativas, en los cuales se observa una mayor proporción de hongos (Cuadro 4), organismos capaces de emplear como sustratos la lignina presente en las acículas de las coníferas (Dix & Webster 1995). Esto confirma los resultados de Flores et al. (1982), quienes señalaron que la sustitución de la sabana nativa por plantaciones de pino en Uverito produce un cambio en la frecuencia génica de las poblaciones, y sustenta los informes que indican que en los suelos ácidos de bosques de coníferas, la biomasa fúngica excede a la bacteriana (Anderson & Domsh 1975, Scheu & Parkinson 1994).
Gran parte de la biomasa fúngica de estos sistemas, se deriva de microorganismos simbiontes tales como los hongos ectomicorrizógenos (Olsson 1999). Finlay & Soderstrom (1989) informaron que estos hongos contribuyen sustancialmente con la biomasa fúngica de bosques de coníferas y son los colonizadores dominantes de las especies de la familia Pinnaceae (Smith & Read 1997). En Uverito las plántulas de pino son inoculadas con la ectomicorriza Pisolithus tintoreus para alcanzar una mejora en la nutrición mineral y sobrevivencia de las mismas (Gross et al. 2004).
En contraste con el dominio de las poblaciones fúngicas en sistemas de pinares, en el sistema de sabana la mayor proporción de bacterias (Cuadro 4) está determinada por la calidad de la materia orgánica incorporada por la vegetación nativa, la cual se caracteriza por poseer una baja relación C:N (Brito et al. 1975). Evidentemente, el cambio de uso de la tierra en Uverito modifica en forma cuantitativa y cualitativa las poblaciones microbianas del suelo.
Los valores de la relación H:B obtenidos en esta investigación están en el ámbito de los señalados por diferentes autores. Para el sistema de pinares se ha informado una relación H:B entre 1.3 y 9.0 (Parkinson 1994), mientras que para suelos madereros se ha indicado una relación de 1.1-1.4 (Alphei et al. 1995) y de 1.5 para la capa orgánica de sistemas de pinares (Scheu & Parkinson 1994). La relación H:B obtenida en esta investigación en el sistema de sabana (0.42) (Cuadro 4), confirma una vez más la dominancia del componente bacteriano en este tipo cobertura; mientras que en sistemas de bosques los hongos comprenden el componente dominante del total de la biomasa microbiana (Anderson & Domsch 1975, Scheu & Parkinson 1994). Por lo tanto, éste es un parámetro sensible que evidencia el cambio de estructura poblacional, y por ende, el cambio del contenido de carbono en el suelo por efecto de la sustitución de la sabana por pinares en Uverito. Si consideramos que la relación H:B permite predecir el potencial de almacenamiento del carbono en el suelo y su longevidad (Bayley et. al 2002); y si se toma en cuenta que los hongos almacenan más carbono en su biomasa por unidad de carbono respirada, es evidente que en el sistema de pinares se producirá una mayor preservación del carbono en el suelo.
Los valores de la relación de aditividad del inhibidor (RAI) obtenidos con los tratamientos estreptomicina-cicloheximida y cloranfenicolcicloheximida resultaron ambos >1.0 tanto para la sabana (1.26-1.39, respectivamente) como para los pinares de 20 (1.70-1.64, respectivamente) y 29 años (1.77-1.69, respectivamente) (Cuadro 5). Bailey et al. (2002) señalaron que cuando el valor del RAI excede a 1.0, el exceso multiplicado por 100% refleja la inhibición de los organismos para los cuales los antibióticos empleados no estaban dirigidos; por lo que existe un enmascaramiento de las actividades de los mismos (West 1986). Los antibióticos pudieron haber afectado una fracción de las poblaciones objeto o no de ataque. Al considerar este razonamiento, podemos inferir que en los bosques de pino existe una elevada inhibición (64 al 77%) de organismos para los cuales los antibióticos no estaban dirigidos. Nuestros valores están en el ámbito de aquellos obtenidos por Imberger & Chiu (2001), quienes informaron sobre un valor del RAI de 1.62 en el suelo mineral de un pinar. Así mismo, Bailey et al. (2002) determinaron para suelos de bosques relaciones de aditividad de inhibidor de 1.25 y 1.13; mientras que Nakamoto & Wakahara (2004) señalaron valores del RAI de 0.97; 1.07; 1.26 utilizando diferentes concentraciones de inhibidores para suelos húmicos andosoles. Las razones que determinan las diferencias en el grado de inhibición de los microorganismos por antibióticos no específicos, es difícil de explicar (Bailey et al. 2002). Una explicación alternativa para un RAI >1.0, dada por West (1986), es que el uso de los antibióticos combinados no es tan eficiente, como cuando estos son aplicados individualmente. Efecto que se ve reflejado en esta investigación en el porcentaje de inhibición sobre la biomasa residual (IBR) (Cuadro 2). Beare et al. (1990) y Velvis (1997) recomendaron que el RAI debiera ser optimizado a 1.0, ya que el inhibidor que no está dirigido al blanco es una fuente de aparente enmascaramiento del efecto inhibitorio de los antibióticos. Por otro lado, West (1986) propuso que maximizar la inhibición total de la combinación de los inhibidores (ITC) era más importante que optimizar el RAI.
En esta investigación, el efecto inhibitorio total de la combinación de los antibióticos (ITC) empleados (estreptomicina-cicloheximida y cloranfenico-cicloheximida), resultó menor en los pinares de 20 y 29 años (Cuadro 5), lo cual confirma que en este sistema existe un mayor porcentaje de biomasa microbiana inhibida para la cual los antibióticos estaban o no dirigidos. Lin & Brookes (1999) señalaron que cuando el valor el RAI=1.0, el valor de ITC es máximo.
Cambio de uso de la tierra en Uverito y su efecto sobre el secuestro de carbono en la biomasa microbiana del suelo: El alarmante incremento de la concentración de dióxido de carbono en la atmósfera, uno de los gases de efecto invernadero, es uno de los principales factores del calentamiento global, y constituye una de las principales preocupaciones de los científicos en la actualidad; por lo que una gran parte de las investigaciones están dirigidas a tratar de contribuir en la solución de esta problemática. En este sentido, es conocido que el secuestro de carbono constituye una de las actividades que contribuye a mitigar los efectos negativos del CO2 sobre el cambio climático.
Los suelos forestales son los mayores depósitos de carbono en los ecosistemas terrestres, éstos contienen cuatro veces la cantidad de carbono que posee la vegetación (Jandl 2001). Los bosques son importantísimas "bombas de succión" de CO2 atmosférico y por lo tanto tienen un efecto depurador del aire. Este carbono secuestrado es mantenido durante mucho tiempo en las plantas vivas, en el mantillo y en el suelo forestal. Estas características de alta capacidad de fijación, retención de carbono, y duración del secuestro del carbono por unidad de superficie, hacen que los bosques constituyan importantes sumideros de CO2 atmosférico. Por eso merece especial atención, cuando se buscan mecanismos mediante los cuales se puede contribuir con el secuestro de carbono para mitigar el problema del calentamiento global del planeta.
Nuestros resultados confirman que la biomasa fúngica y bacteriana, y la relación H:B, determinadas a través del método de la inhibición selectiva, son indicadores sensibles de cambios en el contenido de carbono del suelo. Estos parámetros evidencian que la conversión de la sabana nativa a sistemas de pinares, conlleva a una variación en la composición microbiana del suelo, y que este cambio de uso de la tierra promueve el incremento de las poblaciones fúngicas. Este grupo de organismos juega un papel importante en el sistema de pinares, ya que ellos no sólo reducen las pérdidas por lixiviación y mejoran la absorción de los nutrientes por las plantas (Hernández-Valencia & Montserrat 2005); sino que la eficiencia en la utilización del carbono por parte de estos organismos (Bailey et al. 2002), promueve una mayor preservación del mismo en el suelo. Se ha señalado que en sistemas de pinares los hongos ectomicorrizógenos pueden contribuir a incrementar el pool de carbono en el suelo (Allen 1996). Estos organismos transforman los carbohidratos que toman de su hospedero a carbohidratos específicos tales como manitol y trehalosa, los cuales son almacenados dentro de su biomasa. Sylvia et al. (1999) informó que aproximadamente un 20% del total el carbono asimilado por las plantas puede ser transferido hasta el hongo simbionte. Dada las características de las ectomicorrizas de producir grandes cantidades de hifas sobre las raíces y el suelo (1m de raíz colonizada puede estar asociada con hasta 8km de micelio externo (Smith & Read 1997), y en especial en condiciones de bajo contenido de nutrientes, como es el caso de los suelos de Uverito, estos hongos se convierten en un importante sumidero de carbono que permite contrarrestar el incremento del mismo en la atmósfera. Esta característica cobra especial interés, si se considera que estas hifas persisten por prolongados períodos de tiempo y que se expanden profusamente en el suelo forestal (Dahlberg 1997; Bonello et al. 1998). Asociado a lo anteriormente expuesto, está la eficiencia que presentan los hongos en la utilización el carbono, durante la cual, una menor cantidad de CO2 es perdido por la respiración, mientras que una mayor proporción de carbono es incorporado a los tejidos microbianos (Silva et al. 2007).
Otro aspecto de interés asociado al secuestro de carbono en estudios realizados en Uverito, han demostrado que en esta zona ocurre una baja tasa de mineralización del mismo (Gómez 2004), lo cual permite preservarlo por más tiempo dentro del suelo. Esta reducida tasa de mineralización del carbono, está asociada con la calidad de la materia orgánica característica de este sistema (Melillo et al. 1982, Tian et al. 1992, Bird & Torn 2006). Evidentemente, en este contexto, la sustitución de la sabana nativa por plantaciones de pino caribe, es un manejo del suelo que contribuye al secuestro de carbono en Uverito.
Agradecimiento
Agradecemos al Consejo de Investigación de la Universidad de Oriente por el financiamiento del proyecto de investigación CI-3- 010101-1319/06.
Resumen
Cualquier transformación de un ecosistema natural a un sistema agrícola o forestal conduce a una modificación importante no sólo del pool del carbono total, sino también del carbono asociado con la biomasa microbiana. Su cuantificación es importante en la determinación del impacto de las prácticas agrícolas y el cambio de uso de la tierra sobre la calidad del suelo. El objetivo de este estudio fue determinar, a través del método de inhibición selectiva, la biomasa fúngica y bacteriana y la relación (H:B) en suelos de sabana nativa sustituidos por pinares (Pinus caribaea var. hondurensis), para establecer si éstos parámetros son indicadores sensibles de cambios en el contenido de carbono en suelos de Uverito, Venezuela. La relación de aditividad del inhibidor (RAI) y la inhibición total por efecto combinado del inhibidor (ITC) se llevaron a cabo para determinar, si los inhibidores microbianos tuvieron actividad sobre otros organismos para los cuales éstos no estaban destinados. La cuantificación de la biomasa fúngica y bacteriana se llevó a cabo mediante el uso de la cycloheximida como inhibidor fúngico, y la estreptomicina y el cloranfenicol como inhibidores bacterianos. Esta investigación evidencia que este cambio de uso de la tierra ejerció un efecto significativo sobre la biomasa microbiana del suelo, y muestra que en el sistema de pinares existe una dominancia del componente fúngico, en contraste con la sabana nativa, en la cual domina la biomasa bacteriana. La sustitución de la sabana nativa por plantaciones de pino en Uverito, promueve un mayor secuestro del carbono en el suelo. Los valores de la relación de aditividad del inhibidor (RAI) tanto para la sabana nativa como para el sistema de pinares, resultaron ambos >1.0. La inhibición total combinada (ITC) resultó menor en el sistema de pinares; a partir de lo cual, es posible inferir que una elevada proporción de la biomasa microbiana fue afectada por la combinación de los inhibidores.
Palabras clave: biomasa bacteriana, secuestro de carbono, biomasa fúngica, pinos, savana.
Recibido 01-VII-2008. Corregido 19-II-2010. Aceptado 22-III-2010.
Referencias
Adu, A.K. & J.M. Oades. 1978. Utilizationof organic materials in soil agregates by bacteria and fungi. Soil Biol. Biochem. 10: 117-122. [ Links ]
Alef, K. & P. Nannipieri. 1995. Méthod in applied soil microbiology and biochemestry. Academic, Nueva York, EEUU. [ Links ]
Alef, K. & G.P. Sparling. 1995. Differentiation by selective inhibitor techniques, p. 420-421. In K. Alef & P. Nannipieri (eds.). Method in applied soil microbiology and biochemistry. Academic, Londres, Inglaterra. [ Links ]
Allen, M. 1996. The ecology of arbuscular mycorrhizas: a lock back into the 20th century and a peek into the 21th. Mycol. Res. 100: 769-782. [ Links ]
Alphei, J., M. Bonkowski & S. Scheu. 1995. Aplication of the selective inhibition method to determine bacterial:fungal ratios in three beechwood soils rich in carbon- optimization of inhibitor concentrations. Biol. Fertil. Soils 19: 173-176. [ Links ]
Anderson, J.P.E. & K.H. Domsch. 1975. Measurement of bacterial and fungal contributions to respiration of selected agricultural and forest soils. Can. J. Microbiol. 21: 314-322. [ Links ]
Anderson, J.P.E. & K.H. Domsch. 1978. A physiological method for the quantitative measurement of microbial biomass in soil. Soil Biol. Biochem. 10: 215-221. [ Links ]
Anderson, J.M. & J.S. Ingram. 1993. Tropical soil biology and fertility. A Handbook of methods. CAB International, Wallingford, EEUU. [ Links ]
Badalucco, L., F. Pomarè, S. Grego, L. Landi & P. Nannipieri. 1994. Activity and degradation of streptomycin and cycloheximide in soil. Biol. Fertil. Soils 18: 334-340. [ Links ]
Bauhus, H., D. Paré & L. Coté. 1998. Effects of tree species stand age and soil type on soil microbial biomass and its activity in a southern boreal forest. Soil Biol. Biochem. 30: 1077-1089. [ Links ]
Bayley, V.L., J.L. Smith & H. Bolton Jr. 2002. Fungal-tobacterial ratios in soils investigated for enhanced C sequestrations. Soil Biol. Biochem. 34: 997-1007. [ Links ]
Bayley, V.L., J.L. Smith & H. Bolton Jr. 2003. Novel antibiotics as inhibitors for selective respiratory inhibition method of measuring fungal bacterial ratios in soil. Biol. Fertil. Soils 38: 154-160. [ Links ]
Beare, M.H., C.L. Necly, D.C. Coleman & W.L. Hargrove. 1990. A Substrate induced respiration (SIR) method for measurement of fungal and bacterial biomass on plant residues. Soil Biol. Biochem. 22: 285-594. [ Links ]
Bird, J.A. & M.S. Torn. 2006. Fine roots vs needles: a comparison of 13C and 15N dynamics in a ponderosa pine forest soil. Biogeochemistry 79: 361-382. [ Links ]
Blair, G. J., R.D.B. Lefroy, B.P. Singh & A.R. Hill. 1997. Development and use of a carbon management index to monitor changes in soil C pool size and turnover rate, p. 237-281. In G. Cadisch & K.E. Guiller (eds). Driven in Nature: Plant litter quality and decomposition. CAB International, Londres, Inglaterra. [ Links ]
Bonello, P., T.D. Bruns, M. Gardes.1998. Genetic structure of a natural population of the ectomycorrhizal fungus Suillus pungens. New Phytol. 138: 533-542. [ Links ]
Bremner, J.M. 1865. Total nitrogen, p. 1149-1178. In A. Black (ed.). Methods of soil analisys, part 2.C.A. Agronomy 9. Am. Soc. Agron, Madison, Wisconsin, EEUU. [ Links ]
Brito, P., J. Comerma & R. Carrizales. 1975. Aptitud de las tierras de la zona de Chaguaramas, Estado Monagas para la siembra de Pinus caribaea. Agron. Trop. 25: 255-304. [ Links ]
Carter, M.R., E.G. Gregorich, A. Angers, M.H. Beare, G.P. Sparling, D. Warle & R.P. Voroney. 1999. Interpretation of microbial biomass measurements for soil quality assessment in humid temperate regions. Can. J. Soil Sci. 79: 507-520. [ Links ]
Cedeño, L., C. Carrero, W. Franco & A. Torres.2001. Sphaeropsis sapinea asociado con quema de cogollo muerte regresiva y cáncer en troncos, ramas y raíces del pino caribe en Venezuela. Interciencia 26: 210- 215. [ Links ]
Coleman, D.C. & D.A. Crossley. 1996. Fundamentals of soil ecology. Academic, San Diego, California, EEUU. [ Links ]
Cuevas, E. & E. Medina. 1998. The role of nutrient cycling in the conservation of soil fertility in tropical forested ecosytems, p. 263-278. In B. Gopal, P.S. Patahak & K.G. Saxeana (eds.). An anthology of comtemporary ecological research. Ecol. Today. International Scientific Publications, New Delhi, India. [ Links ]
Dix, N.J. & J. Webster. 1995. Fungal ecology. Chapman & Hall, Londres, Inglaterra. [ Links ]
Dahlberg, A. 1997. Population ecology of Suillus variegatus in old Swedish Scots pine forests. Mycol. Res. 101: 47-54. [ Links ]
Finlay, R.D. & B. Söderstrom. 1989. Mycorrhizal micelia and their role in soil and plant communities, p. 139- 148. In Ecology of arable land-perspectives and changes. Vol. 1. Kluwer Academia, Londres, Inglaterra. [ Links ]
Flores, D.A., V. Malave & H. Bastardo. 1982. Mineralización de fósforo orgánico por actividad microbiana en suelos de sabana y de un bosque de Pinus caribaea var. hondurensis en Venezuela, p. 45-50. In C.C. Cerri, D. Athiè & D. Sodrzeieski (eds.). Coloquio regional sobre materia orgánica del suelo. Piracicaba, São Paulo, Brasil. [ Links ]
Frey, S.D., E.T. Elliot & K. Paustian. 1999. Bacterial and fungal abundance and biomass in conventional and no-tillage agroecosystems along two climatic gradients. Soil Biol. Biochem. 31: 573-585. [ Links ]
Gómez, Y. 2004. Parámetros bioquímicos y microbiológicos en los Llanos Orientales de Venezuela bajo diferentes uso de la tierra y prácticas de manejo. Tesis de Doctorado, Instituto Venezolano de Investigación Científica, Caracas, Venezuela. [ Links ]
Gross, E., L.T. Casagrande & F.H. Caetano. 2004. Ultraestructural study of ectomycorrhizas on Pinus caribeae Morelet. var. hondurensis, Barr & Golf seedling. Acta Bot. Bras. 18: 1-7. [ Links ]
Heilmann, B., M. Lebuhn & F. Beese. 1995. Method for the investigation of metabolic activities and shifts in the microbial community in a soil treated with a fungicide. Biol. Fertil. Soils. 19: 186-192. [ Links ]
Hernández-Valencia, I. & B. Montserrat. 2005. Cambios en el contenido de fósforo en el suelo superficial por la conversión de sabanas en pinares. Bioagro. 17:1-15. [ Links ]
Imberger, K.T. & C.Y. Chiu. 2001. Spatial changes of soil fungal and bacterial biomass from a sub-alpine coniferous forest to grassland in a humid, sub-tropical region. Biol. Fertil. Soils 33: 105-110. [ Links ]
Jandl, R. 2001. Secuestro de carbono en bosques. El papel del suelo. Rev. Forest. Iberoamericana 1: 57-62. [ Links ]
Jenkinson, D.S. & J.N. Ladd. 1981. Microbial biomass in soil: Measurement and turnover, p. 415-471. In E.A. Paul & J.N. Ladd (eds.). Soil biochemistry. Vol.5. Marcel Dekker, Nueva York, EEUU. [ Links ]
Johnson, C.K., M.F. Vigil, K.G. Doxtader & W.E. Beard. 1996. Measuring bacterial and fungal substrateinduced respiration in dry soils. Soil Biol. Biochem. 28: 427-432. [ Links ]
Landi, L., L. Badalucco, F. Pomarè & P. Nannipieri. 1993. Effectiveness of antibiotics to distinguish the contributions of fungi and bacteria to net nitrogen mineralization, nitrification and respiration. Soil Biol. Biochem. 25: 1771-1778. [ Links ]
Leita, L., M. De Nobile, C. Mondini, G. Muhlbachora, L. Marchiol, G. Bragato & M. Contin. 1999. Influence of inorganic fertilization on soil microbial biomass, metabolic quotient and heavy metal bioavailability. Biol. Fertil. Soils 28: 371-376. [ Links ]
Lin, Q. & P.C. Brookes.1999. An evaluation of the substrate induced respiration method. Soil Biol. Biochem. 31: 1969-1983. [ Links ]
Lodge, D.J., W.H. McDowell, & C.P. McSwiney. 1994. The importance of nutrient pulses in tropical forest. Tree 9: 384-387. [ Links ]
López-Hernández, D. & A.D. Ojeda. 1996. Alternativas en el manejo agroecológico de los suelos de las sabanas del Norte de Suramérica. Ecotrópicos 2: 101-107. [ Links ]
Malgor, L.A. & M.E. Valsecia. 1999. Antibióticos de Amplio Espectro: Tetraciclinas – Cloranfenicol- Macrólidos, p. 34-45. In L.A. Malgor & M.E. Valsecia (eds.). Farmacología médica, Cátedra de Farmacología Facultad de Medicina, Universidad Nacional del Noreste, Argentina. [ Links ]
Márquez, O., R. Hernández Gil, W. Franco & F. Visáez. 1994. Factores edáficos y estado nutricional de plantaciones de Pinus caribaea en relación a la muerte regresiva, en Uverito, Estado Monagas. Venesuelos 2: 15-18. [ Links ]
Melillo, J.M., J.D. Aber & J.F. Muratore. 1982. Nitrogen and lignin control of hardwood leaf litter decomposition dynamics. Ecol. 63: 621-626. [ Links ]
Murphy, J. & J.P. Riley. 1962. A modified single solution method for the determination of phosphate in natural water. Anal. Chim. Acta 27: 31-36. [ Links ]
Nakamoto, T. & S. Wakahara. 2004. Development of substrate induced respiration (SIR) method combined with selective inhibition for estimating fungal and bacterial biomass in humic andosols. Plant Prod. Sci. 7: 70-76. [ Links ]
Olsson, P.A. 1999. Signature fatty acids provide tools for determination of the distribution and interactions of mycorrhizal fungi in soil. F E M S. Microbiol. Ecol. 29: 303-310. [ Links ]
Parkinson, D. 1994. Filamentous fungi, p. 329-350. In R.W. Weaver, S. Angle, P. Bottomly, D. Bezdicek & S. Smith (eds.). Methods of analysis. Part 2. Microbiological and biochemical properties. Soil Sci. Soc. Am. Madison, Wisconsin, EEUU. [ Links ]
Paul, E.A. & F.E. Clark. 1989. Soil microbiology and biochemistry. Academic, San Diego, California, EEUU. [ Links ]
Scheu, S. & D. Parkinson. 1994. Changes in bacterial and fungal biomass C, bacterial and fungal biovolume and ergosterol content after drying, remoistening and incubation of different layer of cool temperate forest soils. Soil Biol. Biochem. 26: 1515-1525. [ Links ]
Silva, M.B., H.J. Klieman, P.M. da Silveira & A.C. Lanna. 2007. Atributos biológicos do solo sob influência da cobertura vegetal e do sistema de manejo. Pesq. Agropec. Bras. Brasilia 42: 1755-1761. [ Links ]
Sylvia, D.M. 1999. Mycorrhizal simbiosis, p. 408-426. In Sylvia, D.M., J.J. Fuhrmann, P.E. Hartel & D.A. Zuberer (eds.). Principles and applications of soil microbiology. Prentice-Hall, Londres, Inglaterra. [ Links ]
Smith, S.E. & D.J. Read. 1997. Micorrhizal Symbiosis. Academic, San Diego, California, EEUU. [ Links ]
Stotky, G. 1965. Microbial respiration, p. 1550-1570. In C.A. Black, D.D. Evans, L.E. Esminger, J.L. White & F.E. Clark (eds). Methods of soil analysis, part 2. Chemical and microbiological properties. Agronomy, Madison, Wisconsin, EEUU. [ Links ]
Tian, G., B.T. Kang & L. Brussard. 1992. Biological effects of plant residues with contrasting chemical composition under humid tropical condition, decomposition and nutrient release. Soil Biol. Biochem. 24:1051- 1060. [ Links ]
Visáez, F.J. 2004. Anuario climatológico para el período 1991-2004 en CVG- PROFORCA, CVG- Productos forestales de Oriente. El Merey, Venezuela. [ Links ]
Velvis, H. 1997. Evaluation of the selective respiratory inhibition method for measuring the ratio of fungal:bacterial activity in acid agricultural soils. Biol. Fertil. Soils 25: 354-360. [ Links ]
Wardle, D.A. & D. Parkinson. 1990. Response of the soil microbial biomass to glucose and selective inhibitors, across a soil moisture gradient. Soil Biol. Biochem. 22: 825-834. [ Links ]
West, A.W. 1986. Improvement of the selective respiratory inhibition technique to measure eukaryote:prokaryote ratios in soil. J. Microbiol. Methods 5: 125-138. [ Links ]