Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.47 n.3 San José Sep. 1999
Grande de Santa Marta, Caribe Colombiano
Liliana Torres Castro1 Adriana Santos-Martínez2 Arturo Acero P. 3
Recibido 17-VII-1998. Corregido 9-III-1999. Aceptado 11-III-1999.
Abstract
From February 1993 through January 1994 a total of 890 individuals of Bairdiella ronchus (Cuvier) were captured in the Ciénaga Grande de Santa Marta (CGSM). Most were caught with casting nets, using the "corral" (pen) artisan method. The fish sizes and weights varied between 66 and 231 mm total length (TL), and between 3.5-156.2 g respectively. The species is typically estuarine, distributed in salinities between 7.3 and 37.3. Female gonadosomatic index (GSI) was 2.97-5.09 (males: 0.32-1.09). The serial correlation method did not find a direct relationship between salinity and GSI. Mean eggs size was 198.65 µm, mean fecundity was 188 964 eggs/individual and is directly related to total length and total weight. The condition factor (K) presented an annual mean of 0.013, and its variation seems to be related to that of the GSI. Mean maturity size is 158 mm TL for females and around 154 mm TL for males. The sex rate was 2.7 females per male.
Key words
Bairdiellaronchus, gonadosomatic index, fecundity, mean size maturity.
En la Ciénaga Grande de Santa Marta (CGSM) el siaénido Bairdiella ronchus es una especie muy explotada, como lo demuestra la alta frecuencia de individuos capturados actualmente por pescadores con diferentes artes de pesca (corral, boliche, atarraya). Es un organismo típicamente estuarino con amplia distribución en la ciénaga y representa un importante recurso pesquero para los habitantes de la región. Por lo tanto, es necesario conocer de manera más detallada su biología reproductiva, con el fin de promover el aprovechamiento sostenible y la administración adecuada del recurso.
Esta especie se captura con atarraya en la costa colombiana del Caribe en fondos arenosos, y crece hasta unos 35 cm, aunque la mayoría de los ejemplares capturados no llegan a 30 cm (Dahl 1971). En la CGSM, Barrios (1981) clasificó a esta especie como eurihalina y con una alta abundancia. Santos-Martínez (1989) incluyó a B. ronchus según la frecuencia en la categoría de especie moradora. Santos-Martínez y Acero (1991) registraron 10 géneros con 11 especies de esta familia, todas de importancia comercial, además de las características biológicas más importantes de B. ronchus, como la proporción de sexos, intervalo de tallas y su distribución en la CGSM.
Se investigaron algunos aspectos biológicos como el factor de condición, estados de madurez gonadal, proporción sexual, fecundidad e índice gonadosomático, con el objeto de aportar la información necesaria para planificar el uso sostenible de la especie.
Materiales y Métodos
El estudio se realizó en la CGSM, situada en la costa colombiana del Caribe (NW del Dpto. Magdalena, plano deltaico del Río Magdalena). Se caracteriza por ser un ecosistema lagunar-estuarino, con un área aproximada de 450 km2 (10° 45', 11° 00' N y 74° 30', 74° 15' W). Esta región presenta dos períodos climáticos secos (mayor: diciembre-abril, menor: julio-agosto) y dos lluviosos (mayor: septiembre-noviembre, menor: mayo-junio) (IGAC 1973).
La toma de las muestras se realizó de febrero de 1993 a enero de 1994, en cuatro estaciones en la CGSM: Boca de la Barra (10° 59.2' N y 74° 17.5' W), Río Fundación (10° 43.9' N y 74° 25.6' W), Caño Grande (10° 50.4' N y 74° 28.8' W) y Caño Clarín (10° 57.7' N y 74° 29.7' W). Las muestras se recolectaron semanalmente (cuatro salidas mensuales) durante el día utilizando diversos artes de pesca. En la primera semana de cada mes se emplearon una atarraya grande y una pequeña. En la segunda semana se empleó una red de arrastre y en la tercera y cuarta semana, los ejemplares se adquirieron directamente a los pescadores de la zona, quienes utilizan el método del corral y el método del boliche que emplea un trasmallo bolichero. En cada estación se tomó la temperatura, utilizando un termómetro Brand de escala 1-50 °C; la salinidad, se determinó a tres profundidades (fondo, mitad de la columna y superficie) con un conductímetro WTW L91; la transparencia se midió con el disco Secchi, y la profundidad con una vara metrada.
En el laboratorio del Instituto de Investigaciones Marinas y Costeras (INVEMAR), se analizaron 890 individuos capturados durante el año de muestreo para conocer su sexo y el estado de madurez gonadal mediante la observación macroscópica de las gónadas, tomando como referencia la clasificación cualitativa propuesta por Holden y Raitt (1975) modificada por Santos-Martínez (1989) en:
I Inmaduro: Ovarios y testículos cerca de 1/3 de la longitud de la cavidad abdominal. Ovarios rosáceos, traslúcidos y huevos invisibles a simple vista; testículos blancuzcos.
II Madurando: Ovarios y testículos cerca de 2/3 de la longitud de la cavidad abdominal. Ovarios de color rosáceo amarillo con aspecto granular, no hay huevos transparentes o traslúcidos visibles; testículos blancuzcos a crema.
III Maduro: Ovarios y testículos ocupan 2/3 a toda la longitud de la cavidad abdominal. Ovarios de color naranja rosáceo con vasos sanguíneos superficiales visibles; grandes huevos maduros, transparentes. Testículos blancuzcos crema, blandos.
IV Desovados: Ovarios y testículos contraídos cerca de la mitad de la longitud de la cavidad abdominal. Paredes flojas. Los ovarios pueden contener restos de huevos opacos, maduros, en desintegración, oscurecidos a traslúcidos. Testículos sanguinolentos y flácidos.
Juveniles (indiferenciados). Para obtener el índice gonadosomático se tomó el peso total (PT) y el peso de las gónadas (PG) de cada individuo con una balanza eléctrica Mettler AE 200 de precisión 0.001. La longitud total se midió con un ictiómetro de 350 mm. El Factor de Condición K de Fulton (Bagenal y Tesch 1978) se calculó para estimar la condición, robustez o estado de bienestar de los peces. Para conocer la proporción entre machos y hembras se aplicó la prueba de Chi cuadrado. En la evaluación del desarrollo gonadal se utilizó el índice gonadosomático (IGS), propuesto por Holden y Raitt (1975), para observar la variación estacional de la actividad reproductiva. Para probar la relación entre la salinidad y el IGS, se aplicó el método de correlación serial de Box y Jenkins (1976). Para estimar la fecundidad se extrajo una submuestra de 50 gónadas de las hembras en la fase madura (III), se depositaron en la solución de Gilson modificada (Bagenal y Tesch 1978), posteriormente se determinó el número de ovocitos y el diámetro con un contador de partículas electrónico marca Coulter Counter Model Z.M. La fecundidad se obtuvo con la ecuación propuesta en Holden y Raitt (1975). Se hizo un análisis de regresión simple entre la fecundidad y la longitud total, peso total y peso eviscerado, para conocer cual de estas variables guarda una mayor relación. Se utilizó el método estadístico propuesto por Udupa (1986) para estimar la talla promedio de madurez.
Resultados
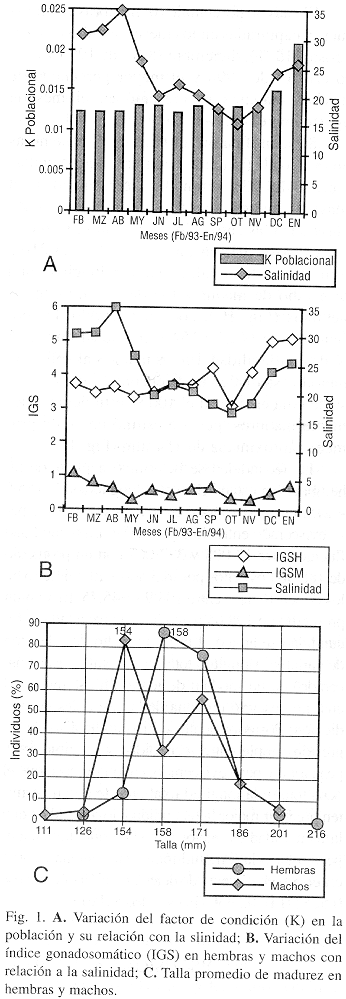
Los individuos de B. ronchus fueron capturados por los métodos de corral en un 66%, atarraya 28%, boliche 5% y red de arrastre 1%, de los cuales se identificaron 643 hembras, 239 machos y 8 indiferenciados. Se encontró una proporción sexual de 2.7 hembras por cada macho, existiendo una diferencia significativa con respecto a una proporción 1:1 (X2 = 185.06 , p= 95%). El promedio anual del factor de condición (K) de la población no varió significativamente ( X = 0.013), presentando un incremento en los meses de diciembre y enero (Fig. 1A), el K promedio anual en las hembras fue de 0.014 y en los machos de 0.013. El índice gonadosomático (IGS) en las hembras varió entre 2.97 y 5.09 y en los machos entre 0.32 y 1.09 (Fig. 1B).
No se probó una correlación directa entre la salinidad y el índice gonadosomático. La temperatura superficial y la transparencia presentaron un patrón definido de acuerdo con los períodos de lluvia y sequía.
En cuanto al número de individuos capturados en cada una de las estaciones, se encontró una gran diferencia entre hembras, machos e indiferenciados. En la Boca de la Barra 72 hembras, 6 machos; Río Fundación 352 hembras, 105 machos, 8 indiferenciados; Caño Grande 69 hembras, 39 machos; Caño Clarín 150 hembras, 89 machos. Con relación a los estados de madurez gonadal en hembras y machos, se observó un mayor número de organismos en estado II (126 hembras, 198 machos) y III (515 hembras, 36 machos). El estado I presentó muy pocos organismos (1 hembra, 5 machos) y en estado IV se encontró una hembra.
El mayor porcentaje de hembras maduras fueron capturadas en los meses de julio (13 %), agosto (15 %), diciembre (8 %) de 1993 y enero (10 %) de 1994 y el mayor porcentaje de machos maduros se presentó en el mes de agosto con el 44.4 %.
Se identificaron un total de 515 hembras en estado III (maduras) con un rango de tallas entre 141.4-231.4 mm (LT), presentándose el mayor número respecto a la captura en cada clase de tallas entre 156.4-171.4 mm; y 36 machos (estado III) en un rango de 141.4-216.3 mm de longitud total. La talla en longitud total promedio de madurez fue de 158 mm en las hembras (Fig. 1C), con un intervalo de confianza entre 142.4 a 154.1 mm de LT con el 95 % de confiabilidad. En los machos al aplicar el método estadístico no se encontró ninguna clase de talla en el cual el 100 % estuvieran totalmente maduros, pero se estimó una talla promedio aproximada de 154 mm (Fig. 1C).
La fecundidad se determinó a partir de 50 hembras (en estado III) entre longitudes de 155.5 y 215.0 mm, peso total entre 53.4 y 130.9 g y peso eviscerado entre 43.5 y 116.0 g. La fecundidad fluctuó entre 17 005 y 337 067 con un promedio de 188 964 ovocitos por individuo. El diámetro de los ovocitos varió entre 108.9 y 345.75 µm con un promedio de 198.65 µm. Una vez calculada la fecundidad se aplicó el procedimiento de selección de variables (longitud total, peso total y peso eviscerado) en un modelo de regresión (Stepwise) el cual no descartó ninguna de las variables de predicción. Posteriormente se hizo un análisis de regresión simple entre fecundidad y longitud total, peso total y peso eviscerado, encontrándose que el peso total y la longitud total en este orden permiten predecir mejor la fecundidad, lo que indica que la fecundidad es mayor a medida que aumenta el peso total o la longitud total, esto teniendo como criterio el coeficiente de determinación que fue r2= 0.5252 (Lt), 0.5439 (Pt) y 0.4675 (Pe).
Discusión
Los resultados del factor de condición están influenciados por la disponibilidad, cantidad y calidad del alimento presente en el medio, por los cambios fisiológicos de la especie y los factores abióticos de cada sistema (Wootton 1990). Para la especie en estudio, el valor del K poblacional varió con relación a los cambios de salinidad, ya que se observó que la condición de los peces mejoró al comienzo de la época de alta salinidad (diciembre-enero). Los demás valores del K en esta época (febrero-mayo) variaron poco, al igual que en la época de baja salinidad (junio-noviembre) (Fig. 1A). El incremento del K no está relacionado con la alimentación ya que todo el año se encontraron estómagos con alimento (70 % de la muestra). Este incremento se atribuye al desarrollo gonadal debido a que en la época de mayor salinidad alcanzó sus valores máximos (Fig. 1B). Mendo y Samame (1988) afirmaron que la condición del pez es un factor importante en el desarrollo de los órganos sexuales. Lo anterior se corrobora con algunas especies que han sido estudiadas en la CGSM, en las que el factor de condición depende de la reproducción como en Mugil incilis (Blanco 1983), M. curema (Flórez 1986) y Oligoplites saurus (Duque et al. 1996).
De acuerdo con nuestras observaciones las hembras de B. ronchus se reproducen todo el año, ya que se registró una alta proporción de hembras maduras en las cuatro estaciones de muestreo, alcanzando la máxima frecuencia de individuos maduros de diciembre a febrero, cuando se observaron las gónadas más desarrolladas con ovocitos de 208.33 µm de diámetro promedio y el índice gonadosomático (IGS) alcanzó sus valores máximos en enero/94, extendiéndose la reproducción hasta finales de mayo cuando el valor del IGS disminuyó. Luego comienza otra etapa menor de maduración y reproducción de junio a septiembre, con un desove menor en octubre. Mendo y Samame (op. cit.) afirman que el índice gonadosomático sugiere un patrón definido de desove, en el cual hay un incremento del IGS en la época de madurez y un decremento de los valores de IGS cuando ocurre la época de desove. De lo anterior se deduce que esta especie presenta desoves poblacionales parciales y dos picos principales de desove durante el año, uno mayor de diciembre a febrero (época de alta salinidad) y otro menor de julio a septiembre (época baja salinidad). Algo similar encontraron Chavance et al. (1984) en la especie Bairdiella chrysoura, la cual realiza su reproducción de noviembre a julio con un pulso de mayor intensidad de febrero a abril, estableciendo con base en otros estudios que esta especie madura todo el año y el desove lo realiza fuera de la Laguna de Términos. Caselles (1994) reportó que en las especies de engraulidos presentes en la CGSM, la reproducción se ve favorecida por el aumento de la salinidad. Resultados similares se encontraron para B. ronchus.
La proporción sexual para esta especie (2.7:1) es resultado de la actividad reproductiva y no de la migración de las hembras, a diferencia de lo observado por Chavance et al. (op. cit.) para B. chrysoura.
La ausencia de hembras desovadas (estado IV) de B. ronchus sugiere que el desove podría ocurrir en el mar adyacente. Barrios (1981) afirmó que en la CGSM el desove de esta especie se realiza en áreas aledañas al mar. Sin embargo, entre mayo de 1993 y enero 1994 no se capturó ningún ejemplar de B. ronchus en el mar, cerca a la Boca de la Barra, lo que concuerda con las observaciones de Hernández (1986) e INPA-CIID-UNIMAGDALENA (1991) para las áreas aledañas al mar en la región de Santa Marta. La presencia de hembras maduras todo el año en las cuatro estaciones de muestreo y la captura esporádica de juveniles en el Río Fundación nos hace pensar que el desove ocurre dentro de la Ciénaga. Estudios de peces en la CGSM, han registrado la presencia de juveniles de B. ronchus en la Boca de la Barra y Caño Clarín (Lamprea 1990), la parte norte, sur, este y oeste de la Ciénaga a excepción de La Rinconada (López 1988). Yáñez-Arancibia et al. (1985) establecieron que B. chrysoura utiliza los pastos dulceacuícolas y los manglares como hábitat de protección para huevos, larvas y juveniles.
La talla promedio de madurez obtenida fue de 158 mm, con un intervalo de confianza entre 142.4 a 154.1 mm de LT. En comparación, Johnson (1978) registró intervalos de madurez para B. chrysoura entre 130-140 mm y 150-210 mm y Chavance et al. (op. cit.), encontraron que la talla de primera madurez ocurrió entre 100 y 104 mm de LT. Por otra parte, los valores de fecundidad absoluta de B. chrysoura según Chavance et al. (op. cit.), fluctuó entre 9 700 y 93 900 ovocitos para peces de 86 a 142 mm de LT con un promedio de 35 068 ovocitos/individuo. En este estudio la fecundidad absoluta de B. ronchus varió entre 17 005 a 337 067 ovocitos/individuo, en organismos de 155.5-215.0 mm de LT con un promedio de 188 964 ovocitos/individuo. Lo anterior muestra que la diferencia en la fecundidad de ambas especies es debido a la diferencia en las tallas.
Chavance et al. (op. cit.) reportaron que en B. chrysoura la longitud total fue el mejor predictor de la fecundidad. Yáñez-Arancibia et al. (op. cit.) encontraron para la misma especie que la fecundidad es alta y está correlacionada con la talla. Estos datos concuerdan con nuestras observaciones para B. ronchus, el peso total y la longitud total están directamente relacionadas con la fecundidad.
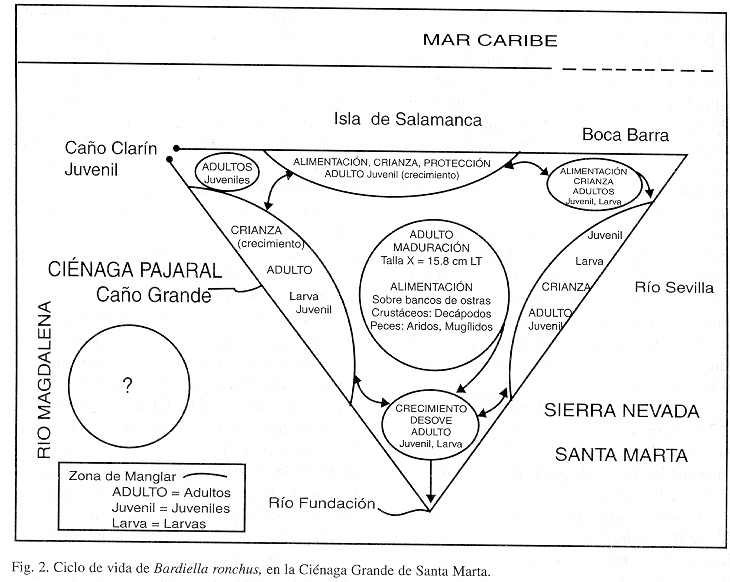
A partir de la información obtenida por este y otros estudios realizados en la CGSM, se propone un modelo esquemático del ciclo de vida de B. ronchus (Fig. 2), en la cual se ilustra en términos generales la ocurrencia de juveniles y larvas en las zonas de manglar, que se caracteriza por ser área de alimentación, crianza y protección de la especie, mientras que los adultos se distribuyen en toda la Ciénaga, especialmente hacia la parte central donde se alimentan sobre bancos de ostras (crustáceos y peces), sur (Río Fundación) y oeste (Caño Clarín). Estas zonas corresponden a sitios de crecimiento y maduración.
Agradecimientos
El desarrollo del presente trabajo se llevó a cabo gracias al aporte económico y logístico del Instituto Colombiano de Ciencia y Tecnología Francisco José de Caldas-COLCIENCIAS y el INVEMAR. Así mismo se agradece aquellas personas que orientaron y ayudaron con sus aportes en la ejecución del trabajo, en especial a Ernesto Mancera, Gerardo Palacio, María José Valencia, Emperatriz Zapata, Ramón Giraldo y Walberto Troncoso.
Resumen
De febrero 1993 a enero 1994 se capturó en la Ciénaga Grande de Santa Marta (CGSM), un total de 890 individuos de Bairdiella ronchus (Cuvier), en su gran mayoría con atarraya mediante el método de corral. La talla y el peso del pez varió entre 66 y 231 mm de longitud total (LT) y 3.5 a 156.2 g de peso total (PT) repectivamente. Es una especie típicamente estuarina y se distribuye entre salinidades de 7.3 a 37.3. Los valores del índice gonadosomático en las hembras (IGS) oscilaron entre 2.97-5.09 y en los machos entre 0.32-1.09. El método de correlación serial, no estableció una relación directa entre la salinidad y el IGS. El tamaño promedio de los ovocitos fue 198.65 µm. La fecundidad promedio fue de 188 964 ovocitos por individuo y esta relacionada directamente con la longitud total y el peso total. El factor de condición (K) presentó un promedio anual de 0.013 y se encuentra relacionado con el IGS. La longitud total promedio de madurez fue de 158 mm en hembras y aproximadamente 154 mm en machos. La proporción de sexos fue de 2.7 hembras por macho.
References
Bagenal, T.B. & F.W. Tesch. 1978. Age and growth, p.101-136. In T. Bagenal (ed.). Methods for assessment of fish production in fresh waters. Blackwell, Oxford. [ Links ]
Barrios, D.M. 1981. Estudio bioecológico de las capturas de peces con redes agalleras en la Ciénaga Grande de Santa Marta. Tesis de Licenciatura, Universidad Nacional de Colombia, Bogotá, Colombia. [ Links ]
Blanco, J. A. 1983. The condition factor of Mugil incilis Hancock (Pisces:Mugilidae) and its seasonal changes in the Ciénaga Grande de Santa Marta, Colombia. An. Inst. Invest. Mar. Punta Betín 13:133-42. [ Links ]
Box, G.E.P. & G. M. Jenkins. 1976. Time series analysis forecasting and control. Holden-Day, San Francisco. 419 p. [ Links ]
Caselles, A. 1994. Aspectos biológicos de algunas especies de Engraulididae (Pisces:Clupeiformes) existentes en la Ciénaga Grande de Santa Marta y Ciénaga de Pajaral, Caribe Colombiano. Tesis de Maestría, Universidad Nacional de Colombia, Bogotá, Colombia. [ Links ]
Chavance, P., D. Flores, A. Yañez-Arancibia & F. Amezcua. 1984. Ecología, biología y dinámica de las poblaciones Bairdiella chrysoura en la Laguna de Términos, sur del Golfo de México (Pisces: Sciaenidae). An. Inst. Cien. del Mar y Limnol. UNAM. 11:123-162. [ Links ]
Dahl, G. 1971. Los peces del Norte de Colombia. INDERENA, Bogotá. 391 p. [ Links ]
Duque, G., A. Acero & A. Santos-Martínez. 1996. Aspectos reproductivos de Oligoplites saurus y Oligoplites palometa (Pisces:Carangidae) en la Ciénaga Grande de Santa Marta, Caribe Colombiano. Carib. J. Sci. 31 (3-4) : 317-26. [ Links ]
Flórez, M. R. 1986. Algunos aspectos biológicos-pesqueros y ecológicos de la "anchoveta" Mugil curema (Valenciennes, 1836) en la Ciénaga Grande de Santa Marta y el mar adyacente, Colombia (Pisces: Mugilidae). Tesis de Licenciatura, Pontificia Universidad Javeriana, Bogotá, Colombia. [ Links ]
Hernández, A. 1986. Desarrollo de la pesca artesanal en la región de Santa Marta. COLCIENCIAS, Bogotá. 261 p. [ Links ]
Holden, M. J. & D.F.S. Raitt. 1975. Manual of fisheries science. Part 2. Methods of resource investigations and their application. FAO Fish. Tech. Pap. 115:1-214. [ Links ]
IGAC. 1973. Monografía del Departamento del Magdalena. Inst. Geog. "Agustín Codazzi", Bogotá. 162 p. [ Links ]
INPA-CIID-UNIMAGDALENA. 1991. Proyecto integral de investigaciones y desarrollo de la pesca artesanal marítima en el área de Santa Marta. INPA-CIID-UNIMAGDALENA, Santa Marta, Colombia. s. p. [ Links ]
Johnson, D.G. 1978. Development of fishes of the mid-atlantic bight. An atlas of egg larval and juvenile stages. IV: 172-179 [ Links ]
Lamprea, L. T. 1990. Aspectos ecológicos de los juveniles de peces en la Ciénaga Grande de Santa Marta con énfasis en las Ciénagas menores del margen occidental. Tesis de Maestría, Universidad Nalcional de Colombia, Bogotá, Colombia. [ Links ]
López, R. 1988. Contribución al estudio bioecológico del ictioplancton de la Ciénaga Grande de Santa Marta, Caribe Colombiano. Tesis de Licenciatura, Universidad Nacional de Colombia, Bogotá, Colombia. [ Links ]
Mendo, J. & M. Samame. 1988. Análisis biólogico-pesquero y poblacional de la cachema (Cynoscion analis) del área de Paita, Perú. Bol. Inst. Mar Perú 12(2):27-57 [ Links ]
Santos-Martínez, A. 1989. Estudio biológico y ecológico de la ictiofauna de la Ciénaga Grande de Santa Marta, Caribe Colombiano. Tesis de Maestría, Universidad Nacional de Colombia, Bogotá, Colombia. [ Links ]
Santos-Martínez, A. & A. Acero. 1991. Fish community of the Ciénaga Grande de Santa Marta (Colombia): Composition and zoogeography. Ichthyol. Explor. Fresh Waters 2(3):247-263. [ Links ]
Udupa, K.S. 1986. Statistical method of estimating the size at first maturity in fishes. Fishbyte 2: 8-10. [ Links ]
Wootton, R.J. 1990. Ecology of teleost fishes. Chapman & Hall, Londres. 404 p. [ Links ]
Yáñez-Arancibia, A., A. L. Lara-Dominguez, A. Aguirre Leon, S. Díaz Ruiz, F. Amezcua Linares, D. Flórez Hernández & P. Chavance. 1985. Ecología de poblaciones de peces dominantes en estuarios tropicales: Factores ambientales que regulan las estrategias biológicas y la producción, p. 311-365. En A. Yáñez-Arancibia (ed.). Ecología de comunidades de peces en estuarios y lagunas costeras. U NAM, México, D.F. [ Links ]
1 Centro Epomex. Av. Agustín Melgar y Juan de la Barrera s/n. AP. 520 Campeche 24030, Campeche. México. Fax: (52) (981) 65954. Correo electrónico: litorres@epomex.uacam.mx
2 Instituto de Estudios Caribeños, Universidad Nacional de Colombia, Edificio Hansa Reef 6,
Archipiélago de San Andrés, Colombia.
3 Universidad Nacional de Colombia (Instituto de Ciencias Naturales), Apartado 1016 (INVEMAR), Santa Marta, Colombia.