Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.46 n.4 San José Dec. 1998
Abstract
Production and biomass of Chione cancellata, an abundant species in Thalassia testudinum sea beds, were studied from March, 1984 to May, 1985 in Guaracayal, Cariaco Gulf, Venezuela. The population distribution ranges were stable. Many individuals were 20-30 mm long (80%) and recruitment was low. The mean density was 45.54 ind m-2 with a mean standing dry weight biomass of 7.37 g m-2, both changed significantly with time. Growth rates in marked bivalves of different size classes was maximum in the period between 14-X-1984 and 10-V-1985. A production of 17.34 g m-2 year-1 was obtained using a method designed to study populations with continuous reproduction and indistinguishable age classes. The greatest production values were obtained for cockles 20 to 30 mm in length. Highest production was between 28-II-1985 and 27-IV-1985. The annual turnover rate (P/B) was 2.65 year-1.
Key words
Chione cancellata, density, biomass, production, P/B ratio, bivalves.
La familia Veneridae es considerada el grupo de bivalvos en el cual las conchas han alcanzado el mejor y más ajustado balance anatómico y fisiológico, con una gran eficiencia hidrodinámica, representando quizás el más alto logro en la evolución de los bivalvos por su belleza tanto en su forma como en color (Waldo 1950). Dentro de esta familia se incluye a Chione cancellata, especie de distribución tropical y subtropical, muy abundante en comunidades litorales someras del Oriente de Venezuela. En el Golfo de Cariaco vive sobre fondos areno fangosos cubiertos por Thalassia testudinum, formando parte de la infauna superficial y junto con otras especies de moluscos en una comunidad relativamente compleja en su organización que se extiende desde 10 cm a 4 m de profundidad. Sobre la especie se conocen aspectos de la embriogénesis y morfología de la concha criada en el laboratorio (D´Assaro 1967). Moore y López (1969) estudiaron su ecología en Key Biscayne (Florida) determinando que la especie madura al alcanzar 15 mm de longitud, se reproduce dos veces al año, estimando una productividad anual del 83% de la cosecha potencial.
Las investigaciones sobre producción secundaria en poblaciones de moluscos de zonas templadas son abundantes (Burke y Mann 1974, Warwick y Price 1975), pero escasas en especies tropicales. De los reportes de la literatura se deduce que la magnitud del compartimiento de producción (P) se relaciona entre otros factores con la producción primaria del área, longevidad de la especie y el grado de organización del ecosistema. Así se han obtenido altas estimaciones en poblaciones de Donax denticulatus (Vélez et al. 1985), Tivela mactroides (Tatá y Prieto 1991), y bajas en Modiolus squamosus (Prieto et al. 1985) y Pinctada imbricata (Verginelli y Prieto 1991). Dada la importancia ecológica de C.cancellata por la abundancia en las comunidades litorales, la presente investigación permitió estimar la producción secundaria anual de la especie en base a determinaciones de densidad, biomasa y crecimiento en peso del tejido; y la tasa de renovación anual de una población del Golfo de Cariaco, Venezuela.
Materiales y Métodos
Se estudió la población de C. Cancellata de Guaracayal (10° 27´ 00'' N y 63° 57´ 45'' W), Golfo de Cariaco, Estado Sucre, Venezuela, durante un año (marzo, 1984 - mayo, 1985). Los organismos se colectaron en un área aproximada de 3 200 m2 efectuando los muestreos en dos estaciones, una de poca profundidad desde 0.3 hasta 1.2 m, y otra de 1.5 m a 3 m de profundidad. Los muestreos se efectuaron en intervalos de uno y dos meses, sobre transectos numerados cada 0.5 m perpendiculares a la costa. Se aplicó un sistema de muestreo al azar, usando un marco metálico de 0.25 m2 el cual se fijaba en el fondo del sustrato, colectando todos los ejemplares contenidos en el interior del marco. Posteriormente los organismos fueron trasladados al laboratorio y colocados en un acuario con aireación constante por un tiempo no menor a 12 horas para eliminar el exceso de sedimentos del tracto digestivo.
Relación longitud-peso y biomasa: En cada muestreo se seleccionaron 30 ejemplares representativos de todas las tallas a las cuales se les determinó la longitud total (Lt) medida desde los bordes anterior y posterior de la concha, el peso húmedo de las partes blandas, y el peso seco (Ps) colocando las partes blandas a 80 °C por 48 horas. Con estos datos se calculó la relación longitud-peso por la ecuación Ps = a Ltb (Wilburg y Owen 1964), ajustada por el método de los mínimos cuadrados. La significación estadística del grado de correlación se comprobó utilizando el método de Hotelling en cada relación (Sokal y Rohlf 1969). La biomasa (B) en gramos de peso seco se calculó convirtiendo los valores de longitud a peso con la ecuación anterior.
Crecimiento: El crecimiento se analizó marcando organismos de diferentes clases de tallas y confinándolos en jaulas plásticas colocadas en áreas cercanas. Este método permitió seguir el crecimiento de las diferentes clases de tallas y obtener las tasas respectivas. El marcaje se efectuó utilizando etiquetas plásticas numeradas adheridas con masilla epóxica de endurecimiento rápido. Los organismos se agruparon en clases de tallas de 4 mm, y para estimar el crecimiento se promedió el incremento al final de cada período. La tasa instantánea específica de crecimiento en peso (G = d log10 Ps/dt x 2.303) se obtuvo a partir de los incrementos en longitud (Lt) según el método de Crisp (1971), donde Ps es el peso en gramos, t es el intervalo de tiempo y 2.303 es la constante de conversión a logarítmo neperiano.
Producción secundaria: Con los datos de biomasa, densidad, tasas de crecimiento y lapsos de tiempo, se calculó la producción anual total para clases de 10 mm de Lt, aplicando el método para poblaciones con reproducción continua y clases de edades no separables según la relación
donde F es la densidad para cada clase de talla en la población, G es la tasa específica de crecimiento en peso seco, Ps es el peso seco promedio de cada intervalo de talla y At es el lapso de tiempo considerado.
Resultados
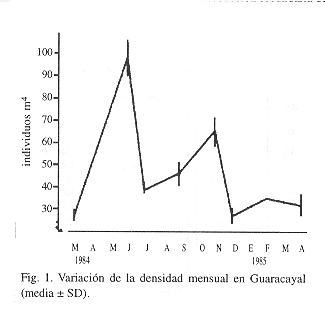
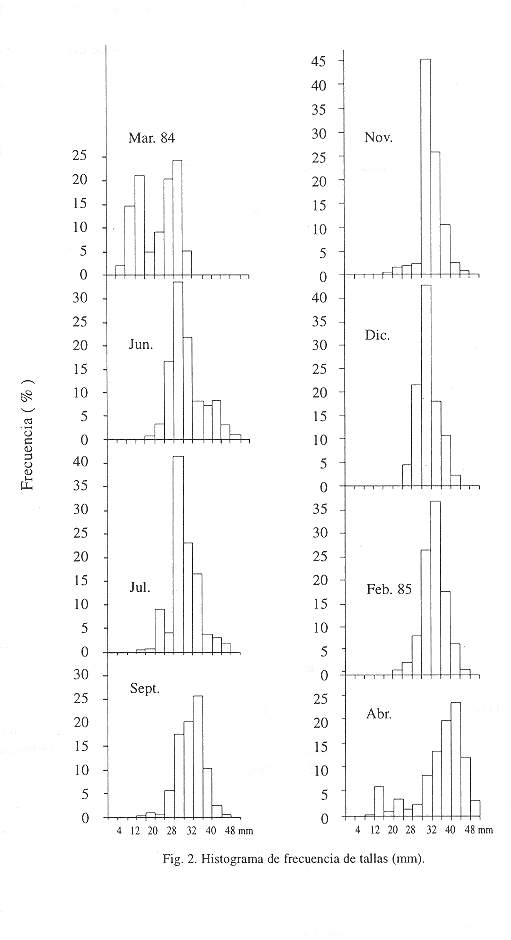
Se recolectaron 1 250 individuos, obteniéndose una densidad promedio de 45.54 ind m-2 (Fig. 1). La máxima densidad (98.5 ind m-2) se obtuvo en junio-1984 y la mínima (24.5 ind m-2) en diciembre-1984, detectándose oscilaciones mensuales significativas de la densidad (Fs = 12.8; P < 0.05), pero no entre las dos estaciones (Fs = 0.469, P > 0.05). La longitud total mínima fue de 5.95 mm y la máxima 43.6 mm, representando el intervalo 20-30 mm el 80% de la población, con una distribución predominantemente unimodal, y con reclutamientos en marzo-1984 y abril-1985 (Fig. 2).
Las relaciones entre el Ps y la Lt obtenidas por el método de los mínimos cuadrados fueron positivas y altamente significativas. El coeficiente de determinación (r2) osciló entre 0.63 (dic-84) y 0.86 (abr-85) (p < 0.001) (Cuadro 1). La relación entre el Ps y el peso húmedo (Ph) mostró una correlación (r2 = 0.956, p < 0.001) altamente significativa, y se expresa por la ecuación común log10 Ps = - 0.798 + 1.453 log10 Ph.
La biomasa en Ps promedio fue de 7.37 g m-2 con un mínimo de 1.76 g m-2 (dic-84) y el máximo de 13.71 g m-2 (jun-84), detectándose diferencias significativas entre los muestreos (Fs = 12.4; P < . 0.05).
Las tasas de crecimiento se obtuvieron de 110 organismos agrupados en clases de tallas de 5 mm de longitud, en los lapsos del 15-VI-84 al 1-II-85 y del 14-X-84 al 10-V-85. Por el método de confinamiento en jaulas, se observó que el crecimiento individual es variable, y la mortalidad fue de 40%. En cada grupo se regresionó el promedio de la longitud en función del tiempo, ajustando la relación por el método de los mínimos cuadrados, obteniéndose dos ecuaciones (Cuadro 2), en la cuales se observa que las pendientes de las ecuaciones del segundo lapso son superiores, y mostraron diferencias significativas en los intervalos 20-25 mm y 25-30 mm. Las tasas de crecimiento en longitud (D Lt) y las tasas instantáneas en peso seco (G) disminuyeron en los intervalos de tallas de los organismos más grandes (Cuadro 3).
Utilizando los promedios de densidad en las dos estaciones, se estimó una producción anual de 17.34 g m-2 año -1, el menor aporte anual correspondió al intervalo 5-10 mm (0.036%), y el máximo fue del intervalo 20-30 mm con 81,71% del total de la producción. En estos valores se excluyeron los correspondientes a la materia orgánica contenida en la concha, y la biomasa liberada como gametos (Cuadro 4). Los períodos de menor producción fueron los lapsos entre el 3-VI-84 al 21-VII-84 y de éste último al 14-X-84. Los incrementos más altos se obtuvieron entre el 28-II-85 al 27-IV-85 y desde el 14-IX-84 al 3-X-843 (Cuadro 4). La relación entre la producción anual y el promedio de la biomasa anual en la población de Guaracayal fue de 2.65 año-1 para todas las clases de tallas.
Discusion
La distribución de grupos de edades en la población estudiada es aparentemente estable, ya que siempre prevalecieron individuos con longitudes comprendidas entre 20 y 30 mm, aún a pesar que se registraron diferencias significativas de la densidad entre los muestreos bimensuales. La composición de la población es unimodal como la descrita para Crassostrea columbiensis, con la mayor proporción de individuos en los grupos de tallas intermedios (Caballero et al. 1996)
La densidad promedio obtenida (45.54 ind m-2) fue la más alta en relación a otras especies que coexisten en la misma área, tales como Modiolus squamosus (31 ind m-2)(Prieto et al. 1985) y Anadara notabilis (14.06 ind m-2) (Manrique 1982); sin embargo es muy superior a las informadas para la misma especie en Key Biscayne, Florida (Moore y López 1969). Las diferencias significativas de la densidad determinadas en los muestreos podrían atribuirse a efectos del mismo, o a la variación de la granulometría y heterogeneidad del sedimento, como ha sido señalada en áreas someras (McNulty et al. 1962).
| | | | |
| | | | |
| | | | |
| | | | |
| | | | |
| | | | |
| | | | |
| | | | |
| | | | |
| | | ||||
| Intervalo de Lt (mm) | | | | | |
| 15 - 20 | | | | | |
| 20 - 25 | | | | | |
| p< .001 | |||||
| 25 - 30 | | | | | |
| p< .001 | |||||
| 30 - 35 | | | | | |
| 35 - 40 | | | | | |
| | | |||
| Intervalo (mm) | |
| |
|
| | ||||
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | ||
Tasa de crecimiento diario en mm (ALt). Tasa instantánea de crecimiento diario en peso seco (G).
| | | | |
| | | | |
| | | | |
| | | | |
| | | | |
| | | | |
| | | ||
| | |
En especies de zonas templadas se ha sugerido que los parámetros poblacionales de los bivalvos varían de acuerdo a su posición sobre la playa (Burke y Mann 1974, Mason 1972, Roberts 1975).
Las estimaciones de densidad obtenidas en este trabajo son típicas para bivalvos que habitan comunidades de T. testudinum las cuales caracterizan costas de baja energía y se corresponden con las observadas para Macoma baltica y Mya arenaria en estuarios canadienses cubiertos por macrofitas (Burke y Mann 1974). No existen hasta el momento otras informaciones sobre la situación actual de la población en el área de Tocuchare.
La producción secundaria en C. cancellata es mucho más alta que las obtenidas para Anadara notabilis (Manrique 1982) y Modiolus squamosus (Prieto et al. 1985) quienes comparten el mismo habitat de fanerogamas marinas: sin embargo son inferiores a las de Tivela mactroides (Tatá y Prieto 1991) y Donax denticulatus (Vélez et al.1985) bivalvos de corto ciclo vital que caracterizan playas arenosas abiertas de alta energía. Los máximos incrementos de producción que ocurrieron entre el 28-II y el 27-IV-85 se corresponden con las altas tasas de crecimiento y biomasa promedio, que se asocian con el período de surgencias costeras que caracterizan la estación seca del Golfo de Cariaco, los cuales oxigenan el agua superficial con temperaturas bajas, altos valores de salinidad y clorofila a; y una alta productividad primaria (Ferráz-Reyes 1987). Los períodos de menor productividad secundaria observados desde 3-VI al 14-IX-84 (Cuadro 4) pudieran estar relacionados con procesos de post-desove en los individuos, el cual no fue estudiado, o más probablemente con una condición fisiológica menor debido a una disminución del fitoplancton en el área, asociada con una mayor utilización de las reservas energéticas de los tejidos. En el Golfo de Cariaco, desde agosto hasta octubre aproximadamente la actividad de los vientos disminuye considerablemente, originando una disminución de la productividad primaria en la zona (Lodeiros y Himmelman en prep.). La estimación de la producción en este trabajo debe considerarse subevaluada, de acuerdo a los enfoques nuevos ya que no se tomó en cuenta la biomasa reproductiva liberada, cuya omisión puede disminuir las estimaciones, dependiendo de la especie (Bayne y Worral 1980, Griffiths 1981, Thompson 1984). El hecho que en la población de C. cancellata el 81.17% de la producción sea aportada por los bivalvos entre 20 y 30 mm, con un aporte muy pequeño para la producción total de las clases de tallas menores, indica una cierta estabilidad. La población posee bajas tasas de reclutamiento debido probablemente a una alta mortalidad de juveniles que es típico en comunidades de fanerogamas marinas con alta diversidad específica y en donde existe una alta estabilidad relativa de factores ambientales, y se conoce que las especies de bivalvos que las habitan son mas eficientes, longevas y menos productivas (Prieto et al. 1985).
La relación P/B estimada (2.65 año-1) es superior a la de otros bivalvos relacionados e indica que al menos la especie es capáz de duplicar su biomasa anualmente, pudiendo ser objeto de estudios futuros que evalúen su potencial para la acuicultura.
Agradecimientos
Agradecemos al Consejo de Investigación, UDO por la subvención a través del proyecto CI-5-024-00333/84-85. A Ysabel Campos y Amalfi Graterol por la ayuda en las labores de campo, y a Rafael Malavé y Fernando Rivero en la elaboración de las figuras.
Resumen
La producción y la biomasa de Chione cancellata un bivalvo abundante en praderas de Thalassia testudinum se estudió desde marzo, 1984 hasta mayo, 1985 en Guaracayal, localidad de la costa sur del Golfo de Cariaco, Venezuela. La población está integrada principalmente por individuos entre 20 y 30 mm de longitud (80%), la cual presentó un bajo reclutamiento. La densidad promedio (45.54 ind m-2) y la biomasa promedio en peso seco de (7.37 g m –2) presentaron variaciones significativas entre los muestreos. Las tasas de crecimiento en individuos marcados en diferentes clases de tallas fueron más altas durante el período comprendido entre el 14-X-1984 al 10-V-1985. Utilizando un método para poblaciones con reproducción continua y clases de edades no separables se obtuvo una producción total de 17.34 g m-2 año-1 durante el período de estudio. Los máximos valores fueron aportados por los bivalvos entre 20 y 30 mm de longitud y la mayor producción ocurrió entre el 28-II al 27-IV-1985. La tasa anual de renovación (P/B) se estimó en 2.65 año -1.
References
Bayne, B. & C Worral 1980. Growth and production of mussel Mytilus edulis from two populations. Mar. Ecol. Prog. Ser. 3:317-328. [ Links ]
Burke, M. & K. Mann 1974. Productivity and production: biomass ratios of bivalve and gastropod populations in an Eastern Canadian estuary. J. Fish. Res. Bd. Can. 31:167-177. [ Links ]
Caballero, A., J. Cabrera & Y. Solano 1996. Descripción del crecimiento y madurez sexual de una población de Crassostrea columbiensis. Rev. Biol. Trop. 44:335-339. [ Links ]
Crisp, D. 1971. Energy flow measurement. p 197-279. In N. A. Holme and A. D. Mc Intire (eds.). Methods for the study of marine benthos. Handbook N° 16. Blackwell Scientific, Oxford. [ Links ]
D´Assaro, C. 1967. The morphology of larvae Chione cancellata Linné 1767 (Eulamelibranchia: Veneridae) reared in the laboratory. Bull. Mar. Sci. 17:949-972. [ Links ]
Ferráz-Reyes, E. 1987. Productividad primaria del Golfo de Cariaco, Venezuela. Bol. Inst. Oceanogr. Venezuela 26:97-110. [ Links ]
Griffiths, R. 1981. Production and energy flow in relation to age and shore level in the bivalve Chromomytilus meridionalis (Kr). Estuar. Coast. Shelf. Sci. 13:477-493. [ Links ]
Manrique, R. 1982. Estudio de la producción y algunos aspectos ecológicos de la pepitona roja Anadara notabilis del Golfo de Cariaco. Tesis Lic. Biol., Universidad de Oriente, Cumaná, Venezuela. p 94. [ Links ]
Mason, J. 1972. The cultivation of the European mussel Mytilus edulis (L). Oceanogr. Mar. Biol. Ann. 10:437-460. [ Links ]
McNulty, J., R. Wark & H. Moore 1962. Level sea-bottom communities in Biscayne Bay and neighbouring areas. Bull. Sci. Gulf. & Carib. 12:204-233. [ Links ]
Moore, H. & N. López 1969. The ecology of Chione cancellata. Bull. Mar. Sci. 19:131-148. [ Links ]
Prieto, A., R. Pereira & R. Manrique 1985. Producción secundaria del mejillón Modiolus squamosus (Beauperthuy, 1967) en Tucuchare, Golfo de Cariaco, Venezuela. Acta Cient. Venezolana 36:258-264. [ Links ]
Roberts, C. 1975. Investigations into a Modiolus modiolus (L) (Mollusca, Bivalvia) community in Strang Ford Lough. N. Ireland. Rep. Underwater Ass. 1:27-49.
Sokal, R. & J. Rohlf 1969. Biometry. W. H. Freeman, San Francisco, California. [ Links ]
Tata, A. & A. Prieto 1991. Producción secundaria en una población del bivalvo tropical Tivela mactroides (Veneridae) en el Oriente de Venezuela. Carib. J. Sci. 21:28-34. [ Links ]
Thompson, R. 1984. Production, reproductive effort value and reproductive cost in a population of the blue mussel Mytilus edulis from a subartic environment. Mar. Ecol. Prog. Ser. 16:249-257. [ Links ]
Vélez, A., B. Venables & L. Fitzpatrick 1985. Growth and production of the tropical beach clam Donax denticulatus (Tellinidae) in Eastern Venezuela. Carib. J. Sci. 21:63-73. [ Links ]
Verginelli, R. & A. Prieto 1991. Producción secundaria de Pinctada imbricata (Röding, 1798) (Pterioida: Pteridae) en una población del Golfo de Cariaco, Venezuela. Acta Cient. Venezolana 42:138-144. [ Links ]
Waldo, M. 1950. Field Book Seashore Life. G. P. Putnam, Nueva York 888 p. [ Links ]
Warwick, R. & R. Price 1975. Macrofauna productions in an estuarine mud-flat. J. Mar. Biol. Ass. U.K. 55:1-18. [ Links ]
Wilburg, K. & G. Owen 1964. Growth. p. 212-242. In K. M. Wilburg & C. M. Young (eds.). Physiology of Mollusca. Academic, Nueva York. [ Links ]
1Laboratorio Ecología de Poblaciones, Dpto. Biología, Escuela de Ciencias, UDO, Cumaná, Sucre, Venezuela, Apartado Postal 245. Tel.-FAX 58-93-514754. Tel. 302445. .
2 IIBCA-UDO, Cumaná, Sucre, Venezuela, darriech@cumana.sucre.udo.edu.ve














