Los trastornos inflamatorios intraoculares son un espectro de enfermedad donde el ojo o sus partes pueden ser reconocidos como antigénicos por el sistema inmune, lo que puede llevar a un deterioro visual grave.1 La uveítis pediátrica representa el 5 - 10 % de las uveítis. Usualmente, existe un retraso en su diagnóstico; además, en niños tienden a ser más crónicas, con recaídas y remisiones frecuentes. Esto lleva a una morbilidad significativa en este grupo etario, con un 50 % de disminución en la visión y un 25 % que llega a ceguera legal.2 Un diagnóstico y un tratamiento precoces pueden disminuir las complicaciones y reducir el riesgo de deterioro visual y ceguera.
En Costa Rica, para la uveítis pediátrica existe una Clínica de Uveítis que se estableció en conjunto entre el Servicio de Inmunología y Reumatología Pediátrica y el Servicio de Oftalmología del Hospital Nacional de Niños, con el fin de darle seguimiento y abordaje a los pacientes con esta patología. Es de suma importancia contar con recomendaciones de manejo vigentes para uveítis no infecciosas y ofrecer una guía adaptada a la realidad costarricense, específicamente para población pediátrica.
Hay una gran cantidad de causas de uveítis, que se pueden categorizar como infecciosas y no infecciosas (Cuadro 1 2-4). El 30 % son de origen infeccioso, la uveítis idiopática (UI) puede corresponder de un 23 % a un 44 % de los casos.3 El diagnóstico amerita un abordaje multidisciplinario entre oftalmología especializada y reumatología o inmunología pediátrica.5
La prevalencia varía según: raza, localización geográfica, edad de la población en estudio, estado socioeconómico, centro académico y fecha del estudio.7 Las mujeres están ligeramente más afectadas. La mayoría de los casos son crónicos y bilaterales, con significativas tasas de complicaciones.8,9
Las uveítis anteriores son más frecuentes, seguidas de la panuveítis, luego las de ubicación posterior y, finalmente, las intermedias. En general, las causas idiopáticas son más comunes en la uveítis anterior, mientras que en la posterior son las infecciosas.2,3,6,8 En niños, la UI varía entre el 30 - 50 %. En Europa, se reporta hasta un 30 % de uveítis asociada a AIJ (UAIJ).8,10,11
Hay pocos reportes en Latinoamérica.12-14 En Costa Rica, la experiencia reportada en UAIJ muestra una menor incidencia que en otros lugares del mundo15,16 y para UI solo hay reportes de adultos.17 Un reporte preliminar en nuestra Clínica de Uveítis mostró una edad de diagnóstico de 6,8 años, con mayor frecuencia de panuveítis (39 %) con compromiso bilateral, donde ni el anticuerpo antinuclear (ANA) ni el HLA-B27 mostraron mayor frecuencia.18
La clasificación de la uveítis se basa en la anatomía (parte de la úvea comprometida), curso clínico (agudo, crónico o recurrente), etiología (infecciosa, no infecciosa), e histología (granulomatosa, no granulomatosa), donde puede estar afectado un ojo o ambos.19 En 2005 se llegó a la Estandarización de la Nomenclatura de la Uveítis (Grupo de Trabajo Internacional de Normalización de la Nomenclatura de Uveítis: SUN, por sus siglas en inglés).19,20
Diagnóstico
Como la uveítis está frecuentemente asociada a enfermedad sistémica, es fundamental una historia clínica y examen físico exhaustivos. Una vez hecho el diagnóstico de uveítis, se debe determinar su clasificación anatómica, que junto a otros factores de la historia y del examen ocular, permiten subcategorizarla. Esto permite escoger los exámenes de laboratorio pertinentes, determinar la etiología de la inflamación intraocular, para la escogencia de la mejor opción de tratamiento.21,22
Los síntomas de la uveítis dependen de la parte anatómica afectada, la rapidez del inicio, su duración y su curso. Por otro lado, la respuesta inflamatoria intraocular produce los síntomas y signos de la uveítis.20
La mayoría de los pacientes requieren pocos exámenes para el diagnóstico, siendo las infecciones por descartar: toxoplasmosis, tuberculosis, sífilis, toxocariasis, herpes y citomegalovirus, las más frecuentes. Los exámenes básicos son hemograma, pruebas de función renal y hepáticas. La proteína C reactiva (PCR) y la velocidad de eritrosedimentación (VES) están elevadas en menos del 10 % de los casos y usualmente asociadas a enfermedad sistémica.3,23-25 Si se sospecha una patología sistémica, losexámenes por solicitar serán acordes con esa enfermedad.21 El HLA-B27 se solicita sobre todo en uveítis intermedia y posterior, y ante la sospecha de espondiloartropatía.26
Cuadro 1. Posible se tiologías de lauveítis pediátrica 2-6
| Etiología | Causas específicas |
| Infecciones | Bacterias: sífilis, tuberculosis, leptospira, brucella, Chlamydia. Parásitos: toxoplasma, toxocara. Virus: herpes, CMV, dengue, chykungunya, varicela, zyka. Hongos: histoplasmosis, aspergillus, cándida |
| Enfermedades Inflamatorias | Artritisidiopáticajuvenil, uveítis HLA-B27 positivas, enfermedad inflamatoria intestinal, enfermedadde Behçet, Vogt-Koyanagi-Harada,nefritis túbulointersticialyuveítis(TUNI),lupus eritematoso sistémico, enfermedad de Blau |
| Otras | Tumores (retinoblastoma y leucemia), birdshot, iridociclitis de Fuchs |
Los estudios por tuberculosis (para descartar esta etiología o cuando se van a usar fármacos biológicos) son: PPD, radiografía de tórax y en casos seleccionados, prueba de cuantiferón para tuberculosis (IGRA). La mayoría de los autores recomiendan la orientación diagnóstica con base en los hallazgos clínicos.3,21,24,26
Algunos exámenes complementarios importantes son: angiografía retiniana fluoresceínica, útil en uveítis posterior; tomografía de coherencia óptica (OCT), que realiza una imagen óptica de las capas de la retina y ayuda en el manejo del proceso inflamatorio retiniano; ultrasonido ocular, útil en la visualización del segmento posterior, y la angiografía con indocianina verde, para el estudio de la coroides. 27-30
En caso de los pacientes que inician inmunosupresión, se deben revisar las serologías por hepatitis B y C, ELISA por VIH, además de la PPD y exámenes de heces por parásitos. Se debe revisar el esquema de vacunas; en caso de que esté incompleto, se debe actualizar antes del inicio de la inmunosupresión, si la condición clínica lo permite.
En la valoración oftalmológica en cada visita se requiere: mejor agudeza visual corregida (AVC), examen biomicroscópico del segmento anterior, medición de presión intraocular (PIO) yfondo de ojo. Idealmente, cuando está disponible el examen de OCT se debe realizar en el diagnóstico de la uveítis, en reactivaciones y según se considere necesario. 21,29-31
El grado de cada uno de los parámetros debe ser registrado: AVC de cada ojo, actividad inflamatoria de acuerdo con SUN para cámara anterior (células y flare) y complicaciones estructurales (hipotonía, hipertensión o glaucoma), sinequias, cataratas, presencia de queratopatía en banda, edema macular, formación de membrana epiretiniana y actividad inflamatoria vítrea. En niños, debido a lo complicado de la valoración, podrían simplificarse algunos de estos parámetros.
Tratamiento
En uveítis, las complicaciones oculares y la pérdida de la visión ocurren con frecuencia, por lo que el tratamiento agresivo de la inflamación intraocular es fundamental para la prevención de la pérdida visual.10,21 Es necesaria la cooperación constante entre el reumatólogo o inmunólogo pediatra y el oftalmólogo.5 Muchas de las recomendaciones se extrapolan de los adultos;20 hay algunas recomendaciones específicas de UI en niños, porque definitivamente existen diferencias entre las dos poblaciones.20,29
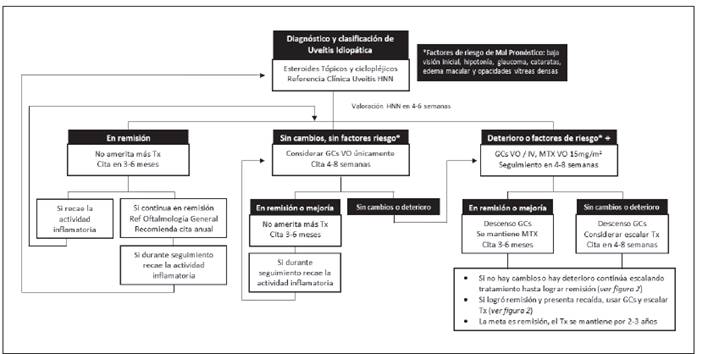
La meta del tratamiento es resolver la inflamación ocular, lograr remisión, prevenir las recurrencias y las complicaciones oculares, y preservar la visión,21 todo en un contexto de la menor cantidad de efectos secundarios asociados a losmedicamentos. La terapia va desde simple observación, hasta tratamiento complejo médico o quirúrgico. Se plantea en la Figura 1 el algoritmo de manejo de la UI en pediatría.
Cuadro 2: Tratamiento tópico, peri e intraocular para UI en pediatría
| Agente | Uso | Medicamentos | Efectosadversos | Comentarios |
| Corticoesteroides tópicos20,21,34,35 | Control de inflamación ocular, en uveítis anterior (nivel de evidencia IA) | Esteroides de mayor potencia (prednisolona 1 %) | Aumento de la presión intraocular | Se pueden administrar gotas (hasta cada hora) durante las horas cuando el niño está despierto: su frecuencia dependerá de la intensidad de la inflamación en la cámara anterior. |
| Agentes midriáticos y cicloplégicos20,21,35,36 | Útiles para prevenir o romper la formación de sinequias posteriores y disminuir la fotofobia provocada por espasmo del cuerpo ciliar | Agentes tópicos de acción cortacomo elciclopentolato al 1 % o la tropicamida | Prurito ocular y mareos | Su frecuencia dependerá de la intensidad de la inflamación enla cámaraanterior. |
| Administración periocular de esteroides20,35 | Uveítis intermedia, posterior o con edema macular | Triamcinolona o la metilprednisolona | Aumento de la presión intraocular | Necesidad de administrarlos con anestesia general o sedación |
| Corticoesteroidesintravítreos20,35 | Tratamiento de la uveítis, aunquede duraciónlimitada | Corticoesteroides dedepósito enimplantesintravítreos | Elevación de la presión ocular, catarata o endoftalmitis | Necesidad de administrarlos con anestesia general osedaciónycosto elevado |
* Los agentes tópico antiinflamatorios no esteroideos son de poca ayuda; podrían usarse en el manejo del edema macular quístico.21,35
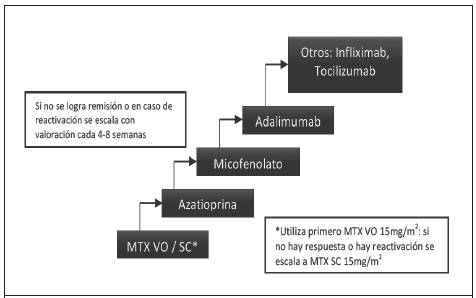
El tratamiento inicial es con esteroides tópicos y solo en aquellos casos de mayor inflamación se usan los esteroides sistémicos. De no haber respuesta, se puede usar un fármaco antirreumáticos modificador de enfermedad (DMARD) como ahorrador de esteroides: metotrexate, azatioprina o micofenolato. En aquellos casos con mala respuesta, se propone el uso de medicamentos biológicos: antifactor de necrosis tumoral (TNF) donde el adalimumab tiene más estudios, pero también hay reportes con infliximab y tocilizumab. Esta escalera terapéutica se describe en la Figura 2 y con mayor detalle a continuación.
Tratamiento tópico
El tiempo que se debe esperar para una respuesta clínica al tratamiento tópico es cada vez menor antes de iniciartratamiento sistémico. Los factores de riesgo por considerar para inicio temprano de DMARD son: baja visión inicial, hipotonía, glaucoma, cataratas, edema macular y opacidades vítreas densas.23,30 Se resumen en el Cuadro 2 los agentes tópicos y tratamiento peri / intraocular.
Tratamiento sistémico
El tratamiento de elección para la etapa aguda de la enfermedad son los corticoesteroides orales, pero una vez que se logra remisión, no se recomienda su uso a largo plazo. La capacidad de lograr una reducción de la dosis de corticosteroides por debajo de un umbral clínicamente significativo, mientras se mantiene inactiva la enfermedad, es un determinante clave del tratamiento exitoso y con menores efectos adversos. Hay pocos fármacos inmunomoduladores no corticoides aprobados para la uveítis que puedan proporcionar un control de la enfermedad a largo plazo.1-3,33-36 (Cuadro 3).
Glucocorticoides o esteroides sistémicos: los esteroides sistémicos continúan siendo el estándar de oro para el tratamiento de la uveítis anterior y posterior.22 Prednisolona es la droga más usada, la dosis de inducción es de 1 mg/kg y se baja según la evolución clínica. Idealmente, se debe administrar en una sola dosis en la mañana para coincidir con el pico normal de producción adrenal.22,36 Además, es necesario considerar la suplementación con calcio y vitamina D en aquellos pacientes que utilicen esteroides por más de 3 meses.36
Los efectos adversos son numerosos e involucran compromiso de múltiples órganos: ojos, endocrino, neuropsiquiátrico, músculo-esquelético, cardiovascular, metabólico, dermatológico e inmunológico. En definitiva, en niños se debe tener especial cuidado con el riesgo de retardo en el crecimiento pondoestatural y el riesgo de osteoporosis.1, 24,28 Para evitar estas complicaciones, se recomienda bajar la dosis al cabo de 4 semanas a menos de 0,15mg/kg y debe restringirse a un máximo de 3 meses. Recientemente, se hapropuesto la utilización de pulsos intravenoso (IV) en vez de su uso vía oral (VO), pero amerita mayores estudios en población pediátrica.22
Es claro que el metotrexate (MTX) es la droga de primera elección para gran parte de los pacientes de acuerdo con la mayoría de guías internacionales.1,22, 25,31-34,36,63 Se prefiere una dosis de 15 mg/m2, dado que aumentar la dosis ha demostrado que no mejora la respuesta terapéutica y aumenta el riesgo de efectos adversos.37 Si es efectivo, se mantiene por 12 - 36 meses desde cuando se documenta inactividad, pero en aquellos con pronóstico visual pobre se debe utilizar por 24 meses como mínimo.33-36 En algunos casos es necesaria su administración parenteral para lograr mayor eficacia y biodisponibilidad.21,37
La azatioprina es un medicamento de tiopurina, usada ampliamente en el tratamiento de niños con enfermedades inmunológicas, como la enfermedad inflamatoria intestinal y la hepatitis autoinmune; sin embargo, se observa una variabilidad interindividual en la aparición de reacciones adversas al medicamento y la respuesta al medicamento. Ha sido utilizado, pero es un medicamento cuya información disponible es limitada.22-21,38-39 Algunos autores han demostrado su efectividad,38,39 por lo que es una opción por considerar en nuestro medio. Sin embargo, en varios sitios del mundo se recomienda la introducción de otros antimetabolitos con menos efectos adversos (ej. micofenolato).21,37 Desde hace varios años existen reportes controversiales de malignidad secundaria después de su uso, que ameritan seguimiento para establecer tal relación.40-44
Cuadro 3: Medicamentos disponibles en el control de la uveítis idiopática y uveítis asociada a artritis idiopática juvenil en pediatría
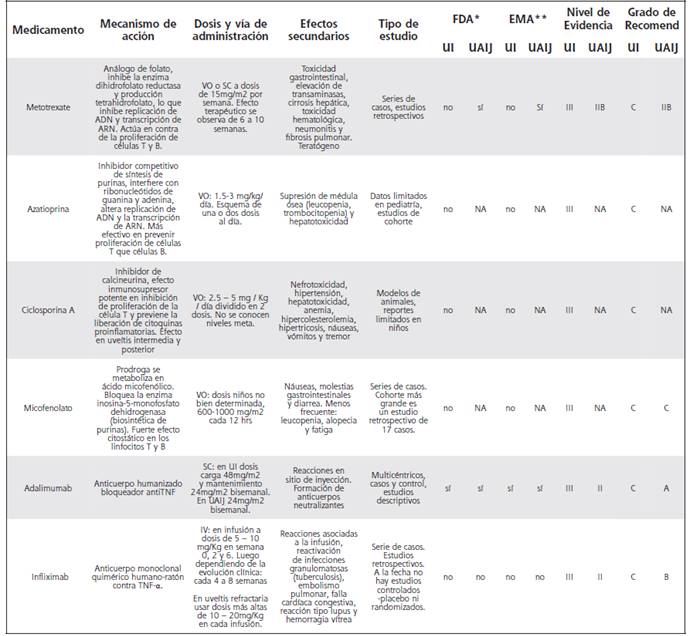
El micofenolato de mofetilo (MMF) se empleó en un inicio en modelos animales de inflamación ocular.45 Posteriormente, su uso se generalizó basado en un estudio de Galor40 con 257 pacientes adultos con inflamación ocular; tuvo dos hallazgos relevantes: se sugirió que el tiempo para controlar la inflamación ocular es más rápido con el MMF que con el MTX, y que la terapia con azatioprina tiene una tasa más alta de efectos secundarios relacionados con el tratamiento en comparación con MTX y MMF. Sin embargo, no se conoce la dosis óptima para uveítis y los niveles de droga no son útiles más que para determinar la adherencia.22,21 Hay dos estudios solo de MMF en pediatría,45,46 en donde fue efectivo y seguro en un número limitado de pacientes. El resto de la información se extrapola de los datos de adultos.22 Sin embargo, su utilización es recomendada en muchas de las guías internacionales para UI.1,21-22,24
Ciclosporina A (CsA): aunque se reporta que es efectiva y ha sido usada por más de 20 años, cada vez se usa menos en pediatría, porque los beneficios se ven limitados por los efectos adversos.20,21,47,48 Si bien, hay estudios que respaldan su uso en adultos,47-49 los estudios pediátricos son limitados y con pocos pacientes.50-53 Recientemente, un estudio multicéntrico demostró que con CsA se logra menos del 24 % de inactividad como monoterapia y su eficacia aumenta al 48 % al combinarla, pero aumenta los efectos adversos. Se debe monitorizar por: nefrotoxicidad, hipertensión, hepatotoxicidad, anemia, nausea, vómitos, hirsutismo e hipercolesterolemia.20,21,54 Su uso debe sopesar seguridad versus eficacia, sobre todo al compararlo con los otros medicamentos disponibles (MTX, MMF y azatioprina), de acuerdo con las recomendaciones internacionales que consideran que existen otras opciones terapéuticas más seguras y con una inducción de remisión más rápida. 20,21,53
Agentes biológicos
Los productos biológicos representan una clase más nueva de medicamentos utilizados para tratar la inflamación ocular. Estos agentes se dirigen contra moléculas en el sistema inmunológico que desempeñan un papel clave en el proceso inflamatorio ocular. Por ejemplo, el TNF-α, otras interleucinas (IL) y los interferones, que son citoquinas proinflamatorias producidas por las células inmunes y están elevadas en el suero y en el humor acuoso de los pacientes con uveítis.20
Los médicos aún enfrentan limitaciones de tratamiento sistémico en la uveítis, ya que solo muy pocos de estos agentes se sometieron a la aprobación regulatoria de esta enfermedad hasta el momento, y el uso no indicado “off label” a menudo restringe el tratamiento actual.55 Impresiona que hay débil asociación de estos medicamentos con malignidad, según los estudios disponibles.56
Adalimumab: es el único agente biológico que cuenta con aprobación de FDA y EMA para uso en UI y UAIJ. Ramanan57 publica un estudio multicéntrico, randomizado, a doble ciego para determinar la eficacia de adalimumab en 90 niños mayores de 2 años con uveítis activa asociada a AIJ. Todos los pacientes habían recibido MTX por 12 semanas. Se demostróque el uso de adalimumab retrasa significativamente la falla a tratamiento comparado con MTX, y que al usar adalimumab se puede disminuir la dosis de glucocorticoides tópicos e incluso suspenderlos. Sheppard58 publica un análisis post hoc que sugiere que el adalimumab se asocia con mejoría clínica (estadísticamente significativa) y en funcionamiento visual en pacientes adultos con uveítis anterior, intermedia, posterior y panuveítis, de origen no infeccioso.
En casos severos, con compromiso ocular, los antiTNF son los medicamentos más efectivos para el tratamiento de la uveítis.59 Se ha reportado que los otros DMARD son insuficientes para controlar estos casos, sobre todo en uveítis posterior y panuveítis,por lo que se recomienda tratamiento agresivo con antiTNF, incluso de primera línea.59,60
Infliximab: no tiene aprobación para el manejo de uveítis en pediatría, pero se ha uitlizado “off label” para el manejo de casos refractarios. La dosis recomendada es de 5 - 10 mg/kg en infusión de 2 horas a las 0, 2, 6 semanas y luego cada 8 semanas, se podría aumentar la dosis de acuerdo con la evolución. Se recomienda el uso concomitante con MTX para disminuir la producción de anticuerpos antidroga.20,21 Como eventos adversos se reportan reacciones infusionales (fiebre, disnea, urticaria, dolor torácico), leucopenia, trombocitopenia, anemia, aumento de riesgo de infección (sobre todo tuberculosis).
Anti IL-6 (Tocilizumab): algunos estudios han demostrado elevación de Il-6 intraocular en pacientes con uveítis crónica refractaria y en modelos animales, con alteración en la diferenciación de las células T CD4 y TH17; por lo tanto, la inhibición de esta citoquina ha sido propuesta dentro del tratamiento,61 pero no cuenta con aprobación de FDA ni EMA para UI. Se ha usado porque la fisiopatología del edema macular involucra IL-6 y factor de crecimiento endotelial vascular (VEGF), que lleva al aumento de permeabilidad vascular y ruptura de vasos. Por lo tanto, se ha propuesto la utilidad de los biológicos antiIL-6 como el tocilizumab.62,63
Otros medicamentos como tacrolimus, sirolimus, ciclofosfamida y clorambucil, han sido reportados, pero no son considerados de forma rutinaria.20,21 Potencialmente, las moléculas pequeñas pueden interferir en diferentes pasos de la cascada inflamatoria y parecen una opción interesante en el algoritmo de tratamiento de la uveítis a futuro.54
Duración del tratamiento: el tipo de enfermedad, tiempo y tipo de terapia sistémica necesaria para lograr inactividad, al ideal que la duración de la uveítis, son algunos de los factores que se han estudiado para definir la duración de la terapia después de lograr la remisión. Por el riesgo de recaída el tratamiento debe mantenerse al menos dos años luego de la remisión.23,63-64
Manejo de las complicaciones
- Queratopatía en banda: se puede remover por raspado con EDTA (ácido etildiaminotetraacético)
- Catarata: lo más importante en el tratamiento de estos pacientes es el control absoluto de la inflamación intraocularpre y posoperatoria con corticoesteroides y terapia inmunomoduladora
- Glaucoma, hipertensión ocular, glaucoma uveítico: es preciso encontrar el origen del aumento de la presión ocular y tratar la inflamación y el aumento de la presión. Puede ser inducido por el uso de corticoesteroides tópicos o sistémicos. Se maneja con hipotonisantes tópicos, a veces orales, o con cirugía.
- Edema macular quístico: se debe controlar primero la inflamación intraocular, y si no mejora, utilizar inyecciones intravítreas de inhibidores del VEGF (Factor de crecimiento endotelial vascular), corticosteroides o implantes intravítreos
- Desprendimiento de retina: es poco frecuente, pero es factor de mal pronóstico visual porque es más difícil de tratar
- Opacificación vítrea o vitreítis: se puede realizar una vitrectomía posterior si la opacificación es importante y permanente
- Neovascularización retiniana o coroidea: se debe tratar la inflamación, y se pueden utilizar inhibidores del VEGF (Factor de crecimiento endotelial vascular)intravítreos, o rayo láser en las zonas de isquemia
- Hipotonía: se trata con terapia corticoesteroide y cicloplejia.
Consideración especial: uveítis asociada a artritis idiopática juvenil
La artritis idiopática juvenil (AIJ) es la enfermedad reumática crónica más frecuente de la infancia65 y está definida de acuerdo con los criterios de ILAR como: una artritis de etiología desconocida que inicia antes de los 16 años y persiste por al menos 6 semanas, donde otras causas conocidas se han excluido, y se describe la uveítis como un posible hallazgo acompañante.66
Cuadro 4 Seguimiento oftalmológico recomendado de los pacientes con AIJ30
| Clasificación de riesgo | Categorías | Seguimiento Inicial | Seguimiento luego del primer año sin uveítis |
|---|---|---|---|
| Alto | AIJoligo, poli o psoriáticaANA+,dx AIJ<6años | Cada 3 meses | Cada 6 meses |
| Mediano | AIJoligo, poli o psoriáticaANA- | Cada 6 meses | Anual |
| Bajo | AIJ sistémica, asociada a entesitis o poli FR+ | Anual | Anual |
Aproximadamente, del 10 al 20 % de los niños con AIJ tienen riesgo de uveítis,64 en poblaciones caucásicas. Los factores de riesgo para la afectación ocular incluyen sexo femenino, artritis oligoarticular, edad temprana de inicio de síntomas de la artritis (menores de 6 años), anticuerpos antinucleares (ANA) positivos y reacción negativa al factor reumatoide.64,67-69 En un estudio en Costa Rica, el ANA positivo no fue demostrado como un factor de riesgo en una muestra pequeña,15 donde se realizó el primer tamizaje de uveítis en enfermedades reumáticas en nuestro país y que dio inicio a la actual Clínica de Uveítis del HNN.
Se reporta que la uveítis asociada a AIJ (UAIJ) compromete el segmento anterior, usualmente es asintomática, bilateral y recurrente. Aparece, en promedio, 4 años después del diagnóstico de AIJ. El inicio de la uveítis antes o poco después de la aparición de la artritis, ha sido reportado como un predictor de mal pronóstico visual.30
El seguimiento oftalmológico rutinario es esencial para el diagnóstico precoz y el tratamiento oportuno. Se recomienda la primera valoración oftalmológica dentro del primer mes posterior al diagnóstico de la AIJ y las visitas de seguimiento se establecen según el riesgo: cada 3 meses para alto riesgo, cada 6 meses para riesgo moderado y cada 12 meses para riesgo bajo (ver Cuadro 4 para seguimiento). Sin embargo, en caso de que se detecte uveítis, las visitas se modifican conforme al grado de actividad y el tratamiento propuesto.
Los pacientes con uveítis asociada a AIJ tienen un alto riesgo de complicaciones oculares, por lo que se debe anticipar la supresión de inflamación con el fin de preservar la visión, evitar recaídas y complicaciones, siempre tratando de evitar efectos secundarios del tratamiento.35
Aún no hay estudios aleatorizados, controlados o comparativos disponibles acerca del uso de la inmunosupresión para tratar a los niños con UAIJ; solo existen informes de observación y estudios de casos,34 por lo tanto, se revisan recomendaciones y guías internacionales para adecuarlas a nuestra realidad.35,70-72
La UAIJ debe tratarse tan pronto se diagnostica con tratamiento tópico y debe referirse a la Clínica de Uveítis delHNN en nuestro país, para un manejo multidisciplinario especializado. El tratamiento sistémico debe contemplar la valoración de oftalmología y articular.35 Se usa DMARD si al cabo de 4 - 6 semanas no hay remisión con tratamiento tópico, o si presenta factores de mal pronóstico, en la primera visita.73
Cuando se inicia tratamiento sistémico, se deben realizar valoraciones cada 4 - 8 semanas para determinar la evolución del paciente y la necesidad de escalar la terapia.
El uso de esteroides orales es similar a UI.35 Como tratamiento sistémico, la primera opción es metotrexate, inicialmente VO, y si no hay respuesta al cabo de 6 - 12 semanas, pasar a subcutáneo (SC).73 Su uso ha sido demostrado en múltiples series de casos.74-77 A diferencia de la UI, si al cabo de 6 - 12 semanas de tratamiento con MTX SC, no hay respuesta adecuada, se debe considerar el uso de agentes biológicos antiTNF.35,73 El adalimumab tiene más estudios específicamente en UAIJ.56,78-84
Puede usarse “off label” infliximab85,86 y golimumab (por ahora no disponible en nuestro medio). No se recomienda el uso de etanercept para UAIJ.73
Hay pocos estudios con otras terapias biológicas. El tocilizumab (anti IL-6) tiene reportes de casos y series retrospectivas que describen su eficacia.30,87-90 El rituximab (anti CD20) podría ser utilizado con base en estudios que han demostrado infiltrado de células B en uveítis, pero hay pocos estudios que demuestran efectividad. Otros medicamentos como azatioprina, ciclosporina A, micofenolato, sulfasalazina y leflunomida, no se utilizan en el tratamiento de la UAIJ.35
En conclusión, la uveítis no infecciosa en la edad pediátrica es poco frecuente, sin embargo, sus complicaciones tanto a nivel estructural como en la función visual, son muy importantes, con evolución a la ceguera frecuente, ya que su diagnóstico es por lo general tardío, y de evolución más tórpida que en el adulto. El manejo interdisciplinario entre oftalmología e inmunología/reumatología pediátrica es fundamental, y es prioritario el manejo agresivo con medicamentos de forma temprana para mejorar el pronóstico visual.