Introducción
Según Cajiao (2015), Costa Rica es un país reconocido a nivel mundial como un destino turístico atractivo gracias a la gran diversidad de opciones que puede ofrecer en una extensión geográfica pequeña, por lo que desde los años 1960 se declaró al turismo como una industria de utilidad nacional. En este sentido, indican Otoya (2006), Benavides (2019) y el ICT (2022), uno de los principales atractivos turísticos que ofrece el país está vinculado al turismo de sol y playa, así como otras actividades asociadas como paseo, buceo, natación y prácticas de deportes acuáticos.
La calidad de los recursos costeros se ha visto impactada por diversas actividades antropogénicas que se realizan en las partes medias y altas de las cuencas hidrográficas, las cuales modifican no solo la superficie sino también generan la descarga de diferentes contaminantes a través de las aguas residuales generadas en las industrias, comercios y domicilios. A esto hay que añadir el aporte de sólidos y nutrientes provenientes de fuentes de emisión difusas; además de fenómenos naturales y antropogénicos que se producen en el mar; según lo estipulado por Escobar (2002), Morales-Ramírez et al. (2009), González (2013), Tavakoly-Sany et al. 2013), Tavakoly-Sany et al. 2014) y Saravia-Arguedas et al. 2019).
En materia regulatoria, el Programa de Estado de la Nación (2008) establece que los espacios marino-costeros son regulados por una legislación específica que establece la Zona Marítimo Terrestre (ZMT) (Ley 6043 de 1977). El modelo de desarrollo que se ha planteado en la ZMT es principalmente turístico, el cual en una cantidad importante de casos no cumple con la normativa de retiros establecida por ley, con permisos del Instituto Costarricense de Turismo (ICT), o poseen concesiones con diversos incumplimientos a los Planes Reguladores vigentes.
El control de la calidad del agua de mar en estos espacios actualmente no existe, dado que los instrumentos vigentes como el Canon Ambiental, el Reglamento de Reuso y Vertido de Aguas Residuales o el Reglamento para la Clasificación de Cuerpos de Agua Superficial no son de aplicación para estas zonas. Por ende, el país no cuenta con un instrumento técnico y legalmente vigente para monitorear la calidad del agua de mar en playas de uso recreativo.
En el país el estudio de la calidad del agua de mar en función de la contaminación bacteriológica comenzó en la década de los años 1960, con Brunker y Fernández (1965), en un estudio en Puntarenas. Posteriormente, y según Mora et al. (1989), el Laboratorio Nacional de Aguas (LNA) ha desarrollado un amplio trabajo de muestreos, caracterización y valoración de riesgos en más de 100 playas, confeccionando instrumentos importantes para la valoración de la calidad del agua de mar, utilizando indicadores biológicos, lo anterior indicado por Mora et al. (2019).
La Contraloría General de la República de Costa Rica presentó en el año 2013 el Informe acerca de la eficacia del Estado para garantizar la calidad del agua en sus diferentes usos, en el que se evidenció la existencia de cinco playas en ambas costas del país no aptas para recreación y con riesgo sanitario. Badilla y Mora (2019) indican que los estudios de calidad sanitaria en playas han estado enfocados principalmente al análisis bacteriológico de coliformes fecales, como son el caso de Escherichia coli y del género Enterococcus spp.
Por su lado, Acuña et al. (2004) y Spongberg (2004) indican que en el país se han realizado estudios de contaminación por hidrocarburos, estos eventos antropogénicos se pueden originar por fuentes externas como descargas accidentales o intencionales ocurridas en rutas de navegación y transportadas por sistemas de corrientes oceánicas, así como internas; el transporte y descarga de estas sustancias ya sea en el sector costero o más adentro del territorio nacional. Sin embargo, estos estudios no se han enfocado en determinar el comportamiento y la dinámica de estos contaminantes en playas recreativas, sino que se han realizado mar adentro y en los golfos del país.
Siguiendo con Spongberg y, posteriormente Lizano et al. (2012), se han realizado también estudios de calidad de agua enfocados a la contaminación por arrastre de materiales vertidos a los ríos y que llegan a desembocar en el mar, evaluando metales pesados como parámetros indicadores de contaminación provenientes de actividades antropogénicas, sin embargo, dichos estudios fueron ejecutados en aguas abiertas y no en las zonas costeras de alta confluencia turística y de uso recreativo.
Briffa et al (2020) indican que los metales pesados presentan características químicas como la formación de enlaces covalentes, así como la formación iones y compuestos lipofílicos en sus formas orgánicas que pueden generar efectos tóxicos al unirse con elementos no metálicos de algunas macromoléculas celulares, además de la presencia de radicales libres que pueden afectar las estructuras de ADN. El mismo Briffa y otros, junto con Pujari y Kapoor (2021) señalan que existen cuatro vías mediante las cuales los metales pueden entrar en el organismo humano, mediante la ingesta de alimentos o agua contaminada, mediante la inhalación desde la atmósfera o mediante el contacto cutáneo. Cuando se da el ingreso de metales pesados por ingesta de agua-alimentos o inhalado se genera el proceso de bioacumulación en el cuerpo, este proceso genera complicaciones biológicas y fisiológicas sobre los organismos, esto según Barletta et al. (2019).
Siguiendo con lo postulado por Briffa, entre las principales fuentes antrópicas de metales pesados se encuentra la minería metálica y la industria metalúrgica, así como la descarga de lixiviados provenientes de rellenos sanitarios y actividades agropecuarias (excretas de ganado y de desechos derivados del cultivo de aves). Por su parte, Luch (2012), Burgos et al. (2017) dicen que otras fuentes importantes de metales pesados son el uso de diferentes fertilizantes que contienen: zinc, cobre y cadmio para su incorporación en suelos deficientes, así como el uso de arsénico, mercurio y sales de cobre como componentes de algunos fungicidas.
El objetivo principal de la investigación fue la elaboración de un estudio exploratorio de la concentración de metales pesados: Fe, Zn, Mn, Cu, Cr, Co, Ni y Pb presente en muestras de agua de mar de playas recreativas de ambas costas de Costa Rica. A la fecha no se cuenta con un estudio preliminar similar publicado en Costa Rica, los datos que se presentan son información valiosa e inédita para actuales y futuras investigaciones en la materia.
Materiales yMétodos
Selección de playas
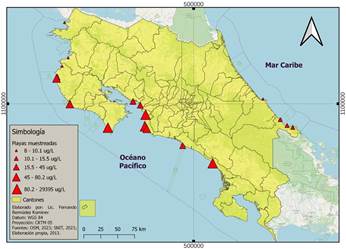
Se estudiaron 18 playas recreativas de Costa Rica distribuidas en cuatro áreas: Pacífico Norte (PN) con siete playas, Pacífico Central (PC) con cinco, Pacífico Sur (PS) con dos y Caribe Sur (CS) con cuatro (Figura 1). Para la selección de las playas se establecieron los siguientes criterios: a) afluencia de turistas y bañistas (ICT, 2010; SINAC & ACG, 2020) historial de contaminación por descarga de aguas servidas (Herrera, 2007; Ávalos, 2008; Cantero, 2008a; Carvajal, 2009; Cantero, 2008b; Agüero, 2010), c) uso del suelo en zonas costeras, tomando aquellas con mayores parches de infraestructura (tanto urbana como industrial).
Muestreo
La recolección de muestras se llevó a cabo entre los meses de abril a noviembre de 2013, cada playa fue muestreada una vez dentro de este periodo. El muestreo se ejecutó aplicando las consideraciones incluidas en la norma mexicana “NMX-AA-120-SCFI-2006”, y fue complementada con la Guía Técnica de Procedimiento de tomas de muestras del agua de mar en playas de baño y recreación de la Dirección de Salud de Perú RM Nº553-2010/MINSA.
Para la toma de muestras en las playas se utilizaron sistemas de información geográfica para determinar de previo a la visita la longitud total de la playa, dicha distancia se dividió entre 0.5km, estableciéndose la cantidad de sitios de muestreo por playa. Posteriormente en campo se utilizó un GPS marca Garmin modelo 62S para medir el distanciamiento entre cada punto de muestreo y georeferenciar puntos de interés como la presencia de desembocaduras o desfogues presentes en la playa muestreada.
Los muestreos se realizaron en un intervalo de tiempo entre las 8:00a.m las 4:00p.m. para cada playa. Las muestras se recolectaron a la orilla de la playa y las condiciones de muestreo variaron según el detalle descrito por la observación del oleaje: a) Oleaje tranquilo: se tomó la muestra en la zona donde la profundidad alcanzó 1m con respecto al nivel del agua; b) Oleaje rompiente cerca de la orilla: en caso de que la pendiente del fondo fuera pronunciada la muestra se tomó en la orilla, donde el nivel del agua estaba entre 20 a 35cm y se llenó el frasco de muestreo procurando que contuviera un mínimo de arena.
Para la recolección de las muestras se utilizaron recipientes de polietileno de alta densidad de 150ml, previamente tratados en un baño ácido nítrico (HNO3) al 10% y lavados tres veces con agua Milli-Q. Todos los recipientes fueron etiquetados con un código particular. En el momento del muestreo cada recipiente se enjuagó tres veces con agua de mar in situ previo a la recolección de la muestra. Una vez recolectadas se colocaron en una hielera con hielo, para mantener una temperatura menor a 4°C hasta que se ingresaran en el laboratorio. Al momento de colectar la muestra se registró el pH del agua de mar in situ medido con un pH-metro marca Orion Star A121 cuyo electrodo fue calibrado utilizando amortiguadores de amino-piridina y trishidroximetilaminometano, o tris; esto de acuerdo con DelValls y Dickson (1998).
Durante el muestreo en cada playa, se tomó un blanco de campo, el cual consistía en una muestra de agua Milli-Q contenida en un recipiente de polietileno de alta densidad de 150 ml. El recipiente de agua Milli-Q identificado como blanco de campo se abrió en una oportunidad durante el período de toma de una muestra, con el fin de detectar posibles eventos de contaminación cruzada. Tanto a las muestras como a los blancos de campo se les añadió HNO3 concentrado hasta un pH < 2 como mecanismo de conservación.
Análisis químico
A partir de cada muestra de agua de mar colectada se tomó una alícuota de 25ml y se vertió en un vaso de precipitados de 150 ml, y se añadieron 2.50ml de HNO3 concentrado. Los vasos de precipitados se calentaron en una placa caliente hasta casi secarse. El material remanente se transfirió cuantitativamente a un balón volumétrico de 25ml. Posteriormente, se volvió a agregar 2.50ml de HNO3 al beaker y se evaporó nuevamente hasta sequedad, volviendo a transferir al balón aforado. Para cada lote de muestras se analizó un blanco de laboratorio y los blancos de campo.
El análisis de metales se llevó a cabo mediante espectrometría de absorción atómica con horno de grafito utilizando un espectrofotómetro AANALYST Perkin Elmer 700 equipado con un muestreador automático. Se utilizaron lámparas de deuterio y de cátodo hueco Perkin Elmer para el análisis de trazas de metales y correcciones de fondo. Las especies de metales se identificaron y cuantificaron por interpolación en las curvas de calibración de siete disoluciones estándar de 10-50 μg/l para Cd, Co, Fe, Ni, Cr, Pb, Cu y soluciones estándar de 5-30 μg/l para Mn, preparadas a partir de disoluciones patrón de 1000 mg/l trazables a NIST marca Perkin Elmer.
Los límites de detección en µg/l, determinados por el método IUPAC, fueron: 0.9 para Cd, 1.1 para Co, 1.5 para Cu, 1.1 para Pb, 1.5 para Cr, 1.0 para Mn, 0.8 para Ni y 4.5 para Fe. Se analizaron los blancos de campo y laboratorio para metales siguiendo el mismo procedimiento empleado para las muestras, obteniendo concentraciones inferiores al 5% de las encontradas en las muestras. La precisión del análisis químico de metales se verificó periódicamente utilizando un estándar certificado (SRM 1648) enriquecido en muestras de agua de mar previamente seleccionadas. Se obtuvo un sesgo general entre -8 y 13% para las concentraciones de metales medidas en las muestras.
Análisis estadístico
Se utilizó el programa InfoStat versión 2020, de Di Rienzo et al. (2020), para la obtención de todos los estadísticos descriptivos de la investigación (cantidad de muestras por playa, media, mediana, desviación estándar (DE), máximos y mínimos, la asimetría y los datos faltantes), y el cálculo de las diferentes pruebas estadísticas. Se ejecutó la prueba de Shapiro-Wilks de cada metal por playa y zona, para determinar si presentan una distribución normal. Seguidamente se analizaron los promedios por playa y zona a partir del análisis de varianza no paramétrica con el método de Kruskall-Wallis, utilizando un nivel de confianza del 95%. Posteriormente en los casos en que se determinara que existía una diferencia significativa, se procedió a la ejecución de pruebas de Tukey para identificar cuáles zonas presentaban diferencias entre sí. Se ejecutó además un análisis de correlación de Pearson entre el pH, temperatura y las concentraciones promedio de cada metal por zona.
Para la graficación de los resultados obtenidos se utilizó el programa R en su versión 3.6.3 por R Core Team (2020).
Resultados
En el Cuadro 1 se presentan la medida de tendencia central y la dispersión para cada metal por zona, incluyendo los valores máximos y mínimos, el cálculo de asimetría en la distribución de los datos y los datos faltantes, este último se refiere a la cantidad de datos que se reportaron por debajo de límite de detección reportado por el laboratorio para cada metal.
Cuadro 1 Estadísticos descriptivos para los diferentes metales pesados por zona, donde PN= Pacífico Norte, PC= Pacífico Central, PS= Pacífico Sur y CS= Caribe Sur.
| Zona | Variable | n | Media±D.E | Mín | Máx | Asmimetría | Datos faltantes |
|---|---|---|---|---|---|---|---|
| CS | Mn(µg/L) | 15 | 833.33 ± 1467.77 | 44 | 4651 | 2.29 | 2 |
| Cd(µg/L) | 17 | ND | - | - | - | 17 | |
| Co(µg/L) | 2 | 10 ± 2.83 | 8 | 12 | 15 | ||
| Fe(mg/L) | 8 | 7.94 ± 9.8 | 0.9 | 28 | 1.55 | 9 | |
| Cr(µg/L) | 17 | 29.29 ± 16.25 | 6 | 62 | 0.47 | 0 | |
| Ni(µg/L) | 17 | ND | - | - | - | 17 | |
| Pb(µg/L) | 17 | 11.59 ± 4.17 | 6 | 19 | 0.46 | 0 | |
| Cu(µg/L) | 13 | 6.77 ± 3.49 | 4 | 16 | 1.82 | 4 | |
| PC | Mn(µg/L) | 32 | 219.1 ± 865.72 | 19 | 4933.4 | 5.55 | 2 |
| Cd(µg/L) | 23 | 5.35±2.59 | 2 | 11 | 0.56 | 11 | |
| Co(µg/L) | 27 | 7.87 ± 16.33 | 2 | 73.62 | 3.56 | 7 | |
| Fe(mg/L) | 32 | 9 ± 29.32 | 0.3 | 161.94 | 4.96 | 2 | |
| Cr(µg/L) | 34 | 63.68 ± 84-01 | 4 | 396.01 | 2.68 | 0 | |
| Ni(µg/L) | 26 | 15.62 ± 14.06 | 3 | 53 | 1.25 | 8 | |
| Pb(µg/L) | 31 | 1939.12 ± 9937.43 | 11 | 55384.53 | 5.54 | 3 | |
| Cu(µg/L) | 33 | 15.2 ± 6.43 | 6 | 34 | 0.95 | 1 | |
| PN | Mn(µg/L) | 27 | 554.28 ± 552.24 | 88 | 2753 | 2.75 | 2 |
| Cd(µg/L) | 29 | ND | - | - | - | 29 | |
| Co(µg/L) | 7 | 4.82 ± 2.07 | 1.58 | 7 | -0.48 | 22 | |
| Fe(mg/L) | 29 | 5.44 ± 6.26 | 0.3 | 21.88 | 1.51 | 0 | |
| Cr(µg/L) | 25 | 25.98 ± 18.37 | 7 | 85 | 1.66 | 4 | |
| Ni(µg/L) | 13 | 13.1 ± 11.06 | 3 | 41 | 1.72 | 16 | |
| Pb(µg/L) | 27 | 45.41 ± 48.64 | 5 | 180.49 | 1.47 | 2 | |
| Cu(µg/L) | 19 | 9.23 ± 4.85 | 3.66 | 19 | 0.81 | 10 | |
| PS | Mn(µg/L) | 12 | 744.67 ± 319.27 | 319 | 1302 | 0.41 | 0 |
| Cd(µg/L) | 7 | 7 ± 2.83 | 3 | 10 | -0.31 | 5 | |
| Co(µg/L) | 12 | ND | - | - | - | 12 | |
| Fe(mg/L) | 12 | 3.32 ± 3.52 | 0.5 | 13.2 | 2.32 | 0 | |
| Cr(µg/L) | 5 | 13.6 ± 9.37 | 5 | 24 | 0.34 | 7 | |
| Ni(µg/L) | 7 | 5.86 ± 5.01 | 3 | 17 | 2.44 | 5 | |
| Pb(µg/L) | 7 | 77.86 ± 42.83 | 16 | 124 | -0.56 | 5 | |
| Cu(µg/L) | 5 | 6.4 ± 2.61 | 5 | 11 | 2.09 | 7 |
Fuente: Elaboración propia.
Los resultados de la prueba de Shapiro-Wilks demostraron que el 48% de los datos de metales por zona rechazan la prueba de normalidad, y el 86% de los datos obtenidos por playa rechaza la prueba de normalidad. A partir de estos resultados, se analizaron los promedios por playa y por zona a través del análisis de varianza no paramétrica Kruskall-Wallis, únicamente cinco metales presentaron una diferencia significativa (P < 0.05).
La zona del PN presentó el promedio de pH más básico del país (Figura 2), además de una diferencia significativa con los valores registrados para las restantes zonas (P=0.0001). El PC, CS y PS no presentaron diferencias de pH significativas entre sí (P>0.05). En la Figura 3 se observa el comportamiento de la temperatura por zona, y se logra identificar que la zona del CS presentó el promedio más elevado (31.10°C), mientras que en el PS se reportó la menor temperatura promedio (27.25°C). La temperatura si presentó una diferencia significativa entre las diferentes zonas analizadas (P < 0.0001), en este sentido el PS y el PC, no poseen una diferencia significativa entre ellas, pero sí con relación a PN y CS.
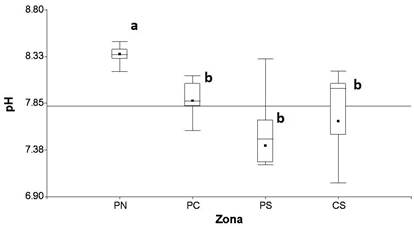
Fuente: Elaboración propia
Figura 2 Box-plot de los resultados de pH en las diferentes zonas del país, los puntos señalan las concentraciones promedio de la zona, las zonas identificadas con letras a y b presentan diferencias significativas entre sí.
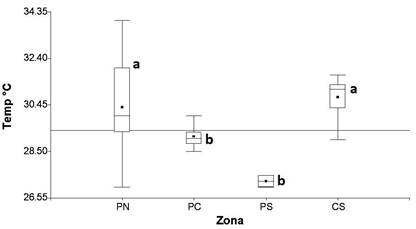
Fuente: Elaboración propia.
Figura 3 Box-plot de la temperatura en las diferentes zonas, los puntos señalan las concentraciones promedio de la zona, las zonas identificadas con letras a y b presentan diferencias significativas entre sí.
El Cd se encontró únicamente en seis playas, 38.8% del total muestreadas, principalmente en las zonas de PC y PS, en esta última se reportó la concentración promedio más elevada para este metal con 7.03 ± 2.83 μg/l. Este metal no presentó una diferencia significativa entre las zonas analizadas, P= 0.1449 y registró una correlación positiva con la temperatura en la zona del PC (r= 0.36).
El Co fue encontrado en un 33.3% del total de playas, la mayoría de ellas ubicadas en la zona de CS (Cahuita y Manzanillo), sin embargo, esta zona presentó la concentración promedio más elevada entre zonas con una media de 10.0± 2.8 μg/l. En esa zona en particular, este metal presentó una muy fuerte correlación con el pH. La segunda zona con concentraciones promedio más elevadas fue PC con 7.9± 16.3 μg/l. En la zona del PN solo en dos de las siete de playas muestreadas se encontraron concentraciones por encima de los límites detectables, Guiones y Playa Carmen de Santa Teresa, respectivamente. En el PS no se encontraron concentraciones por encima del límite de detección.
En la zona del PC se reportó la mayor concentración promedio de Cr del país con 63.7± 84.0 μg/l. La zona del CS fue la segunda con concentraciones promedio más elevadas (Figura 5) con un valor de 29.3± 16.2 μg/l, encontrándose concentraciones máximas de hasta 62 μg/l en playa Cocles. Las mayores concentraciones fueron encontradas cercanas a desembocaduras de ríos como en playa Potrero y playa Jacó; o cerca de desfogues como en playa Potrero y playa Herradura, en esta última las concentraciones máximas se reportaron cerca de la marina y desembocadura (ver Figura 4).
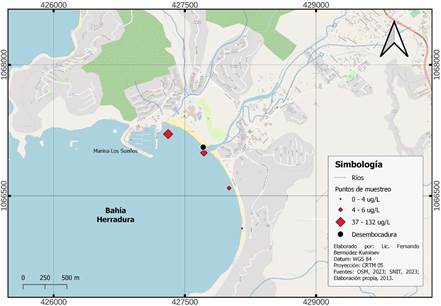
Fuente: Elaboración Propia
Figura 4 Mapa de concentraciones de cromo reportadas en playa Herradura por sitio de muestreo.
Las concentraciones de Cr si presentaron una diferencia significativa entre zonas P= 0.0129, especialmente entre PC y PS. En la zona de Jacó se identificó el mismo patrón de altos niveles cercanos a desembocaduras y desfogues (ver Figura 6).
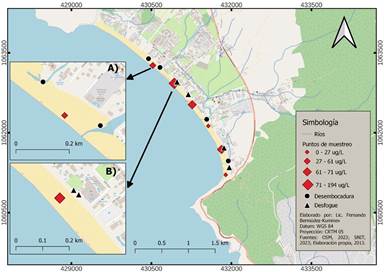
Fuente: Elaboración propia.
Figura 5 Mapa de concentraciones de cromo reportadas en playa Jacó por sitio de muestreo.
En el recuadro A) se detallan el punto de muestreo y la cercanía con desembocaduras, en el recuadro B) se detalla la cercanía del punto de muestreo a dos desfogues.

Fuente: Elaboración propia.
Figura 6 Concentraciones de plomo y cromo para las zonas muestreadas, la línea continua representa en ambos metales el límite permisible de 50ug/L en la normativa australiana y peruana.
Las concentraciones promedio más elevadas de Ni se encontraron en el PC y PN (Figura 7). Este metal presentó una fuerte correlación positiva con el pH y la temperatura en la zona de PN. En CS no se encontraron concentraciones de este metal por encima del límite de detección reportado por el laboratorio. El análisis estadístico no reflejó una diferencia significativa entre las zonas analizadas con P=0.0661.
El Cu presentó una diferencia significativa entre las zonas analizadas (P<0.001), donde PC fue la que presentó una concentración significativamente diferente con relación a las demás (P<0.05) (Figura 5). La concentración promedio más elevada de Cu se ubicó en la zona del PC (Playa Herradura) con 22.7 ± 3.2 μg/l (Fig. 5). En PN, el valor mayor se obtuvo en Playa Langosta 19.0 ± 4.8 μg/l. La zona que presentó menores concentraciones promedio fue PS con 6.40 ± 2.61 μg/L.
En PC, el Pb reportó un promedio de 1 939 ± 9 937 μg/l. Esta desviación de los datos, así como una asimetría pronunciada son efecto de las concentraciones elevadas encontradas en playa Tárcoles, que presentó en el punto más cercano de la desembocadura del Río Grande de Tárcoles una concentración de 55 384 μg/l.
Las concentraciones de Pb presentan una diferencia significativa (P <0.0001) entre las 4 zonas, donde PN y PC registran diferencias significativas con relación al resto. El PN fue la segunda zona que presentó las concentraciones máximas a nivel del país, seguida por el PS y el CS (Cuadro 2).
Cuadro 2 Concentraciones máximas de plomo reportadas para las diferentes playas analizadas.
| Zona | Playa | Concentraciones máximas de Pb (µg/L) |
|---|---|---|
| CS | Bonita | 10.0 |
| Cahuita | 18.0 | |
| Cocles | 19.0 | |
| Manzanillo | 17.0 | |
| PC | Caldera | 62.0 |
| Herradura | 87.0 | |
| Jaco | 115.0 | |
| Puntarenas | 56.0 | |
| Tárcoles | 55384.5 | |
| PN | Coco | 14.0 |
| Guiones | 142.0 | |
| Langosta | 105.0 | |
| Potrero | 20.0 | |
| Rajada | 11.0 | |
| Santa Teresa | 180.5 | |
| Tamarindo | 37.0 | |
| PS | Manuel Antonio | 16.0 |
| Uvita | 124.0 |
Fuente: Elaboración Propia.
El hierro se encontró en todas las playas muestreadas del país, siendo PC donde se encontró la mayor concentración promedio de 9.0 ± 29.3 µg/l y seguida de CS con 7.9 ± 9.8 µg/l (Figura 8), las desviaciones estándar al ser mayores que el promedio, indican una alta variabilidad de datos, principalmente en PC. Este metal no presentó una diferencia significativa entre las zonas analizadas, P=0.244. A nivel de playas, en la zona del PC y el PN si se presentaron diferencias significativas entre playas (P=0.0181 y P=0.0297). Este metal presentó una fuerte correlación con el pH en la zona del CS y con la temperatura en la zona del PS.
Fuente: Elaboración Propia.
Figura 8 Mapa de concentraciones promedio de plomo por playa muestreada.
El Mn fue encontrado en todas las zonas muestreadas (Figura 9), y no se presentó una diferencia significativa entre zonas (P>0.05). Las concentraciones más elevadas se reportaron en el CS y PN, superando los límites establecidos en la normativa australiana.

Fuente: Elaboración propia.
Figura 9 Concentraciones promedio de hierro y manganeso para cada zona muestreada, la línea continua señala el límite máximo establecido en la norma australiana.
Al realizar el análisis de correlación entre los parámetros medidos se encontró que en PN el Mn, Ni, Pb, y Cu presentaron una correlación positiva con el pH, siendo el Ni el que presentó el coeficiente más alto (r= 0.53). En PS y PC únicamente el Cu y el Ni, presentaron una correlación positiva con el pH.
En la zona de CS se encontró que el Mn, Co, Pb, Cu, Cr y Fe presentaron una correlación positiva con el pH, siendo el Fe el que presentó el coeficiente más alto (r= 0.55).
Por otro lado, en la zona del PN el Mn, Fe, Cr, Ni y Cu presentaron una correlación positiva con la temperatura, siendo el Ni el que presentó el coeficiente más alto (r= 0.72). En la zona del CS el Co, Fe y Cu presentaron coeficientes positivos.
Discusión
Tal como se mencionó anteriormente, Costa Rica carece de un modelo que regule la calidad fisicoquímica del agua de mar en playas recreativas, muchas de ellas de gran afluencia de personas turistas nacionales e internacionales, las cuales pudieran estar expuestos a concentraciones de metales que superan los valores máximos recomendados en los esquemas regulatorios existentes en diferentes países. Así, por ejemplo, Ibrahim et al. (2020) dice que el cromo fue encontrado en la mayoría de las playas muestreadas siendo su principal mecanismo de entrada al ambiente de forma no natural, la descarga de aguas residuales procedentes de industrias de pintura y revestimientos metálicos. Por su lado, Anzecc y Armcanz (2000) señalan que la normativa australiana y peruana (Decreto Supremo 015-2015) establecen un límite de protección para la vida acuática para el cromo en 50 μg/l, valor que fue superado en varias muestras colectadas en PC (Figura 6). Más adelante, Tumolo et al. (2020) indican que el cromo puede existir en diferentes estados de oxidación en agua, desde +6 hasta -2, siendo el Cr (VI) altamente tóxico para humanos, animales, plantas y microorganismos, y el Cr (III), es de las especies más estables. Se logró evidenciar que el cromo puede estar asociado al desarrollo de actividades acuáticas como marinas u otras que utilicen combustibles, como fue el caso de playa Herradura donde se reportó la mayor concentración cercana a la marina que opera en dicha playa (Figura 4), mientras que en playa Jacó se encontraron altas concentraciones cerca de desfogues (Figura 5).
Un comportamiento similar se evidenció para el Mn, donde un 45% de las muestras colectadas en CS, PN y PS superaron el valor de 100 μg/l, consignado en las normas de referencia citadas anteriormente. De acuerdo con Longman et al. (2022) entre las principales fuentes que aportan manganeso a los océanos está la actividad agrícola y el arrastre de sedimentos provenientes de suelos de origen volcánico.
Por otro lado, Alfaro et al. (2021) estipulan que los estudios anteriores en la zona del CS han reportado concentraciones de hasta 443 µg/L de plomo en las inmediaciones de la Isla Uvita. Cicerone y otros (2010) dicen que la legislación australiana y argentina establecen los límites permitidos de plomo en agua de mar para su uso recreativo en 50 µg/L, mientras que la normativa chilena (Decreto 144 de 2009) establece un valor máximo de 10 μg/l. Las playas localizadas en PC y PN presentaron concentraciones que exceden los límites establecidos por estas normativas (ver Figura 6). Para Karthikeyan et al. (2021) resulta importante indicar que el Pb se encuentra mayoritariamente en un estado divalente en ambientes acuáticos, por lo que puede acumularse fácilmente en los organismos vivos y es altamente tóxico incluso en bajas concentraciones. Es importante recalcar además que la presencia de este metal en altas concentraciones estuvo muy relacionada a la presencia de desfogues y desembocadura de cuerpos de agua.
La zona de PC presentó las concentraciones más elevadas para diferentes metales y resaltan de forma importante los resultados obtenidos en Playa Tárcoles, Herradura y Jacó, la como fue el caso del plomo, cromo y hierro. Lo anterior indican Doria y Deluke (2015), Burgos et al. (2017), Bridgestock et al. (2018), Ibrahim et al. (2020), Surbakti et al. (2021); tiene su origen en la influencia que ejerce la desembocadura de las cuencas la cuales drenan en muchas ocasiones de zonas ocupadas por diversas actividades humanas que no están cumpliendo con aspectos de protección o resguardo, y como fue se evidencia en la investigación en los puntos de muestreo cercanos a la desembocadura de ríos, quebradas o desfogues fue donde se encontraron las mayores concentraciones. Es importante mencionar que cuando se ejecutó la presente investigación la planta de tratamiento de aguas residuales de Los Tajos no había entrado en operación.
La presente investigación se ejecutó durante el periodo lluvioso y existe un aspecto climatológico que pudo haber influido sobre los resultados obtenidos debido a un mayor aporte de escorrentía por parte de los cuerpos de agua superficial, tanto por una dilución de la concentración de contaminantes como un efecto de aumento en el arrastre de algunos de estos como ha señalado Doria y Deluque (2015).
Al analizar las correlaciones encontradas entre las variables analizadas se encontró que el pH es una variable que influye de forma significativa sobre la concentración de los metales pesados. Un aumento o variación inesperada en el valor de pH puede afectar la biodisponibilidad de estos contaminantes, ya que se favorece la adsorción y precipitación de metales, al unirse con iones OH- y HCO3-, siendo susceptibles a ser liberados y transportados fácilmente. Se logró evidenciar una diferencia significativa entre las playas del CS y el PN con relación a los promedios de pH encontrados. La presencia de arrecifes en la costa pacífica es un elemento que puede influir sobre el pH debido a la presencia de reservas de carbonato de calcio como ha sido señalado por estudios previos de Salazar et al. (2004), y Schneider y Erez (2006), en las diferentes playas muestreadas hay presencia cercana de arrecifes como: en el archipiélago de Islas Murciélago, Bahía Culebra, Bahía Brasilito, Reserva absoluta Cabo Blanco, Punta Leona, Herradura, Punta mala, Parque Nacional Manuel Antonio, Punta Uvita y Parque Marino Ballena; lo anterior de acuerdo con Cortés y Guzmán (1998). Además, recalcan Carstensen y Duarte (2019), la zona PN sí fue significativamente diferente con relación al resto de zonas analizadas, el pH se ve influenciado por la temperatura y por las fluctuaciones en el carbono inorgánico disuelto producto del desequilibrio metabólico.
En PN, el Ni y el Pb presentaron una correlación positiva moderada con el pH, r= 0.53 y r= 0.6 respectivamente, lo cual se corresponde con lo indicado por Surbakti et al. (2021) dado que niveles de pH más básicos permiten una mayor solubilidad de los metales. De esta forma, indican Li et al. (2013) y Surbakti et al., (2021), un pH más ácido tiende a disminuir la solubilidad de los metales pesados.
De igual forma, Miravet et al (2009), y Surbakti et al., (2021) indican que la temperatura es una propiedad que afecta la solubilidad de sales y gases en el agua, ya que mayores temperaturas pueden generar una disminución de los metales pesados debido a la formación de iones de metales pesados, y estos tienden a asentarse y entrar en el sedimento marino. Se encontró una diferencia significativa entre la temperatura de la costa del pacífico y la costa caribeña (P=0.0004). La dinámica de las corrientes, así como la morfología del fondo marino explica que se presenten menores temperaturas en el Pacífico que en el Caribe; lo anterior propuesto por Gordon (1967) y Lizano (2016).
Conclusiones
El desarrollo de este primer estudio exploratorio permite tener una noción general sobre la presencia de metales pesados en agua de mar en algunas de las playas recreativas a nivel del país, su relación con los diferentes elementos hídricos como ríos o quebradas y los elementos humanos como la ocupación del suelo o la disposición de aguas residuales, así como la presencia de algunos de estos metales que superan las concentraciones máximas establecidas en legislaciones de países como Perú y Australia. Esta presencia podría estar generando problemas en salud humana que necesitan ser estudiados con más profundidad y regulado por las autoridades competentes, como se ha hecho en otros países de la región.
Además, se presentan variaciones importantes entre las diferentes zonas costeras del país y entre las playas, en este sentido se pueden estar presentando afectaciones a los diferentes ecosistemas marinos que son además un atractivo turístico importante como los arrecifes de coral. De igual forma se identifica que el aporte de las descargas de aguas residuales o naturales a las playas juega un rol importante, al obtenerse concentraciones mayores de estos metales en zonas cercanas a estos sitios en las playas del PN y PC, en esta última fue donde se reportó mayor cantidad de desfogues hacia la playa. Sin embargo, es necesario ejecutar estudios donde se analice el comportamiento de metales y bacterias en el transcurso de un día esto por la afluencia de turistas, las descargas ilegales que existan, y poder estudiar el comportamiento de los contaminantes dentro de la columna de agua.
Lo anterior debe ser analizado bajo un estudio estadístico que permita determinar qué elementos espaciales y temporales son significativamente influyentes sobre el método de muestreo y así poder determinar con mayor claridad los horarios y la determinación de puntos de toma de muestra más adecuados para el muestreo. Los resultados serán un insumo importante para la toma de decisiones por parte de las autoridades en salud para regular la calidad de las aguas y su adecuado monitoreo, con el objetivo de resguardar los ecosistemas y la salud humana.

















