Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.3 n.2 San José Aug. 2001
Introducción
La insuficiencia cardíaca congestiva (ICC) es un síndrome que resulta de la alteración de la función de la bomba ventricular izquierda, caracterizado por un impedimento al vaciamiento ventricular izquierdo o al llenado del mismo. Síntomas típicos incluyen disnea, edema, hasta la disfunción orgánica. Recientemente se ha clasificado como insuficiencia cardíaca de disfunción sistólica, de disfunción diastólica; este artículo trata de la disfunción sistólica primordialmente.
La insuficiencia cardíaca es una entidad que afecta 4.8 millones de personas en los Estados Unidos, y la prevalencia se acerca a 6-10% en pacientes mayores de 65 años, siendo su prevalencia general de 1.5 a 2 %.
Se dice que se presentan unos 400 mil a 700 mil casos nuevos por año, y hay cerca de 20 millones de pacientes asintomáticos que desarrollarán síntomas dentro de 1 a 5 años.
En cuanto a la importancia en relación a la demanda de atención médica debido a esta entidad, hay datos de que en los Estados Unidos se producen unos 3.5 millones de hospitalizaciones por año; siendo la primera causa de hospitalizaciones en pacientes mayores de 65 años. Además, un tercio de pacientes hospitalizados por ICC son reingresados al hospital en los siguientes 90 días, y el costo de hospitalización es el doble en comparación con pacientes con cáncer, lo cual denota su importancia para el sistema de salud de una población.
Se dice que 250 mil personas mueren por año como consecuencia directa o indirecta de insuficiencia cardíaca; y el riesgo de muerte es 5-10% por año en pacientes con síntomas leves, y hasta 30-40% por año en casos de enfermedad avanzada.
Etiología y fisiopatología.
Este síndrome clínico es el resultado de la evolución de diversas entidades que pueden afectar la función y estructura del corazón. Dentro de las causas de la insuficiencia cardíaca, se encuentra que un 60% corresponde a cardiopatía isquémica, un 18% se debe a miocardiopatía dilatada, 12% está relacionado a valvulopatías, y un 10% se atribuye a cardiopatía hipertensiva. (1)
Existe una gran variabilidad de síntomas en relación al grado de disfunción cardíaca, que puede ir desde alteraciones de predominio diastólico a sistólico, pasando por las entidades mixtas; a pesar de esto, un 80-90% de los pacientes con insuficiencia cardíaca tienen síntomas por disfunción sistólica ventricular izquierda, con fracción de eyección menor o igual a 40% (1).
La relación entre la disfunción y los síntomas no es directamente proporcional, y existen pacientes con grados de disfunción ventricular importante sin la presencia de síntomas.
Existen factores no cardíacos involucrados en esta entidad, y que repercuten sobre la función cardíaca, dentro de estos factores se puede citar la función vascular periférica, la fisiología musculoesquelética, la dinámica pulmonar, y la actividad neurohumoral y autonómica.
Los factores neurohumorales endógenos cumplen un rol importante en la aceleración del proceso de remodelación ventricular. Estas sustancias como la norepinefrina, angiotensina II, aldosterona, endotelina, vasopresina, citocinas, factores de crecimiento, especies reactivas de oxígeno y el óxido nítrico, afectan la estructura y función del corazón(2). En los últimos 20 años se ha descubierto que en la insuficiencia cardíaca hay una activación importante del sistema nervioso adrenérgico, se ha visto que los niveles de norepinefrina en el plasma de los pacientes con insuficiencia cardíaca, son 50 veces más de lo normal en pacientes sin tratamiento; lo cual es equivalente a los niveles liberados observados en el individuo con corazón sano durante los momentos de máximo esfuerzo. Con estas altas concentraciones de norepinefrina, hay daño directo sobre las células miocárdicas, llevando a muerte celular. (3) En la clínica, las investigaciones muestran una relación significativa entre mortalidad y concentraciones de noradrenalina. (4)
Por otra parte, de los 5 receptores (beta 1, beta 2, alfa 1, AT1 y AT2) en la célula miocárdica, solo beta 1 y AT1 muestran una reducción en la densidad, y aumentan la densidad de beta 2, AT2 y alfa 1. Con esto disminuye en un 50 a 60 % la señal de la vía de los beta receptores, y se reduce la reserva de la capacidad de ejercicio.(5) (6)
Conociendo la fisiopatología de la insuficiencia cardíaca, se conciben tres vías de intervención terapéutica para mejorar la función ventricular izquierda:
1. Drogas que incrementan la FE por estimulación directa de la contractilidad: Dobutamina y Milrinone.Evaluación.
2. Relajación vascular periférica: Vasodilatadores.
3. Drogas que afectan el proceso de remodelación cardíaca: inhibidores de la enzima convertidora de angiotensina (IECA), beta bloqueadores y nitratos.
La evaluación de un paciente con insuficiencia cardíaca debe hacerse de manera sistemática, siguiendo pasos escalonados:
1. Clasificación según New York Heart Association (NYHA).No se justifica la valoración hemodinámica, neurohumoral o electrofisiológica, o por métodos de imágenes no invasivas para FE en pacientes estables.
2. Evaluación de la retención de líquidos.
3. Valoración de la función sistólica y diastólica delventrículo izquierdo.
Para valorar la evolución se puede recurrir a medidas de progresión de la enfermedad tales como:
1. Muerte.Con estas medidas, se puede valorar la respuesta al tratamiento, o la necesidad de hacer cambios en el manejo de estos pacientes, y el uso en investigación.
2. Paciente resucitado después de muerte súbita.
3. Empeoramiento de los síntomas.
4.Necesidad de nuevos medicamentos.
5. Necesidad de hospitalización.
Tratamiento.
Las metas a corto plazo de la terapia están dirigidas al alivio de los síntomas, lo cual debe mejorar la capacidad funcional y la calidad de vida del paciente. Las metas a largo plazo incluyen la reducción de la mortalidad y la reversión o el enlentecimiento de la progresión de las anomalías estructurales del ventrículo izquierdo, referidas como remodelación. (7)
Prevención.
Es muy importante evitar que el paciente llegue a tener insuficiencia cardíaca. Si ya tiene algún grado de disfución es fundamental retrazar la aparición de síntomas o el empeoramiento de estos. En cuanto a medidas preventivas se recomienda:
1. Intervención sobre los factores de riesgo de enfermedad arterial coronaria.Medidas generales.
2. Reperfusión y antagonistas neurohumorales luego de infarto agudo al miocardio.
3. Los pacientes con disfunción ventricular reciente o antigua deben tratarse con inhibidores de la ECA y beta bloqueadores.
Se recomiendan medidas generales como:
1. Disminuir el riesgo de nueva lesión.Tratamiento
2. Mantener el balance de líquidos. (<3 g. NaCl / día)
3. Mejorar la condición física. (incentivar y limitar la actividad física).
4. Medidas selectivas para algunos pacientes (tratamiento de arritmias, anticoagulación y terapia de revascularización en pacientes con angina).
5. Medidas farmacológicas a evitar: antiarrítmicos en arritmias ventriculares asintomáticas, mayoría de calcio antagonistas, AINES (Anti-inflamatorios no esteroideos).
6. Otras recomendaciones: Inmunización contra influenza y pneumococo, supervisión cercana de los pacientes.
Drogas aprobadas y recomendadas para uso general:
Diuréticos.– Diuréticos.
– Inhibidores de ECA.
– Beta bloqueadores.
– Digitálicos.
Los diuréticos son drogas que aumentan la excreción urinaria de sodio, por lo que funcionan en los pacientes con insuficiencia cardíaca al atenuar la sobrecarga de líquidos. Dentro de las razones fundamentales para usar diuréticos en insuficiencia cardíaca, está el hecho de que alivian los síntomas más rápido que otros fármacos, constituyen el único grupo de drogas adecuado ante la retención de líquidos, y su uso apropiado es un elemento clave en el tratamiento exitoso con otras drogas.
La meta con el uso de diuréticos es mejorar o eliminar los síntomas en los pacientes con insuficiencia cardíaca, sin embargo sus efectos sobre morbimortalidad aún no se conocen, por lo que no deben usarse solos, sino en combinación con otras drogas. Se recomienda la combinación con IECA y beta bloqueadores, y se ha visto que el uso a largo plazo de estas drogas puede disminuir la necesidad de diuréticos en ciertos pacientes. En grandes estudios multicéntricos realizados con pacientes bien controlados en relación con síntomas y retención de líquidos, se ha demostrado que los diuréticos solos son incapaces de mantener estabilidad clínica a largo plazo, sin embargo el riesgo de descompensación se disminuye al combinar diuréticos con digoxina o IECA. (8) (9) (10) (11).
Ante la resistencia a los diuréticos, que puede aparece en la evolución de la insuficiencia cardíaca, se puede corregir con la administración intravenosa de estas drogas, con la combinación de dos a más diuréticos, o utilizando fármacos que incrementen el flujo renal por corto tiempo como Dopamina o Dobutamina. Debe evitarse el uso de AINES ya que pueden inhibir el efecto natriurético de muchos diuréticos (especialmente los de asa), y potenciar la tendencia de estos a causar azotemia.
El uso de diuréticos acarrea riesgos para el paciente tales como el desbalance de electrolitos (potasio y magnesio), la activación neurohumoral especialmente del sistema renina angiotensina aldosterona, hipotensión y azotemia.
IECA.
Hay cinco IECA aprobados por la FDA para el tratamiento de la insuficiencia cardíaca: Captopril, Enalapril, Lisinopril, Quinapril y Fosinopril. El Ramipril está aprobado para la insuficiencia cardíaca post infarto agudo al miocardio.
En muchos (pero no todos) modelos experimentales de insuficiencia cardíaca, los IECA tienen efectos favorables sobre la remodelación cardíaca y la supervivencia. (12) (13) (14) (15)

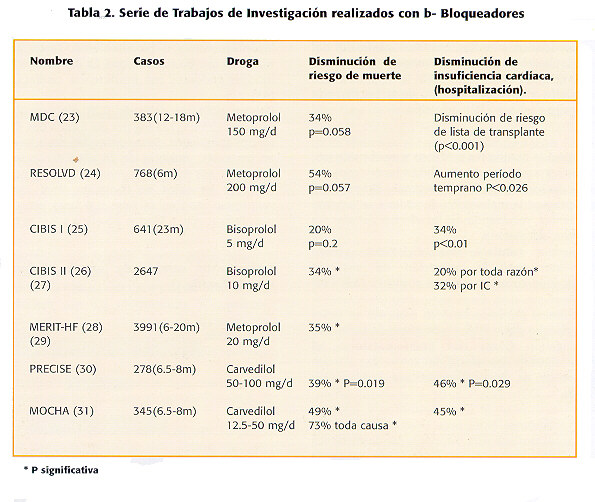
Todo paciente con insuficiencia cardíaca NYHA clase II o III, debe recibir un beta bloqueador; sin embargo no deben usarse para estabilizar pacientes con descompensaciones agudas incluyendo aquellos que tienen retención significativa de líquidos, que estén recibiendo terapia intravenosa para la insuficiencia cardíaca, o que requieran hospitalización por la enfermedad. Aún se necesitan más datos para confirmar el uso de estas drogas en pacientes con insuficiencia cardíaca NYHA clase IV. Sin embargo, el estudio COPERNICUS, valoró el uso de carvedilol en 2289 pacientes con NYHA clase IV de insuficiencia cardíaca, con un tasa de mortalidad con placebo de 18.5%, y un efecto marcadamente positivo del carvedilol sobre estos pacientes. Esta serie se detuvo el 14 de marzo del 2000, (32) demostrando un beneficio significativo con el uso de carvedilol, con una reducción de un 35% de todas las causas de mortalidad en comparación con placebo.
El uso combinado de beta bloqueadores con IECA muestra beneficios aditivos.
Antes de iniciar tratamiento con beta bloqueadores, se debe asegurar que la dosis de diuréticos es óptima. La mejoría sintomática se observa 2 a 3 meses después del inicio con ésta droga, sin embargo, a pesar de no haber mejoría sintomática en este período el riesgo de progresión de la enfermedad disminuye.
A pesar de que varios beta bloqueadores han mostrado ser efectivos en series clínicas controladas, solo Carvedilol ha sido aprobado por la FDA para el manejo de la insuficiencia cardíaca. La hipótesis de las ventajas de bloqueadores no selectivos sobre los selectivos esta siendo evaluada por el estudio COMET, con más de 3 mil pacientes por 4 años, con resultados hasta el 2001.

Los efectos secundarios pueden aparecer al inicio del tratamiento, sin embargo hay buena tolerancia a largo plazo. Dentro de los riesgos del tratamiento están la hipotensión, la retención de líquidos y el empeoramiento de la insuficiencia cardíaca, el bloqueo cardíaco y la bradicardia.
Digitálicos.
Estas drogas inhiben la bomba Na K ATPasa a nivel sistémico; la inhibición de ésta a nivel vagal sensibiliza barorreceptores cardíacos lo que causa disminución de estímulo simpático; a nivel renal se disminuye la reabsorción de sodio y se suprime la secreción de renina, reduciendo así los efectos del sistema renina angiotensina aldosterona.
En la insuficiencia cardíaca, los digitálicos actúan principalmente atenuando la activación de sistemas neurohormonales, y no como inotrópicos positivos. (33) (34) (35) (36).
La digoxina es el único glucósido cardíaco evaluado en series controladas con placebo por la FDA. En un grupo de series DIG (Digitalis Investigation Grop) con 6800 pacientes, el tratamiento con digoxina no afectó la sobrevida, aunque disminuyó el riesgo de hospitalización por insuficiencia cardíaca en un 28%. (37)
Usos clínicos de la digoxina:
La digoxina está recomendada para mejorar la condición clínica en la disfunción sistólica ventricular izquierda, y debe ser usada en combinación con diuréticos, IECA y beta bloqueadores. También se recomienda su uso en los casos de fibrilación auricular. No hay datos para recomendar el uso de digoxina en pacientes con NYHA clase I. Tampoco esta indicada para estabilizar pacientes con descompensaciones agudas de insuficiencia cardíaca, excepto ante fibrilación auricular.
Existe poca relación entre los niveles séricos de digoxina y los efectos terapéuticos, y no se sabe si grandes dosis son más efectivas que pequeñas dosis en el manejo de la insuficiencia cardíaca. En cuanto a la toxicidad con digoxina, ésta puede ocurrir con niveles menores, especialmente si hay hipokalemia, hipomagnesemia o hipotiroidismo, casos en que hay que valorar el uso de estas drogas. La digoxina es bien tolerada en muchos pacientes con insuficiencia cardíaca. (38) (39) (40) (41).
Pueden utilizarse dosis de 0,25 mg por día, aunque dosis menores como 0,125 mg por día o cada dos días pueden tener efectos apropiados. Se recomiendan dosis bajas especialmente en pacientes mayores de 70 años o con insuficiencia renal crónica. Dosis mayores, como 0,375-05 mg por día son a veces utilizadas en casos de fibrilación atrial con alta respuesta ventricular. Aún no se sabe si a largo plazo el uso de dosis terapéuticas ejerce efectos adversos sobre el corazón.
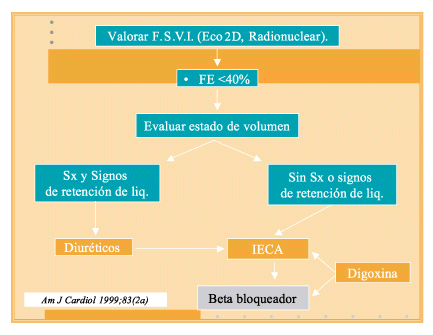
En pacientes con disfunción ventricular izquierda (FE<40%), en caso de retención de líquidos se utilizan inicialmente los diuréticos, puede agregarse terapia con IECA. Los beta bloqueadores se pueden utilizar cuando no hay datos clínicos de retención de líquidos. En pacientes sin retención de líquidos, se inicia la terapia con IECA y beta bloqueador. La digoxina se utiliza asociado a IECA y beta bloqueador tempranamente cuando los pacientes son sintomáticos, o cuando aparecen síntomas durante la terapia con estas dos drogas. (42).
Otras drogas.
Drogas no aprobadas, recomendadas para el uso en algunos pacientes.
1. Hidralazina y Dinitrato de isosorbide.Hidralazina y Dinitrato de isosorbide.
2. Bloqueadores de receptores de angiotensina.
3. Antagonistas de Aldosterona.
4. Calcio antagonistas.
5. Antiarrítmicos.
6. Anticoagulantes.
El uso de vasodilatadores por vía intravenosa tiene efectos hemodinámicos favorables para el tratamiento a corto plazo de descompensaciones agudas de insuficiencia cardíaca; sin embargo el uso a largo plazo no produce beneficios, e incluso puede incrementar el riesgo de insuficiencia cardíaca y muerte. (43) (44) (45)
Hay evidencia reciente que sugiere que la hidralazina y el dinitrato de isosorbide actúan a un nivel principalmente bioquímico. Mientras la hidralazina tiene efectos antioxidantes que pueden interferir con los mecanismos bioquímicos y moleculares responsables de la progresión de la insuficiencia cardíaca, los nitratos inhiben el crecimiento anormal del miocardio y los vasos, atenuando el proceso de remodelación ventricular. (46) (47) (48) (49) (50) (51).
En el estudio V-HeFT I se muestra que la combinación de los dos medicamentos reduce la mortalidad de 25-30% en comparación con Prazosin. (52)
El estudio V-HeFT II muestra que el tratamiento con Enalapril se relaciona con una reducción del riesgo de muerte a los 2 años de un 28% en comparación con la combinación de vasodilatadores. Sin embargo, la combinación de vasodilatadores tuvo efectos más favorables sobre la fracción de eyección y la tolerancia al ejercicio que los IECA. (53)
La combinación de hidralazina y dinitrato de isosorbide es una terapia alternativa efectiva ante la intolerancia y/o contraindicación a los IECA, sin embargo aún faltan datos para comprobar su beneficio (54). Estos fármacos no están aprobados por la FDA.
Dosis: Al inicio con hidralazina 25 mg TID y dinitrato de Isosorbide 10 mg TID, hasta 75 mg de hidralazina TID y 40 mg de dinitrato de isosorbide TID.
Bloqueadores del receptor de angiotensina.
El estudio ELITE con Losartan se asoció con un 46% de menor riesgo de muerte en comparación con Captopril, sin embargo no hubo significancia en cuanto a sobrevida, y tampoco hubo diferencia en cuanto a la frecuencia de hospitalización por insuficiencia cardíaca, ni en el riesgo combinado de morbilidad y mortalidad. (55)
El estudio ELITE II (68), con 288 centros en 45 países, con 3152 pacientes en tratamiento con Losartan, realizado para evaluar los efectos de éste medicamento comparado con Captopril sobre la mortalidad de pac. con ICC sintomática por un período de seguimiento promedio de 1,5 años; mostró que el Losartan no fue superior al Captopril en reducir la mortalidad en pac. mayores de 60 años con ICC. Sin embargo, Losartan fue mejor tolerado que el Captopril. Otros estudios en proceso son ValHeFT y CHARM. (56)
Por falta de evidencia concluyente que soporte el uso de los bloqueadores del receptor de angiotensina II, estas drogas se prescriben solo al haber intolerancia a IECA. Sin embargo, estas drogas, al igual que IECA también producen hipotensión, empeoramiento de función renal e hiperkalemia.
Muchos bloqueadores del receptor de angiotensina II se han aprobado para el uso en hipertensión arterial, pero ninguno se ha aprobado en insuficiencia cardíaca.
Antagonistas de aldosterona.
La aldosterona puede tener efectos adversos sobre la estructura y función del corazón así como de la circulación periférica; por esto, el bloqueo de la aldosterona puede jugar un papel importante sobre la disminución del riesgo de progresión de la insuficiencia cardíaca.
En el estudio RALES, realizado con 1663 pacientes NYHA clase IV, se utilizaron dosis de 25 mg/d de espironolactona por 24 meses asociado a terapia convencional, randomizado con placebo; y se demostró que la espironolactona se asoció con una reducción de la mortalidad en un 27%, disminución en hospitalizaciones por insuficiencia cardíaca de un 36%, y reducción de un 22% en el riesgo combinado de muerte u hospitalización.
El uso de dosis bajas de espironolactona debe considerarse en pacientes con clase IV, sin embargo, su eficacia y seguridad en insuficiencia cardíaca de leve a moderada aún se desconoce. (57) (58)
Calcio antagonistas.
La administración de los calcio antagonistas no produce mejoría sintomática ni mayor tolerancia al ejercicio, además el tratamiento a corto o largo plazo puede ocasionar reacciones adversas a nivel cardiovascular.
Recientes estudios han enfocado el uso de nuevos calcio antagonistas en pacientes con insuficiencia cardíaca crónica, tales como amlodipina, felodipina. El estudio RAISE, realizado con 1153 pacientes utilizando amlodipina, no muestra ningún efecto sobre el riesgo combinado de muerte y hospitalización; a pesar de esto se observó una tendencia a la disminución de todas las causas de mortalidad. En casos de miocardiopatía no isquémica, amlodipina se ha asociado con una disminución del 45% en el riesgo de muerte. (59) Por falta de evidencia que apoye, los calcio antagonistas no deben ser usados para el tratamiento de la insuficiencia cardíaca.
Antiarritmicos.
Todos los antiarrítmicos pueden suprimir ritmos ventriculares ectópicos en pacientes con insuficiencia cardíaca, pero esta acción no ha llevado a la reducción del riesgo de muerte súbita en series controladas. En general estos fármacos no son recomendados para pacientes con arritmias ventriculares asintomáticas o no sostenidas. Sí debe considerarse el uso de antiarrítmicos o dispositivos especiales en:
1. Taquicardia ventricular sostenida o hemodinámicamente desestabilizante, fibrilación ventricular, o historia de resucitación de muerte súbita.
2. Arritmias atriales recurrentes o sostenidas, asociadas a síntomas, inestabilidad hemodinámica o alta respuesta ventricular.
Los antiarrítmicos clase I no deben ser usados en pacientes con ICC. Algunos de clase III no parecen incrementar el riesgo de muerte en pacientes con ICC, y pueden usarse para el tratamiento de arritmias atriales en disfunción ventricular izquierda como Amidarona.
La amiodarona no se recomienda como uso general para prevenir la muerte en pacientes con ICC que ya estén tratados con drogas que reduzcan la mortalidad.
Al utilizar antiarrítmicos, se debe monitorear y corregir los niveles de potasio y magnesio.
Anticoagulantes.
El riesgo de tromboembolismo en pacientes clínicamente estables es bajo (1-3% por año) aún en aquellos con FE deprimida o con evidencia ecocardiográfica de trombos intracardíacos. (60) (61) (62) (63) (64)
Algunos autores describen que el accidente vascular cerebral (AVC) no tiene relación con la severidad de la insuficiencia cardíaca; sin embargo, estudios muestran un 18% de aumento en el riesgo de eventos cerebrovasculares en hombres por cada 5% que disminuya la fracción de eyección, pero el incremento de éste riesgo no es significativo. Para las mujeres, existe un 58% de aumento en el riesgo de eventos de tromboembolismo por cada 10% de disminución de la fracción de eyección. Mientras la tasa de AVC en mujeres es de 1.4% anual con FE de 21 a 30%, esta incrementa 2.4% por año con FE de 10% o menos; esto demuestra que las pacientes femeninas con fracciones de eyección menor tienen mayor tendencia al AVC.
Por otro lado, la tasa de AVC recurrente es mucho mayor que la tasa del primer episodio de AVC en pacientes con insuficiencia cardíaca. Se documenta que la tasa de AVC recurrente a los cinco años del primer episodio es de un 45%. En cuanto a la tasa de hemorragia intracerebral, esta es de 0.3% por año con el uso de warfarina (INR 2.8-4.8), y se acerca a 0.2% con aspirina; y la tasa de sangrado mayor es de 1.3-1.5%; se deduce entonces que la anticoagulación en prevención primaria tiene beneficio limitado.
Para definir el beneficio de la anticoagulación en la disfunción ventricular sistólica hay dos estudios en proceso, WATCH y WARCEF, los cuales tienen una duración de 3 a 5 años, y se espera definan la utilidad de la terapia anticoagulante en la insuficiencia cardíaca (65).
Dentro de las recomendaciones para el uso de Warfarina están: (54) (66) (67)
1. Trombos ventriculares documentados por ecocardiografía.Terapia inotrópica positiva.
2. Fibrilación atrial.
3. Embolismo pulmonar y trombosis venosa profunda crónica, o eventos embólicos previos.
4. Post infarto agudo al miocardio de cara anterior.
Por la falta de datos que demuestren eficacia y consenso acerca de la toxicidad; el uso intermitente de infusiones de inotrópicos positivos no se recomienda en el tratamiento de la insuficiencia cardíaca, incluso en estadios avanzados. Más aún, el uso a largo plazo de inotrópicos positivos intravenosos pueden aumentar el riesgo de muerte; sin embargo pueden ser necesarios en pacientes seleccionados como aquellos refractarios a tratamiento, quienes no pueden dejar la terapia intravenosa, o aquellos que no pueden egresar del hospital debido a su pobre respuesta al tratamiento.
Conclusiones
La Insuficiencia Cardíaca Congestiva Crónica es una enfermedad común con incidencia y prevalencia crecientes que representa un reto a la Salud Pública en siglo XXI. Existen variadas opciones terapéuticas, algunas de ellas con suficiente soporte científico que respaldan su uso en la mayoía de los pacientes, si no existen contraindicaciones (IECA, algunos betabloqueantes y la Espironolactona) y otras alternativas dependiendo de la condición individual de cada paciente, también de demostrada efectividad pero sin influencias significativas sobre la mortalidad.
En último caso y como todo en Medicina, de acuerdo al juicio sabio y actualizado del médico que mantiene un estrecho seguimiento de la terapútica, haciendo los ajustes pertinentes, durante una fluida relación con su paciente, se lograrán los mayores beneficios en una enfermedad que hoy por hoy no tiene cura definitiva.
Referencias
1. Khan, M. G. Heart disease diagnosis and therapy: a practical approach. Williams & Wilkins, 1996: 191. [ Links ]
2. Colucci, W. S. Molecular and cellular mechanisms of myocardial failure. Am J Cardiol 1997;80(11A)15L-25L [ Links ]
3. Esler, M., et al. Adrenergic nervous system in heart failure. Am J Cardiol 1997;80(11A):7L-14L [ Links ]
4. Francis, G. S., Cohn, J. N., Johnson, G. et al. Plasma norepinephrine, plasma renin activity and congestive heart failure. Relations to survival and the effects of therapy in V-HeFT II follow-up. Circulation 1993; 87(Suppl VI): VI-40-8. [ Links ]
5. Bristoco, M. R. Mechanism of action of beta-blocking agents in heart failure. Am J Cardiol 1997;80(11A)26L-40L [ Links ]
6. Jackson, G., et al. ABC of heart failure: pathophysiology. BMJ 2000; 320: 167-169. [ Links ]
7. Cohn, J. N. Overview of the treatment of heart failure. Am J Cardiol 1997;80(11A-6L) [ Links ]
8. Wilson JR, et al. Effect of diuresis on the performance of the failing left ventricle in man. Am J Med 1981; 70:234-239 [ Links ]
9. Parker JO. The effects of oral ibopamine in patients with mild heart failure: a double-blind placebo controlled comparison of furosemide. Int J Cardiol 1993;40:221-227. [ Links ]
10. Richardson A, et al. Double- blind comparison of captopril alone against frusemide plus amiloride in mild heart failure. Lancet 1987;2:709-711. [ Links ]
11. The Captopril-Digoxin Multicenter Research Group. Comparative effects of therapy with captopril and digoxin in patients with mild to moderate heart failure. JAMA 1988;259:539-544. [ Links ]
12. McDonald KM, et al. Relative effects of 1-adrenoreceptor blockade, converting enzyme inhibitor therapy and angiotensin II subtype 1 receptor blockade on ventricular remodeling in the dog. Circulation 1994;90:3034-3046. [ Links ]
13. Mc Donald KM, Mock J, D`Aloia, Parrish T, Hauer K, Francis G, Stillman A, Cohn JN. Bradykinin antagonism inhibits the antigrowth effect of converting enzyme inhibition in the dog myocardium after discrete transmural myocardial necrosis. Circulation 1995;91:2043-2048. [ Links ]
14. Lambert C, et al. Comparative study of converting enzyme inhibition and angiotensin II receptor antagonism on survival from chronic heart failure in cardiomyopathic hamsters. (Abstr.) Eur heart J 1998;19 (suppl):132.
15. Schieffer B, et al. Comparative effects of chronic angiotensin – converting enzyme inhibition and angiotensin II type 1 receptor blockade on cardiac remodeling after myocardial infarction in the rat. Circulation 1994:89:2273-2282. [ Links ]
16. Pfeffer MA, Braunwald E et al. On behalf of the SAVE Investigators. Effect of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction: results of the survival and ventricular enlargement trial. N Engl J Med 1992;327:669-677. [ Links ]
17. The Acute Infarction Ramipril Efficacy (AIRE) Study Investigators. Effect of ramipril on mortality and morbidity of survivors of acute myocardial infarction with clinical evidence of heart failure. Lancet 1993;342:821-828. [ Links ]
18. Kober L, Torp-Pedersen C et al. For the Trandolapril Cardiac Evaluation (TRACE) Study Group. A clinical trial of the angiotensin-converting-enzyme inhibitor trandolapril in patients with left ventricular dysfunction after myocardial infarction. N.Engl J Med 1995;333:1670-1676. [ Links ]
19. The SOLVD Investigators. Effect of enalapril on mortality and the development of heart failure in asymptomatic patients with reduced left ventricular ejection fractions. N Engl J Med 1992;327:685-691. [ Links ]
20. The SOLVD Investigators. Effect of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure. N Engl J Med 1991;325:293-302. [ Links ]
21. Garg R, Yusuf S, for the Collaborative Group on ACE Inhibitor Trials. Overview of randomized trials of angiotensin-converting enzyme inhibitors on mortality and morbidity in patients with heart failure. JAMA 1995;273:1450-1456. [ Links ]
22. Das Gupta, P. D., Lahiri, A. Can intravenous B-blockade predict long-term haemodynamic benefit in chronic congestive heart failure secondary to ischemic heart disease? J Cardiovasc Pharmacol 1990; 19 (Suppl 1):s62-s67. [ Links ]
23. Waagstein F, Bristow MR, Swedberg K, Camerini F, Fowler MB, Silver MA, Gilberth EM, Johnson MR, Goss FG, Hjalmarson A, for the Metroprolol in Dilated Cardiomyopathy (MDC) Trial Study Group. Beneficial effects of metoprolol in idiopathic dilated cardiomyopathy. Lancet 1993;342:1441-1446. [ Links ]
24. Tsuyuki RT, et al. Combination neurohormonal blockade with ACE inhibitors, angiotensin II antagonists and beta-blockers in patients with congestive heart failure: design of the Randomized Evaluation of Strategies of Left Ventricular Dysfunction (RESOLVD) Pilot Study. Can J Cardiol 1997;13:1166-1174. [ Links ]
25. CIBIS Investigators and Committees. A randomized trial of B-blockade in heart failure: the Cardiac Insufficiency Bisoprolol Study (CIBIS). Circulation 1994;90:1765-1773. [ Links ]
26. CIBIS II Scientific Committee. Design of the Cardiac Insufficiency Bisoprolol Study II (CIBIS II) Fundam Clin Pharmacol 1997;11:138-142. [ Links ]
27. CIBIS II Investigators and Committees. The Cardiac Insufficiency Bisoprolol Study (CIBIS-II): a randomised trial. Lancet 1999;353:9-13. [ Links ]
28. The International Steering Committee. Rationale, design and organization of the Metoprolol CR/XL. Randomized Intervention Trial in Heart Failure (MERIT-HF). Am J Cardiol 1997;80(suppl 9B):54J-58J. [ Links ]
29. MERIT-HF Investigators. Communication with Gottlieb SS. Goldstein S, Wedel H concerning the results of the MERIT –HF Trial. October-November, 1998. [ Links ]
30. Packer M, Colucci WS et al. For the PRECISE Study Group. Double-blind, placebo-controlled study of the effects of carvedilol in patients with moderate to severe heart failure. Circulation 1996;94:2793-2799. [ Links ]
31. Bristow MR, Gilberth EM et al. For the MOCHA Investigators. Carvedilol produces dose-related improvements in left ventricular function and survival in subjets with chronic heart failure. Circulation 1996;94:2807-2816. [ Links ]
32. COPERNICUS investigatores, Carvedilul Prospective Randonmised Cumulative Survivaql Trial No publia, Roche, F. Holffman - La Roche Ltd., Switzeriand 2000. [ Links ]
33. Fergusson DW, Berg WJ et al. Sympathoinhibitory responses to digitalis glycosides in heart failure patients: direct evidence from sympathetic neural recording. Circulation 1989;80:65-77. [ Links ]
34. Covit AB, et al. Suppression of the renin-angiotensin system by intravenous digoxin in chronic congestive heart failure. Am J Med 1983;75:445-447. [ Links ]
35. Ferguson DW, et al. Sympathoinhibitory responses to digitalis glycosides in heart failure patients: direct evidence from sympathetic neural recordings. Circulation 1989;80:65-77. [ Links ]
36. Gheorghiade M, et al. A neurohormonal modulator in heart failure? Circulation 1991;84:2181-2186. [ Links ]
37. The Digitalis Investigation Group. The effect of digoxin on mortality and morbidity in patients with heart failure. N Engl J Med 1997;336:525-533. [ Links ]
38. Arnold SB, et al. Long-term digitalis therapy improves left ventricular function in heart failure. N Engl J Med 1980;303:1443-1448. [ Links ]
39. Slatton ML, et al. Does digoxin provide additional hemodynamic and autonomic benefit at higher doses in patients with mild to moderate heart failure and normal sinus rhythm? J Am Coll Cardiol 1997;29:1206-1213. [ Links ]
40. Fogelman AM, et al. Fallibility of plasma-digoxin in differentiating toxic from non-toxic patients. Lancet 1971;2:727-729. [ Links ]
41. Ingelfinger JA, et al. The serum digitalis concentration does it diagnose digitalis toxicity? N Engl J Med 1976;294:867-870. [ Links ]
42. Milton Packer y Jay N. Cohn. Consensus Recommendations form the management of chronic heart failure. Am J Cardiol 1999. Vol 83-24 A. [ Links ]
43. Franciosa JA, et al. Contrating inmediate and longterm effects of isosobide dinitrate on exercise capacity in congestive heart failure. Am J Med 1980;69:559-566. [ Links ]
44. Conradson TB, et al. Clinical efficacy of oral hydralazine in chronic heart failure. One year- double-blind placebo controlled study. Am Heart J 1984;108:1001-1006. [ Links ]
45. Cowley AJ, et al. Long-term evaluation of treatment of chronic heart failure: a 1-year comparative trial of flosequinan and captopril. Cardiovasc Drug Ther 1994;8:829-836. [ Links ]
46. Garg UC, et al. Nitric oxide- generating vasodilators and 8-bromocyclic guanosine monophosphate inhibit mitogenesis and proliferation of cultured rat vascular smooth muscle cells. J Clin Invest 1989;83:1774-1777. [ Links ]
47. Calderone A, et al. Nitric oxide, atrial natriuretic peptide and cyclic GMP inhibit the growth-promoting effects of norepinephrine in cardiac myocytes and fibroblasts. J Clin Invest 1998; 101:812-818. [ Links ]
48. Munzel T, et al. Hydralazine prevents nitroglycerin tolerance by inhibiting activation of a membrane-bound NADH oxidase. A new action of an old drug. J Clin Invest 1996;98:1465-1470. [ Links ]
49. Yue T-L, et al. Carvedilol, a new vasodilator and beta-adrenoceptor antagonist, is an antioxidant and free radical scavenger. J Pharmacol Exp Ther 1992;263:92-98. [ Links ]
50. Dhalla AK, et al. Role of oxidative stress in transition of hypertrophy to heart failure. J Am Coll Cardiol 1996;28:506-514. [ Links ]
51. Keith M, et al. Increased oxidative stress in patients with congestive heart failure. J Am Coll Cardiol 1998;31:1352-1356. [ Links ]
52. Cohn JN, et al. Effect of vasodilator therapy on mortality in chronic congestive heart failure: results of the Veterans Administration Cooperative Study. N Engl J Med 1986;314:1547-1552.g [ Links ]
53. Cohn JN, et al. A comparison of enalapril with hydralazine-isosorbide dinitrate in the treatment of chronic congestive heart failure. N Engl J Med 1991;325:303-310. [ Links ]
54. Marso, S. P., et al. Manual of cardiovascular medicine. Lippincott Williams & Wilkins, 2000: 110-112. [ Links ]
55. Pitt B, Segal R, Martínez FA et al. On behalf of ELITE Study Investigators. Randomised trial of losartan versus captopril in patients over 65 with heart failure (Evaluation of Losartan in the Elderly Study, ELITE). Lancet 1997;349:747-752. [ Links ]
56. ELITE II Investigators y Commuttee: Efectos de Losartan versus Captopril sobre la mortalidad en pacientes con insuficiencia cardiaca sistomática: razón fundamental, diseño y características básicas de los pacientes en el estudio de supervivencia de Losartan en la insuficiencia cardiaca. ELITE II. Journal of Cardiac Failure Vol 5 N.2 June 1999 P 146-151. [ Links ]
57. The RALES Investigators. Effectiveness of spironolactone added to an angiotensin-converting enzyme inhibitor and a loop diuretic for severe chronic congestive heart failure (The Randomized Aldactone Evaluation Study RALES). Am J Cardiol 1996;78:902-907. [ Links ]
58. Pitt B. Presentation of the results of the RALES Trial. American Heart Association Scientific Sessions. Dallas, Texas, November 1998. [ Links ]
59. Packer M, O Connor Cm et al. For the Prospective Randomized Amlodipine Survival Evaluation Study Group. Effect of amlodipine on morbidity and mortality in severe chronic heart failure. N Engl J Med 1996;335:1107-1114.
60. Dunkman WB, Johnson GR et al. Incidence of thromboembolic events in congestive heart failure. Circulation 1993;87 (suppl VI):94-101. [ Links ]
61. Dunkman WB. Thromboembolism and antithrombotic therapy in congestive heart failure. J Cardiovasc Risk 1995;2:107-117. [ Links ]
62. Cioffi G, et al. Systemic thromboembolism in chronic heart failure. A prospective study in 406 patients. Eur Heart J 1996;17:1381-1389. [ Links ]
63. Baker DW, et al. Management of heart failure. IV. Anticoagulation for patients with heart failure due to left ventricular systolic dysfunction. JAMA 1994;272:1614-1618. [ Links ]
64. Katz SD. Left ventricular thrombus and the incidence of thromboembolism in patients with congestive heart failure: Can clinical factors identify patients at increased risk? J Cardiovasc Risk 1995;2:97-102. [ Links ]
65. Pullicino, P. M., et al. Stroke in patients with heart failure and reduced left ventricular ejection fraction. Neurology 2000; 54. [ Links ]
66. Murphy, J. G., et al. Mayo Clinic Cardiology Review. Futura Publishing Company, Inc, 1997:597-612 [ Links ]
67. Milton Packer, et al. Consensus recommendations for the management of chronic heart failure. Am J Cardiol 1999 83:30 A. [ Links ]
68. Pitt B., Poole-Wilson PA, Segal R, et al. Lancet 2000, 355: 1582-1587. [ Links ]
*Servicio de Cardiología, Hospital Max Peralta, CCSS, Cartago,Costa Rica.














