Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de Biología Tropical
On-line version ISSN 0034-7744Print version ISSN 0034-7744
Rev. biol. trop vol.53 n.1-2 San José Jun. 2005
Efecto tóxico de DDT y endosulfan en postlarvas de camarón blanco, Litopenaeus vannamei (Decapoda:Penaeidae)de Chiapas,México
Vicente Castro-Castro, Yadira Siu-Rodas, Luz V.González-Huerta & Mikhail Y.Sokolov
Laboratorio de Ecología Microbiana Aplicada, Departamento de Biotecnología Ambiental, El Colegio de la Frontera Sur, Unidad Tapachula. Apdo. Postal 36, Tapachula, Chiapas, México CP.30700. Fax:+52 (962)6289806; cvicente@tapecosur.edu.mx
Recibido 30-VIII-2004. Corregido 10-VIII-2004. Aceptado 11-VIII-2004.
Abstract
Toxic efect of DDT and endosulfan in white shrimp postlarvae Litopenaeus vannamei (Decapoda: Penaeidae) from Chiapas, Mexico .We analized acute toxicity in white shrimp (Litopenaeus vannamei) postlarvae exposed to two chlorinated pesticides, DDT and endosulfan, under laboratory conditions during 168 hours, with controlled temperature (29 ± 1°C), salinity (3 ± 1 ) and pH (8 ± 1). Median lethal concentrations (LC50 ), "incipient" LC50, median lethal time (LT50 ) the "maximum acceptable concentration of the toxic compound" (MACT) and "the safety level" (SL) were determined. The concentration of the compounds at which organism growth was reduced by 5 and 50% (EC5 and EC50 ), as well as changes in oxygen consumption patterns were determined in the surviving postlarvae.They were very sensitive to both compounds and DDT was thrice as toxic as endosulfan. Growth rate decreased 50 % and 80 % with endosulfan and DDT, respectively, at the experimental pestice concentration.The low resistance of postlarvae to DDT and endosulfan suggests that additional inflow of these pesticides into the aquatic system could affect the rate of shrimp production in the area. Rev. Biol. Trop. 53(1-2):141-151. Epub 2005 Jun 24.
Key words: Ecotoxicology, Litopenaeus vannamei, DDT, endosulfan, pesticides.
Los compuestos organoclorados constituyen uno de los grupos más peligrosos de plaguicidas, ya que presentan una baja solubilidad en agua, una alta solubilidad en la mayoría de los disolventes orgánicos, baja presión de vapor, elevada estabilidad química y una considerable resistencia al ataque de los microorganismos (Arias et al. 1990). Aunque en México varios de estos compuestos (como el aldrin, dieldrin, endrin, DDT y lindano) han sido prohibidos o restringidos desde 1991 (Anónimo1998), la presencia de compuestos organoclorados en sistemas acuáticos ha sido plenamente descrito por diversos autores (Gutiérrez-Galindo et al. 1992, Gold-Bouchot et al. 1993, 1995, Noreña-Barroso et al.1998, Galindo et al. 1999). Así, el aumento de los aportes de plaguicidas hacia los ecosistemas acuáticos, producto de su amplia utilización en la agricultura y en campañas de combate de vectores transmisores de enfermedades, ha despertado gran preocupación a nivel regional debido a la alta toxicidad sobre la biota acuática, a su bioacumulación, a su biomagnificación y a su persistencia en el medio (Espina y Vanegas 1996, Coll et al. 2004, Spongberg 2004a, b, c), además de su fácil acceso a los sistemas acuáticos y la movilidad que tienen en la red trófica.
En Chiapas existe una preocupante falta de información al respecto, a pesar de ser una importante zona de agricultura intensiva y una región propicia para el desarrollo de mosquitos transmisores de enfermedades como el paludismo y dengue. Esto ha generado un uso intensivo de plaguicidas desde hace más de 30 años, entre los que destacan el DDT y el endosulfan. Actualmente sólo se encontraron tres trabajos que muestran la presencia de organoclorados en sistemas acuáticos de Chiapas (Anónimo 1986a, Botello et al.1995,Cruz 1998),en todos los casos el endosulfan y DDT estuvieron presentes. Ambos compuestos son considerados como plaguicidas críticos (Benítez y Bárcenas 1996).
Entre la biota acuática de importancia ecológica y económica como el camarón, los plaguicidas ocasionan una serie de trastornos moleculares y fisiológicos entre los que destacan: la inhibición del almacenamiento de reservas asociadas a los procesos de reproducción, activación de hormonas durante el proceso de muda, reducción de la capacidad osmorreguladora, alteración de la tasa respiratoria y el consumo de oxígeno, disminución de los niveles internos de proteínas, etc. Estas alteraciones implican una disminución de la tasa reproductiva, modificación en la relación depredador-presa y en casos extremos la muerte, además de ocasionar daños en el equilibrio ecológico del ambiente acuático (Galindo et al. 1992, 1994, Espina y Vanegas 1996, Galindo et al. 1996a, b, 1999). En la costa de Chiapas la riqueza biológico-pesquera se centra principalmente en la captura de camarón (Anónimo 1996a), siendo las especies de mayor explotación el camarón blanco (Litopenaeus vannamei, Boone, 1931) y el camarón azul (L.stylirostris, Stimpson, 1874) (Anónimo 1991), y hasta la fecha no se tiene conocimiento de estudios que hayan evaluado los efectos tóxicos de plaguicidas sobre camarones en la zona.
El objetivo de este estudio fue conocer los efectos tóxicos de formulaciones comerciales de DDT y endosulfan en postlarvas de camarón blanco (L.vannamei ) de la costa de Chiapas, y establecer los límites de seguridad para la sobrevivencia de la especie.
Material y métodos
Material biológico: Los organismos de prueba fueron capturados con un "chayo" (arte de captura artesanal de postlarvas) en octubre de 1999, frente a las playas de Puerto Madero, Chiapas (14° 41 37" N y 92° 24 48" W), posteriormente se trasladaron al laboratorio donde se colocaron en contenedores plásticos de 60 L de capacidad con filtros biológicos y a la misma salinidad y temperatura de captura (29 y 30 °C respectivamente). En el laboratorio, los animales se aclimataron por un período de cinco días a 3 ± 1 ,29 ± 1 °C,14:10 h. luz: oscuridad, 8 ± 1 de pH y 5 ± 1 mg/L de oxígeno disuelto (OD),estas condiciones se mantuvieron a lo largo del experimento. Las condiciones fisicoquímicas se establecieron de acuerdo a los resultados promedio de los meses de mayo y junio de 1999, meses incluidos en el período de lluvias de la Laguna Pampa El Cabildo, Chiapas, y etapa en el que arriban a la laguna las postlarvas de camarón blanco. El agua de mar y el agua de dilución (agua potable municipal) utilizada durante la aclimatación y en las pruebas de toxicidad se pasaron por un filtro de arena y carbón activado, y se mantuvo en oxigenación constante por dos días antes de usarla.
Las postlarvas se alimentaron diariamente con alimento balanceado (elaborado en el laboratorio de Ecofisiología de la Facultad de Ciencias de la UNAM, sede Cd. del Carmen, Campeche), 30-35% de proteína (Colvin y Brand 1977) dos veces al día (10:00 y 16:00 h) y complementado en las noches (22:00 h) con nauplios de artemia; el alimento remanente, las heces producidas y las exuvias se retiraron diariamente.
Bioensayos: Se realizaron pruebas de toxicidad aguda mediante bioensayos estáticos, con recambio de agua cada 24 horas, por un periodo de 168 horas (Petrocelli 1985, Anónimo 1986b, 1996b). Con la finalidad de minimizar el estrés de las postlarvas por manipulación, éstas se pesaron y colocaron en los acuarios 12 horas antes de iniciar los experimentos. En los bioensayos se utilizaron postlarvas con un peso húmedo (PH) promedio inicial de 4 mg. Las pruebas se realizaron en acuarios de vidrio de 9 L de capacidad, conteniendo 10 organismos cada uno, y se establecieron 7 lotes experimentales y un control sin plaguicida. Cada condición se realizó por triplicado. Dada la alta insolubilidad del DDT en agua, se adicionó éste a los acuarios disuelto en acetona, por lo que se estableció un control con acetona. Las concentraciones experimentales fueron 0 (control), 17, 22, 28, 34, 43, 64 y 96 ng/L para DDT y 0, 42, 62, 88, 115, 148, 222 y 323 ng/L para endosulfan. Todos los días se realizaron recambios de agua y plaguicidas a razón del 40% una hora después de la primera alimentación del día. Como criterio de muerte de los camarones se utilizó la falta de respuesta a la estimulación mecánica (Anónimo 1986b). En el presente estudio, se utilizó el DDT y endosulfan grado comercial (Fertimex S.A., 75% de pureza y Thiodan 35 CE AgrEvo respectivamente).
En los organismos sobrevivientes se determinó el crecimiento absoluto, crecimiento relativo y se estableció la relación ganancia relativa de peso (GRP)-concentración del tóxico (CT) para determinar la concentración que reduce al 5 y 50% el crecimiento de los organismos (CE5 y CE50 ) (Busacher et al.1990, Chen y Chen 1992, Chen y Lin 1992). Para medir el consumo de oxígeno de los organismos, se colocaron mínimo 2 postlarvas en cámaras respirométricas individuales de 200 ml por concentración de prueba, el oxígeno disuelto se midió con el Checkmate 90 (Corning, NY 14831) (± 0.1 mg/l) y el consumo de oxígeno de los animales se calculó por la diferencia entre la concentración de las muestras iniciales y después de 2 h de sellado de las cámaras. Los datos se corrigieron con un control sin organismo y se expresaron en porcentaje (%) de cambio con respecto al control sin contaminante.
Análisis estadístico: A partir de los registros de mortalidad (%) se determinó la Concentración Letal Media (LC50 ) con el programa de cómputo DORES y utilizando el modelo Y =PROBIT P: Log X (Ramírez 1989), seguidamente se determinó la LC50 incipiente (concentración letal media en la que la curva de toxicidad se vuelve asintótica), la cual se multiplicó por un factor de aplicación empírico de 0.1 y se obtuvo el Nivel de Seguridad (LS)(Sprague1971). A partir de la relación mortalidad (M)-tiempo (T), se realizó un ajuste de cuadrados mínimos no lineal, calculando seguidamente la tasa de mortalidad (m ) y estableciendo la correlación entre m y la concentración del plaguicida. Los tiempos medios de muerte (LT50 ) se calcularon de acuerdo al procedimiento establecido (Anónimo 1986b). También se calculó la concentración máxima aceptable del tóxico (MACT) según las recomendaciones de Buikema et al.(1982) y Gelber et al.(1985). El análisis para calcular la MACT se realizó mediante un análisis de varianza (ANOVA)de una vía para detectar si existían diferencias significativas en la sobrevivencia de las postlarvas entre los grupos con contaminantes y el control sin contaminante, seguida por la prueba de Dunnetts (Gelber et al. 1985), análisis de comparación múltiple diseñado específicamente para comparar varios muestras experimentales con respecto a un control. Además se utilizó el ANOVA de una vía para determinar si existió diferencia estadísticamente significativa en el crecimiento de las postlarvas expuestas a los contaminantes y postlarvas control sin contaminante. Para la realización de las ANOVAS se utilizó el programa STATISTICA (Anónimo 1995).
Resultados
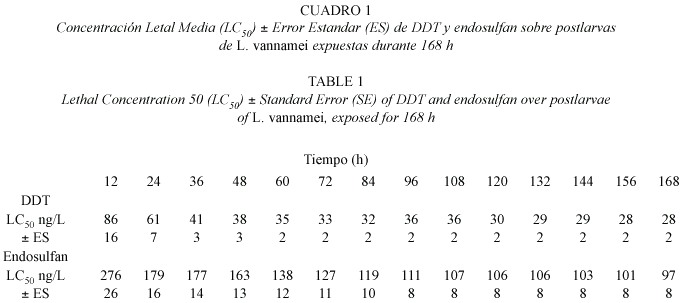
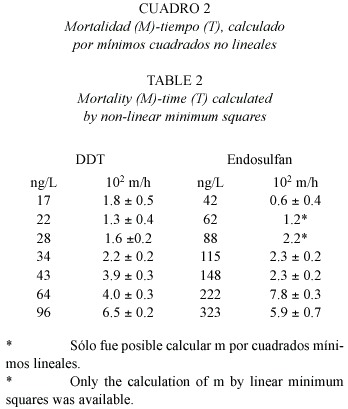
Al inicio de los bioensayos el peso de los organismos no presentó diferencia significativa (ANOVA, p>0.05)entre los grupos de prueba. La mortalidad mínima y máxima de postlarvas de L.vannamei después de 168 horas fue de 23% y la máxima de 97% para ambos compuestos (Dunnetts p<0.05). La mortalidad en los controles de cada experimento fue de 0%. En el caso del DDT la LC50 -12 h fue de 86 ± 16 ng/1 y la LC 50 -168 h fue de 28 ± 2 ng/L; para el endosulfan la LC50 -12 h fue de 276 ± 26 ng/L y la LC50 -168 h fue de 97 ± 8 ng/1 a las 168 h (Cuadro 1). El coeficiente de determinación (R2 ) más bajo del modelo (Y =PROBIT P: Log X) fue de 0.87 y 0.86 para DDT y endosulfan respectivamente. La LC50 incipiente calculada para el DDT fue de 30 ng/L y para el endosulfan fue de 105 ng/L; así, el LS para el DDT fue de 3 ng/L, mientras que para el endosulfan fue de 10.5 ng/L. Los resultados del ajuste por mínimos cuadrados no lineales entre mortalidad y tiempo se presentan en el Cuadro 2,a partir del cual se obtuvieron las correlaciones entre m y los contaminantes: m =(6.6 ± 0.6) x 10-4 [DDT, ng L-1 ], y m =(2.3 ± 0.6) x 10-4 [endosulfan, ng L-1 ],de lo cual se infiere que el DDT es casi 3 veces más tóxico para las post- larvas de camarón que el endosulfan.
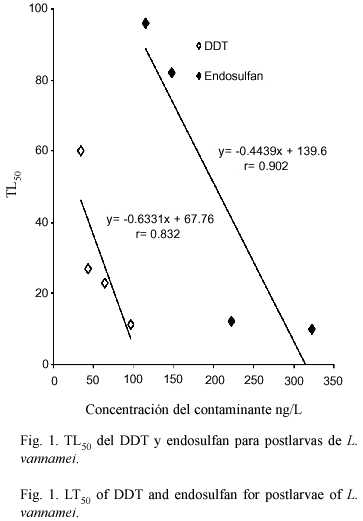
El LT50 para endosulfan y DDT sólo se pudo calcular en las cuatro concentraciones más altas, esto debido a que a las 168 h sólo esas concentraciones presentaron más del 50% de mortalidad; sin embargo, en ambos casos se observó una relación negativa entre la concentración del tóxico y el LT50 (Fig.1). Los tiempos medios de muerte (intervalo de confianza, 95%) para el DDT fueron de 60 (146-25), 27 (66-11), 23 (48-11) y 11 (18-7) horas, para 34, 43,64 y 96 ng/L respectivamente, mientras que para el endosulfan fueron de 96 (167-55), 82 (134-50),12 (32-5) y 10 (20-5) horas, para 115, 148, 222 y 323 ng/L. La MACT fue de 60.8 y menor a 17 ng/L para el endosulfan y el DDT, respectivamente.
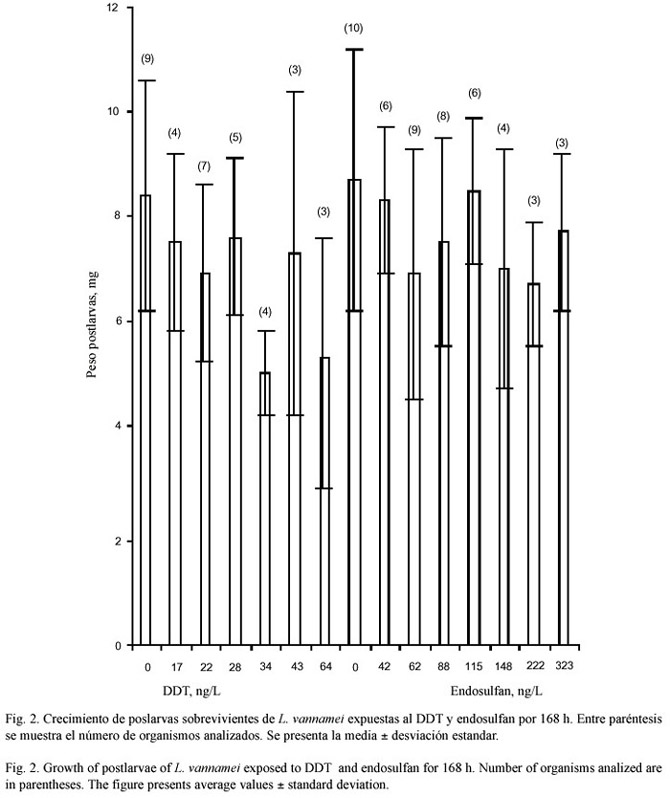
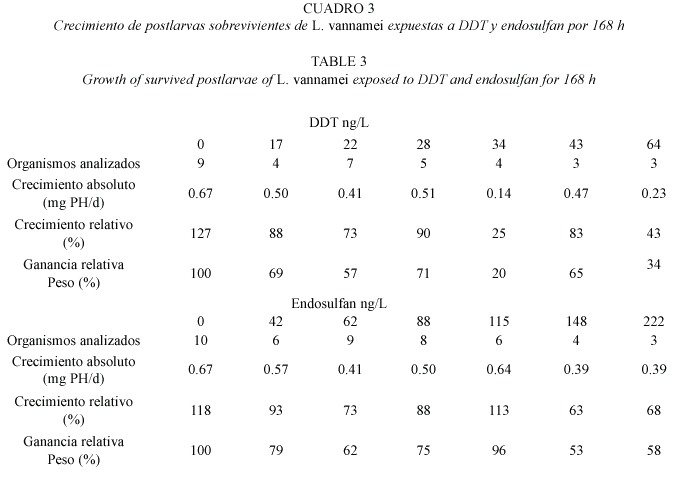
Al final de los experimentos, el crecimiento de los organismos sobrevivientes expuestos a las diferentes concentraciones DDT y endosulfan, no se vio modificado significativamente (ANOVA,p>0.05), con respecto al control sin plaguicida. En ambos casos se observó una ligera tendencia hacia la disminución del crecimiento conforme aumentó la concentración del tóxico (Fig.2,Cuadro 3). La CE5 y CE50 para el DDT fue de 1 y 38 ng/L respectivamente, mientras que para el endosulfan la relación no fue significativa (Cuadro 4).
El consumo de oxígeno de los organismos sobrevivientes expuestos a DDT y endosulfan, presentó grandes variaciones con respecto al control, registrándose cambios de +82, -18, -41, +27 y +27% para 17, 22, 28, 43 y 64 ng/L de DDT, mientras que para el endosulfan los cambios fueron de -32, +82, +36, +59, +95 y +14% para 42, 62, 88, 115, 148 y 222 ng/L.
Discusión
En México, el uso del DDT ha disminuido considerablemente en los últimos años, dada la prohibición para usarlo en agricultura, su uso en acciones de combate a vectores del paludismo y dengue en la costa de Chiapas siguió vigente hasta finales del año 2000. Así, en la región del Soconusco, Chiapas, de 1995 a 1997 se utilizaron 1080 kg de este producto (Cruz 1998). Por su parte, el endosulfan se usa para el combate de diversas plagas que atacan a los cultivos de la región como el café, algodón y chile, entre otros. El ingreso de estos compuestos a las lagunas costeras se ve facilitado por la cercanía de los campos de cultivo y el gran número de comunidades rurales cercanas a estos ecosistemas en donde se han aplicado dichos compuestos.
Los bioensayos agudos permiten obtener un conocimiento del impacto de los compuestos en los organismos acuáticos y donde las larvas y juveniles son más vulnerables que los adultos (Martínez 1991, Espina y Vanegas 1996). De tal forma, conocer el efecto tóxico de compuestos químicos en los organismos acuáticos, resulta de especial importancia en el esfuerzo por conservar los ecosistemas y las especies.
Algunos estudios informan que el DDT puede ser extremadamente tóxico para las especies acuáticas, pudiendo reducir las poblaciones de larvas de camarón (Von Osten 1990, Albert et al. 1996). En el presente trabajo el DDT fue más tóxico que el endosulfan, ya que la CL50 del endosulfan fue 3.5 veces mayor que la del DDT a las 168 h. La mayor toxicidad del DDT también se observo a partir de los LT50 , que es un indicador de la potencia de un tóxico para peces y crustáceos (Chen et al.1990), ya que mientras una cantidad de 323 ng/L de endosulfan requirió de 10 h para que el 50% de los organismos de prueba muriera; sólo fue necesario 96 ng/L de DDT para tener la misma respuesta en 11 h. La MACT y el nivel de seguridad obtenidos para ambos compuestos reafirman la mayor toxicidad del DDT. Así mismo, en lo que se refiere a crecimiento y respiración de los organismos de prueba, las variaciones más fuertes se registraron para el DDT.
En general, los compuestos organoclorados modifican la cinética de permeabilidad de los iones Na+, K+ y Ca++ de la membrana del axón, pudiendo producir efectos sobre el sistema nervioso de los diferentes organismos que se exponen a estos contaminantes (Repetto et al. 1995). Galindo et al. (1996b) informaron una disminución en el contenido relativo de ácidos nucleicos, sugiriendo un efecto deletéreo en el material genético de larvas de L. vannamei expuestas a 130 ng/L de DDT; asimismo, informaron una baja en la tasa de síntesis de glucógeno de las larvas, lo que indica que el DDT tiene un efecto inhibitorio en los procesos bioquímicos relacionados con la síntesis de carbohidratos o que las larvas consumen más carbohidratos para resistir el estrés causado por el tóxico. También mencionaron que las alteraciones en el consumo de oxígeno indican efectos en el metabolismo que pueden afectar el crecimiento de las larvas.
Por su parte, el endosulfan en crustáceos y moluscos disminuyó los aminoácidos libres en la hemolinfa e inhibe la Na-K-ATPasa branquial. A su vez, estas perturbaciones modifican la osmorregulación y el consumo de oxígeno, lo que repercute en su actividad normal. En general, estos efectos se asocian a la acción neurotóxica de este compuesto, alterando finalmente la reproducción y el crecimiento (Naqvi y Vaishnavi 1993).
A pesar que en el presente estudio no se realizaron análisis a nivel bioquímico, seguramente que los efectos antes mencionados para el DDT y endosulfan fueron, entre otros, el inicio de las alteraciones observadas en este trabajo en cuanto a crecimiento, consumo de oxígeno y sobrevivencia. En este trabajo se tuvo la temperatura elevada (29 ± 1 °C), pH básico (8 ± 1)y baja salinidad (3 ± 1 ), características promedio del agua de Laguna Pampa El Cabildo durante el periodo de ingreso de las postlarvas. Es así que las MACT y CL50 obtenidas en este estudio son menores a las informadas en otros trabajos (Cuadro 5), esto es debido, entre otros factores, a la diferencia de especies empleadas, estadio de desarrollo, a las condiciones de temperatura, salinidad y pH utilizadas en cada caso. En los plaguicidas se ha determinado que una amplia variedad de estos compuestos presentan una mayor toxicidad a altas temperaturas y a valores de pH básicos (Nimmo 1985); así mismo, estudios realizados con Cancer magister y Hemigrapsus nudus mostraron un mayor efecto tóxico de plaguicidas a bajas salinidades (Caldwell 1974).
De acuerdo con Tarzwell (1962), el objetivo de la investigación de efectos letales y subletales debe ser la habilidad para predecir niveles de los contaminantes que son seguros bajo condiciones de exposición continua, en términos de sobrevivencia, crecimiento, reproducción, bienestar general y producción de cultivos (acuacultura). El «nivel de seguridad» ha sido utilizado ampliamente con este objetivo en peces y camarones (Sprague 1971, Chen y Lin 1991, Lin et al.1993). De esta forma, los «niveles de seguridad» calculados en este trabajo para las postlarvas de camarón expuestas al DDT y endosulfan, representarían los límites máximos aceptables de estos compuestos para estos organismos. Dichos niveles de seguridad se aplicarían para Laguna Pampa El Cabildo, Chiapas, y otras lagunas con condiciones similares, dado que las pruebas se realizaron con parámetros físicos del agua similares a los registrados en el periodo que ingresan las post-larvas de camarón a la laguna.
Es importante considerar que la interacción del DDT y endosulfan, y con otros contaminantes y factores ambientales, puede modificar los «niveles de seguridad», presentándose casos de efectos antagónicos, aditivos o sinergísticos, lo que evidencia la necesidad de profundizar con este tipo de investigaciones, especialmente en regiones con alto uso de agroquímicos, muy pobres en la generación de información científica de ecosistemas acuáticos y con importantes recursos acuáticos como lo es la Costa de Chiapas, México.
Considerando que las concentraciones máximas de DDT y endosulfan encontrados en agua de la laguna (2.9 y 6.4 ng/L respectivamente) (Castro-Castro 2002) son muy próximas a los niveles de seguridad establecidos en este trabajo (3 y 10.5 ng/L de DDT y endosulfan respectivamente), es posible que las concentraciones de estos plaguicidas en agua, constituyan un factor de riesgo para los organismos, ya que el mínimo incremento de estos compuesto (por nueva incorporación a la laguna o por resuspensión a partir del sedimento), haría que los niveles de seguridad fueran superados y por lo tanto que los organismos sufrieran algún grado de afectación.
Resumen
Con el fin de conocer la toxicidad del DDT y endosulfan sobre postlarvas de camarón blanco (Litopenaeus vannaei), se realizaron pruebas de toxicidad aguda en condiciones de laboratorio por 168 h, con temperatura de 29 ± 1 °C, salinidad de 3 ± 1 y pH en 8 ± 1.Se calculó la concentración letal media (LC50 ), la LC50 "incipiente", los tiempos medios de muerte (LT50 ), la Máxima Concentración Aceptable del Tóxico (MACT) y el "Nivel de Seguridad" (LS); así mismo, en los organismos sobrevivientes se determinó la concentración a la que el crecimiento de los organismos se reduce en un 5 y 50% (CE5 y CE50 ). Se evaluaron además las alteraciones en el consumo de oxígeno. El DDT fue 3 veces más tóxico que el endosulfan; sin embargo, los organismos resultaron ser muy sensibles a ambos compuestos. La tasa de crecimiento de las postlarvas disminuyó en un 80 y 50% para el DDT y endosulfan respectivamente. La baja resistencia de las postlarvas al DDT y endosulfan, y las concentraciones de estos compuestos en la laguna, sugieren que si se diera un ingreso adicional de estos plaguicidas al sistema, es muy probable un potencial impacto en la producción de camarón del sistema.
Palabras clave: Ecotoxicología, Litopenaeus vannamei, DDT, endosulfan, pesticidas.
Agradecimientos
Los autores agradecen el apoyo brindado por el CONACyT, G. Mejia, G.Gaxiola y J. Valle; así como los comentarios de T. Álvarez, M. Arce, F. González y los revisores anónimos para el mejoramiento del manuscrito.
Referencias
Alabaster, J. S. 1969. Survival of fish in 164 herbicidaes, insecticides, fungicides, wetting agents and miscellaneous substances.Int.Pest.Control.11:29-35. [ Links ]
Albert, L. A., R. Loera & C. Bárcenas. 1996. Química y ecotoxicología de los insecticidas, p. 125-137. In A. V. Botello, J. L. Rojas Galaviz, J. A. Benítez & D. Zárate- Lonielí (eds.).Golfo de México, Contaminación e Impacto Ambiental: Diagnóstico y Tendencias. EPOMEX Serie Científica 5.Universidad Autónoma de Campeche, México. [ Links ]
Anónimo. 1986a. Estudio para la detección de contaminantes en los esteros y cuerpos de agua causados por agroquímicos en la región del Soconusco, Chiapas. Documento Base. SEDUE-Gobierno del Estado de Chiapas. 189 p. [ Links ]
Anónimo. 1986b.Test of the acute lethal toxicity of pollutants to marine fish and invertebrates. Reference Methods for Marine Pollution Studies. UNEP/FAOI/ IAEA. No. 43 (draft). UNEP. 23 p. [ Links ]
Anónimo. 1991. Reserva de la Biósfera "La Encrucijada". Plan operativo 1991-1992. Instituto de Historia Natural. Tuxtla Gutiérrez, Chiapas, México. 27 p. [ Links ]
Anónimo. 1995. STATISTICA for Windows [Computer program manual ]. StatSoft. Tulsa. [ Links ]
Anónimo. 1996a. Programa de Ecología, Recursos Naturales y Pesca 1995-2000. COPLADE. Tuxtla Gutiérrez, Chiapas. 162 p. [ Links ]
Anónimo. 1996b. Penaeid acute toxicity test. USEPA. EPA 712-C-96-137. OPPTS 850. 1045. "Public Draft". [ Links ]
Anónimo. 1998. Comisión Intersecretarial para el Control del Proceso y Uso de Plaguicidas, Fertilizantes y Sustancias Tóxicas (CICOPLAFEST). Catálogo Oficial de Plaguicidas. México. 42 p. [ Links ]
Arias, V. F., C. Riera, D. Rojas, N. Cabrera & G. Dierkmeier. 1990. Plaguicidas Organoclorados. Serie vigilancia 9. CPEHS/PSA/OPS/OMS. Metepec, Estado de México, México, p. 7-22. [ Links ]
Benítez, J. A. & C. Bárcenas. 1996. Patrones de uso de los plaguicidas en la zona costera del golfo de México, p.155-167. In A. V. Botello, J. L. Rojas Galaviz, J. A. Benítez & D. Zárate-Lonielí (eds.). Golfo de México, Contaminación e Impacto Ambiental: Diagnóstico y Tendencias. EPOMEX Serie Científica 5.Universidad Autónoma de Campeche. México. [ Links ]
Botello, A. V., S. Villanueva, L. Rueda & G. Díaz. 1995. Impactos Ecológicos de los Plaguicidas en las Lagunas Costeras de Chiapas, México. Informe Técnico. UNAM-IHN. 115 p. [ Links ]
Buikema, A. L., R. Niederlehner & J. Cairns. 1982. Biological monitoring. Part IV-Toxicity testing. Water Res. 16:239-262. [ Links ]
Busacher, G. P., R. Adelman & M. Goolish. 1990. Growth, p.363-387. In B. Schreck & P. B. Moyle (eds.). Methods for Fish Biology.Am.Fish.Soc.USA. [ Links ]
Caldwell, R. S. 1974. Osmotic and ionic regulation in Decapod Crustacea exposed to methoxychlor, p. 165-180. In J. Vernberg & B. Vemberg (eds.). Pollution and Physiology of Marine Organims. Academic, New York. [ Links ]
Castro-Castro, V. 2002. Contaminación por plaguicidas organoclorados en Laguna Pampa El Cabildo, Chiapas, y su efecto tóxico en postlarvas de camarón blanco (Litopenaeus vannamei). Tesis de grado. ECOSUR. 51 p. [ Links ]
Chen, J. C., Y. Ting, N. Lin & N. Lin. 1990. Lethal effects of ammonia and nitrite on Penaeus chinensis juveniles. Mar. Biol. 107:427-431. [ Links ]
Chen, J. C. & Y. Lin. 1991. Lethal effects of ammonia and nitrite on Penaeus penicillatus juveniles at two salinity levels. Comp. Biochem. Physiol. 100C:477-482. [ Links ]
Chen, J. C. & F. Chen. 1992. Effects of nitrite on growth and molting of Penacus monodon juveniles. Comp. Biochem. Physiol. 101:453-458. [ Links ]
Chen, J. C. & Y. Lin. 1992. Effects of ammonia on growth and molting of Penaeus monodon juveniles. Comp. Biochem. Physiol. 101:449-452. [ Links ]
Coll, M., J. Cortés & D. Sauma. 2004. Características físico-químicas y determinación de plaguicidas en el agua de la laguna de Gandoca, Limón, Costa Rica. Rev. Biol. Trop. 52 (Suppl.2): 33-42. [ Links ]
Colvin, L. B. & W .Brand. 1977. The protein requirement of penaeid shrimp at various life stages with compounded diets in a controlled environment system. Proc. World Maricult. Soc. 8:821-840. [ Links ]
Cruz, L. 1998. Determinación de plaguicidas en agua y sedimentos en los estuarios y lagunas costeras de la región del Soconusco, Chis. Tesis de licenciatura, Esc. Ing. Quím. BUAP. 68 p. [ Links ]
Espina, S. & C. Vanegas. 1996. Ecotoxicología y contaminación, pp. 69-106. In A. V. Botello, J. L. Rojas Galaviz, J. A. Benítez & D. Zárate Lomelí (eds.).Golfo de México, Contaminación e Impacto Ambiental: Diagnóstico y Tendencias. EPOMEX Serie Científica 5. Universidad Autónoma de Campeche. México. [ Links ]
Galindo, G., M. Ibarra, V. Lizárraga & Q. Urenda. 1992. Contaminación por plaguicidas en almejas y camarones en dos ecosistemas costeros de Sinaloa, México. Cienc. Mar 1:6-11. [ Links ]
Galindo, G., A. Ibarra, V. Lizárraga, M. Jasso & A. Mulloz. 1994. Efectos de la contaminación por plaguicidas en camarones peneidos de Sinaloa, México. Cienc. Mar 1:34-38. [ Links ]
Galindo, R. J. G., A. Medina & C. Villagrana. 1996a. Toxic effects of organochlorine pesticides on Penaeus vannamei shrimps in Sinaloa, México. Chemosphere 33:567-575. [ Links ]
Galindo, R. J. G., A. Medina & C. Villagrana. 1996b. Physiological and biochemical changes in shrimp larvas (Penaeus vannamei) intoxicated with organochlorine pesticide. Mar. Pollut. Bull. 32:872-875. [ Links ]
Galindo, R. G., C. Villagrana & A. Lazcano. 1999. Environmental conditions and pesticide pollution of two coastal ecosystems in the Gulf of California, México. Ecotox. Environ. Safety 44:280-286. [ Links ]
Gelber, R. D., T. Lavin, R. Mehta & A. Schoenfeld. 1985. Statistical Analysis, p.110-123. In M. Rand & R. Petroccili (eds.). Fundamentals of Aquatic Toxicology. Hemisphere. New York. [ Links ]
Gold-Bouchot, G., T. Silva-Herrera & O. Zapata-Pérez. 1993. Chlorinated pesticidas in the Río Palizada, Campeche, México. Mar. Pollut. Bull. 26:648-650. [ Links ]
Gold-Bouchot, G., T. Silva-Herrera & O. Zapata-Pérez. 1995. Organochlorine pesticide residue concentrations in biota and sediments from Río Palizada, México. Bull. Environ. Contam. Toxicol. 54:554-561. [ Links ]
Gutiérrez-Galindo, E., G. Flores, M. Ortega & J. Villaescua. 1992. Pesticidas en las aguas costeras del Golfo de California: Programa de vigilancia con mejillón 1987-1988. Cien. Mar. 18:77-99. [ Links ]
Lin, H. P., P. Thuct, P. Trilles, R. Mounet-Guillaume & G. Charmantier. 1993. Effects of ammonia on survival and osmoregulation of various development stages of the shrimp Penaeus japonicus. Mar. Biol. 117: 591-598. [ Links ]
Macek, K. J., A. Lindberg, S. Sauter, S. Buxton & A. Costa. 1976. Toxicity of four pesticides to water fleas and fathead minnows. EPA-600/3-76-099. Duluth, Minn., U. S. Environmental Research Laboratory. [ Links ]
Martínez, J. F. 1991. El papel del bioensayo en la evaluación de la toxicidad acuática, p.57-65. In M. Figueroa, C. Alvarez, A. Esquivel & M. Ponce (eds.). Fisicoquímica y Biología de las Lagunas Costeras Mexicanas. Serie Grandes temas de la Hidrobiología 1. UAM-I. [ Links ]
Martínez-Tabche, L., M. Romero, E. López & M. Gala. 1999. Efecto tóxico del DDT, clordano y agua de la presa Ignacio Ramírez (México), sobre Daphnia magna (Crustacea: Daphnidae). Rev. Biol. Trop.47: 681-690. [ Links ]
Mayer, F. L. 1987. Acute toxicity handbook of chemicals to estuarine organisms. Washington, D.C. US. Department of Commerce, NTIS. 173 p. [ Links ]
Naqvi, S. & Ch. Vaishnavi. 1993. Bioaccumulative potencial and toxicity of endosulfan insecticide to non-target animals. Mini-Review. Comp. Biochem. Physiol. 105C:347-361. [ Links ]
Nimmo, D. R. 1985. Pesticides, p.335-373. In M. Rand & R. Petrocelli (eds.). Fundamentals of Aquatic Toxicology. Methods and Applications. Hemisphere, USA. [ Links ]
Noreña-Barroso, E., O. Zapata-Pérez, Y. Ceja-Moreno & G. Gold-Bouchot. 1998. Hydrocarbon and Organochlorine residue concentrations in sediments from Bay of Chetumal, México. Bull. Environ. Contam.Toxicol. 61:81-87. [ Links ]
Petrocelli, S. R. 1985. Chronic toxicity test, p.96-109. In M. Rand & R. Petrocelli (eds.). Fundamentals of Aquatic Toxicology. Hemisphere, New York. [ Links ]
Ramírez, E. 1989. DORES-Programa de computo. Curso regional sobre ensayos biológicos y pruebas de toxicidad. INDERENA/PAC/PNUMA/FAO/COI. Cartagena de Indias, Colombia, Junio 3-28,1989. [ Links ]
Repetto, M., D. Martínez & P. Sanz. 1995. Actualización de la toxicología de los plaguicidas, p.557-601 . In M. Repetto (ed.).Toxicología avanzada. Díaz de Santos, Madrid. [ Links ]
Spongberg, A. L. 2004a. PCB contamination in surface sediments in the coastal waters of Costa Rica. Rev. Biol. Trop. 52 (Suppl.2):1-10. [ Links ]
Spongberg, A. L. 2004b. PCB concentrations in sediments from the Gulf of Nicoya estuary, Pacific coast of Costa Rica. Rev. Biol. Trop. 52 (Suppl.2):11-22. [ Links ]
Spongberg, A. L. 2004c. PCB contamination in marine sediments from Golfo Dulce, Pacific coast of Costa Rica. Rev. Biol. Trop. 52 (Suppl.2):23-32. [ Links ]
Sprague, J. B. 1971. Measurement of pollution toxicity to fish-III.Sublethal effects and «safe» concentrations. Water Res. 5:245-266. [ Links ]
Tarzwell, C. M. 1962. The need and value of water quality criteria with special reference to aquatic life. Can. Fish. Cult. 31:35-41. [ Links ]
Von Osten, J. R. 1990. Los insecticidas organoclorados, p. 99-120. In L.Albert (ed.).Los plaguicidas, el ambiente y la salud. Centro de Ecodesarrollo, México. [ Links ]