
Diagnóstico molecular de cromosomopatías fetales en Costa Rica
(Molecular Diagnosis of Fetal Chromosomal Defects in Costa Rica)
Wendy Malespín-Bendaña, Fernando Ortiz-Morales, Isabel Castro-Volio1
Resumen
Justificación y objetivos: En Costa Rica, el diagnóstico de anomalías cromosómicas fetales se realiza solo mediante el análisis citogenético convencional de cromosomas obtenidos de cultivos celulares. Además de que la espera por los resultados puede ser larga, con alguna frecuencia fracasa el cultivo, por contaminación o por mala calidad de la muestra, o las figuras mitóticas no se pueden analizar, por lo que es necesario disponer de una metodología sencilla y barata, para obtener un diagnóstico prenatal rápido y fiable de trisomía 21, 18 ó 13, en embarazos de alto riesgo genético sometidos a amniocentesis o cordocentesis.
Métodos: Se diseñaron tres PCRs multiplex para amplificar cuatro distintas repeticiones cortas en tándem, de cada uno de los cromosomas 21, 18 y 13. Se colectaron 93 muestras (88 líquidos amnióticos y 5 sangres fetales), recibidas en el laboratorio entre 2006 y 2008, con solicitud de análisis cromosómico. Los resultados de la reacción en cadena de la polimerasa cuantitativa fluorescente, fueron comparados con el cariotipo obtenido de las mismas muestras para demostrar la fiabilidad del ensayo
Resultados: Para este grupo de datos, la exactitud del ensayo fue del 100% y se consiguió obtener resultados en 48 horas. Se logró realizar el análisis de repeticiones cortas en tándem en el 77% de las muestras en las que no se pudo obtener crecimiento celular.
Conclusión: La reacción en cadena de la polimerasa cuantitativa fluorescente demostró ser una metodología sencilla, fiable y rápida, por lo que podría convertirse en una herramienta complementaria del análisis cromosómico convencional. La obtención de resultados rápidos en casos de diagnóstico prenatal podría disminuir el periodo de ansiedad parental por la espera de los resultados, así como permitir un mejor abordaje terapéutico de los fetos afectados.
Descriptores: diagnóstico prenatal, Costa Rica, trisomía, cromosoma 13, romosoma 18, cromosoma 21
Justification and aims: In Costa Rica, the diagnosis of chromosomal fetal anomalies is realized only by conventional cytogenetic analysis of chromosomes obtained from cellular cultures. The waiting for the results can be long. Moreover with some frequency culture fails due to contamination or bad quality of the sample or they cannot be analyzed. This makes it necessary to have a simple and cheap methodology to obtain an accurate and rapid fetal diagnosis of trisomy 21, 18 or 13, in pregnancies of high genetic risk submitted to amniocentesis or cordocentesis.
Materials and methods: Three multiplex PCRs were designed to amplify four different short tandem repeats of each of the chromosomes 21, 18 and 13. There were collected 93 samples (88 amniotic fluids and 5 fetal bloods), received in the laboratory between 2006 and 2008 with request ofor chromosomal analysis. The results of the quantitative fluorescent PCR were compared with the obtained cariotype of the same samples to stablish the accuracy demonstrate the reliability of the assay.
Results: Accuracy of the assay was 100% and it was possible to obtain results within 48 hours. STRs analysis could be made in 77% of the samples where the cellular culture could not be done.
Conclusion: The quantitative fluorescent PCR demonstrated to be a simple, accurate and rapid methodology, from what it might turn into a complementary tool of the chromosomal conventional analysis. The securing of rapid results in cases of antenatal diagnosis might diminish the period of anxiety parental for the waiting of the results, as well as to allow a better therapeutic management of the affected fetuses.
Key words: prenatal diagnosis, Costa Rica, trisomy, chromosome 13, chromosome 18, chromosome 21.
Los defectos cromosómicos son una causa importante de enfermedad y mortalidad en el feto, ya que producen abortos espontáneos, óbitos, mortinatos y muerte neonatal, malformaciones congénitas, así como retardo mental y del desarrollo. Por lo anterior, el diagnóstico precoz de cualquier defecto cromosómico en el feto es de vital importancia, ya que así se podrá valorar la posibilidad de tratamiento intrauterino, interrupción del embarazo o preparación del núcleo familiar y del personal de salud, para la atención óptima del neonato afectado, con el fin de minimizar el daño y mejorar el tratamiento o la rehabilitación.1
El método de diagnóstico cromosómico fetal más utilizado es el que se realiza mediante amniocentesis y cultivo de las células fetales descamadas en el líquido amniótico, empleado para obtener el cariotipo fetal, que implica el estudio del número y la estructura de los cromosomas. A pesar de considerarse como el estándar de oro para el análisis cromosómico, muchas veces no se detectan duplicaciones o deleciones de menos de 5 Mb.2 Aunado a esto, el cultivo celular tiene la gran desventaja de que es laborioso y las células demoran entre una y tres semanas en crecer lo suficiente. Este lapso a menudo es angustioso para la madre, quien ha sido sometida a una amniocentesis por presentar algún factor de riesgo para defectos cromosómicos fetales. Además, para realizar un cariotipo fetal es necesario obtener metafases en suficiente cantidad y con calidad, lo cual no siempre se logra con éxito.
La introducción de técnicas de biología molecular ha proporcionado los medios para estudiar de manera más fina la estructura y segregación de los cromosomas, lo que ha mejorado y facilitado su análisis convencional.3 Además, presentan la gran ventaja de que algunas de las técnicas se pueden aplicar en células en interfase, de manera que no se precisa el cultivo celular y el estudio se efectúa directamente sobre el material celular, ya sea líquido amniótico u otras muestras. Esto representa un gran ahorro de tiempo y recursos.2
Hibridación in situ con fluorescencia (FISH). Esta técnica utiliza sondas específicas de ADN marcadas con nucleótidos modificados, que fluorescen directamente o que pueden ser detectados por medio de la unión de una molécula fluorescente reportera. Estas sondas de ADN en hebra sencilla pueden ser hibridizadas no solo a cromosomas metafásicos, sino también a núcleos en interfase o a células que no se dividen. Posteriormente, y con el filtro apropiado, la señal es detectada en el microscopio. La FISH es una técnica muy informativa y con gran aplicabilidad, pero presenta varias limitaciones. La primera de ellas es de orden económico, ya que las sondas, microscopios y software requeridos tienen un costo muy elevado.4 También existen limitaciones técnicas. Por ejemplo, el tamaño de la sonda puede variar desde 100 hasta 150 kb, por lo que podría contener secuencias de ADN repetitivo capaces de hibridizar en muchas posiciones cromosómicas, no solo en la secuencia específica con la que tiene completa homología. Como resultado de este inconveniente se obtendrían falsos positivos.5 La FISH muestra niveles altos de pruebas no informativas en edades gestacionales tardías, debido a la degradación de la cromatina, ya que las sondas no pueden hibridarse adecuadamente.6 La manera de solucionar estos problemas parece ser una metodología basada en la reacción en cadena de la polimerasa (PCR), asistida por analizadores computarizados de ADN, llamada PCR cuantitativa fluorescente, que ofrece resultados más rápidos y confiables y a un costo mucho menor.
]]> PCR cuantitativa fluorescente (QF-PCR). Conocida también como amnio-PCR .7-9 consiste en la amplificación y cuantificación de regiones específicas de ADN por medio de PCR, utilizando "primers" (iniciadores o cebadores) marcados con fluorescencia, que permiten que un secuenciador de ADN basado en capilares, registre los fragmentos de la PCR como picos de excitación en un gráfico denominado electroforetograma.10La QF-PCR es un método rápido y eficiente para detectar el número de copias de uno o varios cromosomas, por medio de la amplificación de secuencias específicas de ADN altamente polimórficas en longitud entre individuos, denominadas STR (Short Tandem Repeats) o microsatélites. Los STRs están presentes en todo el genoma y consisten en secuencias formadas por dos a seis nucleótidos repetidos varias veces en tándem, formando secuencias de diferentes longitudes. La cantidad de repeticiones de un determinado STR varía de alelo a alelo, lo cual permite distinguir entre ellos.11 Los STRs amplificados con esta técnica, brindan información para conocer el número de copias de cada cromosoma. En un individuo normal que tiene diferente número de repeticiones en cada alelo, se observan en el electroforetograma dos picos con una razón de 1:1 por cada región cromosómica analizada, con lo cual el individuo es heterocigoto y se dice que el marcador es informativo. Las trisomías son visualizadas como un pico extra en sujetos trialélicos, o bien, con una razón de picos 2:1 ó 1:2. Estas razones de picos se calculan con el área y con la altura de los picos.12
Una de las características más notables de esta técnica es la poca cantidad de líquido amniótico requerido, pues se precisan de 0,2 a 1 ml para una extracción exitosa de ADN. La extracción se realiza con un método de chelex, que necesita unos 20 minutos por muestra, y es posible extraer ADN de calidad a partir de líquido amniótico fresco o congelado, incluso de las células provenientes de los cambios de medio de cultivo de amniocitos. De igual manera y con el mismo protocolo se puede extraer ADN de muestras de vellosidades coriónicas y sangre fetal y neonatal.12
La amnio-PCR tiene otras aplicaciones derivadas del diagnóstico de aneuploidías, como la determinación de cigosidad en gemelos en embarazos múltiples.13, 14 Asimismo, el análisis de STRs en aneuploidías fetales también puede brindar información adicional en las trisomías, si se dispone de muestras de los padres, como el origen parental del cromosoma extra, y determinar si la no disyunción ocurrió en la meiosis I o II.15-17
Muchos reportes de los últimos años han demostrado la eficiencia y fiabilidad de la QF-PCR en la detección de aneuploidías, en países europeos,10, 16, 18-22 asiáticos23-25 y, recientemente, en los Estados Unidos26 y en Argentina.27 Junho-Pena y colaboradores (2003)28 reportaron su aplicación en Brasil para el estudio de aneuploidías en abortos espontáneos. En Costa Rica, hasta la fecha no se cuenta con el apoyo de las técnicas moleculares para el diagnóstico de aneuploidías fetales, por lo que la introducción de una técnica como la QF-PCR, con todas las cualidades descritas, tendría un impacto muy positivo en la detección de cromosomopatías. Por lo anterior, el objetivo de este estudio es implementar la técnica QF-PCR para el diagnóstico prenatal de cromosomopatías, de manera que sea una herramienta molecular complementaria del análisis citogenético convencional.
Materiales y métodos
Este fue un estudio prospectivo realizado desde enero de 2006 hasta marzo de 2008, de las muestras que llegaron al INISA para que se les realizara un análisis cromosómico. Se colectó un total de 93 muestras: 88 de líquido amniótico, entre las semanas 15 y 37 de gestación, y 5 de sangre fetal por cordocentesis, entre las semanas 18 y 35 de gestación. Estas muestras provinieron de hospitales estatales (n=77) o de consulta privada (n=16), con la solicitud de determinar el cariotipo fetal, por considerarse un embarazo de alto riesgo de cromosomopatía. La mayoría de las veces la razón de referencia fue ecografía anormal, seguida por la edad materna avanzada. Para todas las muestras se realizó la QFPCR, así como el análisis cromosómico, considerado como el patrón de referencia. De cada una de las muestras se tomó una pequeña alícuota para realizar la extracción de ADN, y el resto se procesó para su análisis citogenético convencional. Se diseñaron tres PCRs multiplex para amplificar cuatro STRs ubicados en diferentes loci de cada uno de los cromosomas 21, 18 y 13. Del par de iniciadores, uno estaba marcado con una molécula fluorescente distinta para permitir la visualización de los productos, los cuales fueron analizados en los secuenciadores genéticos ABI 310 y ABI 3130, ubicados en otros centros de investigación de la Universidad de Costa Rica. El análisis de los fragmentos se efectuó con los softwares Genescan Analysis y Peak Scanner. Para interpretar un resultado como normal o anormal, al menos tres de los marcadores debían mostrar patrones alélicos consistentes con un genotipo disómico o trisómico, respectivamente. El cultivo celular y el análisis citogenético se realizaron según los procedimientos normalizados y validados, utilizados de rutina en el laboratorio. La comparación de los resultados de la QF-PCR con los del cariotipo permitió evaluar el desempeño de la QF-PCR.
Resultados
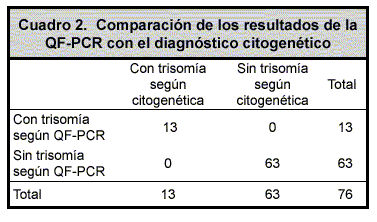
Se pudo obtener el cariotipo en el 72% de las muestras. En el 28% restante fue imposible, debido al fracaso en el cultivo o a la ausencia de figuras mitóticas analizables. La extracción de ADN y QF-PCR se pudo realizar en el 82% de las muestras. Se logró procesar al análisis de STRs en el 73% de las muestras en las que no se pudo efectuar el cultivo celular (Cuadro 1). Fue posible comparar 76 parejas de datos (QF-PCR-cariotipo) y se identificaron correctamente todas las aneuploidías de los cromosomas 21 (n=8) y 18 (n=5), sin falsos positivos ni falsos negativos, así como a todos los individuos sin cromosomopatía (Cuadro 2). Para este grupo de datos, la sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo de la QF-PCR, fueron del 100%. Fue posible la obtención de los resultados dos días después de la llegada de la muestra al laboratorio, y en casos excepcionales podían durar hasta 10 días.
Discusión
]]> Para el estudio no se pudo obtener el cariotipo por métodos convencionales en el 28% de los líquidos amnióticos. Esta imposibilidad de lograr el cariotipo en cifras superiores al 20% de los cultivos de amniocitos recibidos en cerca de 2 años en el INISA (desde 2006 hasta los primeros tres meses de 2008), ya ha sido reportada con anterioridad1, 4, 29, 30 y se ha mantenido constante. Uno de los factores que contribuye en gran medida con esta tasa alta de fracaso en el cultivo celular, es el hecho de que en el INISA no se rechazan muestras de mala calidad (con contaminación hemática o edad gestacional avanzada) o en cantidad insuficiente, a pesar de que se ha demostrado que tienen pocas posibilidades de crecimiento exitoso.30En el contexto del diagnóstico prenatal, las estimaciones tan altas de los valores predictivos son de mucha utilidad para el médico que atiende a una gestante a quien se le realizó una prueba invasiva. El conocimiento de la trisomía fetal diagnosticada por la amnio-PCR, con el respaldo de un valor predictivo positivo del 100%, podría evitar la necesidad de una segunda amniocentesis, y con ello evitar el riesgo de una otra punción, tanto para la madre como para el feto. De igual manera, con un valor predictivo negativo del 100%, la QF-PCR podría adelantar el diagnóstico a la gestante de que su hijo está libre de trisomía, lo cual podría disminuir la ansiedad en la futura madre, mientras espera el resultado definitivo del cariotipo completo. Asimismo, podría brindar la información necesaria para valorar la realización de una cirugía fetal.
Es muy importante destacar el hecho de que en varios casos fue posible obtener el diagnóstico rápido de la QFPCR, incluso hasta dos días después de la llegada de la muestra al laboratorio. Esto es un tiempo menor comparado con los 16 días requeridos, en promedio, para el resultado del cultivo de amniocitos31. En muchos casos este lapso de espera es de gran ansiedad para la madre, principalmente si hay sospechas de Síndrome de Down, por lo que sería muy beneficioso contar con métodos más rápidos para obtener los resultados.
El diagnóstico rápido y fiable que brinda la QF-PCR es valioso en casos urgentes, de los que dependan intervenciones médicas importantes, tales como cirugías fetales, o la decisión de terminar el embarazo por cromosomopatía. En países donde el aborto selectivo es permitido, el diagnóstico de trisomía fetal mediante QF-PCR que indique trisomía fetal, se considera razón suficiente para realizar el aborto, sin necesidad de esperar el resultado del análisis cromosómico. Esto es particularmente útil en los casos que están por cumplir el límite de edad gestacional permitido para abortar (usualmente 20 semanas).32 Lo anterior no implica que no se necesite efectuar el análisis citogenético completo, aunque se haya optado por terminar el embarazo, ya que la información del cariotipo puede ser de utilidad para ofrecer asesoría genética a los padres. Cabe resaltar que, por motivos legales, el aborto selectivo no es una opción para las costarricenses.
En conclusión, los resultados del presente estudio confirman que la QF-PCR es una metodología fiable, rápida, fácil de realizar y analizar, y que puede convertirse en un excelente complemento del análisis citogenético, por lo que su introducción al servicio de diagnóstico cromosómico del país, podría ser una realidad en poco tiempo.
Agradecimientos.
A Vincenzo Cirigliano, de General Lab, Barcelona, por la capacitación brindada y revisión de resultados; al personal de la Unidad de Medicina Materno-fetal del Hospital Dr. Rafael Angel Calderón Guardia, en particular al perinatólogo Kay Sander Mangel y a la enfermera Paula Obando Murillo, por su excelente apoyo logístico; al Ministerio de Ciencia y Tecnología, por el aporte económico brindado a esta investigación.
Recibido: 11 de noviembre de 2008 Aceptado: 28 de julio de 2009
Referencias
]]>1. Castro-Volio I, Sander K, Vargas M, Sánchez L, Escalante G. Cariotipos fetales en embarazos de alto riesgo genético provenientes de hospitales de la seguridad social y de la consulta privada, de 1993 a 1998. Acta méd costarric 2000; 2: 25-30. [ Links ]
2. Wolfe K, Herrington C. Interphase cytogenetics and pathology: a tool for diagnosis and research. J Pathol 1997; 181:359–61. [ Links ]
3. Pergament E. New molecular techniques for chromosome analysis. Clin Obstetr Gynecol. 2000; 14: 677-690. [ Links ]
4. Wachtel S, Tharapel A. FISH and PRINS: competing or complementary technologies? Am J Med Genet. 2002; 107: 97–98 [ Links ]
5. Findlay I, Matthews P, Toth T, Quirke P. Same day diagnosis of Down’s syndrome and sex in single cells using multiplex fluorescent PCR. J Clin Pathol Mol Pathol. 1998; 51:164–167 [ Links ]
6. Pertl B, Kopp S, Kroisel PM, Häusler M, Sherlock J, Winter R et al. Quantitative fluorescence polymerase chain reaction for the rapid prenatal detection of common aneuploidies and fetal sex. Am J Obstet Gynecol. 1997; 177:899-906. [ Links ]
7. Verma L, Mcdonald F, Leedham P, McConachie M, Dhanjal S, Hulten M. Rapid and simple prenatal DNA diagnosis of Down’s syndrome. Lancet. 1998; 352:9–12. [ Links ]
8. Levett L, Liddle S, Meredith J. A large-scale evaluation of amnio-PCR for the rapid prenatal diagnosis of fetal trisomy. Ultrasound Obstet Gynecol. 2001; 17:115–8. [ Links ]
9. Leung W, Lau E, Lao T, Tang M. Can Amnio–polymerase chain reaction alone replace conventional cytogenetic study for women with positive biochemical screening for fetal Down syndrome? Obstet. Gynecol. 2003; 101: 856-861. [ Links ]
10. Nicolini U, Lalatta F, Natacci F, Curcio C, Bui T. The introduction of QF-PCR in prenatal diagnosis of fetal aneuploidies: time for reconsideration. Hum Reprod Up. 2004; 10: 541-548. [ Links ]
11. Ochshorn Y, Bar-Shira A, Jonish A, Yaron Y. Rapid prenatal diagnosis of aneuploidy for chromosomes 21, 18, 13, and X by quantitative fluorescent polymerase chain reaction. Fetal Diagn Ther 2006; 21:326–331. [ Links ]
12. Mann K, Ogilvie C, Donaghue C, Mountford T, Mcanulty C, Warner I et al. QF-PCR for the diagnosis of aneuploidy. ACC Best practice Guidelines. Association for Clinical Cytogenetics. General Best Practice Guidelines. British Society for Human Genetics. En: www.cytogenetics.org.uk/info/ACC_QF-PCR Consultado el 10 de octubre de 2006. [ Links ]
13. Chen C, Chern S, Wang W. Rapid determination of zygosity and common aneuploidies from amniotic fluid cells using quantitative fluorescent polymerase chain reaction following genetic amniocentesis in multiple pregnancies. Hum Reprod. 2000; 5: 929-934. [ Links ]
14. Cirigliano V, Camadas P, Plaja A, Ordóñez E, Mediano C, Sánchez C et al. Rapid prenatal diagnosis of aneuploidías and zigosity in multiple pregnancies by amniocetesis with single insertion of the needle and quantitative fluorescent PCR. Prenat Diagn. 2003; 23: 629-633. [ Links ]
15. Valero R, Marfany A, Gil-Benso R, Ibáñez M, López-Pajares I, Prieto F et al. Molecular characterization of partial chromosome 21 aneuploidies by fluorescent PCR. J Med Genet. 1999; 36: 694-697. [ Links ]
16. Diego D, García M, Trujillo M, González C, Rodríguez de Alba M, Ayuso C et al. Application of quantitative fluorescent PCR with short tandem repeat markers to the study of aneuploidies in spontaneous miscarriages. Hum Reprod. 2005; 20:1235-1243. [ Links ]
17. Machatkova M, Brouckova A, Matejckova M, Krebsova A, Sperling K, Vorsanova S et al. QF-PCR examination of parental and meiotic origin of trisomy 21 in Central and Eastern Europe. J Histochem & Cytochem. 2005; 53: 371–373. [ Links ]
18. Pertl B, Kopp S, Kroisel P, Tului L , Brambati T, Adinolfi M. Rapid detection of chromosome aneuploidies by quantitative fluorescence PCR: first application on 247 chorionic villus samples. J Med Genet. 1999; 36:300–303. [ Links ]
19. Schmidt W, Jenderny J, Hecher K,Hackeloer B, Kerber S, Kochan L et al. Detection of aneuploidy inchromosomes X, Y, 13, 18 and 21 by QF-PCR in 662 selected pregnancies at risk. Mol. Hum. Reprod. 2000; 6: 855-860. [ Links ]
20. Cirigliano V, Ejarque M, Cañadas M, Lloveras E, Plaja A, Pérez A et al. Clinical application of multiplex quantitative fluorescent polymerase chain reaction (QF-PCR) for the rapid prenatal detection of common chromosome aneuploidías. Mol Hum Reprod. 2001; 7: 1001-6. [ Links ]
21. Cirigliano V, Voglino G, Camadas P, Marongiu A, Ejarque A, Ordóñez E et al. Rapid prenatal diagnosis of common chromosome aneuploidies by QF-PCR. Assesment on 18 000 consecutive clinical samples. Mol Hum Reprod. 2004. 10: 839-446. [ Links ]
22. Mann K, Fox S, Abbs S, Yau A, Scriven P, Docherty S et al. Development and implementation of a new rapid aneuploidy diagnostic service within the UK National Health Service and implications for the future of prenatal diagnosis. Lancet. 2001 358: 1057-61. [ Links ]
23. Ghosh S, Dey S. DNA Diagnosis of Down syndrome using polymerase chain reaction and polymorphic microsatellite markers. Int J Hum Genet. 2003; 3:17-20. [ Links ]
24. Lee M, Ryu H, Kim D, Lee B, Cho E, Yang E et al. Rapid prenatal diagnosis of Down syndrome using quantitative fluorescent PCR in uncultured amniocytes. J Korean Med Sci. 2004; 19: 341-4 [ Links ]
25. Fang Z, Xin X, Yuan-Zhen Z, Xiao-bo S, Jian-hong P, Chun-Hong W et al. Rapid prenatal diagnosis of trisomy 21 by fluorescent quantitative multiplex polymerase chain reaction. Chin Med J. 2006; 119: 514-51 [ Links ]
26. Brown L, Abigania M, Warburton D, Brown S. Validation of QF-PCR for prenatal aneuploidy screening in the United States. Prenat. Diagn 2006; 26: 1068-74 [ Links ]
27. Primost I, Mincman J, García P, Coco I, Gismondi F, Neuspiller N et al. Determinación de aneuploidías por PCR fluorescente. Reproducción. 2007; 22: 69-86 [ Links ]
28. Junho S, Belo H, Fontoura E, Sturzeneker R. Investigação genética dos abortamentos espontâneos pelo DNA. Rev Med Minas Gerais 2003; 13: 164-73 [ Links ]
29. Castro-Volio I, Escalante G, Mora H, Guerra D, Sánchez L, Peña C. Cariotipo de células fetales en el diagnóstico prenatal en Costa Rica. Rev Biol Trop 1995; 43(1-3): 31-37 [ Links ]
30. Castro-Volio I, Sander K, Vargas M, Sánchez L, Escalante G. Diagnóstico prenatal citogenético mediante amniocentesis durante los trimestres II y III de gestación en Costa Rica. Rev Biol Trop 2001; 49(3-4): 1227-1236 [ Links ]
31. Castro-Volio I, Ortiz F. Cariotipos fetales mediante amniocentesis y cordocentesis en Costa Rica. Perinatol Reprod Hum. 2004;18: 187-198 [ Links ]
32. Pertl B, Pieber D, Lercher A, Orescovic E, Haeusier M, Winter R et al. Rapid prenatal diagnosis of aneuploidy by quantitative fluorescent PCR on fetal samples from mothers at high risk for chromosome disorders. Mol Hum Reprod. 1999; 5: 1176-79. [ Links ]
1 Instituto de Investigaciones en Salud (INISA), Universidad de Costa Rica
Correspondencia: Isabel Castro-Volio Apartado postal 2060 San Pedro. Email: isabel.castro@ucr.ac.cr
Fuentes de apoyo: Proyecto VAS-ED-323 de la Universidad de Costa Rica, Ministerio de Ciencia y Tecnología.
Abreviaturas: PCR, reacción en cadena de la polimerasa. QF-PCR, reacción en cadena de la polimerasa cuantitativa fluorescente. STRs, short tandem repeats o repeticiones cortas en tándem. FISH, hibridación in situ con fluorescencia.
]]>