Concepto de equivalencia sustancial aplicado alimentos derivados de cultivos
genéticamente mejorados
The concept of substantial equivalence as applied to foodstuffs derived from
genetically-modified crops
PhD María Eugenia Villalobos Hernández1,
PhD Ana Mercedes Espinoza Esquivel2,3
1 Ministerio de Salud, (506) 22 33 95 16, correo electrónico: mevillalo@gmail.com ]]>
2 Universidad de Costa Rica, Centro de Investigación Biología Celular y Molecular (CIBCM), San Pedro de Montes de Oca, Costa Rica.
3 Universidad Costa Rica, Facultad Ciencias Agroalimentarias, Escuela Agronomía, San Pedro de Montes de Oca, Costa Rica.
Recibido: 10/9/07 Revisado: 6/5/08 Aprobado: 25/6/08
Resumen
El objetivo del presente artículo es describir la aplicación del concepto de equivalencia sustancial, el cual es utilizado y aceptado internacionalmente para realizar la evaluación de la inocuidad de un alimento nuevo derivado de cultivos genéticamente mejorados. La metodología utilizada fue revisión de literatura actualizada, considerando, información tanto de revistas nacionales como internacionales y documentos de la Organización Mundial para la Agricultura y la Alimentación (FAO), Organización Mundial de la Salud (OMS), Codex Alimentarius, Organización Económica de Cooperación y Desarrollo (OECD), la Food and Drug Administration, (FDA) y otras. El artículo presenta la tendencia mundial en la siembra de cultivos genéticamente mejorados, así como la situación actual en Costa Rica con respecto a la siembra de cultivos genéticamente mejorados para incremento de semilla. Además, se detalla el concepto de equivalencia sustancial y se describe el conjunto de características de calidad que se deben evaluar los procedimientos metodológicos a seguir para demostrar que un alimento, derivado de un cultivo genéticamente mejorado (adCGM), es seguro para el consumo humano y animal. Como conclusión el concepto de equivalencia sustancial es el grupo de técnicas y metodologías, vigentes y aceptadas internacionalmente para evaluar la inocuidad de un nuevo alimento desarrollado mediante biotecnología moderna.
Palabras claves: alimentos derivados de cultivos genéticamente mejorados, equivalencia sustancial, biotecnología moderna, desregulación de alimentos, Costa Rica.
Abstract
The objective of this article is to describe the complete application of the concept of substantial equivalence, which is internationally accepted and widely used for food safety evaluation of new foods. The methodology consists of a literature review of current documents from several agencies such as the World Health Organization (WHO), Food and Agriculture Organization of the United Nations (FAO), Organization for Economic Cooperation and Development (OECD), the Food and Drug Administration of the USA (FDA), and others. This article presents the global trends related to the planting of genetically modified crops, and the Costa Rican situation on planting genetically modified crops for increasing seed yield. The article introduces the concept of substantial equivalence, and discusses several tests that should be applied in order to demonstrate that a genetically modified food derived from a GM crop is safe for human and animal consumption. As conclusion, the concept of substantial equivalence is the internationally
and currently accepted criteria the food safety assessment of crops developed by modern biotechnology.
Key words: genetically modified crop-derived foods, substantial equivalence, modern biotechnology, food deregulation, Costa Rica.
]]> IntroducciónEn el mundo se reporta una tendencia al aumento en las áreas de siembra de cultivos genéticamente mejorados (CGM), conocidos también como transgénicos, y que han sido desregulados, mediante el concepto de equivalencia sustancial. Acorde con James (13) se suman 11 años de cultivar CGM en el mundo y con ello un importante consumo humano de alimentos derivados de cultivos genéticamente mejorados (adCGM).
En general se reporta que en el año 2006 10.3 millones de agricultores (90% de escasos recursos) en 22 países sembraron 102 millones de hectáreas de CGM, lo que refleja un incremento en sesenta veces el área sembrada por primera vez en 1996. Los Estados Unidos, Argentina, Brasil, Canadá y China son los principales productores en el mundo de CGM, donde la soya es el cultivo más sembrado (12,13). También, la Organización Mundial de la Salud (18), menciona que los CGM cubren alrededor del 4% de de la tierra cultivable total del mundo.
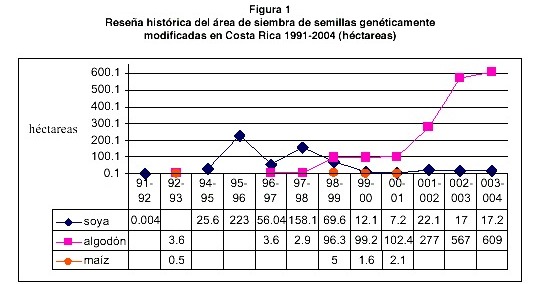
En Costa Rica se reportan desde 1991, siembras de CGM únicamente para incremento de semilla en la época de invierno del hemisferio norte. En la en la figura 1 se muestra las hectáreas sembradas y el tipo de semilla cultivada. También, existen proyectos de investigación con pruebas de campo controladas y todas estas siembras son autorizadas por el Programa de Biotecnología del Ministerio de Agricultura y Ganadería. A la fecha no se han reportado autorizaciones para el consumo y la comercialización de alimentos mejorados genéticamente desarrollados en el país (1, 20, 21).
Para que un cultivo genéticamente mejorado sea desregulado, debe someterse a consideración ante las autoridades regulatorias nacionales competentes, principalmente las correspondientes al Ministerio de Agricultura y Ganadería y al Ministerio de Salud. De manera que debe reunirse toda la información de los estudios de equivalencia sustancial y toda la información científica disponible, que se presenta en un dossier. También, se puede solicitar la desregulación en varios países suministrando la documentación científica que cada país requiera; sin embargo, la tendencia es reconocer el criterio del país que liberó el nuevo cultivo y se acepta su uso (19, 17).
]]> Para determinar la equivalencia sustancial, se considera que este concepto es un punto de inicio que permite la comparación entre el adCGM con su par convencional, y también permite identificar las diferencias intencionadas y no intencionadas, en las cuales se requiere hacer mayor énfasis en la evaluación del nuevo CGM. Por lo tanto, existen tres posibilidades de conclusiones después de aplicar el concepto de equivalencia sustancial (14, 16):- Primero: hay equivalencia sustancial cuando el adCGM no presenta diferencias importantes en el contenido nutricional, toxicológico o alergénico con respecto a su par convencional.
- Segundo: pueden ser equivalentes en todo, excepto en las diferencias definidas por la modificación genética a que fue sometido el nuevo producto; para ello se debe evaluar las implicaciones de esas diferencias.
- Tercero: no hay equivalencia sustancial con respecto al par convencional, y el nuevo OGM debe ser evaluado en más detalle.
Con toda la información analizada y sistematizada, es que se puede hacer alguna de las conclusiones mencionadas. Es por ello que el concepto de equivalencia sustancial debe ser considerado como una herramienta para aplicar procedimientos en la inocuidad de los nuevos alimentos y no como el criterio de evaluación de la inocuidad o seguridad de los alimentos.
El presente artículo tiene el objetivo de describir el concepto de equivalencia sustancial, que consiste en la aplicación de una serie de pruebas y procedimientos metodológicos, recomendados por organismos internacionales para la evaluación de la inocuidad del
nuevo adCGM y demostrar que es seguro para el consumo humano y animal. Con la información de los resultados de la aplicación del concepto equivalencia sustancial, las autoridades regulatorias en salud pública pueden tomar decisiones para autorizar o
rechazar su comercialización para el consumo humano o animal. (3, 6).
Materiales y métodos
Se realizó una revisión bibliográfica donde se reporta el concepto de equivalencia sustancial y su importancia para la desregulación de alimentos derivados de cultivos genéticamente mejorados (adCGM). Para ello se procedió a la búsqueda de artículos científicos publicados recientemente sobre el tema, tanto de revistas nacionales como internacionales, considerando como documentos principales los de la Organización Mundial para la Agricultura y la Alimentación (FAO), Organización Mundial de la Salud (OMS), Codex Alimentarius, Organización Económica de Cooperación y Desarrollo (OECD) y otra literatura.
]]> Resultados y discusiónLa calidad alimentaria se determina por múltiples criterios, pero principalmente es el ser humano quien la determina con su aceptación y consumo. Algunos criterios de calidad son:
- cualidades sensoriales, tóxicas y alergénicas de los alimentos, determinados mediante estudios sensoriales, organolépticos;
- valor nutritivo, valorado mediante tablas de composición de los alimentos o el análisis químico del contenido de nutrientes;
- condiciones higiénicas, reflejado por la inocuidad del alimento, es decir ausencia de microorganismos patógenos al humano; y
- de servicio, se refiere a las posibilidades de conservación, estabilidad del producto y el tiempo que se mantiene sin alteraciones (2).
El concepto de equivalencia sustancial se refiere a la comparación de los alimentos mejorados genéticamente con su contraparte convencional, para identificar diferencias inesperadas o no intencionadas, ocurridas durante el proceso de la modificación genética.
El concepto se aplica caso por caso y de forma simultánea, al alimento mejorado y a su par convencional. Se somete a las pruebas, desde el momento de su cultivo, para comparar comportamiento agronómico, hasta las pruebas de laboratorio con estudios aceptables que demuestren la inocuidad del alimento nuevo, su uso específico, la seguridad en el ambiente y en la salud humana. Para ello se contempla aspectos agronómicos, genéticos y químicos; y sólo cuando el producto se considera seguro recibe aprobación para su comercialización (6, 14,18).
En el caso de adCGM estas características de calidad deben ser las mismas que presenta el alimento de referencia que le dio origen o también llamado par convencional. Por ello OECD, FAO, OMS y Food and Drug Administration de los Estados Unidos (FDA), así como otros organismos internacionales, han propuesto el concepto de equivalencia sustancial para su aplicación en las pruebas a que todo adCGM debe someterse, previo a ser liberado al mercado. Es claro que este concepto debe aplicarse a cada alimento, caso por caso, tomando en consideración el tipo de modificación introducida (3, 5, 7, 14).
El concepto de equivalencia sustancial presenta limitaciones, ya que, omite estudios más profundos de los efectos no esperados que los adCGM puedan producir en el consumidor, en especial las posibles consecuencias en personas susceptibles a componentes alergénicos y en el largo plazo (4, 8, 9,10).
]]> En reuniones de expertos organizadas por la FAO/OMS, se revisaron las técnicas actuales utilizadas para la evaluación de alimentos derivados de la biotecnología y se concluyó que hay nuevas técnicas en proceso de validación, pero que aún no son contundentes; por lo tanto el concepto de equivalencia sustancial continua siendo el parámetro para evaluar los adCGM (3, 6, 11, 14, 15, 18).Con esta base, los procedimientos metodológicos incluidos en el concepto de equivalencia sustancial, se describen de forma resumida a continuación (3,6):
a. Identificación del alimento mejorado
- Recopilación de información de las características de la modificación genética realizada en el alimento.
- Descripción de la función y propiedades del gen o genes insertados y que lo diferencian del convencional.
b. Fuente del factor modificado
- Recopilación y descripción del organismo de origen del gen introducido: clasificación taxonómica, nombre científico, relación con otros organismos, historia de su uso como alimento, historia de la producción de toxinas, factores alergénicos, inocuidad, presencia de factores antinutricionales, presencia de sustancias activas fisiológicamente tanto en la especie del alimento fuente como de especies cercanas; y presencia de nutrientes asociados con la especie de origen.
c. Procesos de transformación genética
- Descripción de los métodos de transformación utilizados en la modificación genética, vector del gen, descripción de las secuencias de ADN, promotores y su fuente.
d. Características fenotípicas del alimento convencional y del mejorado
]]> - Descripción de la morfología, crecimiento, rendimiento, resistencia a enfermedades, y otras.e. Composición del alimento convencional y del mejorado
- Determinación de la composición química del alimento convencional y el mejorado.
- Determinación de componentes tóxicos conocidos que están presentes y que pueden afectar la salud humana, así como aquellos factores tóxicos que pueden haber sido expresados por la inserción del gen en el genoma del alimento.
- Determinación de la presencia de microorganismos patógenos en iguales condiciones de manejo poscosecha.
f. Expresión de la proteína producto del gen insertado
- Determinación de la seguridad de la proteína expresada en el alimento mejorado, estructura, función, especificidad, potencial alergénico.
- Análisis de la estructura del ADN insertado, valoración de su potencial de transferencia horizontal.
- Determinación de factores inesperados en la expresión proteica.
- Determinación de características microbiológicas y de apariencia física durante el proceso de almacenamiento industrial y en el hogar.
- Determinación de características físicas durante el proceso de cocción.
- Evaluación de las características organolépticas de ambos alimentos convencional y mejorado.
- Valoración del potencial alergénico en el consumidor.
h. Consumo potencial e impacto dietético de la introducción de alimentos mejorados genéticamente
- Valoración de la aceptación del alimento genéticamente mejorado, por los consumidores.
- Determinación del tipo de consumidor, ante la oferta de estos nuevos alimentos en el mercado.
- Valoración de las implicaciones dietéticas y nutricionales en la población por la oferta de este tipo de alimento.
i. Determinación de la equivalencia sustancial
]]> - Se determina al comparar los resultados obtenidos en las diferentes pruebas aplicadas, tanto al alimento convencional, como del genéticamente mejorado.Conclusiones
A lo largo de los 11 años de siembra de cultivos genéticamente mejorados, se observa una tendencia mundial de incremento en las áreas de siembra de cultivo y en el número de países que los siembran, lo que incluye cultivos para uso industrial, alimentación animal y consumo humano. Todos esos cultivos GM han sido evaluados para demostrar que no presentan efectos nocivos al ambiente, al suelo, a los animales y a los humanos. Dicha evaluación se realiza con la aplicación del concepto de equivalencia sustancial, reconocido por autoridades regulatorias de todo el mundo.
El concepto de equivalencia sustancial involucra múltiples y diversas pruebas que incluyen desde la descripción detallada del origen y tipo de gen introducido en el nuevo alimento, características agronómicas, hasta las implicaciones en la dieta por la disponibilidad del nuevo alimento. Las pruebas deben ser realizadas por laboratorios reconocidos, utilizando técnicas conocidas y aceptadas internacionalmente, se deben aplicar caso por caso y de forma simultánea tanto al producto original, como al genéticamente mejorado, para verificar la equivalencia entre ambos.
La información científica que genera la aplicación del concepto de equivalencia sustancial es una herramienta útil para las autoridades en salud y facilita el proceso de análisis sobre la calidad agronómica, inocuidad y características nutricionales que todo alimento genéticamente mejorado debe demostrar antes de su aprobación para ser desregulado y consumido por el ser humano.
Bibliografía
1. Cabrera, J. 2004. Informe sobre el Marco Regulatorio Nacional en Materia de Biotecnología y Bioseguridad. Proyecto UNEP-GEF Desarrollo de un Marco Nacional en Bioseguridad para Costa Rica. San José Costa Rica. [ Links ]
2. Cervera, P.; Clapes, J.; Rigolfas, R. 1993. Alimentación y dietoterapia. 2da. Edición. Interamericana-McGraw-Hill, Madrid. p. 88-91. [ Links ]
3. CODEX ALIMENTARIUS COMMISSION, 2003. Reprot of the third session of the CODEX AD HOC Intergovernamental Task Force on Foods Deived from Biotechnology. ALINORM 03/34. Joint FAO/WHO Food Standard Programme. Rome Italy. [ Links ]
4. Dommefen, A. Van. 1999. Scientific requirements for the assessment of food safety. Biotechnology and Development Monitor 38:3-7. [ Links ]
5. FAO (FOOD AND AGRICULTURE ORGANIZATION OF UNITED NATIONS); 1996. Biotechnology and food safety. Report of a joint FAO/WHO consultation FAO Food and Nutrition Paper 61. Rome. [ Links ]
6. FAO (FOOD AND AGRICULTURE ORGANIZATION OF UNITED NATIONS); WHO (WORLD HEALTH ORGANIZATION); 2000. Safety aspects of genetically modified foods of plant origin. Report of a joint FAO/WHO Expert consultation on foods derived from biotechnology. Geneva, Switzerland, 29 May- 2 June. 36 p. [ Links ]
7. FDA (U. S. FOOD AND DRUG ADMINISTRATION) 1996. Safety assurance of foods derived by modern biotechnology in the United States. Center for Food Safety and Applied Nutrition. Disponible en: htt://vm.cfsan.fda.gov/ [ Links ]
8. Goodman R.; Hefle S.; Taylor S.; van Ree R.; 2005, Assesing genetically modified crops to minimize the risk of increased food allergy: a review. Int Arch Allergy Immunol 137:153-166. [ Links ]
9. Goodman R.; Hefle S.; 2005, Gainning perspective on the allergenicity assessment of genetically modified food crops. Expert Rev. Clin. Inmunol. 1(4):561-578. [ Links ]
10. ILSI (INTERNATIONAL LIFE SCIENCES INSTITUTE) 2000. Scientific program session #4: (ILSI North America) Biotechnology and health. Disponible en: http://www.ilsi.org/newsletter18/page17.html [ Links ]
11. Haslberger, A., 2003. GM Food: The risk assessment of immune hypersensitivity reactions covers more than allergenicity. Food, Agriculture & Environment 1(1):42-45. [ Links ]
12. James, 2005. Global Status of Commercialized Biotech/ GM Crops:2005. ISAAA Briefs #34 ISAAA: Ithaca NY. Consultado el 28 enero 2007. Disponible en: http://www.isaaa.org [ Links ]
13. James, 2006. Global Status of Commercialized Biotech/GM Crops:2006. ISAAA Briefs #35 ISAAA: Ithaca NY. Consultado el 28 enero 2007. Disponible en: http://www.isaaa.org [ Links ]
14. Nordic Council, 2000. Safety assessment of novel food plants. Chemical analytical approaches to the establishment of substantial equivalence. TemaNord 1998:591. Nordic Council of Ministers, Copenhagen. [ Links ]
15. Kuiper, H. 2000. Topic 5: Profiling techniques to identify differences between foods derived from biotechnology and their counterparts. Report of a joint FAO/WHO Expert consultation on foods derived from biotechnology. Geneva, Switzerland, 29 May- 2 June. 11 p. [ Links ]
16. Kuiper H., Kleter G., Noteborn H., Kok E. 2001. Assessment of the food safety issues related to genetically modified foods. The plant journal 27(6):503-528. [ Links ]
17. OECD, 2005. An introduction to the biosafety consensus documents of OECD´s working group for harmonization in biotechnology. Series on harmonization oversight in biotechnology No. 32 . France. 19 pp. [ Links ]
18. OMS (Organizacion Mundial de la Salud), 2005. Biotecnología moderna de los alimentos, salud y desarrollo humano: estudio basado en evidencias. Departamento de Inocuidad Alimentaria. Ginebra, Suiza. 84 p. [ Links ]
19. Schauzu M., 2000. The concept of substantial equivalence in safety assessment of foods derived from genetically modified organisms. AgbiotechNet ABN 044 2 (april):1-4. [ Links ]
20. UNEP-GEF, 2004. Situación actual de organismos vivos mejorados resultantes de la biotecnología moderna en Costa Rica, Desarrollo marco nacional en bioseguridad, San José Costa Rica, 52 pag. [ Links ]
21. Valdez M., López R., Jiménez R., 2004. Estado Actual de la Biotecnología en Costa Rica. Revista Biología Tropical 52(3):73-743. [ Links ] ]]>