Efecto de la vacunación anti-leptospira en bovinos lecheros sobre la producción de anticuerpos anti-leptospira en trabajadores de lecherías de cuatro zonas de Costa Rica
Rafael González1
Louise Maranda2
Juan José Romero3*
1 Ministerio de Salud. Costa Rica.
2 Department of Environmental and Population Health International ᆳcine. Massachussets. USA.
3 Programa de Investigación en Medicina Poblacional. Universidad Nacional. Costa Rica.
* Autor para correspondencia Teléfono (506) 260 - 2155. Fax: (506) 260 - 2155. P.O. Box: 304-3000, Heredia. Costa Rica. E-mail: jromero@medvet.una.ac.cr
Resumen
]]> Objetivo: Este estudio experimental midió el efecto indirecto de la vacuna anti-Leptospira Leptoferm-5® (Pfizer®) en la producción de anticuerpos anti-Leptospira en trabajadores de lecherías de cuatro zonas lecheras de Costa Rica. Materiales y Métodos: Tomaron parte en el estudio 171 vaqueros, 94 en el grupo tratamiento y 77 en el grupo control. A cada vaquero se le tomó una muestra sanguínea en tres diferentes momentos durante un año: la primera, antes de aplicar la vacuna en los animales, la segunda a los 6 meses y la tercera un año después de la primera vacunación. Se utilizó la técnica de micro aglutinación para la detección de anticuerpos anti-Leptospira interrogans serovares pomona, hardjo, canícola y grippotyphosa en el laboratorio del INCIENSA. Se utilizó la razón de prevalencias y el riesgo relativo para determinar si existió asociación entre la vacunación anti-Leptospira a las vacas y la seropositividad en los vaqueros. Resultados: En los tres muestreos se obtuvo un 10.27% (50/487) de muestras positivas a cualquiera de los serovares de Leptospira interrogans a los que fueron analizados. Tanto en el grupo tratamiento como en el control se observaron cambios en la seropositividad entre los distintos muestreos, con un aumento entre el primer y segundo muestreo (p < 0.05); así como una disminución entre el segundo y el tercer muestreo (p < 0.05), mientras que entre el primer y el tercer muestreo no hubo diferencias en ningún grupo. En ninguno de los tres muestreos hubo asociación significativa entre la vacunación de las vacas y el porcentaje de vaqueros se-ropositivos. Conclusión: La aplicación de la vacuna anti-Leptospira al ganado no tiene efecto sobre los niveles de anticuerpos anti-Leptospira que presentan los vaqueros para los serovares analizados en este estudio.Palabras clave: leptospirosis, anticuerpos, vacunación, Costa Rica, trabajadores de lechería.
Abstract
Objective: This experimental study assessed the indirect effect of the anti-Leptospira vaccine Leptoferm-5® (Pfizer®) regarding the production of anti-Leptospira antibodies in dairymen from four dairy areas in Costa Rica. Materials and Methods: 171 dairymen took part in the study; 94 in the treatment group and 77 in the control group. Three blood samples were taken from each worker three times throughout a year period: before the vaccination of the animals, and six and twelve months after the initial vaccination. The microscopic agglutination test (MAT) was used to detect anti-Leptospira interrogans antibodies, specifically towards pomona, hardjo, canicola and grippotyphosa serovars. All samples were assayed in the laboratory of Instituto Costarricense de Investigación y Educación en Nutrición y Salud (INCIENSA: Costa Rican Institute of Investigation and Education in Nutrition and Health). The prevalence ratio and the relative risk were used to determine whether or not the anti-Leptospira vaccination in cattle has association with the seropositivity of dairymen. Results: The global amount of seropositive samples to any Leptospira interrogans serovars in the three samplings was 10.27% (50/487). Changes in seropositivity for both treated and control groups of the three samplings were observed; thus, there was an increase between the first and second sampling (p< 0.05), and a decrease between the second and third samplings in both groups (p < 0.05); whereas, between the first and third sampling there was no difference. Finally, the vaccination of the cattle and the percentage of seropositive dairymen to Leptospira interrogans did not show association. Conclusion: The vaccination of cattle with anti-Leptospira did not have an effect on the anti-Leptospira antibody titers of the dairymen for the serovars analyzed in this study.
Keywords: leptospirosis, vaccination, antibodies, Costa Rica, dairymen.
Introducción
La leptospirosis es una enfermedad zoonótica con amplia distribución mundial, producida por bacterias de la especie Leptospira interrogans; más común en climas húmedos y cálidos de las regiones tropicales en zonas urbanas y rurales.1 Los agentes causales son las leptospiras, bacterias que pertenecen al orden Spirochaetales.2-4 Se reconocen dos especies, Leptospira interrogans a la que pertenecen las Leptospiras patógenas y L. biflexa que son de vida libre.5 La L. interrogans es la de interés como agente zoonótico y se ha subdividido en serovares de los que se conocen más de 200, agrupadas en 23 serogrupos según similitudes serológicas y de aglutinación.3, 4
La presentación de la enfermedad en las personas es muy variada en las diferentes regiones del mundo, principalmente debido a las variaciones en los serovares prevalentes y a las condiciones ambientales en que se desarrollan los hospedadores y la bacteria.1 Asimismo, la letalidad por esta enfermedad depende del serovar infectante, la oportunidad del diagnóstico, el tratamiento y la edad del paciente, pudiendo alcanzar hasta un 20%.3 La infección sucede accidentalmente en forma directa o indirecta por contacto de piel escoriada y mucosas con orina o tejidos de animales portadores,6 o por contacto con tierra, agua u objetos contaminados con la orina de los animales infectados.1, 3, 4
Se afirma que lavacunación de animales domésticos es eficaz para prevenir la enfermedad en éstos y, en menor proporción, la infección y la leptospiruria ya que, si los animales fueron vacunados, al infectarse no presentan síntomas y el período de leptospiruria es más corto.1, 7, 8 La inmunidad a una serovariedad específica surge después de la infección o la vacunación, pero no confiere protección contra los otros serovares. Por lo tanto, algunas medidas preventivas deben ser orientadas a proteger las personas expuestas en su trabajo con indumentaria adecuada o brindando las condiciones ambientales mínimas para reducir la probabilidad de infección.1
En el comercio existen vacunas monovalente, bivalente y pentavalente para la protección del ganado vacuno contra los serovares: hardjo, icterohaemorrhagiae, canícola, pomona y grippotyphosa. Sin embargo, lo más recomendable es usar una vacuna contra los serovares prevalentes en los reservorios de cada región.2, 8 En contraste, la inmunización en personas no se ha aplicado ampliamente, pero algunos países que la han utilizado como China y Rusia obtuvieron resultados de entre el 70 y 80% de eficacia.9-11 En Costa Rica, actualmente no se dispone de vacuna para los seres humanos.
]]> El ganado vacuno portador de leptospirosis constituye un factor de riesgo importante para los vaqueros que trabajan en fincas lecheras.1, 2 En Costa Rica, des-de 1999 se aplican vacunas pentavalentes a las reses, siguiendo un programa de inmunización con una primera dosis a partir de los 3 a 4 meses de edad, luego, una segunda dosis al mes de la primera y un refuerzo al año de haber aplicado la primera. Sin embargo, la vacunación de animales domésticos contra Leptospira no es sistemática ni está regulada por algún ministerio, institución o colegio profesional afín.La información sobre vigilancia epidemiológica de la leptospirosis en Costa Rica documenta relación con grupos ocupacionales como agricultores del cultivo caña de azúcar,12 médicos veterinarios y criadores de animales como ganado lechero.3, 8, 13 Sin embargo, en el país no existen reportes que determinen cuánta protección confiere la vacuna al ganado y si la vacunación de los animales protege a las personas que trabajan con ellos.
Con el propósito de dar respuesta a estas interrogantes, se realizó el presente estudio experimental, longitudinal y prospectivo en vaqueros de cuatro zonas lecheras de Costa Rica.
Materiales y métodos
Población en estudio
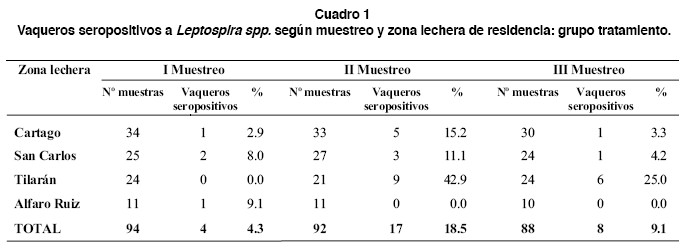
La población fue seleccionada entre los trabajadores de 180 fincas lecheras de cuatro zonas como son Cartago, San Carlos, Alfaro Ruiz y Tilarán, en las cuales se tamizó el ganado para detectar anticuerpos anti-Leptospira, como parte de otro estudio que evaluó el efecto de la vacuna anti-Leptospira en el ganado a través del estudio experimental "Efectos de la Vacuna Leptofern-5 en Ganado Lechero, en Costa Rica", realizado entre junio de 2001 y junio de 2002.14 De aquellos hatos con niveles de seroprevalencia mayores o iguales a un 20% se escogieron inicialmente 185 vaqueros distribuidos en 43 fincas de las cuatro zonas. Las personas ingresaron al estudio luego de firmar un consentimiento informado, de manera completamente voluntaria, luego que les fueron presentados los objetivos, la metodología y los alcances. Un total de 14 vaqueros abandonaron el estudio quedando un total de 171 distribuidos en 42 fincas (cuadros 1 y 2). Estos trabajadores se dividieron en un grupo tratamiento (ganado vacunado) y un grupo control (ganado no vacunado).

Grupo tratamiento
Al inicio del estudio, el grupo estuvo formado por 94 vaqueros que trabajaban en las fincas con ganado al que se le aplicó vacuna pentavalente anti-Leptospira (Leptoferm-5® Pfizer®). A los seis meses, este grupo disminuyó a 92 y al final se redujo a 88. La principal causa de este descenso fue por deserción voluntaria. Los trabajadores de este grupo se distribuyeron en 23 fincas de las cuatro zonas como se muestra en el cuadro 1.
Grupo control (placebo)
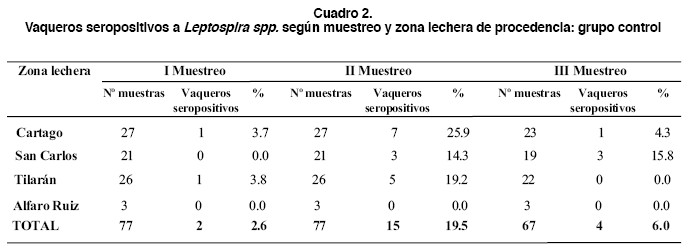
Este grupo incluyó 77 vaqueros que trabajaban en las fincas en las cuales se aplicó al ganado suero fisiológico como placebo. A los 6 meses se mantenía la cantidad inicial de trabajadores; sin embargo, al año disminuyó a 69. Al igual que en el grupo tratamiento, la principal razón fue la deserción voluntaria. Los integrantes de este grupo se distribuyeron en 19 fincas en las cuatro zonas estudiadas (cuadro 2).
Toma de muestras
Se tomó una muestra de sangre de aproximadamente 5 ml, a los vaqueros en tres diferentes oportunidades con un intervalo de 6 meses entre cada muestra. La toma se hizo por punción venosa de la vena humeral del antebrazo. Las muestras fueron tomadas por el investigador en los lugares de trabajo de cada vaquero y, para su conservación y traslado al laboratorio se colocaron en termos portátiles a temperatura entre 4° y 7° C. El tiempo entre la toma de la muestra y su sepaparación fue menor a 12 horas. En el laboratorio fueron centrifugadas a 4000 revoluciones por minuto, durante 10 minutos. Luego se separaron los sueros y se colocaron en viales plásticos debidamente rotulados, que se refrigeraron a 20° C hasta su procesamiento para la detección de los anticuerpos.
Detección de anticuerpos
]]> Los tipos y niveles de anticuerpos anti-Leptospira fueron detectados a través de la técnica de microaglutinación (MAT), en el INCIENSA. Las muestras con resultados de 1:100 o más diluciones para cualquiera de los cinco serovares estudiados se consideraron como positivas. Los serovares para los que se determinó seropositividad fueron pomona, hardjo, canícola y grippotyphosa (cuadro 3).

Captura, edición y análisis de los datos
Se creó una base de datos con los resultados de las pruebas serológicas correspondientes a cada vaquero del estudio, utilizando el programa Excel de Microsoft Office 2000. Esta base de datos fue analizada en primer término, mediante estadística descriptiva y pruebas de normalidad, para detectar inconsistencias.
La estadística descriptiva se enfocó en el cálculo de proporciones de vaqueros positivos por muestreo. Asimismo, se realizaron pruebas de chi-cuadrado para detectar la existencia de diferencias en los porcentajes de seropositividad entre grupos dentro de cada muestreo, o entre muestreos dentro de cada grupo. Estos procedimientos se realizaron usando el programa EpiInfo 6.0. Para determinar si existió asociación entre la vacunación de las vacas y la seropositividad en los vaqueros se calculó la razón de prevalencias (RP) en cada muestreo, asumiendo que cada uno de los muestreos constituyó un estudio transversal independiente. Sin embargo, por tratarse de un estudio longitudinal, en el que lo que interesa es la incidencia de casos que sero-, convirtieron de un muestreo a otro, se centró el análisis en el cálculo del riesgo relativo (RR) para el segundo y el tercer muestreo. Estos cálculos se realizaron con la ayuda del paquete WinEpiscope 2.0.
Resultados
Resultados generales
]]> Durante todo el estudio se obtuvo un 10.27% (50/ 487) de muestras con resultados positivos a cualquiera de los serovares de Leptospira spp. para los que fueron analizados; sin embargo, un 64% de los casos se dieron en el segundo muestreo (32/50).El mayor número de vaqueros seropositivos en el grupo tratamiento, en un solo muestreo, se presentó en Tilarán durante el segundo muestreo. En el grupo control, el mayor número de vaqueros seropositivos en un mismo muestreo, se observó en Cartago. Es de hacer notar el hecho que en Alfaro Ruiz solamente se presentó un caso seropositivo durante los tres muestreos (cuadros 1 y 2).
Resultados generales en el grupo tratamiento
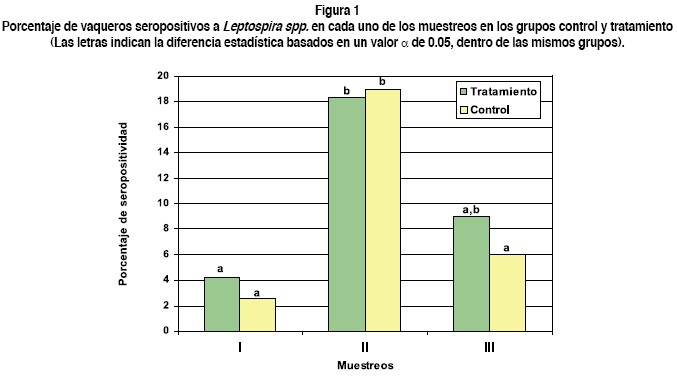
Del total de muestras procesadas durante los tres muestreos, la seropositividad encontrada fue 10.6% (29/274). En este mismo grupo, al analizar los resultados según cada muestreo, se observó un incremento significativo del primer al segundo muestreo (p<0.05) siendo 4.3% y 18.5%. Asimismo, a pesar de que hubo una reducción importante en el número de casos positivos en el tercer muestreo, esta no resultó ser significativa aunque muy cerca del límite de la significancia (p=0.06). No existió diferencia entre el primero y el tercer muestreo (figura 1, cuadro 1). Todos los serovares analizados presentaron al menos un caso positivo en alguno de los tres muestreos (cuadro 3), excepto para el serovar grippotyphosa. Los serovares con mayor frecuencia de seropositividad fueron: hardjo y pomona para los que se observó 2.1 %, 8.7 %, 3.4% y 2.1%, 7.6% y 3.4%, en el primer, segundo y tercer muestreo respectivamente. El rango de títulos de anticuerpos a cualquiera de los serovares analizados varió entre 1: 100 y 1:6,400.
Resultados generales en el grupo control
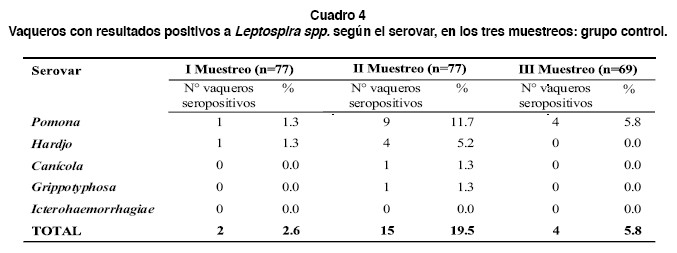
En este grupo la seropositividad global encontrada fue de 10.3% (21/213), observándose un mayor númemero de muestras positivas para los mismos serovares que en el grupo tratamiento. Los resultados de seropositividad observados en los muestreos de este grupo fueron 2.6%, 19.5% y 6.0%, del primero al tercero respectivamente. El incremento en el número de casos positivos entre el primer y segundo muestreo, y la reducción del segundo al tercero fueron significativos (p <0.05), mientras que no lo fue entre el primero y el tercero (Figura 1, Cuadro 2). El rango de títulos de anticuerpos para los controles fue de 1:100 a 1:400, inferior al grupo tratamiento (p < 0.05). Los serovares para los que se determinó seropositividad en el grupo fueron pomona, hardjo, canícola y grippotyphosa, no así para icterohaemorrhagiae (cuadro 4). En este grupo, al igual que el grupo tratamiento, el serovar pomona fue el más frecuentemente diagnosticado, con un 66.7% de los casos positivos, siguiendo en frecuencia el hardjo con un 23.8%.
Análisis de resultados por muestreo
Primer muestreo
El porcentaje de vaqueros con resultados positivos encontrados en cada uno de los grupos al inicio del estudio (primer muestreo) fue de 4.3 % en el grupo tratamiento y 2.6 % en el grupo control (figura 1, cuadros 1 y 2). La RP de vaqueros seropositivos fue de 1.6 [IC 95%, 0.3-8.7] lo cual indica que al inicio de estudio, cuando aún no se había aplicado las vacunas o el placebo al ganado con que trabajan los vaqueros, la prevalencia de vaqueros seropositivos en el grupo tratamiento es 1.64 veces mayor a la del grupo control.
La mayor proporción de casos positivos en el primer muestreo es aportada principalmente por los serovares pomona y hardjo.
Segundo muestreo
En ambos grupos hubo un incremento significativo en el porcentaje de vaqueros seropositivos a los 6 meses. La prevalencia global de seropositividad en el grupo tratamiento fue 18.5% mientras que en el grupo control fue 19.5%, por lo que la RP fue de 0.9 (IC 95%, 0.5-1.8).
Se encontraron 13 vaqueros incidentes en el grupo control,paraunaincidenciadeseropositividadde17.3%. Asimismo, en el grupo tratamiento seroconvirtieron 15 vaqueros para una incidencia de seropositividad de 17.0%. El RR fue 1.0 (IC 95%, 0.6-1.9), lo que indica que al segundo muestreo la vacunación a las vacas no tuvo efecto para los vaqueros de ningún grupo.
Tercer muestreo
]]> En este muestreo, resultaron seropositivos 9.1% de los vaqueros en el grupo tratamiento y 6.0% en el grupo control, con una RP de 1.5 (IC 9%, 0.5-4.8). Esto indica que la prevalencia en el grupo tratamiento es 50% mayor que en el grupo control. Sin embargo, esta diferencia no resultó ser significativa. Por otra parte, el RR fue 1.5 (IC 95%, 0.5 -4.8), lo que significa que al final del estudio los vaqueros del grupo tratamiento tienen 1.5 veces más riesgo de ser seropositivos, comparados con el grupo control. Sin embargo, esta diferencia no resultó ser estadísticamente significativa.Discusión
En Costa Rica son escasos los estudios publicados sobre leptospirosis, a pesar de existir antecedentes de brotes y defunciones producidas durante éstos.15, 16 Aún más escasos son los estudios de seropositividad en poblaciones humanas con alta exposición, según las tareas que realizan, necesarios para planificar, priorizar y dirigir adecuadamente las intervenciones en la prevención y control de la leptospirosis.17
Este estudio se realizó en cuatro zonas del país con diferentes patrones de pluvialidad, humedad, temperatura, relieve y altura sobre el nivel del mar; sin embargo, la distribución de vaqueros seropositivos por zona no es estadísticamente significativa, excepto en la zona de Alfaro Ruiz, donde la seropositividad encontrada fue mínima (un vaquero). Es probable que las las condiciones geomorfológicas y ambientales predominantes en esta zona, como el relieve quebrado con menor humedad a nivel de piso y menor probabilidad de estancamiento de aguas contaminadas por orina de animales, que constituyen fuentes potenciales de infección, sean las responsables de esta baja proporción de vaqueros seropositivos. Además, no hay que dejar de lado que la cantidad de vaqueros involucrados en el estudio provenientes de Alfaro Ruiz, fue la menor de las cuatro zonas estudiadas, siendo únicamente 14 al inicio y 13 al final del estudio, lo que pudo afectar significativamente la probabilidad de encontrar vaqueros seropositivos en esa zona.
El marcado incremento en el número de vaqueros seropositivos en el segundo muestreo, puede deberse a varias razones: 1) nuevas infecciones con los serovares analizados, como producto de una mayor exposición a las leptospiras, lo que aumentaría su presencia en el ambiente aprovechando las condiciones ambientales, 2) infecciones durante épocas secas con serovares diferentes a los analizados, 3) reinfecciones con los serovares analizados, 4) reacciones cruzadas por infecciones con serovares diferentes a los analizados, y 5) errores de diagnóstico. Si bien es cierto que en todo proceso diagnóstico existe la posibilidad del error en el diagnóstico, resulta muy improbable que tal incremento hacia el segundo muestreo sea producto de este factor.
Un hecho más probable es el incremento en la cantidad de leptospiras disponibles en el ambiente, como producto de las condiciones ambientales imperantes en el segundo muestreo. Hay que recordar que el primer y el tercer muestreo se realizaron en los meses de enero y febrero, época de verano en la mayoría del territorio nacional, especialmente en los cantones donde se realizó el estudio. El segundo muestreo se llevó a cabo en julio y agosto, época con mayor humedad y existencia de aguas estancadas, que favorecen la presencia de las leptospiras en el ambiente y los reservorios, lo que podría considerarse como un aumento en el nivel de exposición para los vaqueros.
Por otra parte, es posible que algunos de los casos de seroconversión no fueran por una primoinfección sino más bien por reinfecciones, que podrían haberse dado en los períodos de mayor precipitación pluvial que coincidieron con el segundo muestreo. Esto podría explicar la escasa cantidad de casos reportados de enfermedad durante el período de estudio, inclusive en los vaqueros que ocurrió la seroconversión. Es posible que el período entre los muestreos haya sido lo suficientemente extenso para permitir que el estímulo antigénico no fuera constante y estimulara el sistema inmune a mantener los títulos de anticuerpos en los niveles de positividad, llegando incluso a descender a niveles cercanos o dentro de la negatividad. Si bien es probable que los cambios en la seropositividad pudieran deberse parcialmente a reacciones cruzadas con otras serovariedades diferentes a las incluidas en el panel con que se trabajó para este estudio, no se considera que esta sea la razón de los cambios tan sustanciales entre un muestreo y otro.
Quizás estas condiciones fueran las responsables del incremento en el segundo muestreo en que se alcanzó el máximo nivel de seropositivos, independientemente del hecho de que las vacas estuvieran vacunadas o no, lo que hace pensar que la posible fuente de infección en los vaqueros no está únicamente en las vacas. Sin embargo, no se puede obviar que este estudio solo incluyó cinco serovares de L. interrogans que, si bien es cierto, son lo más frecuentemente documentados, no incluye otros serovares presentes en el territorio nacional, lo que podría estar subestimando el número de seropositivos.
Conclusiones y recomendaciones
]]> De acuerdo con los alcances del presente estudio, la aplicación de vacuna anti-Leptospira al ganado con que trabajan los vaqueros no tiene efecto en los niveles de anticuerpos que ellos presentan. Esta experiencia refleja la necesidad de extender el monitoreo de los anticuerpos anti-Leptospira en los individuos expuestos por un periodo mayor a un año y debido a la situación epidemiológica de esta enfermedad en nuestro país, se recomienda incrementar las serovariedades del panel de antígenos para realizar el MAT.Referencias bibliográficas
1. Faine, S. 1999. Leptospira and Leptospirosis. 2ª ed. S. Faine, editor. MediSci®, Melbourne, Australia. 296 p. [ Links ]
2. Organización Panamericana de la Salud 1995. Manual de Enfermedades Transmisibles. 1ª ed. Organización Panamericana de la Salud. Washington, D.C. [ Links ]
3. Ochoa, J.E., Sánchez, A., Ruíz, I. 2000. Epidemiología de la leptospirosis en una zona andina de producción pecuaria. Rev. Panam. Salud Pública, 7(5):325-31. [ Links ]
4. Chin, J., Ascher, M. 2001. EL control de las enfermedades transmisibles. 17ª ed. Vol. 1, No. 1. Washington, D.C.: Organización Panamericana de la Salud. pp. 395-421 [ Links ]
5. García R. 1998. Leptospira interrogans: Primeros Aislamientos Humanos en Costa Rica. Rev. Costarric. Cienc. Méd. 19, 3-4, pp.147-154. [ Links ]
6. Ministerio de Salud. 1995. Mortalidad por enfermedades de Declaración Obligatoria. San José: Ministerio de Salud de Costa Rica. [ Links ]
7. Muñoz, G., López, J., Fuentealba, J. 1997. Seroprevalencia, de leptospirosis en médicos veterinarios expuestos al riesgo. Cuadernos Médico Sociales, Santiago, Chile. 38: 40-3. [ Links ]
8. Amstutz, H. 1988. Leptospirosis. El manual Merck de Veterinaria, 3ª ed. Español. Merck. & Co., Inc. España. pp. 437-42. [ Links ]
9. Chen, T.Z. 1986. Development and present status of leptospiral vaccine and technology of production of the vaccine in China. Ann Immunol Hung. 26:125151. [ Links ]
10. lagokin,E.,Kostina,N.,Vachaev,B.,Romantsova,T.,Kondratenko, V., Bunin, I., Gol,denshtein, Z., Anan,ina, I. 1990. Theimprovement of immunobiological preparations against leptospirosis. An experimental study of a new concentrated purified vaccine against icterohemorrhagic leptospirosis for human immunization. Zh Mikrobiol Epidemiol Immunobiol. (2):4751. [ Links ]
11. Yan Y., Chen Y., Liou W., Ding J., Chen J., Zhang J., et al. 2003. An evaluation of the serological and epidemiological effects of the outer envelope vaccine to leptospira. J Chin Med Assoc. 66, (4):22430. [ Links ]
12. Ministerio de Salud, 2000. Leptospirosis Memoria. San José: Ministerio de Salud de Costa Rica. [ Links ]
13. Medina, M. Borja, G., Vasco, L., Jaramillo, G., Mosquera, J. Hernández, G. 1997. Leptospirosis, un tema de actualidad. EDIMEC. Quito, Ecuador. 115 p. [ Links ]
14. Maranda, L. 2003. Estudio Experimental Sobre Efectos de la Vacuna Leptofern-5 en Ganado Lechero, en Costa Rica, 2001". PhD Tesis. Universidad de Davis, California. [ Links ]
15. Villegas H. 1999. Leptospirosis. Memorias de la Semana Epidemiológica # 44 Organización Panamericana de la Salud. CostaRica. [ Links ]
16. Sáenz,A.C.,Rodríguez,G.2004.Leptospirosisenlapoblación de la Región Huetar Norte durante el período comprendido entre 1997 y 2000. Acta méd. Costarric. 46, (4): 184-189. [ Links ]
17. Organización Panamericana de la Salud, 2001. Zoonosis y enfermedades transmisibles al hombre y a los animales. 3ª ed. Organización Panamericana de la Salud. Washington, D. C. [ Links ] ]]>