Introducción
Es altamente conocido que las enfermedades cardiovasculares (ECV) son la principal causa de muerte en el mundo y en Costa Rica (Ministerio de Salud, 2017; Organización Mundial de la Salud, 2018). Dentro de la gama de las ECV, la enfermedad arterial coronaria (EAC) es la más prevalente en los últimos 15 años; actualmente, mueren por esta causa un total de 15.2 millones de personas por año (Organización Mundial de la Salud, 2018), mientras que en Costa Rica fallecieron 2670 personas solo en el año 2015 (Ministerio de Salud, 2017).
La EAC es generada principalmente por daños estructurales o funcionales en el corazón o los vasos sanguíneos (Fleg et al., 2013) desarrollado por una disfunción endotelial que predispone la vasoconstricción, adherencia de los leucocitos, activación plaquetaria, proliferación, coagulación alterada, inflamación, trombosis y aterosclerosis (Dod et al., 2010; Widlansky et al., 2003). La EAC tiene una fisiopatología compleja, la cual se caracteriza principalmente por la acumulación de lípidos y elementos fibrosos en las arterias (Pinto et al., 2012).
La fase inicial de esta enfermedad es generada por lesiones en los vasos sanguíneos (Frostegård et al., 1999; Stemme et al., 1995), lo que da lugar a un proceso inflamatorio derivado de una respuesta inmunológica (Pérez-Fernández & Kaski, 2002; Ross, 1999) y al desarrollo de disfunción endotelial y placa de ateroma (Widlansky et al., 2003). Los biomarcadores inflamatorios están involucrados en estos procesos, ya que existe una alta relación entre la inflamación endotelial, el progreso de desarrollo de la aterosclerosis y la generación de un evento cardiovascular como el infarto agudo al miocardio (IAM) (Fioranelli et al., 2018).
Uno de los principales biomarcadores inflamatorios asociados con la disfunción endotelial y progreso de la EAC es la interleucina-6 (IL-6) (Pinto et al., 2012). La IL-6 es una glucoproteína localizada en el cromosoma 7, que tiene funciones tanto antiinflamatoria como proinflamatoria a nivel de las estructuras circulantes (Ohsuzu, 2004). La IL-6 promueve el incremento en las quimiocinas y moléculas de adhesión, lo que da lugar al proceso de aterosclerosis (Del Giudice & Gangestad, 2018; Fioranelli et al., 2018). El incremento de este biomarcador puede desencadenar un mayor riesgo de desestabilización y rotura de las placas ateroscleróticas, y un aumento de la mortalidad del paciente con EAC (Fioranelli et al., 2018; Libby & Theroux, 2005; Madjid & Willerson, 2011; Pinto et al., 2012).
Se ha demostrado que altos niveles de IL-6 incrementa el riesgo de EAC y se relaciona con todas las causas de mortalidad por ECV (Tabaei et al., 2020). Principalmente por ser uno de los causantes de la fase inicial de inflamación en la pared endotelial (Christodoulidis et al., 2014) y por estar involucrado en la generación de estiramiento miocárdico, lesión de miocitos, fibrosis, remodelación de la pared miocárdica, estrés oxidativo y la activación neurohumoral (Chow et al., 2017; Yancy et al., 2017). El conocimiento del desarrollo y control de biomarcadores inflamatorios son de suma importancia ya determina la evolución del paciente, aplicación del tratamiento y progresión de la EAC (Panagiotakos et al., 2004).
Existe una relación significativa entre los altos niveles de actividad física y la disminución de inflamación endotelial (Reuben et al., 2003). Principalmente porque el ejercicio físico contribuye a la mejora de la función endotelial y la disminución en los marcadores inflamatorios como la IL-6, proteína C-reactiva (PCR) y molécula de adhesión celular vascular 1 (VCAM-1) (Swardfager et al., 2012), atenuando así la progresión de la aterosclerosis y el riesgo de trombosis (Alter et al., 2009).
Actualmente, el ejercicio aeróbico (EA) es el más investigado y aplicado dentro de los programas de rehabilitación cardíaca (PRC) para generar adaptaciones cardiovascular en pacientes con EAC debido a su eficacia y seguridad (Taylor et al., 2014). Se ha encontrado que el EA aumenta el consumo máximo de oxígeno (VO2máx) entre el 11% y el 36%, aumenta la capacidad funcional, mejora la respuesta hemodinámica y mejora el perfil de lípidos y disminución de la presión arterial (Araya-Ramírez et al., 2013; Leon et al., 2005; Oldridge et al., 2019). Sin embargo, el mejor método de entrenamiento sigue en discusión y ha surgido nuevas alternativas (Ponikowski et al., 2016; Vanhees et al., 2012).
Una de estas alternativas es la combinación del EA con el ejercicio de contra resistencia (ER), lo que se conoce como entrenamiento concurrente (EC). El ER ayuda a mejorar la fuerza, hipertrofia, la función física y calidad de vida de pacientes con ECV (Haykowsky et al., 2016). Mientras que EC está presentado similares efectos en adaptaciones cardiovasculares, aunque es necesario más investigación en esta área (Marzolini et al., 2012; Swardfager et al., 2012). Por lo tanto, el propósito de la presente revisión sistemática de literatura es analizar el efecto del EA versus EC sobre IL-6 en pacientes con EAC.
Metodología
Esta revisión sistemática de literatura se desarrolló siguiendo los acuerdos PRISMA para los ítems de informes preferidos para revisiones sistemáticas y meta-análisis (Moher et al., 2009).
Criterios de Elegibilidad
Los criterios de elegibilidad fueron determinados por el autor y siguen la normativa PICOS. Se tomaron en cuenta estudios que cumplieran con los siguientes criterios: a) estudios controlados; b) estudios con un tratamiento de al menos 4 semanas; c) con medición de pre y post; d) reporte de la media y desviación estándar en la variable de IL-6; e) pacientes de ambos sexos con diagnóstico de EAC; d) estudios publicados entre el año 2002 y 2021; e) estudios publicados en inglés, español o portugués.
Búsqueda de literatura
La búsqueda de los artículos científicos para esta revisión sistemática se llevó a cabo mediante bases de datos electrónicas, tales como: “PubMed”, “ScienceDirect”, “Academic Search Ultimate” y “SportDiscus”, se accede a estas bases de datos por medio de la plataforma “EBSCO host”. Los términos de búsqueda (frase booleana) o palabras clave fueron los siguientes: ("coronary artery disease" OR ‘‘cardiac disease’’ OR “cardiovascular disease”) AND (‘‘exercise’’ OR ‘‘training’’ OR “cardiac rehabilitation”) AND (“IL-6” OR “Interleukin-6” OR “inflammatory markers”) NOT ("animals" OR “rat”). Se revisaron las referencias de los artículos incluidos para identificar otros estudios potencialmente elegibles. Se buscó el texto completo de los estudios en las mismas bases de datos, por medio de las plataformas virtuales como ResearchGate o se solicitaron a los autores por vía de correo electrónico. Las búsquedas fueron realizadas entre marzo y abril de 2021.
Selección de estudios y codificación de la información
La búsqueda y extracción de los estudios fue realizada por el investigador principal, se analizaron de forma independiente los títulos y resúmenes de cada artículo encontrado, con el fin de observar y considerar cuál era un posible artículo elegible. Posteriormente se analizaba el texto completo para conocer si cumplían con los criterios de elegibilidad. Para la extracción de los datos se confeccionó una hoja de codificación de datos utilizando el programa Excel (Excel 2016; Microsoft). Además, se evaluó la calidad metodológica de los estudios mediante el uso de la herramienta Escala PEDro. Se revisaron los aspectos de la población de estudio, la intervención realizada, el período de seguimiento y las mediciones de los resultados.
Resultados
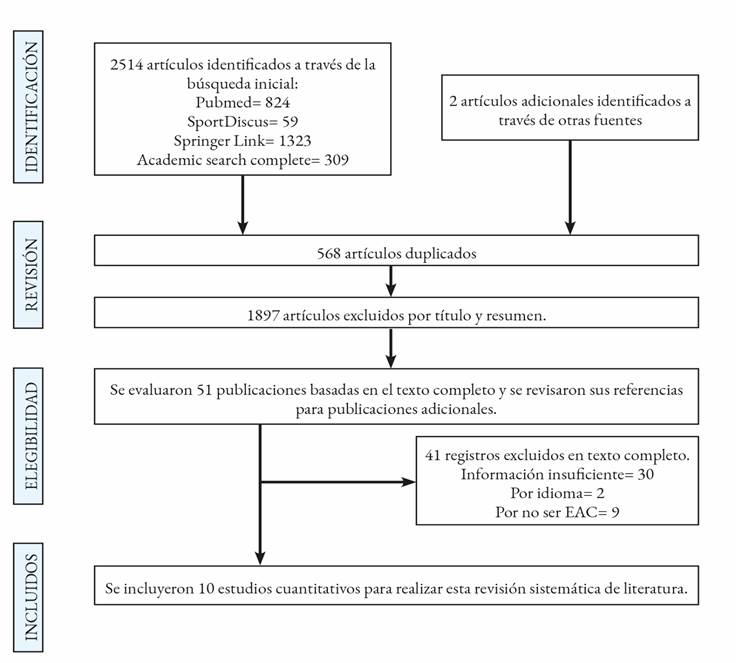
Se revisaron un total de 2516 estudios, donde finalmente se incluyeron 10 estudios cuantitativos que cumplieron con los criterios de elegibilidad (ver Figura 1). Se encontraron estudios publicados entre el año 2002 y 2018, no se evidenció ningún estudio posterior al año 2018. Los estudios incluidos obtuvieron en promedio un puntaje de 8.3 en la escala de calidad PEDro, lo cual representa una buena calidad de los estudios incluidos. Se analizaron un total de 413 pacientes con EAC de ambos sexos, con una edad promedio de 47.4 ± 18.4 años. Los programas de ejercicio físico promediaron 9.3 ± 6.1 semanas y 32.3 ± 15.4 sesiones.
Con respecto al tratamiento farmacológico, dos estudios indicaron que no existía diferencia significativa en la ingesta de anticoagulantes, beta-bloqueadores, diuréticos, estatinas y metformina, clopidogrel e inhibidores de ECA y sistema renina-angiotensina-aldosterona (Dod et al., 2010; Shin et al., 2006). Cuatro estudios no indicaron el tratamiento farmacológico utilizado por los pacientes (Akbarpour, 2013; Beckie et al., 2010; Buchan et al., 2011; Roca-Rodríguez et al., 2015). En los demás estudios incluidos utilizaron betabloqueadores en más del 60% de la muestra, en un 95% se utilizó anticoagulantes, entre un 80% y 95% utilizaron otros medicamentos hipertensivos, sin evidenciar diferencia entre los grupos (Conraads et al., 2002; Sandor et al., 2014; Subiela et al., 2018). No se puede afirmar que exista influencia del tratamiento farmacológico en los resultados encontrados, dado que existe faltante de información y heterogeneidad en los tratamientos utilizados.
Se encontró que el EA disminuye significativamente la IL-6 entre un 36.6% y un 74% (Akbarpour, 2013; Dod et al., 2010; Kim et al., 2013; Shin et al., 2006), como se muestra en la tabla 1. Se observaron mejoras no significativas entre un 5% y un 36.2% (Buchan et al., 2011; Subiela et al., 2018). Las diferencias entre los estudios con efectos significativos recaen en haber generado protocolos de EA con mayor volumen o tiempo de ejercicio físico durante las sesiones.
Tabla 1 Resumen de las características y resultados de los estudios que realizaron entrenamiento aeróbico (EA).
| Estudio | Sexo | Edad | n | Volumen (min) | Intensidad (%) | Sesiones | %Δ | p |
|---|---|---|---|---|---|---|---|---|
| Akbarpour (2013) | H | 23 ± 2 | 30 | 15 - 30 | 75 - 85 | 36 | -74.0 | < .050 |
| Buchan et al., (2011) | A | 16 ± 1 | 15 | 20 | 70 | 21 | -5.0 | > .050 |
| Buchan et al., (2011) | A | 17 ± 1 | 13 | 4-6 sprints (des: 20s) | 100 | 21 | -36.2 | > .050 |
| Dod et al., (2010) | A | 56 | 27 | 60 | Moderado | 36 | -51.0 | < .020 |
| Kim et al., (2013) | A | 56 ± 7 | 17 | 40 | 60 - 85 | 18 | -51.2 | < .050 |
| Shin et al., (2006) | A | 61 ± 3 | 14 | 30 - 40 | 50 - 85 | 18 | -36.6 | < .010 |
| Shin et al., (2006) | A | 59 ± 2 | 15 | 30 - 40 | 50 - 85 | 18 | -41.3 | < .001 |
| Subiela et al., (2018) | H | 54 ± 8 | 17 | 30 | 60 - 80 | 36 | -8.9 | > .050 |
Abreviaciones: H= hombre; A= ambos sexos; n= participantes por grupo; min= minutos; des= descanso; s= segundos; %Δ= porcentaje de cambio; p= significancia. La intensidad se calculó utilizando la FCmáx, Vo2máx o Vo2pico.
Con respecto al EC, se encontraron mejoras significativas entre un 52.4% y 58.8% (Beckie et al., 2010; Sandor et al., 2014), donde los estudios que realizaban una mayor intensidad en el EA presentaban efectos significativos y un mayor porcentaje de cambio (%Δ), como se muestra en la tabla 2. No se evidenció diferencias entre los protocolos utilizados en el EA y en el entrenamiento de contra resistencia. En este último caso, los estudios incluidos no detallaron correctamente la cantidad de series, repeticiones, intensidad o metodologías utilizadas, lo que dificulta su análisis.
No se denota una diferencia en la disminución de la IL-6 entre los métodos de EA y de EC, ambas modalidades de ejercicio físico son efectivos para la disminución de este biomarcador inflamatorio. Además, ambas modalidades presentaron mejores efectos significativos en comparación con los pacientes que integraban los grupos controles, es decir, aquellos que no realizaban ejercicio físico (ver tabla 3). Sin embargo, se observó una gran disminución de un 46.6% en el grupo control, sin ser estadísticamente significativo (Kim et al., 2013). Los investigadores de este estudio indicaron que esta disminución en la IL-6 fue provocada, posiblemente, por los fármacos suministrados y por la heterogeneidad de la muestra utilizada.
Tabla 2 Resumen de las características y resultados de los estudios que realizaron entrenamiento concurrente (EC= aeróbico en combinación con contra resistencia)
| Estudio | Sexo | Edad | n | Volumen (min) | Intensidad (%) | Sesiones | %Δ | p |
|---|---|---|---|---|---|---|---|---|
| Beckie et al., (2010) | M | 61 ± 9 | 43 | EA: 35 - 45 EC: NR | EA: 60 - 85 EC: poleas en la pared y propio peso | 36 | -58.8 | < .050 |
| Beckie et al., (2010) | M | 61 ± 9 | 48 | EA: 35 - 45 EC: NR | EA: 60 - 85 EC: poleas en la pared y propio peso | 36 | -55.6 | < .050 |
| Conraads et al., (2002) | A | 57 | 23 | EA: 20 EC: 9 ej - 3 series - 10 rep | EA: 90 (UV) EC: 50 (RM) | 48 | -27.6 | = .800 |
| Roca-Rodríguez et al., (2015) | A | 55 ± 8 | 36 | EA: 30 EC: NR | EA: moderada EC: peso libre (1-2 kg) | 24 | -2.3 | > .050 |
| Sandor et al., (2014) | A | 65 ± 6 | 79 | EA: 40 EC: NR | EA: 50 - 70 EC: propio peso y ej estáticos | 72 | -52.4 | = .060 |
Abreviaciones: M: mujer; A= ambos sexos; n= participantes por grupo; min= minutos; EA: ejercicio aeróbico; EC: entrenamiento concurrente; ej= ejercicios; rep= repeticiones; NR= no registra; UV: umbral ventilatorio; RM= repetición máxima; %Δ= porcentaje de cambio; p= significancia. La intensidad del ejercicio aeróbico se calculó utilizando la FCmáx, Vo2máx o Vo2pico.
Tabla 3 Resumen de las características y resultados de los casos controles
| Estudio | Sexo | Edad | n | %Δ | p |
|---|---|---|---|---|---|
| Buchan et al., (2011) | A | 16 ± 1 | 21 | 5.0 | > .050 |
| Kim et al., (2013) | A | 54 ± 8 | 15 | -46.6 | > .050 |
Abreviaciones: A= ambos; n= participantes por grupo; %Δ= porcentaje de cambio; p= significancia.
Discusión
El objetivo de este estudio fue analizar la evidencia científica sobre la efectividad del EA versus EC en la disminución de la IL-6 en pacientes con EAC. Se encuentra que la mayoría de los estudios indicaron que el EA es favorable en la mejora de este biomarcador, mientras el EC es contradictorio en sus resultados. Se demuestra que el EA mejora la inflamación endotelial, causando un decrecimiento en el riesgo de un evento coronario y disminuyendo la mortalidad de los pacientes con EAC (Lindmark et al., 2001), mientras que con respecto al EC se debe realizar más investigación al respecto. Como se demuestra en un estudio realizado por Swardfager et al. (2012),el ejercicio físico disminuye significativamente la IL-6 (TE= −0.546, 95% CI -0.739 a -0.353, n = 280, p < .001), no obstante, no existió una diferencia significativa al comparar los resultados con aquellos pacientes con EAC que no realizaron ejercicio físico. Solo la proteína C-reactiva y el fibrinógeno mostraron cambios significativos contra los grupos controles.
En general, ambas modalidades de entrenamiento inciden en una disminución de los factores de riesgo, eventos coronarios como el infarto agudo al miocardio (IAM) y en la disminución de la mortalidad entre un 20% y 25% de los pacientes con EAC (Dod et al., 2010; Leon et al., 2005). Sin embargo, los estudios de EC incluidos no detallaron correctamente el entrenamiento de contra resistencia, por lo cual se debe tomar con cautela los resultados expuestos y su comparación con el EA. Además, los cambios observados no pueden ser atribuidos solo al ejercicio físico, dado que los resultados pueden haber sido influenciados por el estilo de vida, la dieta, el manejo médico, la recuperación de eventos coronarios y la heterogeneidad en las poblaciones incluidas al inicio del estudio (Swardfager et al., 2012).
Dentro de los estudios incluidos que realizaban EA, se observa que aquellos que presentaban protocolos de EA con mayores intensidades, es decir, superiores al 80% de VO2máx o frecuencia cardíaca máxima (FCmáx) fueron los que obtuvieron efectos significativos con el entrenamiento (Akbarpour, 2013; Kim et al., 2013; Shin et al., 2006). Tal como lo reporta Akbarpour (2013), al aplicar un protocolo de entrenamiento con intensidades entre un 75% y un 85% de la FCmáx, se evidencia una disminución de un 74% en la IL-6, pasando de 7.4 ± 3.2 pg/mL a 1.93 ± 0.7 pg/mL (p < .050). Otro estudio que demuestra lo anteriormente comentado, fue el realizado por Beckie et al. (2010), donde encontraron una disminución en la IL-6 de un 58% (p < .050), utilizando un protocolo de EA que llegaba hasta el 85% de la FCmáx y con una combinación de entrenamiento de contra resistencia utilizando poleas. Mientras estudios que presentaron intensidades moderadas no reportaron efectos significativos, como el realizado por Roca-Rodríguez et al., (2015) donde encontraron una disminución de tan solo 2.3% (p > .050) con un protocolo de EA de intensidad moderada y un trabajo de contra resistencia utilizando el peso corporal y mancuernas livianas (1 a 2 kg).
Otro aspecto importante en la disminución significativa de la IL-6 fue el volumen de entrenamiento, donde un mayor tiempo total de la sesión favoreció a superiores beneficios significativos. Como se demuestra en el estudio de Dod et al. (2010), donde se aplicó un protocolo de 60 minutos totales con una intensidad moderada, dando como resultado una disminución de 51%, la IL-6 pasó de 2.5 ± 0.6 pg/mL a 1.2 ± 0.3 pg/mL (p < .020); mientras tanto, aquellos estudios basados en sesiones de EA con un tiempo total entre 20 a 30 minutos, no presentaron efectos significativos (Buchan et al., 2011; Subiela et al., 2018).
De lo anterior se infiere que, aunque se realice el EA con altas intensidades, se necesita un tiempo total de 30 minutos o más por sesión. Esto se demuestra en lo reportado por Buchan et al., (2011), donde reportaron que la IL-6 no disminuyó de manera significativa, ya que pasó de 3.8 ± 5.8 pg/mL a 2.4 ± 5.5 pg/mL (p > .050), para lo cual utilizaron un protocolo de intervalos de alta intensidad (HIIT, por sus siglas en inglés), el cual consistía en realizar de 4 a 6 repeticiones de sprints al 100% de la FCmáx, con descansos con pausas completas entre 20 a 30 segundos, lo que correspondía a sesiones menores a 15 minutos.
Dentro de los posibles efectos fisiológicos provocados tanto por EA como el EC para generar una disminución de la IL-6 se considera el aumento de la vasodilatación arterial desarrollado por un aumento en la segregación de óxido nítrico (Ridker et al., 2000; Starkie et al., 2003) , así como una disminución de las neurohormonas vasoconstrictoras como la angiotensina II, aldosterona, vasopresina, epinefrina y norepinefrina (Braith et al., 1999; Hambrecht et al., 2000). El ejercicio físico provoca múltiples beneficios cardiovasculares que indirectamente logran mejorar la producción y eliminación de los marcadores inflamatorios como la IL-6. Estas adaptaciones suceden tanto a nivel central como periférico, como la mejora en el volumen sistólico máximo, en la contractibilidad cardíaca y en la diferencia arteriovenosa de oxígeno máximo (Montero et al., 2015). También, se observan cambios acompañados de mejorías en las enzimas antioxidantes y proteínas relacionadas con el estrés oxidativo que ayuda a mejor la contractividad cardíaca, además de una disminución de los niveles de mieloperoxidasa (MPO) (Crimi et al., 2009; Fu et al., 2013).
Conclusiones
Tanto el EA como el EC son beneficiosos en la disminución del IL-6 en pacientes con EAC. Independientemente de la edad, sesiones de entrenamiento semanales y de la etapa inicial de los pacientes con EAC. Sin embargo, se debe tomar con cautela estos resultados, dado la poca evidencia en EC y la falta de información de los protocolos utilizados en el ER. Se denota que la alta intensidad incide en una mayor disminución del IL-6, pero se debe continuar investigando el comportamiento de la intensidad en ambas modalidades para conocer si existe mayor eficacia y seguridad para los pacientes con EAC.