Introducción
La hemofilia es una deficiencia congénita de un factor de la coagulación, la cual consta en un trastorno recesivo asociado al cromo- soma X, generando disminución o ausencia de actividad funcional del factor. (Ministerio de Salud. “Guía Clínica hemophilia”. Santiago: Minsal, 2013)
Dependiendo de la deficiencia del factor afectado, existen diferentes tipos de hemofilia: hemofilia A, en caso de que exista ausencia o disminución del factor VIII, con una incidencia de 1 por cada 5.000 - 10.000 varones nacidos. Siendo la más común (representa entre el 80 - 85% del total de hemofílicos). Hemofilia B en caso de que exista deficiencia o ausencia del factor la cascada de la coagulación, cuya incidencia es de 1 por cada 30.000 - 50.000 varones nacidos.(Srivastava et al., 2013a) (Liras & Romeu, 2019) (Sachdeva et al., 2018)
En la mayoría de los casos de hemofilia, los hombres son quienes heredan y manifiestan el trastorno, mientras que las mujeres son portadoras, sin embargo, también pueden presentar leves sintomatologías. Cuando una mujer que es portadora tiene hijos, existe un 50% de probabilidades de que sus hijos presenten el trastorno y un 50% de probabilidades que sus hijas sean portadoras. En caso de que el padre sea hemofílico y la madre sea sana, el 100% de los hijos serán sano y el 100% de las hijas serán portadoras, por último, en caso de que el padre sea hemofílico y la madre sea portador, el 50% de los hijos pueden ser hemofílicos y el 100% de las hijas serán portadoras. (Mingot-Castellano, Núñez, & Rodríguez-Martorell, 2017; Srivastava et al., 2013b)
Es importante señalar que un 30% de los enfermos no presentan antecedentes familiares relacionados con hemofilia.(Peyvandi, Garagiola, & Young, 2016)
La hemofilia es clasificada de acuerdo con la cantidad del factor presente en la sangre y se agrupa en hemofilia, leve, moderada y severa. (Tabla 1).
El diagnóstico suele realizarse con una evaluación detallada de la historia clínica del paciente junto a antecedentes de respuestas hemorrágicas espontáneas o secundaria pequeños traumatismos. (Liras & Romeu, 2019)(Benson et al., 2018).
En estos pacientes es indispensable solicitar exámenes específicamente de la coagulación pero finalmente la confirmación diagnóstica de hemofilia es al detectar disminución o ausencia significativa del factor VIII o IX.(Casas Patarroyo et al., 2019).
Tabla 1 Clasificación de la hemofilia según severidad
| Gravedad | Nivel del factor (% de actividad - UI/ml) | Características |
| Hemofilia Leve | 6-40% | Hemorragias leves y de fácil control. Hemorragias graves con traumatismos o cirugías |
| Hemofilia Mode- rada | 1-5% | Hemorragias espontáneas ocasionales y por lesiones menores. Hemorragias graves con traumatismos o cirugías |
| Hemofilia Severa | <1% | Hemorragias espontáneas semanales, principalmente en articulaciones y múscu- los |
(Peyvandi et al., 2016)(Knobe & Berntorp, 2011)(Alemandi S., M., L., & M.X., 2014)
Tabla 2 Exámenes de laboratorio que se pueden solicitar
| Tiempo de protrombina (TP) |
| Tiempo de tromboplastina parcial activado (TTPA) |
| Hemograma completo |
| Recuento de plaquetas |
| Dosaje de factor VIII |
| Dosaje de Factor IX |
Respecto a los exámenes de la coagulación que pueden ser solicitados, se incluye (tabla 2).
En caso de presentar TTPA prolongado con TP y hemograma normal en pacientes sintomáticos, se debe plantear la sospecha de un déficit de coagulación congénito.
Las características clínicas de ambas hemofilias son similares: hemorragias espontáneas, hematomas musculares, artropatía hemofílica, entre otros. Es por ello que surge la necesidad de tratamiento con el factor deficiente, para así evitar secuelas incapacitantes e incluso mortales.
Hasta la década de los años 60, los pacientes hemofílicos eran tratados con sangre o plasma, pero debido a la baja concentración del factor era necesario utilizar grandes cantidades lo cual podría generar hipervolemia. Posteriormente, al refinar la técnica, los productos obtenidos lograban mayores concentraciones en menores volúmenes y sin tantos riesgos de reacciones anafilácticas. La inmunoprecipitación con anticuerpos monoclonales para aislar estos factores del plasma fue desarrollada alrededor de 1982, y aún continúa siendo un mecanismo para la obtención de los factores.
El aislamiento y clonación de los genes que producen el factor VIII y IX fue desarrollado recién en 1984 y 1985 respectivamente, y a partir de ese momento la ingeniería recombinante hizo posible la síntesis de estos factores evitando la contaminación con agentes patógenos externos.
El tratamiento en la actualidad está basado en la administración intravenosa del factor, ya sea de manera profiláctica o bajo solicitud. Las opciones del tratamiento pueden ser de productos derivados del plasma bajo inmunoprecipitación, tratados con calor y detergente para inactivar agentes patógenos o factores de origen recombinante carente de proteínas humanas. (Liras & Romeu, 2019)
Existen varios esquemas para tratar estos pacientes, dentro de los cuales se destacan los siguientes debido a su nivel de evidencia:
Profilaxis primaria: Consta en una terapia a largo plazo y de forma regular, el cual se administra antes del inicio del daño articular y comienza antes de la segunda hemartrosis.
Profilaxis secundaria: Al igual que la profilaxis primaria, es una terapia regular y continua, que se establece luego de la segunda hemartrosis o después de los dos años.
Profilaxis transitoria: Administrado para prevenir sangra miento por periodos no mayor a 45 semanas, se utiliza en pacientes con sangrado a repetición en periodos cortos de 4 a 8 semanas.(Srivastava et al., 2013a)(Hua et al., 2016)(Peters & Harris, 2018)
Caso clínico
Al postgrado de Cirugía y Traumatología Bucomaxilofacial de la Universidad Andrés Bello acude un paciente de sexo femenino, de 18 años, derivada para realizar exodoncia de terceros molares debido al término de su mecánica ortodóntica. Al realizar la anamnesis próxima se consignó que la paciente presenta como antecedente médico hemofilia tipo A leve, donde relató haber presentado un 38% del factor VIII hace 6 meses. En sus antecedentes familiares, relata que su padre es hemofílico Tipo A, operado de ambas articulaciones de rodilla. No se encontraba en tratamiento médico en la actualidad, no relataba episodios de alergia, ni antecedentes ginecológicos relevantes tales como menarquia prematura, menorragia y/o abortos espontáneos, el cual reflejaba un control adecuado de la patología.
Dentro de los antecedentes odontológico-quirúrgico relató una exodoncia de un supernumerario sin complicaciones.
Al consignar signos vitales, la paciente se presentó normocárdico, eupneico y una presión arterial de 122/80 mmHg.
En el examen físico segmentario de cabeza y cuello, no se apreció alteraciones de ningún tipo y en el examen bucal, solo se pesquisó gingivitis asociada a placa. y dentición permanente completa con contención lingual en grupo V.
En base al motivo de consulta, se apreció el diente 1.8 erupcionado completamente, el diente 2.8 se encuentró semi-erupcionado, y, tanto el diente 3.8 como el diente 4.8, se observaron semi-erupcionados en posición horizontal e impactados y el capuchón pericoronario de ambos dientes se apreció sin edema ni salida de contenido de ningún tipo.
Tabla 3 Valores recomendados según procedimiento a realizar
| Procedimiento | Nivel del factor (% de actividad - UI/ml) |
| Bloqueo anestésico local | Entre un 20 a un 40% |
| Extracciones dentales | Entre 50 a 75% |
| Valor de referencia | Entre 50 a 150% |
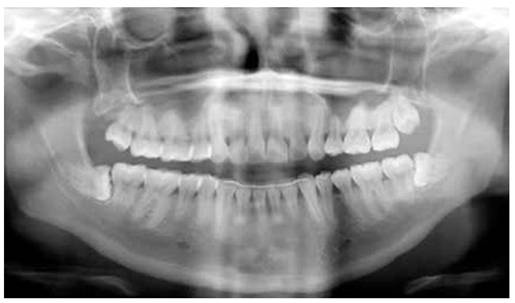
Como examen complementario se solicitó una ortopantomografía (figura N°1), en el cual se aprecia densidad ósea, número de raíces y la posición de los terceros molares respecto a estructuras anatómicas cercanas de relevancia.
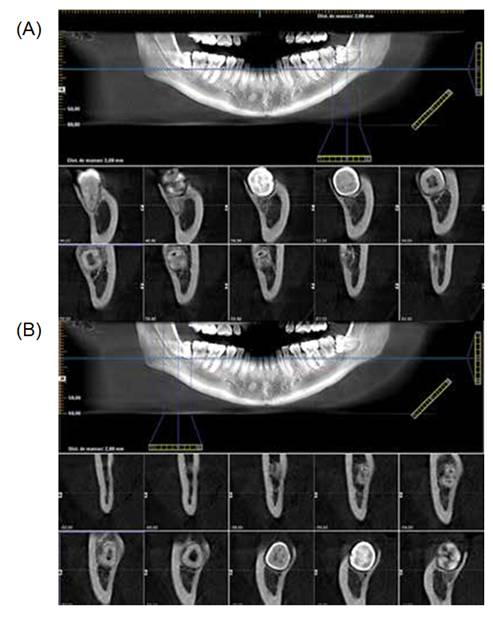
Los dientes 1.8 y 2.8 se apreciaron horizontales y con pérdida de la cortical superior del canal mandibular, así como ápices abiertos. Por este motivo, se solicitó además como examen complementario un cone beam (CBCT) en el cual se determinó la cercanía de las raíces de los terceros molares inferiores en relación con el nervio dentario inferior (figura N°2).
Con los antecedentes clínicos y radiográficos obtenidos, se consideró que el diagnóstico definitivo de los terceros molares 2.8, 3.8 y 4.8 es dientes semi-incluidos. 1.8 completamente erupcionado.
Plan de tratamiento
Se realizó una interconsulta con el hematólogo tratante para pedir indicaciones prequirúrgicas para realizar el procedimiento de desinclusión en ambiente ambulatorio. El tratante indicó la administración de 1.000 U.I. de liofilizado de factor VIII, una hora antes del procedimiento, endovenoso; así como al día siguiente y subsiguiente del procedimiento. Además, se recetó ácido tranexámico 500 mg, comprimidos, 1 comprimido cada 8 horas por 7 días.
Por otro lado, se solicitó un hemograma completo, el cual no presentó alteraciones en sus resultados y el tiempo de tromboplastina parcial activado, el cual dio un resultado de 29 segundos, correspondiente a un valor dentro de estándares normales.
De acuerdo con el protocolo de pabellón quirúrgico ambulatorio de la universidad, se administró 1 g de Cefazolina, 4 mg de Dexametasona y 1 g de Paracetamol de forma endovenosa 30 minutos antes de la intervención quirúrgica.
En el intraoperatorio se realizó monitorización de signos vitales no invasiva durante toda la intervención, antisepsia en piel con clorhexidina gluconato 2% y antisepsia oral con colutorio de clorhexidina gluconato 0.12%. Se utilizó técnica anestésica local con lidocaína 2%, 1:100.000 epinefrina. Para la exodoncia del diente 1.8, se realizó anestesia infiltrativa vestibular 1.8ml y se complementó con anestesia infiltrativa palatina 1.8ml, se realizó sindemostomía, se logró decolar la encía con legra Molt, la luxoavulsión se realizó con elevador recto mediano, y finalmente se realizó el acondicionamiento alveolar y síntesis con seda 3-0 con punto simple.
En lo que respecta al diente 2.8, se realizó anestesia infiltrativa vestibular 1.8ml y se complementó con anestesia infiltrativa palatina 1.8ml, se realizó un colgajo crevicular lineal distal con bisturí frio y hoja N°15, sindesmotomía, luxoavulsión con elevador recto media- no, acondicionamiento alveolar, reposicionamiento de colgajo y síntesis con seda 3-0, también con punto simple. En los dientes 3.8 y 4.8, se anestesió con técnica spix bilateral, 2 tubos de 1.8ml cada uno, cada lado respectivamente, donde se realizó en ambos un colgajo crevicular con descarga distal con bisturí frio y hoja 15, decolado mucoperiostico, osteotomía y odontosección de ambos dientes con micromotor, finalizando con desinclusión de ambos dientes con elevador recto mediano, se deja esponja hemostática en ambos lechos quirúrgicos y la reposición del colgajo se realizó mediante puntos simples con sutura seda 3-0. Se logra hemostasia y se finaliza el pabellón sin incidentes.
En cuanto al manejo postoperatorio, se entregaron indicaciones de forma oral y escrita similares a las de una extracción simple. Se informó a la paciente sobre las posibles hemorragias postoperatorias, así como la posible formación de hematomas. Se indicó aplicación de frío local cada una hora en períodos de 20 minutos por una duración de dos días, además, para el control del dolor de recetó 1 g de Paracetamol cada 8 horas durante 5 días y se citó a control en un periodo de 48 horas, 5 días y a los 7 días.
Al controlar al paciente a las 48 horas, 5 y 7 días, se observaron los lechos quirúrgicos en proceso de cicatrización normal. A los 7 días se hizo retiro de la sutura y se dio de alta.
Discusión
A nivel nacional, las guías ministeriales de Chile (“Guía clínica de urgencias odontológicas”, 2011) solo nos propone que este tipo de pacientes debe ser tratado en centros hospitalarios en conjunto con hematología. Mientras que la guía de la Federación Mundial de la Hemofilia (WFH) (“Guidelines for the management of hemophilia”, 2012) nos menciona que el manejo debe ser en conjunto con el hematólogo, tomando en cuenta el riesgo hemorrágico del paciente, el tipo y severidad del desorden congénito, y el tipo de cirugía oral a realizar. (Anderson et al., 2013)
Dentro de las estrategias sugeridas por la guía clínica británica (“Guidance on the dental management of patients with haemophilia and congenital bleeding disorders”, 2013) nos menciona que en general el manejo de estos pacientes es:
Terapia de reemplazo del Factor de la coagulación
Liberación de depósitos de factor VIII endógeno utilizando desmopresina
Mejorar la estabilidad del coágulo mediante fármacos antifi- brinolíticos, por ejemplo, ácido tranexámico
Manejo de la hemostasia local, tanto con sutura como compre- sión de la zona intervenida
El tratamiento no quirúrgico puede ser realizado sin problemas, ocasionalmente se puede utilizar agentes antifibrinolíticos.
Con respecto a la utilización de anestésico locales no hay restricciones en cuanto al tipo de agente anestésico local utilizado, aunque se recomienda la utilización de vasoconstrictores ya que nos entregan hemostasia local adicional. Otro punto importante es la inoculación lenta, lo que permite una correcta difusión en los tejidos. (Bravo, 2012)
Al momento de hacer un bloqueo anestésico troncular y una exodoncia, es importante conocer los niveles mínimos necesarios para realizar el procedimiento de forma segura (tabla 3)
Respecto al manejo farmacológico del dolor de estos pacientes, WFH en su guía (“Guidelines for the management of hemophilia”, 2012) señala que, como primera instancia, para dolor agudo, es recomendable utilizar paracetamol/ acetaminofeno, en caso de que el dolor no disminuya, como segunda línea, se recomienda el uso de los inhibidores de la Cox-2, con el fin de no interferir con el proceso de homeostasis vascular, como es el caso de Celecoxib y Meloxicam.
Conclusión
Es fundamental el conocimiento y manejo multidisciplinario de las discrasias sanguíneas de parte del cirujano dentista, ya que diversos tratamientos que se realizan en la cavidad oral activan procesos hemostáticos, especialmente en los tratamientos cotidianos, como es el caso de la extracción dental.
La hemofilia, es un trastorno que requiere un minucioso manejo tanto pre, intra y postoperatorio de parte del odontólogo, donde los exámenes complementarios, comunicación con el hematólogo, procedimiento atraumático y un correcto manejo de la hemostasia, son fundamentales para el éxito del tratamiento.
Anexo
Recomendaciones posteriores a cirugía de terceros molares
Morder la gasa por lo menos por 30 minutos y luego sacarla con mucho cuidado.
En caso de sangrar más de lo normal, colocar y apretar nuevamente un algodón seco y limpio en el lugar de la extracción.
No escupir.
No enjuagarse ni hacer buches con ningún tipo de líquido (in- cluyendo enjuague bucal).
No comer cosas duras mientras dure el efecto de la anestesia.
No fumar ni beber alcohol durante al menos 3 días.
Alimentación blanda y líquida por 2 días. Masticar del lado contrario a la extracción.
No consumir alimentos calientes, idealmente tibios o temperatura ambiente al menos por 48 horas.
No aspirar, no succionar. (No utilizar bombillas).
No realizar ejercicios físicos ni esfuerzos durante 48 horas, para evitar sangrado.
Mantener buena higiene bucal, cepillado habitual menos en el área de la extracción (3 veces en el día).
En extracciones complicadas, colocar compresa con hielo en las primeras 24 horas.
En caso de dolor fuerte, mal olor o aumento de volumen consultar a urgencia dental.
Consumir la medicación en los horarios indicados por el tratante.
Asistir a los controles.
**Informar inmediatamente al odontólogo la aparición de sangrado prolongado y/o dificultad para hablar, tragar o respirar.
Autores:
Parada F1, Fonseca D1, Palavecino F2, Farías M1, Hill S3, Montero S4
1.- Cirujano Dentista, Universidad Andrés Bello, Santiago de Chile
2.- Residente postgrado Cirugía Maxilofacial, Universidad Andrés Bello, Santiago de Chile
3.- Estudiante de odontología, Universidad Andrés Bello, Santiago de Chile
4.- Cirujano Maxilofacial, Docente pre y postgrado, Universidad Andrés Bello, Santiago de Chile.
CHILE