Introducción
El manejo de un ápice en proceso de formación, es complicado desde el punto de vista dental. Una serie de factores hace que tal situación sea difícil, influyendo la corta edad del paciente, la consecuente falta de cooperación, raíces cortas y conductos muy amplios, entre otros. (Cortés, M. y cols. 2002).
También se debe recalcar que el potencial de respuesta, diferenciación y formación de las células relacionadas con pulpa, cuando el ápice se encuentra abierto, es muy alto. Esto convierte a la pulpa en un importante reservorio de células indiferenciadas con capacidad de respuesta ante eventos adversos de gran tamaño. (Murray, P. y cols.2007).
Quitar el dolor en un paciente pediátrico es usualmente complicado, pero este es otro aspecto que no se debe obviar durante la consulta. Es preciso tener buena comunicación con él y con los padres de familia.
Así también, es importante hacer ver a los familiares que los tratamientos que implican el cierre apical, en su mayoría requieren múltiples citas. (Cortés, M. y cols. 2002).
Objetivo
Demostrar el potencial de supervivencia y capacidad de diferenciación de las células madre a nivel dental, mediante un caso clínico que se orientó hacia la revascularización.
Marco teórico
En 1961 Ostby describió por primera vez el procedimiento de revascularización, mencionando que el nuevo tejido vascularizado podría inducir la formación de la porción apical en piezas con necrosis y lesiones apicales. Esta teoría también mostró la importancia de crear un coágulo, que funcione como base o andamiaje y provea soporte al nuevo tejido en formación. (Ostby, 1966).
Más tarde, en 1966, se destaca la necesidad de desinfectar el conducto con una pasta antibiótica a la hora de realizar la apexificación, y fue la primera vez que se menciona la utilización intraconducto, de medicamentos en este tipo de procedimiento. (Rule y Winter, 1966).
También en 1966, se describió una técnica para lograr el cierre apical, la cual implicaba el uso repetido de hidróxido de calcio. La técnica describía cambios de hidróxido de calcio aproximadamente cada 3 a 6 meses. (A. L. Frank, 1966).
En 1972, se logró demostrar en dientes de monos, desvitalizados, el cierre apical. Se describió como un tejido granulomatoso, el cual generó la estimulación de las células cementoblásticas y mesenquimatosas a nivel del periápice, creando el depósito de material cálcico en el ámbito apical y en las paredes dentinales. (Ham y cols,1972). Torneck y colaboradores describieron, en una serie de artículos, que el cierre del ápice no se daba del todo, debido a la aplicación del hidróxido de calcio, sino también a la estimulación de la papila residual y las pocas células que allí habían sobrevivido luego de la infección. (Torneck y cols. 1970 - 1973).
Por otro lado, la técnica de apexificación tiene una desventaja: el número de visitas que se requiere para lograr buenos resultados.
Recientemente, se ha descrito el procedimiento en una sola cita con la utilización de mineral trióxido agregado (MTA), el cual la hace más previsible en comparación con los recambios de hidróxido de calcio. (Torabinejad y cols 1999).
Una serie de estudios posteriores demostró que la técnica con MTA era lo suficientemente previsible y una opción razonable en sustitución del hidróxido de calcio, además de ofrecer una cicatrización muy favorable. (Simón, S. y cols. 2007). (Mente, J. y cols. 2009).
La revascularización como tal, es una importante opción para dientes no vitales con ápices abiertos e incluso avulsionados. Lo que se procura lograr con este tipo de tratamiento es el cierre del ápice pero de forma natural, de manera que la principal ventaja que brinda es conseguir un engrosamiento de las paredes radiculares, objetivo que no es posible con otras técnicas. Al mismo tiempo, se cree que cuanto mayor sea el diámetro del foramen, mejor pronóstico tiene la técnica, pues hay mayor posibilidad de restablecer el nuevo tejido por medio del abastecimiento sanguíneo.(Kling M. y cols, 1986). (Skoglund A, y cols. 1981).
Por mucho tiempo se pensó que este tratamiento era ideal y casi exclusivo para pacientes jóvenes.
Sin embargo, conforme esta técnica se ha implementado cada vez más, se ha empezado a utilizar en gentes de edad más avanzada. En un estudio efectuado en 2015, se realizó un tratamiento a una mujer de 39 años de edad. Las piezas fueron dos premolares inferiores que presentaban necrosis pulpar, con radiolucidez extensa y ápices abiertos. Se utilizó plasma rico en plaquetas como andamiaje. Después de un seguimiento de 30 meses la lesión desapareció y la paciente estaba asintomática. (Wang, Y. y cols. 2015).
El término revascularización fue introducido en el 2001. Iwaya realizó estudios donde tomó segundas premolares mandibulares con necrosis y el ápice inmaduro con presencia de un absceso apical crónico y demostró que después de 30 meses había engrosamiento de las paredes del conducto, además de continua formación de la raíz. (Iwaya SI, y cols. 2001).
Trope y colaboradores mencionan que sí es posible revascularizar piezas dentales con importantes lesiones a nivel apical. La técnica, como tal, comienza con una serie de mejoras como la aplicación del lavado con hipoclorito de sodio y gluconato de clorhexidina, y finalmente se sella con una pasta tri antibiótica.
Luego de 24 meses, los resultados mostraron un desarrollo radicular muy similar al de la pieza adyacente y contralateral. A partir de este momento, se introdujo un nuevo protocolo en la técnica de revascularización en piezas desvitalizadas e infectadas con ápice inmaduro.(Banchs F., Trope M. 2004).
El procedimiento se describió como simple, económico y con adaptabilidad a los instrumentos actuales y medicamentos disponibles en el mercado.(Murray P y cols. 2007).
El uso del término revascularización ha estado en discordia.
Algunos autores sugieren otros nombres, como madurogénesis o revitalización. Sin embargo, se ha mencionado un término más generalizado como lo es la endodoncia regenerativa. La Asociación Americana de Endodoncia (AAE por sus siglas en inglés), define la endodoncia regenerativa como:
“procedimiento con base biológica diseñado para reemplazar fisiológicamente estructuras de diente dañado, incluyendo la dentina y estructuras de la raíz, así como las células del complejo dentino pulpar”(Lenzi R., Trope M. 2012) (Weisleder R, Benítez CR. 2003) (Patel R, Cohenca N. 2006).
En la endodoncia regenerativa y en el proceso de revascularización hay muchas estructuras que juegan un papel primordial. Se describió la posible importancia de las células indiferenciadas que se encuentran a nivel del ligamento periodontal, lo que podría explicar por qué en algunas ocasiones se ha detectado formación de cemento en las paredes del conducto. (Huang. 2008).
También, se ha descrito que el sangrado que se produce a nivel del ápice es capaz de llevar células mesenquimatosas. Aunque la fuente primaria de estas células no está bien definida, se piensa que pueden ser originadas por el tejido adyacente al ápice y no por la circulación sanguínea propiamente. (Lovelace y cols. 2011).
Se ha comprobado mediante estudios histológicos en dientes diagnosticados con pulpitis irreversible y luego de la remoción del tejido vásculo-nervioso que presentaron una vez realizada la técnica de revascularización ensanchamiento de las paredes radiculares, así como evidencia radiográfica de alargamiento radicular, tejido semejante a pulpa y a dentina (Peng C. y cols. 2017).
Artículos recientes mencionan que el hecho de que haya radiolucidez a nivel del ápice de una pieza dental y ausencia a la respuesta térmica o eléctrica, no se puede considerar más como un determinante en sí, haya o no, vitalidad pulpar.
En ambas situaciones puede haber presencia de células indiferenciadas y de la papila apical. (Wigler R. y cols. 2013).
La técnica de revascularización ha ido tomando más presencia en las prácticas clínicas conforme más estudios demuestran su éxito. Uno de los estudios más actualizados lo demostró en un diente que se indujo a la revascularización luego de ser autotrasplantado. Sin embargo, hacen falta más estudios similares a estos y un mayor seguimiento para validar los resultados de este caso en particular. (Jakse N y cols. 2018).
Los pasos de la técnica de revascularización actual son los siguientes: en la primera cita, se debe evaluar el caso y obtener el consentimiento informado del paciente. El diente tiene que ser anestesiado y se debe colocar el dique de hule como aislamiento.
Luego, hay que realizar el acceso a la cámara pulpar seguido de irrigación. La remoción de todo el tejido necrótico y bacteriano es vital para el éxito de la terapia de revascularización. La remoción mecánica está contraindicada. (Cvek M. 1992).
Una lima manual de forma pasiva o una gutapercha, puede ser introducida al conducto, con el propósito de determinar la longitud de trabajo (Chen MY. y cols. 2012).
La solución irrigadora que se deberá utilizar es 20 ml de hipoclorito de sodio al 2,5% con una jeringa de calibre 20. El hipoclorito es un potente agente antimicrobiano el cual tiene la capacidad de disolver tejido orgánico e inorgánico (Chueh LH. y cols. 2006).
Sin embargo, se debe tener especial cuidado en no utilizar concentraciones demasiado altas de hipoclorito de sodio, pues la toxicidad del irrigante puede generar daños a nivel del periápice y células indiferenciadas (Stojicic S. y cols. 2010).
Algunos estudios han demostrado que la supervivencia de las células madre presentes en la papila apical expuestas a hipoclorito de sodio a concentraciones de 6%, seguido de EDTA al 17% y luego nuevamente hipoclorito de sodio al 6%, fue de un 74% (Trevino EG, y cols. 2011).
En la técnica se recomienda introducir la jeringa de irrigar 2 mm antes del ápice, para evitar el riesgo de dañar las células del periápice. (Parirokh M. y cols. 2010).
Luego de la irrigación inicial, se debe irrigar 5ml de solución salina, con el fin de prevenir la interacción entre el hipoclorito de sodio y el gluconato de clorhexidina al 2% el cual se utiliza como último lavado.
La aplicación de esta última irrigación ayuda, debido al efecto de sustantividad. (Haapasalo M y cols. 2010).
Una vez concluida la irrigación, se debe secar los conductos con puntas de papel estériles. Se tendrá que colocar una medicación intraconducto. La pasta debe ser colocada hasta 2 mm antes del foramen apical. Estos dos últimos milímetros permitirán el espacio suficiente para la formación del nuevo tejido.(Bose R. 2009).
El objetivo de utilizar la pasta intraconducto es disminuir significativamente la carga bacteriana que podría estar presente en los conductos. Hoshino y colaboradores introdujeron la pasta triantibiótica, la cual implicaba tres componentes con una misma dosis de cada componente (250 mg de ciprofloxacina, metronidazol, yminociclina, mezclada en solución salina). Posteriormente, se eliminó la minociclina debido a que causaba pigmentación, y se sustituyó por cefaclor (Hoshino y cols. 1996)(Reynolds K y cols. 2009).
La pasta antibiótica debe ser insertada en el conducto con la ayuda de un léntulo. Una vez colocada, se tiene que empacar utilizando una torunda de algodón. La pasta debe llegar 2mm antes del foramen apical y hasta la unión amelo-cemento. (Banchs F., Trope M. 2004).
Diversos estudios muestran la biocompatibilidad de la pasta triantibiótica propuesta por Hoshino. (Gomes-filho y cols. 2012).
No obstante, hoy en día la utilización de hidróxido de calcio en revascularización es bien aceptada.
Sin embargo, ciertos autores advierten que el alto pH del hidróxido de calcio 12,5 tiene potencial de toxicidad, lo cual podría dañar las células que se encuentran a nivel del ápice. Igualmente otros autores aducen que se puede inducir una calcificación descontrolada. (Huang GT, 2008).
La utilización del hidróxido de calcio en apexogénesis ha sido apoyada a lo largo de muchos años, y se le concede el potencial de material estimulador de tejido duro. En muchos casos, cuando el paciente es alérgico a algunos de los componentes de la pasta triantibiótica, se recomienda el uso de hidróxido de calcio.(Chen MY et ál. 2012).
Diversos autores advirtieron la utilización del hidróxido de calcio en la terapia de revascularización cuando la pasta se deja en el tercio medio y cervical. Los resultados observados fueron exitosos y con ausencia de sintomatología. Se destaca que el acceso debe ser sellado con CavitTM (3M) y la pasta tiene que permanecer en el conducto como mínimo 7 días.(Chen MY y cols. 2012). (Cehreli, 2011).(Jung IY y cols. 2008).
En la cita número dos se evalúa el procedimiento. En caso de dolor se recomienda manejar el tratamiento como una apexificación. (Huang GT, 2008).
El diente debe estar anestesiado y bajo aislamiento con dique de hule. Se recomienda anestesia sin vasoconstrictor para evitar daño al riego sanguíneo a nivel apical. (Miller y cols. 2012).
Luego de remover la restauración temporal, la medicación intraconducto se elimina por medio de irrigación utilizando 20 ml de hipoclorito de sodio al 2,5%. A diferencia de la irrigación en la cita uno, en la segunda cita final se hará únicamente con 10ml de EDTA al 17%, con el propósito de abrir los túbulos dentinarios y crear mayor exposición de las fibras colágenas. (Galler KM, y cols. 2011).
Se demostró que la clorhexidina no permite una formación del andamiaje natural inicial a nivel de ápice, el cual es un paso muy importante en el éxito de la revascularización.(Trevino EG. y cols. 2011).
El andamiaje es parte fundamental en la revascularización, ya que genera un tejido base, el cual induce y guía la formación de tejido nuevo regenerativo. Este andamiaje se lleva a cabo por medio de la creación de un coágulo. Utilizando una lima estéril de calibre #20 más allá del ápice (2mm) se provoca el sangrado; este coágulo junto con las células que queden adheridas a las paredes del conducto, es la base imprescindible en el proceso de revascularización.(Thibodeau B. y cols. 2007).
El sangrado que se provoca debe ser controlado, limitándolo a 3 mm antes de la unión amelo - cemento.
El tiempo aproximado para establecer el coágulo es de alrededor de 15 minutos. (Jung IY. y cols, 2008).
Finalmente, se sella con MTA hasta llegar a la unión amelo - cemento.
Se coloca una torunda estéril húmeda de algodón sobre el material y se sella de forma provisional.(Wigler R, y cols, 2013).Se acepta también usar otros biocerámicos.
Se ha comprobado en estudios que el MTA es un material ideal para este tipo de tratamiento. En un estudio se demuestra la tasa de éxito del MTA en procedimientos de revascularización, ligeramente mayor en comparación con tratamiento de apexificación donde de igual manera se utilizó MTA.(Siluijai J. 2017).
En la tercera cita, se remueve la torunda de algodón y se coloca una restauración permanente.(Thibodeau B. y cols, 2007).
Informe de caso clínico
Hace ocho años y siete meses, se presentó a la consulta privada un paciente masculino de 7 años de edad, referido por una especialista en odontopediatría.
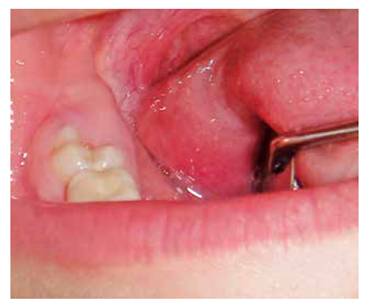
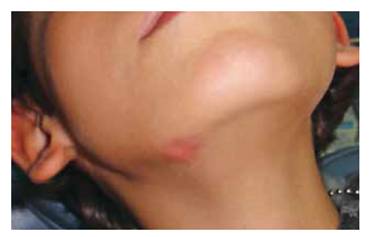
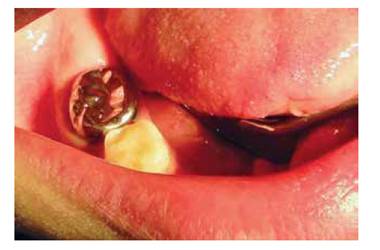
La pieza 4.6 se encontraba parcialmente erupcionada(Figura 1). A la vez, se observa cicatriz de drenado por tejido suave a nivel submandibular (Figura 2)luego de estar internado en el hospital con antibiótico de amplio espectro vía intravenosa.
No hay evidencia clínica a nivel oclusal de importante caries (nótese en la Figura 1). Sin embargo la toma radiografía periapical evidencia presencia de caries dental profunda.(Figura 3).
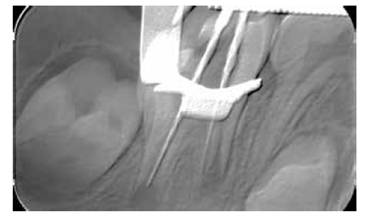
En la primera cita, se procede a anestesiar al paciente con la técnica mandibular y dos carpules de lidocaína al 2%. Se elimina el tejido gingival que cubre el área disto- oclusal de la pieza. Se aísla y se procede a realizar el acceso. Se irriga con clorhexidina al 2%. Se instrumenta con limas manuales tipo K #40 y la ayuda de limas gates #2 y #3 en la entrada de los conductos (Figura 4).
Se coloca hidróxido de calcio con yodoformo-Vitapex®- dentro de los conductos a longitud de 13,5 mm el conducto distal y 15 mm el conducto mesial. No se logra encontrar el segundo conducto en mesial.(Figura 5).
En la segunda cita, se realiza cambio del material intraconducto, (Vitapex®), para un total de tres cambios en un período de tres meses.
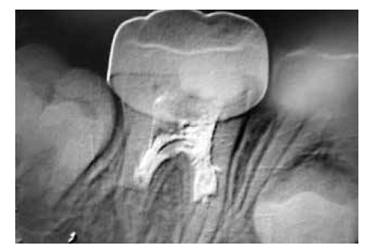
Posteriormente el paciente no vuelve a la clínica y no es hasta luego de 10 meses que asiste a consulta pues se le fractura la corona. Se le reconstruye con un biocerámico (Biodentine®). Sin embargo, se evidencia por medio radiográfico el proceso de formación radicular.(Figura 6).
El paciente se ausenta y regresa 22 meses después, encontrándose asintomático. Por medio radiográfico se observa el avance en la formación radicular.(Figura 7).
A los 4 años y 7 meses de iniciado el tratamiento, se realiza un seguimiento y se da una clara evidencia de la formación de la raíz y la ausencia de lesión a nivel apical; el paciente se encuentra asintomático y con su pieza dental funcional.(Figura 8).
A los seis años, en otra cita de control del paciente, se observan los ápices bastante formados y que ya le colocaron -de parte del referidoruna corona completa metálica, para proteger la pieza dental de una posible fractura.(Figuras 9 y 10).
Después de 8 años de realizada la revascularización, la pieza está asintomática; sin embargo, se observa cierta radioopacidad en raíz distal;se decide no intervenir y dar seguimiento a distancia.(Figura 11).
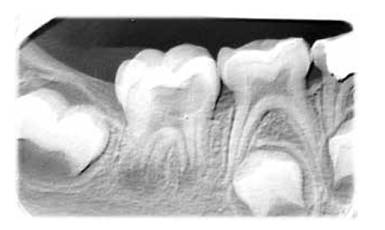
Figura 3. Radiografía periapical, donde se observa presencia de caries profunda y formación de un tercio radicular
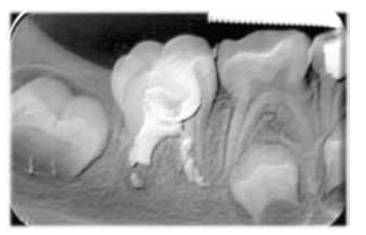
Figura 5. Radiografía periapical donde se muestra en la primera cita la colocación de hidróxido de calcio e yodoformo (Vitapex) intraconducto
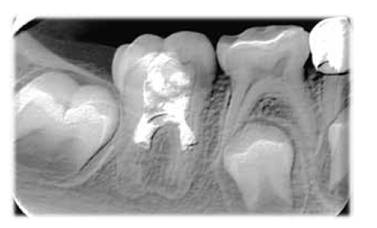
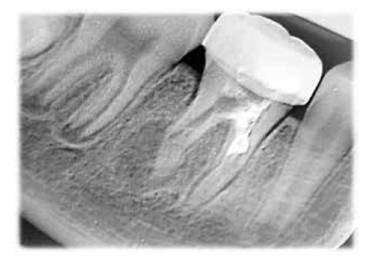
Figura 6. Radiografía periapical donde se muestra la reconstrucción con material biocerámico (Biodentine®) y se evidencia el proceso de formación radicular
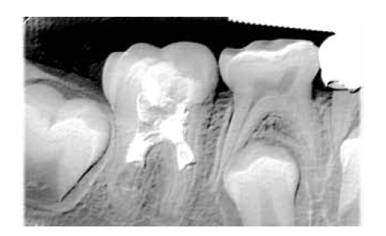
Figura 7. Radiografía periapical 22 meses después de la última cita. Paciente se encuentra asintomático y con avance en la formación radicular
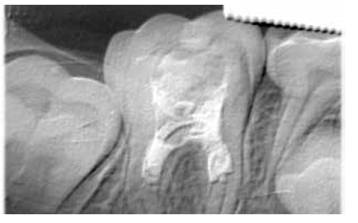
Figura 8. Radiografía periapical control a los 4 años y 7 meses del tratamiento. Nótese en la imagen el tercio apical completo y con ausencia de lesión apical
Discusión
A pesar de que el caso anteriormente expuesto no siguió los pasos que actualmente advierte el tratamiento de revascularización, se evidencia que hay una formación de las raíces. Por consiguiente, se considera que quizás el éxito en el procedimiento de revascularización se basa en reducir significativamente la presencia de bacterias en el área como lo mencionan diversos autores. (Hoshino y cols. 1996).(Reynolds K y cols. 2009).
El uso del hidróxido de calcio ha sido criticado por diversos autores. Branchs F. y Trope M. mencionaron la falta de utilización del hidróxido, para lograr preservar cualquier remanente de tejido pulpar viable y la vaina epitelial de Hertwig, dado que por su alto pH puede provocar necrosis de los tejidos que logran diferenciarse.(Branchs F, Trope M. 2004).
Sin embargo, estudios más recientes avalan la utilización del hidróxido de calcio. Este caso clínico logra evidenciar el potencial de formación e inducción tan importante que tiene el hidróxido de calcio. (Chen MY. y cols. 2012).(Cehreli ZC. y cols. 2009). (Iwaya SI. y cols. 2001). (Neha K y cols. 2011).
La clorhexidina ha sido otro punto donde diversos autores no comparten opinión; se menciona que su uso puede ocasionar un daño a las células indiferenciadas pues causa fallas en el andamiaje que se procura crear dentro del conducto.(Trevino EG. y cols. 2011).
El uso de la clorhexidina en este tipo de procedimientos y con base en lo visto en este caso clínico, no es perjudicial; la baja citotoxicidad, precisamente, y el poco daño informado, hacen que pueda ser un material por tomar en cuenta en la terapia de revascularización. Y artículos publicados muestran el éxito de la terapia utilizando clorhexidina como irrigación. (Reynolds K. y cols. 2009). (Shin SY. y cols. 2009).
El hecho de que se haya dado un drenaje extraoral, sumado al empleo de antibióticos de amplio espectro vía intravenosa, pudo haber ayudado a la reducción bacteriana y a mantener la viabilidad de las células indiferenciadas a nivel de la papila apical.
Si bien es cierto se buscó en principio solamente el selle a nivel apical, lo más importante de resaltar fue que no solo hubo un cierre, sino que la formación de la raíz continuó pese a que no se utilizó pasta antibiótica ni se intentó a propósito realizar la formación de un coágulo apical, y en relación con el andamiaje, si bien es cierto que se utilizó el Biodentine®, no fue planeado. Con base en estos resultados es importante destacar que quizás la introducción de las limas al conducto generó un coágulo y la posterior colocación del Vitapex, por su consistencia pastosa, logró la formación de un andamiaje suficiente para generar un proceso de revascularización.(Thibodeau B. y cols. 2007).
Recientes estudios informan calcificaciones intraconducto de dientes luego de la revascularización.(Song M. y cols. 2017).El estudio describe una incidencia de un 62,1% de calcificaciones intraconducto.
Entre los factores que podrían producirlas se menciona el tipo de medicamentos que se utilizó durante la terapia, así como la inducción del sangrado. Sin embargo, se sugiere que este tipo de calificaciones o proceso no interfiere en el correcto sanado de las lesiones periapicales presentes en este tipo de tratamiento.
Conclusiones
La revascularización como tal es un proceso que aún hoy en día es impredecible.
Seguir la técnica paso a paso como se describe, no garantiza el éxito del tratamiento. Pero como se evidenció, también hay otros caminos mediante los cuales se logra el éxito y la formación de las raíces en las piezas dentales. El hidróxido de calcio es un material que presenta una capacidad de inducción muy importante, y no debe ser descartado.
Luego de un seguimiento de 8 años y 2 meses en el caso descrito, se puede concluir que está en vías de éxito desde el punto de vista endodóntico.