Prólogo
Cardio-imaging es una sección de la Revista Costarricense de Cardiología, orientada a la difusión de casos clínicos en los cuáles la imagen cardiovascular ha demostrado un papel preponderante en el diagnóstico, pronóstico y/o terapéutica de una determinada patología cardíaca. Además, está diseñada para la difusión de imágenes cardíacas de gran interés, ya sea por la aplicación de nuevas técnicas, por la rareza de la patología, por la dificultad en obtenerlas, o simplemente por el hecho de ser un buen ejemplo para otros colegas con situaciones clínicas similares. Siendo el pilar fundamental la ecocardiografía (y sus múltiples variantes), esta sección está abierta a casos que involucren el uso de la tomografía cardíaca, la resonancia magnética cardíaca, la medicina nuclear cardiológica y la hemodinamia.
El caso clínico es acerca de un hombre de 46 años, de la zona sur del país, comerciante, y sin patologías crónicas conocidas, hasta la presentación de su padecimiento actual (Fig. 1). Con el antecedente de un procedimiento dental no especificado 15 días antes, presenta un cuadro subagudo de fiebre de 38-39°C de predominio vespertino, asociado a fatiga, cansancio, malestar general e hiporexia. Luego de 2 semanas de síntomas persistentes, consulta en el servicio de emergencias del hospital de su localidad, y como parte de su exploración clínica inicial, se corrobora la presencia de fiebre (38.6°), y además se documenta la presencia de soplo cardíaco, con las siguientes características: sistólico, predominante en foco mitral, intensidad 4/6. No hay datos clínicos, hemodinámicos, o de laboratorio que sugieran la presencia de sepsis severa, respuesta inflamatoria sistémica severa o choque séptico. En vista de la ausencia de evidencia de algún otro foco séptico asociado (pulmón, orina, cerebro, tejidos blandos, gastrointestinal, COVID-19), se toman hemocultivos y se inicia terapia antibiótica empírica, bajo el diagnóstico presuntivo de endocarditis bacteriana.
Inicialmente se realiza ecocardiograma transtorácico, que documenta la presencia de masa móvil en la válvula mitral y en la pared de la aurícula izquierda, ambas compatibles con vegetaciones; de acuerdo a estos hallazgos, se procede a realizar ecocardiograma transesofágico 2D/3D, el cual se comentará detalladamente a continuación.
En el video N.º 1 y video N.º 2, correspondientes a una vista medio-esofágica del eje largo del ventrículo izquierdo, es posible observar una masa oscilante y móvil sobre la valva anterior de la válvula mitral, y otra masa de similares características ubicada sobre la pared interna de la aurícula izquierda, relacionada con la raíz de la aorta. Ambos hallazgos congruentes con vegetaciones. No parece existir compromiso de la fibrosa mitro-aórtica, ni de la válvula aórtica.
Adicionalmente, la valva anterior presenta un prolapso importante del segmento correspondiente a A2. En la vista en cámara lenta (video N.º 2), se puede apreciar la presencia de al menos 2 defectos de continuidad de la valva mitral anterior (uno proximal y otro distal), correspondientes a perforaciones (Fig. 2).
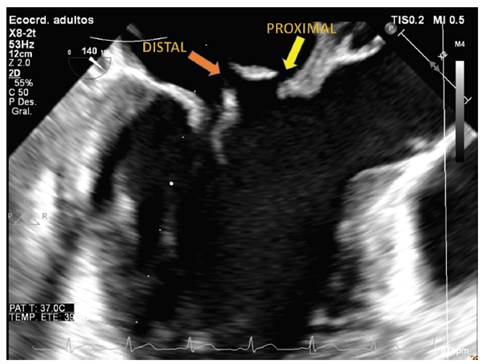
Figura 2 Fotograma de vista medio-esofágica del eje largo del ventrículo izquierdo; se observan 2 perforaciones en la valva mitral anterior.
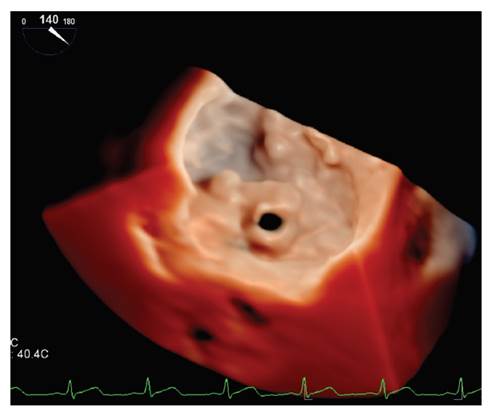
Figura 3 Fotograma de adquisición volumétrica 3D modo zoom de la válvula mitral, vista de cirujano, con técnica de transiluminación; se aprecia con gran definición la perforación distal de la valva anterior mitral (segmento A2).
En el video N.º 3 se aprecia que la insuficiencia mitral es severa, y se origina de 3 sitios diferentes: las 2 perforaciones, y el defecto de coaptación secundario al prolapso de la válvula mitral; fisiopatológicamente correspondiendo a los mecanismos I y II de Carpentier (dilatación anular, perforación valvular, prolapso). La visualización tridimensional del comportamiento del Doppler color también ejemplifica con claridad la severidad y los mecanismos de la insuficiencia mitral (video N.º 4).
La ecocardiografía transesofágica 3D permite caracterizar de mejor manera la patología degenerativa mitral que posee este paciente; en el vídeo N.º 5 se observa con claridad la perforación distal de la valva anterior (segmento A2), prolapso del segmento P1 (no visualizado previamente), y la vegetación mural en la aurícula izquierda. El video N.º 6 brinda las reconstrucciones multiplanares 2D de esta misma adquisición volumétrica.
La figura 3 muestra la aplicabilidad de la técnica de “transiluminación” sobre una adquisición volumétrica 3D, que permite una visualización diferente y más explícita de la perforación distal de la valva mitral anterior (segmento A2); también permite una definición anatómica de mayor calidad y nitidez respecto a la caracterización de los prolapsos valvulares (video N.º 7).
La ecocardiografía 3D también permite la manipulación omnidireccional de los bloques de datos volumétricos; gracias a esa característica, es factible observar la perforación proximal de la valva anterior mitral, la cual es un poco más pequeña y alargada (fusiforme) que la perforación distal (video N.º 8).
En base a los hallazgos ecocardiográficos, el diagnóstico es:
Endocarditis bacteriana complicada:
Vegetaciones en válvula mitral (segmento A2 predominantemente).
Vegetación mural en pared de aurícula izquierda (relacionada con la raíz de aorta).
Perforación doble de valva mitral anterior.
Insuficiencia valvular mitral severa, mecanismo de Carpentier I y II (perforación valvular, dilatación anular, prolapso).
Enfermedad degenerativa de la válvula mitral:
Degeneración mixomatosa leve.
Prolapso de segmentos A2 y P1.
“Forme-fruste”.
En vista de la llamativa estabilidad clínica del paciente, se decidió diferir el momento quirúrgico hasta completar 10-12 días de terapia antibiótica parenteral; al respecto, presentó un hemocultivo positivo por Streptococcus agalactie sensible a ampicilina y gentamicina. Posteriormente se llevó a sala de operaciones para reemplazo mitral mecánico N.º 29 y extirpación de la vegetación mural. La cirugía no tuvo complicaciones inmediatas, y el paciente tuvo un curso sin eventualidades en la Unidad de Cuidado Intensivo, y posteriormente en el Salón General. Curiosamente, el cultivo de la pieza quirúrgica fue positivo por Staphylococcus saprophyticus multisensible.
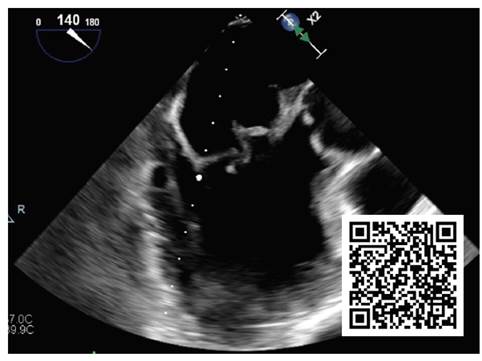
Video 1 Vista medio-esofágica del eje largo del ventrículo izquierdo; vegetación en valva mitral anterior y vegetación mural en aurícula izquierda.
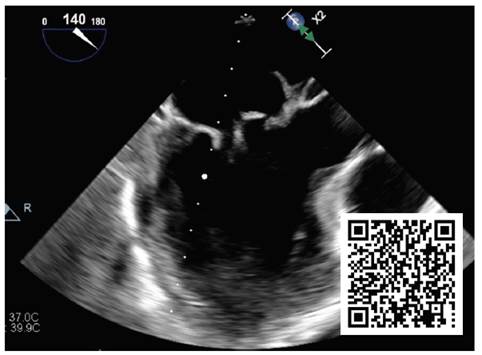
Video 2 Vista medio-esofágica del eje largo del ventrículo izquierdo (versión en cámara lenta); vegetación en valva mitral anterior y vegetación mural en aurícula izquierda; además prolapso de valva anterior.
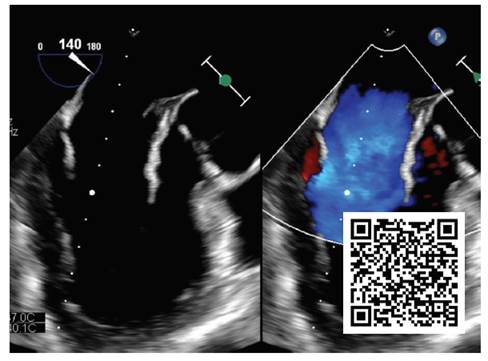
Video 3 Vista medio-esofágica del eje largo del ventrículo izquierdo, con Doppler color; la insuficiencia mitral es severa, y se origina de 3 puntos distintos (las 2 perforaciones, y el defecto de coaptación secundario a prolapso valvular).
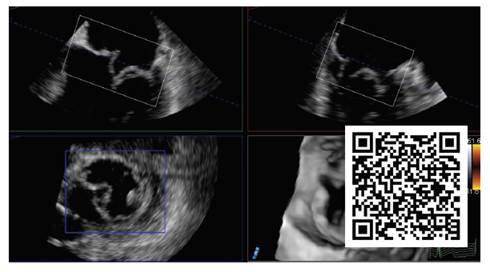
Video 4 Adquisición volumétrica 3D modo zoom de la válvula mitral, con reconstrucción multiplanar y Doppler color; se observa magnitud, dirección y mecanismo de los chorros de regurgitación, así como enfermedad degenerativa mitral subyacente.
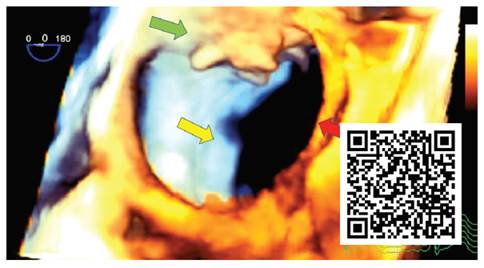
Video 5 Adquisición volumétrica 3D modo zoom de la válvula mitral, vista oblicua superior y medial; se observa: perforación distal de valva anterior (flecha roja), prolapso del segmento P1 de la valva posterior (flecha amarilla) y vegetación mural en aurícula izquierda (flecha verde).
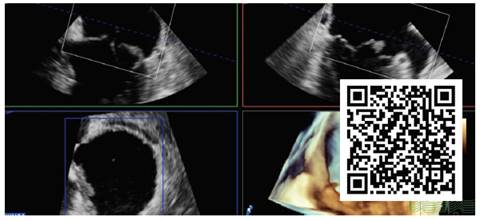
Video 6 Adquisición volumétrica 3D modo zoom de la válvula mitral, vista oblicua superior y medial, con las respectivas reconstrucciones multiplanares 2D (ver descripción de video #5).
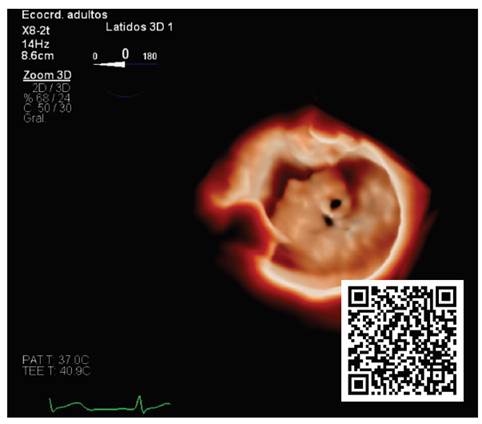
Video 7 Adquisición volumétrica 3D modo zoom de la válvula mitral, vista de cirujano, con técnica de transiluminación; caracterización anatómica de la patología degenerativa mitral y visualización de perforación distal de segmento A2.
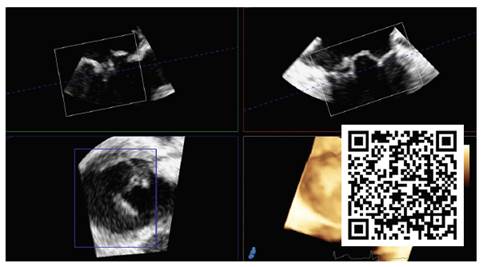
Video 8 Adquisición volumétrica 3D modo zoom de la válvula mitral, vista de cirujano, con reconstrucción multiplanar y manipulación omnidireccional del “data-set”; se observa inicialmente la perforación distal del segmento A2 (circular), y luego la perforación proximal (más pequeña, alargada, fusiforme).
Mensajes para recordar:
La ecocardiografía es la técnica de elección para el diagnóstico de endocarditis infecciosa, y se debe de realizar tan pronto como sea sospechada.
La ecocardiografía transtorácica es la primera modalidad recomendada para la evaluación por endocarditis.
La ecocardiografía transesofágica está indicada cuando el ecocardiograma transtorácico es positivo por endocarditis, cuando el diagnóstico es dudoso, en caso de sospecha de complicaciones asociadas, o cuando hay presencia de dispositivos o cables intracardíacos.
En caso de que un primer ecocardiograma transesofágico sea negativo, pero la sospecha clínica de endocarditis sea alta, es válido repetir el estudio.1
En caso de sospecha de endocarditis de válvula nativa, el ecocardiograma transesofágico tiene una sensibilidad de 90-100%, y una especificidad de 90% para la detección de vegetaciones; es superior a la modalidad transtorácica para la detección de complicaciones, y debería de ser considerado en bacteremia por Staphylococcus aureus.2
Los criterios ecocardiográficos mayores para endocarditis son: vegetación, absceso, y dehiscencia de novo de una prótesis valvular.
El ecocardiograma transtorácico tiene un papel relevante en 3 escenarios: endocarditis nativa de válvulas izquierdas (con excelente ventana acústica), endocarditis de válvula tricúspide, y en la detección de absceso aórtico anterior, en especial en endocarditis de prótesis valvular.
El diagnóstico diferencial (desde el punto de vista ecocardiográfico) de una vegetación incluye: fibroelastoma papilar, enfermedad degenerativa mixomatosa de la válvula mitral, endocarditis trombótica no bacteriana, trombos, y variantes anatómicas normales, como las excresencias de Lambl.
La ecocardiografía transesofágica 2D puede subestimar las características anatómicas de una vegetación, comparativamente con la modalidad 3D.3
La principal limitación de la ecocardiografía 2D es la selección del diámetro máximo de una masa usualmente irregular (como lo es una vegetación); dicha limitación es solventada por la ecocardiografía 3D, que permite obtener múltiples planos, y una reconstrucción volumétrica de las masas.
La ecocardiografía 3D, en especial por vía transesofágica, permite una mejor evaluación del tamaño y morfología de la vegetación, y consecuentemente, una mejor predicción del riesgo embólico.4,5















