Introducción
Las enfermedades cardiovasculares (ECV) son la principal causa de muerte en el mundo y en Costa Rica (Ministerio de Salud, 2016; Organización Mundial de la Salud (OMS),2017) .
Además, es el principal problema de salud pública en Estados Unidos y a nivel mundial debido a los altos costos médicos del tratamiento, como los costos de los servicios hospitalarios, los medicamentos recetados y de los profesionales en salud (Mozaffarian et al., 2015; Ziaeian & Fonarow, 2016). Dentro de las ECV, la insuficiencia cardíaca (IC) es una de las patologías más prevalentes y junto con la enfermedad isquémica causan 8.7 millones de muertes en todo el mundo (Ballesta, Rubio, Ramos, Martínez, & Carrasco, 2018). Alrededor de 37.7 millones de personas en todo el mundo presentan algún grado de IC, afectando así su calidad de vida y generando mayor índice de incapacidad, esto debido principalmente a los sus múltiples síntomas adyacentes, como disnea, fatiga, poca tolerancia al ejercicio o actividades diarias y por la retención de líquidos (Sayago, García, & Segovia, 2013; Ziaeian & Fonarow, 2016). En Estados Unidos, las muertes por IC han presentado un aumento del 40.8% en los últimos 20 años, pasando de 286.800 a 403.900, cuya principal razón se debe al aumento de los factores de riesgo coronario, como la hipertensión, la dislipidemia, el tabaquismo, la obesidad, la diabetes mellitus y a la inactividad física (Mozaffarian et al., 2015).
Por lo tanto, es fundamental por medio de los Programas de Rehabilitación Cardíaca (PRC) lograr un incremento de la función sistólica del ventrículo izquierdo (VI), del consumo máximo de oxígeno (VO2máx) y de la capacidad funcional para producir una disminución en la mortalidad y mejorar la calidad de vida de los pacientes con IC (Andersson & Vasan, 2014; M. F. Piepoli, Davos, Francis, & Coats, 2004; Taylor et al., 2014). A nivel general, se ha reportado que los pacientes con ECV que realizan un PRC obtienen aumentos entre el 11% y el 36% del VO2máx, lo cual podría disminuir el riesgo de mortalidad cardiaca entre un 20% y 25% (Leon et al., 2005; Williams et al., 2006). Adicionalmente, los PRC reportan aumentos en la FEVI en los pacientes con IC después de 12 semanas de entrenamiento (Fu et al., 2013; Wisløff et al., 2007). Esta mejoría se asocia con un menor riesgo de mortalidad en aquellos pacientes con IC que logran tener una FE ≥ 40% (Höllriegel et al., 2016; Tucker et al., 2018; Ziaeian & Fonarow, 2016).
En la actualidad, el ejercicio aeróbico continuo de intensidad moderado (MICT) es la modalidad más utilizada, investigada y mejor desarrollada para obtener beneficios cardiovasculares de los pacientes con IC, debido a su eficacia y seguridad (Taylor et al., 2014). No obstante, el mejor protocolo de entrenamiento sigue en discusión, ya que nuevos métodos de entrenamiento han surgido, como el entrenamiento interválico de alta intensidad (HIIT) (Ponikowski et al., 2016; Vanhees et al., 2012). El HIIT es una modalidad de entrenamiento físico que se caracteriza por periodos breves e intermitentes de alta intensidad, intercaladas por períodos de descanso o ejercicio de baja o moderada intensidad (Fox et al., 1973; Gibala, Little, Macdonald, & Hawley, 2012). El HIIT es una metodología de entrenamiento eficiente para inducir adaptaciones cardiovasculares similares o incluso superiores a las generadas por con el MICT (Ellingsen et al., 2017; Gibala et al., 2012; Wisløff et al., 2007). Este tipo de entrenamiento está generando efectos positivos en los marcadores cardiovasculares tales como: aumentos en el consumo máximo de oxígeno (VO2máx) y en la FEVI, así como una mejora en la frecuencia cardíaca y presión arterial (Benda et al., 2015; Fu et al., 2013; Wisløff et al., 2007). Además, muestra mayores adherencias a los programas de ejercicio en pacientes con IC (Ellingsen et al., 2017; Ponikowski et al., 2016; Vanhees et al., 2012).
El HIIT es un ejercicio alternativo y complementario al MICT dentro de un programa de rehabilitación cardíaca (Gayda, Ribeiro, Juneau, & Nigam, 2016). Se ha demostrado que el HIIT es seguro y con una mayor efectividad que el MICT para mejorar el VO2máx y la capacidad funcional (Benda et al., 2015; Chrysohoou et al., 2015; Ellingsen et al., 2017; Fu et al., 2013; Pattyn, Coeckelberghs, Buys, Cornelissen, & Vanhees, 2014). También, se demuestra que aumenta significativamente la FEVI pero no presenta una mayor efectividad versus el MICT (Guiraud et al., 2012; Haykowsky et al., 2013). Sin embargo, otros estudios han demostraron lo contrario, como el publicado por Wisløff et al. (2007), donde demostraron un efecto significativo del entrenamiento HIIT en la FE en reposo, pasando de 28.0 ± 7.3% en las evaluaciones pre a 38.0 ± 9.8% en post tratamiento (p < .010). En años más recientes, un estudio realizado por Fu et al. (2013) también demostró que el HIIT presenta mayores aumentos que el MICT en la FEVI, pasando de 38.3 ± 3.5% en las evaluaciones pre a 48.6 ± 3.3% en post tratamiento (p < .050). Estos resultados muestran evidencia científica sobre la efectividad del HIIT versus el MICT en la FEVI y deja la posibilidad de continuar investigando en esta línea a más largo plazo.
No obstante, aunque en el HIIT está altamente demostrado su efecto positivo sobre las adaptaciones cardiovasculares y que éste sea más efectivo que el MICT, se requieren estudios que analicen los efectos a largo plazo y su relación con un aumento en eventos cardiovasculares mortales o mayor incidencia de arritmias cardíacas (Elliott, Rajopadhyaya, Bentley, Beltrame, & Aromataris, 2015). Por lo anterior, el propósito de la presente revisión sistemática de literatura es determinar las adaptaciones cardiovasculares del HIIT en comparación con el MICT en cuanto al VO2máx, FEVI y remodelación ventricular de pacientes con IC con FEVI reducida.
Metodología
Esta revisión sistemática se desarrolló realizando una búsqueda de los artículos científicos mediante bases de datos electrónicas, tales como: “PubMed”, “Academic Search Complete”, “SportDiscus” y “ScienceDirect”. Los términos de búsqueda (frase boolena) o palabras clave fueron los siguientes: (‘‘Heart Failure’’) AND (‘‘high intensity interval training’’ OR ‘‘continuous training’’) AND (“ejection fraction” OR “VO2peak” OR “functional capacity” OR “ventricular remodeling”) NOT (“animals”). Se utilizaron las bases de datos electrónicas de la Universidad Nacional para acezar a la plataforma “EBSCO host” e ingresar a las bases de datos anteriormente mencionadas.
Adicionalmente, se revisaron las referencias de los artículos incluidos con el fin de identificar otros estudios potencialmente elegibles. Las búsquedas se realizaron entre marzo y junio del 2018. El año de publicación de los estudios incluidos estuvo entre el 2007 y 2018.
Todas las búsquedas y revisiones de los artículos fueron realizadas por el autor principal. Se revisó de forma independiente los títulos y resúmenes de cada artículo encontrado, con el fin de observar y considerar cuál era un posible estudio elegible. Seguidamente, se obtuvo el texto completo de cada artículo, ya sea por medio de la misma base de datos, encontrados por medio de las plataformas “ResearchGate” o “Cross Ref” o se solicitaron a los autores por vía de correo electrónico.
Luego, se revisaron de forma independiente el texto completo de los artículos seleccionados para verificar si cumplían con los criterios de elegibilidad. La calidad de los estudios fue medida por la herramienta “PEDro Scale”.
Se utilizaron criterios de elegibilidad que siguen la normativa PICOS para determinar la inclusión y calidad de los artículos a consultar. Donde se analiza aspectos de la población de estudio, la intervención, el período de seguimiento, los resultados obtenidos y el diseño de estudio. Se tomaron en cuenta estudios que cumplieran con los siguientes criterios: a) estudios controlados y aleatorios; b) pacientes adultos, mayores de 18 años, de ambos sexos, con diagnóstico de IC; c) pacientes con una FE ≤ 40%; d) estudios publicados en inglés, español o portugués.
Resultados
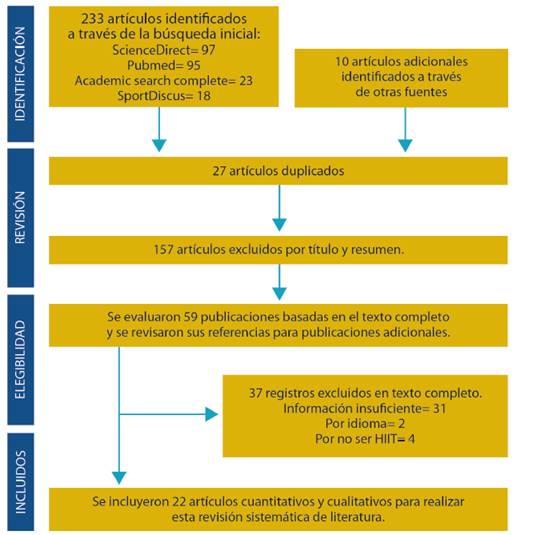
Se revisaron un total de 243 estudios, donde al final se incluyeron 22 estudios cuantitativos con un total de 658 pacientes para realizar esta revisión sistemática de literatura (ver Figura 1). Se encontró que el HIIT es efectivo en el incremento del VO2máx en pacientes con IC, representando aumentos entre el 5.7% y el 46.2% (se muestra en la tabla 1).
Existe mucha variedad en la aplicación del método de HIIT, entre los más efectivos se encuentra el de intervalos de 3×4, donde se realiza tres minutos en baja intensidad y cuatro minutos en alta intensidad. Como el diseñado por Wang et al. (2013) donde aplicaron ese método durante 30 minutos y encontraron una mejoría de 31.3%, pasando de 16.6 ± 0.7 ml/ kg/min a 21.8 ± 0.9 ml/kg/min (p < .05). Por su parte, Iellamo et al. (2013), encontró una mejoría del 19.0% (p < .05) utilizando el mismo protocolo pero con intensidades más bajas de entrenamiento, entre el 75% y 80% de la FCreserva. Fu et al. (2013) encontraron resultados similares, ellos utilizaron un protocolo de 3x3 con intensidades entre el 40% y el 80%, encontrando una mejoría de un 22.5% (p < .050).
Sin embargo, protocolos con menores tiempos por intervalos también generaron mejorías, como el realizado por Freyssin et al. (2012) que utilizaron un protocolo 30seg×1min, donde la intensidad máxima fue al 80% y se realizaba una recuperación completa durante 30 segundos, se encontró un cambio de 27.1% (p < .001). Similarmente, Chrysohoou et al. (2015) aplicaron un protocolo con un periodo de recuperación total pero con un intensidad alta que llegaba hasta 100% durante 30 segundos y encontraron mayores mejorías, ya que reportan un aumento de 31.3% (p < .001). Esto respalda la teoría que entre más alta sea el intervalo de alta intensidad mayor es la mejoría en el VO2máx.
En un reciente meta-análisis publicado por Hannan et al. (2018) demuestran que el HIIT es efectivo en pacientes con ECV en el aumento del VO2máx y presenta mayores mejorías con respecto al MICT, con PRC que son mayores a 6 semanas.
Similarmente, Liou, Ho, Fildes, & Ooi (2016) concuerdan en su meta-análisis al indicar que el HIIT es más efectivo en el aumento del VO2máx en pacientes con enfermedad arterial coronaria (Tabla 2). Sin embargo, reportan que el MICT se asoció con una mayor disminución de la frecuencia cardíaca en reposo y el peso corporal. Específicamente en pacientes con IC, Ballesta et al. (2018) encontraron en su meta-análisis que el HIIT es un método eficaz y seguro para mejorar el VO- 2máx, y es más efectivo que el MICT siempre y cuando los intervalos de baja intensidad sean activos y que se desarrollen entre el 40% y el 60% de la FCreserva. Adicionalmente, otro meta-análisis realizado por Gomes et al. (2018) confirma la mayor efectividad del HIIT en el aumento del VO2máx, pero agregan que la superioridad frente al MICT se iguala cuando se comparan protocolos isocalóricos.
Las mejoras del VO2máx se determinan tanto por adaptaciones centrales como periféricas, principalmente generado por cambios en el volumen sistólico máximo y en la contractibilidad del corazón, además de una mejora en diferencia arterio/venosa de oxígeno máximo (Crimi, Ignarro, Cacciatore, & Napoli, 2009; Hambrecht et al., 2000; Montero, Diaz, & Lundby, 2015). También, se encontraron mejorías en la disminución de los péptido natriurético cerebral (BNP) en un 40% (Wisløff et al., 2007). A nivel periférico, se ha encontrado que el HIIT induce mayores adaptaciones en la función mitocondrial en comparación con el entrenamiento MICT, específicamente se induce aumentos en el contenido mitocondrial en el músculo esquelético, incrementado la actividad enzimática del citrato sintetasa y mayor capacidad de fosforilación oxidativa (MacInnis et al., 2017)2017. Además, existe un aumento en el contenido de proteína IV de subunidad de citocromo C oxidasa, lo que conlleva a una mayor extracción de oxígeno a nivel muscular (MacInnis et al., 2017)2017. También, el HIIT refleja una mejor función mitocondrial al presentar un mayor aumento del nivel de peroxisome proliferator-activated receptor γ co-activator 1 α (PGC-1α) y del ciclo de calcio en el músculo esquelético (Wisløff et al., 2007).
En relación a la FEVI, se han encontrado aumentos entre un 2.6% y 35.7%, en algunos casos sin ser estadísticamente significativa (ver tabla 3). En un estudio realizado por Wisløff et al. (2007) encontraron un aumento de 35.7%, pasando de 28.0 ± 7.1% a 38.0 ± 9.8% (p < .001), utilizando un protocolo de HIIT de 3×4, donde la intensidad baja fue entre el 50% y el 60% de la FCreserva y la alta intensidad entre el 90% y el 95% de la FCreserva, durante 47 minutos. Por su parte, Iellamo et al. (2013) encontraron un resultado adverso aplicando un protocolo de HIIT similar, ya que reportan un incremento no significativo de un 2.6%, pasando de 33.7 ± 4.8% a 34.6 ± 5.6%, la diferencia del protocolo radicó en el volumen total de la sesión que para este último caso fue de 28 minutos. Similarmente, Fu et al. (2013) en su estudio utilizaron HIIT similar al anterior, con intensidades entre el 40% y el 80%, con intervalos de 3×3 y con un volumen total de 30 minutos y esta ocasión sí encontraron diferencias significativas, ya que la FEVI aumentó un 26.9%, pasando de un 38.3 ± 3.3% a 48.6 ± 5.6% (p < .050).
Tabla 1: Resumen de las características y resultados del HIIT de los estudios incluidos en la variable de VO2máx.
| Estudio | Sexo | Edad (año) | NYNA | VO2 máx-pre (ml/kg/min | n | Volumen (min) | Intervalos (min) | Intensidad (%) | #ses | % Δ | P |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Angadi et al. (2015) | A | 71± 9 | ll-lll | 19.2±5.2 | 9 | 16 | 3×4 | 50X80-100 | 12 | 9.4% | = 0.04 |
| Benda et al. (2015) | A | 63±8 | ll-lll | 19.1±4.1 | 10 | 35 | 30seg×1min | 30×90-95 | 24 | 6.8% | = 0.10 |
| Chrysohoou et al. (2015) | A | 63±8 | ll-lV | 16.0±6.0 | 33 | 45 | 30seg×30seg | rec×100 | 36 | 31.3% | < .001 |
| Dimopoulos et al. (2006) | A | 59±9 | ll-lll | 15.4±4.7 | 10 | 40 | 30seg×30seg | rec×80-100 | 36 | 7.8% | < .001 |
| Ellingsen et al. (2017) | A | 65±9 | ll-lll | 17.6±4.8 | 68 | 28 | 3×4 | 60-70×90-95 | 48 | 9.1% | < .050 |
| Freyssin et al. (2012) | A | 54±9 | NR | 10.7±2.9 | 12 | 54 | 30seg×1min | rec×80 | 36 | 27.1% | < .001 |
| Fu et al. (2013) | A | 67±2 | ll-ll | 16.0±1.0 | 15 | 30 | 3×3 | 40×80 | 36 | 22.5% | < .050 |
| Iellamo et al. (2014) | A | 67±6 | l-ll | 15.3±4.0 | 18 | 28 | 3×4 | 45-60×75-80 | 36 | 19.0% | < .050 |
| Iellamo et al. (2013) | H | 62±8 | l-ll-lll | 18.8±4.3 | 8 | 28 | 3×4 | 45-60×75-80 | 36 | 22.6% | < .050 |
| Isaksen et al. (2015) | A | 69±9 | l-ll-lll | 17.4±4.6 | 24 | 28 | 3×4 | 60×95 | 36 | 5.7% | < .001 |
| Koufaki et al. (2014) | A | 59±7 | l-ll-lll | 15.3±4.7 | 16 | 30 | 2×1 | 20-30×80-100 | 36 | 13.1% | < .050 |
| Panagopoulou et al. (2017 | A | 54±9 | l-ll-lll | 17.2±4.9 | 18 | 40 | 2×1 | 50×80-100 | 36 | 16.3% | < .050 |
| Roditis et al. (2007) | A | 63±2 | l-ll-lll | 14.2±3.1 | 11 | 40 | 30seg×30seg | rec×80-100 | 36 | 8.5% | = .030 |
| Safiyari et al. (2016) | A | 57±8 | ll-lll | 10.1±3.1 | 14 | NR | NR | NR | 36 | 10.9% | = .040 |
| Ulbrich et al. (2016) | H | 53±7 | ll-lll | 21.4±4.1 | 12 | 40 | 3×3 | 30-40×90-95 | 36 | 13.1% | < .050 |
| Wang et al. (2013) | A | 62±2 | NR | 16.6±0.7 | 29 | 30 | 3×3 | 40×80 | 36 | 31.3% | < .050 |
| Wang et al. (2013) | A | 62±2 | NR | 14.1±0.7 | 28 | 30 | 3×3 | 40×80 | 36 | 25.5% | < .050 |
| Wisløff et al. (2007) | A | 76±9 | NR | 13.0±1.6 | 9 | 38 | 3×4 | 50-60×90-95 | 36 | 46.2% | < .010 |
Abreviaciones: H= hombre; A= ambos; NYHA= clasificación funcional de insuficiencia cardíaca; NR= no reportado; VO2máx pre= volumen de oxígeno máximo al inicio de la intervención; HIIT= entrenamiento interválico de alta intensidad; MICT= entrenamiento continuo de intensidad moderada; n= participantes por grupo; min= minutos; seg= segundos; rec= recuperación total; ses= sesiones; ×= por (signo para dividir los intervalos de baja y alta intensidad); %Δ= porcentaje de cambio; p= significancia.
Tabla 2: Resumen de las características y resultados del MICT de los estudios incluidos en la variable de VO2máx.
| Estudio | Sexo | Edad (años) | NYHA | VO2máx-pre (ml/kg/min) | n | Volumen (min) | Intensidad (%) | # ses | %Δ | p |
|---|---|---|---|---|---|---|---|---|---|---|
| Aksoy et al. (2016) | A | 59 ± 7 | II-III | 13.3 ± 3.7 | 15 | 35 | 50-75 | 30 | 5.7% | > .050 |
| Atehortua et al. (2011) | A | 59 ± 9 | II-III | 26.4 ± 6.4 | 22 | 45 | 60-75 | 36 | 30.6% | < .010 |
| Benda et al. (2015) | H | 64 ± 8 | II-III | 21.2 ± 3.6 | 10 | 30 | 60-70 | 24 | 0.5% | > .050 |
| Dimopoulos et al. (2006) | H | 61 ± 7 | II-III | 15.5 ± 3.7 | 14 | 40 | 50 | 36 | 5.8% | < .020 |
| Ellingsen et al. (2017) | A | 60 ± 9 | II-III | 16.9 ± 5.1 | 55 | 47 | 60-70 | 36 | 4.1% | = .680 |
| Freyssin et al. (2012) | A | 55 ± 9 | NR | 10.6 ± 4.1 | 14 | 45 | 50 | 48 | 1.9% | > .050 |
| Fu et al. (2013) | A | 66 ± 2 | II-III | 15.9 ± 0.7 | 15 | 30 | 60 | 36 | 0.6% | > .050 |
| Höllriegel et al. (2016) | A | 60 ± 3 | III | 15.3 ± 0.3 | 17 | 30 | 50-60 | 36 | 16.3% | = .001 |
| Höllriegel et al. (2016) | A | 60 ± 3 | III | 15.3 ± 0.3 | 17 | 30 | 50-60 | 72 | 24.2% | < .001 |
| Höllriegel et al. (2016) | A | 60 ± 3 | III | 15.3 ± 0.3 | 15 | 30 | 50-60 | 144 | 27.5% | < .001 |
| Iellamo et al. (2013) | H | 63 ± 9 | I-III | 18.4 ± 4.3 | 8 | 45 | 45-60 | 36 | 22.2% | < .050 |
| Iellamo et al. (2014) | A | 68 ± 8 | I-II | 16.2 ± 5.0 | 18 | 45 | 45-60 | 36 | 16.1% | < .050 |
| Kerrigan et al. (2014) | A | 53 ± 9 | NR | 13.3 ± 5.5 | 18 | 30 | 60 | 18 | 13.5% | < .050 |
| Koufaki et al. (2014) | A | 58 ± 9 | I-III | 17.6 ± 7.1 | 17 | 40 | 40-60 | 36 | 12.5% | < .050 |
| Koufaki et al. (2014) | A | 58 ± 9 | I-III | 17.6 ± 7.1 | 17 | 40 | 40-60 | 72 | 7.4% | > .050 |
| Roditis et al. (2014) | A | 61 ± 8 | I-III | 15.3 ± 4.4 | 10 | 40 | 50 | 36 | 8.5% | = .030 |
| Smart et al. (2012) | H | 59 ± 9 | II-III | 12.4 ± 2.5 | 13 | 30 | 70 | 48 | 12.9% | = .120 |
| Ulbrich et al. (2016) | H | 54 ± 9 | II-III | 18.4 ± 4.3 | 10 | 40 | 75 | 36 | 9.8% | < .050 |
| Wisloff et al. (2007) | A | 74 ± 9 | NR | 13.0 ± 1.1 | 9 | 47 | 70 | 36 | 14.6% | < .010 |
Abreviaciones: H= hombre; A= ambos; NYHA= clasificación funcional de insuficiencia cardíaca; NR= no reportado; VO2máx pre= volumen de oxígeno máximo al inicio de la inter vención; HIIT= entrenamiento interválico de alta intensidad; MICT= entrenamiento continuo de intensidad moderada; n= participantes por grupo; min= minutos; seg= segundos; rec= recuperación total; ses= sesiones; ×= por (signo para dividir los intervalos de baja y alta intensidad); %Δ= porcentaje de cambio; p= significancia.
Tabla 3: Resumen de las características y resultados del HIIT y MICT de los estudios incluidos en la variable de FEVI.
| Estudio | Sexo | Edad (años) | NYHA | FEVI pre (%) | Tipo | n | Volumen (min) | Intensidad (%) | # ses | %Δ | p |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Aksoy et al., 2015 | A | 59 ± 7 | II-III | 52.0 ± 4.9 | MICT | 15 | 35 | 50-75 | 30 | 5.8 | < .050 |
| Atehortúa et al., 2011 | A | 59 ± 9 | II-III | 32.7 ± 8.8 | MICT | 22 | 45 | 60-75 | 36 | 18.8 | < .001 |
| Benda et al., 2015 | A | 63 ± 8 | II-III | 37.0 ± 6.0 | HIIT | 10 | 35 (1×2.5) | 60-70×90-95 | 24 | 12.5 | = .090 |
| Benda et al., 2015 | H | 64 ± 8 | II-III | 38.0 ± 6.0 | MICT | 10 | 30 | 60-75 | 24 | 0.0 | = .090 |
| Ellingsen et al., 2017 | A | 65 | II-III | 29.0 ± 6.2 | HIIT | 68 | 28 (3×4) | 60-70×90-95 | 36 | 10.3 | > .050 |
| Ellingsen et al., 2017 | A | 60 | II-III | 29.0 ± 6.2 | MICT | 55 | 47 | 60-70 | 36 | 0.0 | > .050 |
| Fu et al., 2013 | A | 67 ± 2 | II-III | 38.3 ± 3.5 | HIIT | 15 | 30 (3×3) | 40×80 | 36 | 26.9 | < .050 |
| Fu et al., 2013 | A | 66 ± 2 | II-III | 38.6 ± 4.8 | MICT | 15 | 30 | 60 | 36 | 11.7 | > .050 |
| Höllriegel et al., 2016 | A | 60 ± 2 | III | 24.0 ± 1.1 | MICT | 17 | 30 | 50-60 | 36 | 39.6 | < .001 |
| Iellamo et al., 2013 | H | 62 ± 8 | I-II-III | 33.7 ± 4.8 | HIIT | 8 | 28 (3×4) | 45-60×75-80 | 36 | 2.6 | > .050 |
| Iellamo et al., 2013 | H | 62 ± 9 | I-II-III | 31.5 ± 6.9 | MICT | 8 | 45 | 45-60 | 36 | 1.9 | > .050 |
| Isaksen et al., 2015 | A | 69 ± 9 | I-II-III | 37.0 ± 10.9 | HIIT | 24 | 28 (3×4) | 60-70×85 | 36 | 4.5 | = .008 |
| Smart & Steele, 2012 | H | 63 ± 9 | II-III | 27.5 ± 7.2 | MICT | 13 | 30 | 70 | 48 | 0.7 | = .410 |
| Ulbrich et al., 2016 | H | 53 ± 7 | II-III | 35.4 ± 6.7 | HIIT | 12 | 40 (3×3) | 70×95 | 36 | 12.7 | = .005 |
| Ulbrich et al., 2016 | H | 54 ± 9 | II-III | 32.8 ± 7.7 | MICT | 10 | 40 | 75 | 36 | 8.8 | > .050 |
| Wang et al., 2013 | A | 62 ± 2 | - | 38.5 ± 3.2 | HIIT | 29 | 30 (3×3) | 40×80 | 36 | 26.0 | < .050 |
| Wang et al., 2013 | A | 63 ± 2 | - | 36.4 ± 4.1 | HIIT | 28 | 30 (3×3) | 40×80 | 36 | 19.2 | < .050 |
| Wisløff et al., 2007 | A | 74 ± 12 | - | 28.0 ± 7.3 | HIIT | 9 | 38 (3×4) | 50-70×90-95 | 36 | 35.7 | < .001 |
| Wisløff et al., 2007 | A | 76 ± 9 | - | 32.8 ± 4.8 | MICT | 9 | 47 | 70 | 36 | 2.1 | > .050 |
Abreviaciones: H= hombre; A= ambos; NYHA= clasificación funcional de insuficiencia cardíaca; FEVI pre= fracción de eyección del ventrículo izquierdo al inicio de la intervención; HIIT= entrenamiento interválico de alta intensidad; MICT= entrenamiento continuo de intensidad moderada; n= participantes por grupo; min= minutos; ses= sesiones; x= por (signo para dividir los intervalos de baja y alta intensidad); %Δ= porcentaje de cambio.
Más recientemente, en un estudio realizado por Benda et al. (2015) tampoco encontró efectos significativos aplicando HIIT aunque reportan un aumento de un 12.5% (p =.070).
No obstante, fue superior al MICT, ya que esta metodología no generó ningún tipo de cambio. Por su parte, Ulbrich et al. (2016) encontró un resultado similar, donde la FEVI aumentó un 12.7% pero para este caso sí presentó un diferencia significativa (p = .013), para este estudio utilizaron una metodología 3×3, donde entrenaban entre 30% y 40% de la FCreserva por tres minutos y luego realizaban tres minutos entre el 90% y 95% de la FCreserva. En otro estudio realizado por Isaksen et al., (2015) registraron un leve aumento en la FEVI de 4.5% pero al igual que el estudio anterior, fue estadísticamente significativo (p = 0.008) pasando de 37.6 ± 10.9% a 39.3 ± 10.5% después de una intervención con el HIIT de 3×4 y conintensidades entre el 60% y 95% de la FCreserva. el mismo protocolo de HIIT, Ellingsen et al. (2017) encontraron diferencias significativas en el FEVI a las 12 semanas de entrenamiento, donde presentaron un aumento del 10.3%, pasando de 29.0 ± 6.2% a 32 ± 7.9% (p < 0.050).
Los efectos fisiológicos en la mejora de la FEVI son muy variados, uno de ellos es el aumento del flujo sanguíneo coronario y del contenido de cardiomioglobina, así como el incremento de enzimas antioxidantes y proteínas relacionadas con el estrés oxidativo que ayuda a mejor la contractividad cardíaca (Crimi et al., 2009). Además, aspectos como la disminución de los niveles de mieloperoxidasa (MPO) e interlucina 6 (IL-6) en plasma se asocian con una mayor protección contra el estrés oxidativo y la inflamación endotelial asociados con los procesos disfuncionales cardíacos, lo que conlleva a una mejor circulación coronaria, volumen sistólico y por ende de mejor fracción de eyección (Fu et al., 2013). Otra adaptación cardiovascular que se le atribuye al HIIT es el aumento de la contractibilidad del corazón (Wisløff et al., 2007), ligado principalmente con el aumento del volumen sistólico (Benda et al., 2015), volumen telediastólico del VI (volumen diastólico final) y una disminución entre un 18% y 25% en volumen sistólico final del VI (Haykowsky et al., 2007; Wisløff et al., 2007).
Otro factor que puede incrementar la FEVI es la remodelación cardíaca que se le atribuye al ejercicio en pacientes con IC, donde se ha demostrado que logra aumentar la función y estructura cardíaca con entrenamientos aeróbicos de 6 meses (Haykowsky et al., 2007).
Con respecto a las mejorías en la remodelación del VI, el HIIT genera una disminución en la remodelación del VI, reportándose una reducción de la dimensión ventricular izquierda diastólica (LVEDD) entre un 7.4% y un 11.5% y de la dimensión ventricular izquierda sistólica (LVESD) en un 14.5%. Mientras tanto, se ha demostrado que el MICT genera disminuciones de las paredes ventriculares solo en aquellos pacientes con la patología avanzada y que presenten un grave grado de hipertrofia concéntrica (Höllriegel et al., 2016). Lo cual concuerda con lo reportado por Van De Heyning et al. (2018), que en pacientes con ECV con función sistólica conservada y sin hipertrofia ventricular, no encontraron disminuciones en las dimensiones ventriculares en el volumen sistólico o diastólico.
Por su parte, Höllriegel et al. (2016) encontraron disminuciones significativas en el volumen diastólico (p = .002) y en el volumen sistólico (p < .001) en pacientes con IC severa.En un estudio realizado por Wisløff et al. (2007), el HIIT generó una disminución tanto en los volúmenes como en las dimensiones del VI (p < .010). Se encontró una reducción de la dimensión diastólica del VI (LVEDD) de un 11.5% y de la dimensión sistólica del VI (LVESD) de un 14.5%. Además, encontraron reducciones del volumen sistólico final de un 9.3%. Contrariamente, Iellamo et al. (2013) no encontraron disminuciones significativas en la LVEDD con el HIIT, ya que reportan una leve disminución de un 1.5% (p > 0.050) (ver tabla 4).
Tabla 4: Resumen de los resultados del HIIT en las dimensiones del VI.
| Artículo | Sexo | Edad | NYHA | n | Variable (mm) | Vol (min) | Intervalos | Intensidad | # de ses | %Δ | p |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Ellingsen et al. (2017) | A | 65 ± 9 | II-III | 68 | LVEDD | 28 | 3×4 | 60-70×90-95 | 36 | -7.4% | - |
| Iellamo et al. (2013) | H | 62 ± 8 | I-II-III | 8 | LVEDD | 28 | 3×4 | 45-60×75-80 | 36 | 1.5% | > .050 |
| Wisløff et al. (2007) | A | 76 ± 9 | - | 9 | LVEDD | 38 | 3×4 | 50-60×90-95 | 36 | -11.5% | < .010 |
| Wisløff et al. (2007) | A | 76 ± 9 | - | 9 | LVESD | 38 | 3×4 | 50-60×90-95 | 36 | -14.5% | < .010 |
Abreviaciones: HIIT= entrenamiento interválico de alta intensidad; n= participantes por grupo; vol= volumen total de la sesión; min= minutos; x= por (signo para dividir los inter valos de baja y alta intensidad); %Δ= porcentaje de cambio; LVEDD= dimensión diastólica del VI; LVESD= dimensión sistólica del VI.
Un mecanismo por el cual el ejercicio físico puede mejorar la remodelación del VI es una reducción la poscarga cardíaca, al disminuir la resistencia que debe generar el VI para expulsar la sangre hacia los grandes vasos sanguíneos (Höllriegel et al., 2016; Piepoli et al., 2006). Además, se ha encontrado mejoría en la disminución de las neurohormonas vasoconstrictoras y una disminución de la carga hemodinámica presentes en el VI (Braith, Welsch, Feigenbaum, Kluess, & Pepine, 1999). Específicamente, el ejercicio físico logra reducir los niveles plasmáticos de angiotensina II, aldosterona, vasopresina, péptido natriurético atrial, péptido natriurético cerebral, epinefrina y norepinefrina en reposo (Hambrecht et al., 2000), los cuales están ligados con una disminución del tono simpático y un aumento de la actividad vagal en pacientes con IC (Coats et al., 1992).
Conclusiones
El HIIT es una metodología que genera amplias adaptaciones cardiovasculares, como el aumento del VO2máx, la disminución de la remodelación del VI y el aumento de la FEVI.
Se demuestra la alta efectividad que presenta el HIIT en la mejora en el VO2máx, presentando superiores mejorías que con el MICT. Con respecto a la remodelación ventricular y a la FEVI, el HIIT presenta mejorías significativas, pero no está demostrado que sea más efectivo que el MICT. Se debe analizar el efecto del HIIT a largo plazo, para identificar el riesgo asociado a morbilidad y mortalidad en pacientes con IC.