Introducción
Paciente masculino de 48 años con historia de 3 años de evolución de episodios de fibrilación auricular paroxísticos con respuesta ventricular rápida sintomática a pesar de medicación con betabloqueadores y propafenona. El paciente tiene antecedente de ablación de vía accesoria en el año 2013, dislpidemia y SAHOS moderado. Se encuentra bajo medicación con Rivaroxaban 20 mg PO, Metoprolol 50 mg PO cada 12 horas, Omeprazol 20 mg PO, Propafenona 150 mg VO PO cada 12 horas y Sucralfato 1 gramo PO tres veces al dia. Se le realizó ecografía transesofágica que mostró dilatación moderada de la aurícula izquierda con volumen indexado de 48 cc/m2, ausencia de trombos o masas endocavitarias, función sistólica del ventrículo derecho normal y FEVI del 52%. Tomografía axial computarizada con reconstrucción tridimensional de la aurícula izquierda y venas pulmonares mostro como variante anatómica la presencia de vena accesoria anterior derecha.
El paciente se decidió llevar a aislamiento percutáneo de venas pulmonares con Sistema de navegación y mapeo tridimensional Carto 3 (Biosense Webster, Diamond Bar, CA, USA).
Procedimiento
Bajo anestesia general, en sala de electrofisiología, se canalizaron con guía de ultrasonido en tiempo real 2 accesos venosos femorales derechos para paso de camisa no deflectable LAM 90 (St Jude Medical, Sylmar, CA, USA) y camisa deflectable Agilis Nxt 8.5 Fr (St Jude Medical, Sylmar, CA, USA), 1 accesos venoso femorales izquierdo para introductor 11 Fr y paso de sonda de ecografía intracardiaca y 1 acceso venoso yugular derecho para introductor 7 fr y paso de catéter duodecapolar para mapeo de auricula derecha y seno coronario.
Se realizaron 2 punciones transeptales para paso a auricula izquierda. Se utilizó catéter LASSO Nav deflectable (Biosense Webster) y catéter de ablación Smart Touch thermocool bidireccional DF (Biosense Webster). Se realizó reconstrucción electroanatómica de la auricula izquierda, auriculilla y venas pulmonares. Se inciaon aplicaciones seriadas de radiofrecuencia a nivel antral de las venas pulmoanres, controladas por fuerza de contacto e integral tiempo velocidad objetivo (ITF) de 400 gramos/segundo con lo que se completó aislamiento circunferencial antral de las venas pulmonares sin lograr terminación de la fibrilación auricular. Se procedió a realizar línea de ablación anterior y aislamiento de la pared posterior y durante ablación se consigue terminación de la fibrilación y paso a ritmo sinusal. Se comprobó bloqueo de entrada y salida de estimulación en las 4 venas pulmonares y techo de la aurícula. Se completó infusión de isoprenalina a dosis de 20 ug/minuto hasta por 20 minutos sin documentar reconección de las venas o techo y corroborando de nuevo bloqueo de entrada/salida de las 4 venas.
Se retiran catéteres de cavidades izquierdas, se revirtió anticoagulación con protamina, se retiran introductores del paciente y se da por concluido el procedimento.
El conteo de tiempo de radiofrecuencia fue de 94 puntos y el tiempo de radiofrecuencia de 50.9 minutos. Balance hídrico de +3 850 cc al término del procedimiento.
Paciente es trasladado a recuperación y en la noche a salón general. Al día siguiente del AVP, se evalúa y en ausencia de síntomas o complicaciones se egresa.
48 horas post egreso el paciente se presenta al servicio de Urgencias médicas con dificultad respiratoria de 2 horas de evolución, diaforesis, disnea en reposo y sensación de febril no cuantificada.
Al examen físico se documentó temperatura de 37.9 grados, corazón rítmico con frecuencia cardiaca de 90 LPM, Frecuecia respiratoria de 26/minuto, tensión arterial de 90/60 mmHg. Al exámen físico se evidenció hipo ventilación de ambas bases pulmonares, crépitos pulmonares y ausencia de frote pericárdico. Saturación por pulsioximetria del 69% y Presión de oxigeno por gasometría arterial (PaO2) de 39 mmHg. Se ingresa a Cuido Intensivo. Se toman hemocultivo y cultivo por cepillado de vía aérea (fibrobosncoscopia). Se inició cobertura antibiótica con Piperazilina-Tazobactan y vancomicina. Se colocó ventilación NO invasiva y se inició terapia diurética endovenosa.
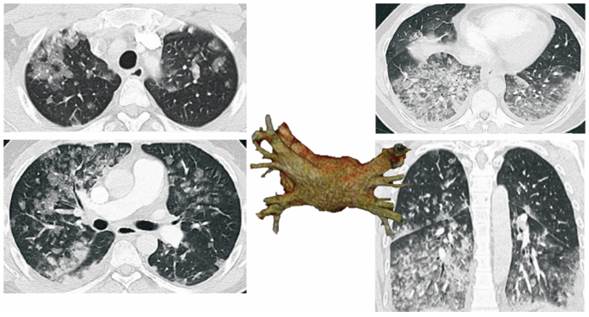
Figura 1. Reconstruccion auricula izquierda con set de lesiones y registro de electrograma con bloqueo de salida.
Hemograma mostró 13 400 leucocitos con 92% neutrófilos, Hemoglobina de 16.5 g/dL y plaquetas normales. Proteína C reactiva de 133 mg/dL.
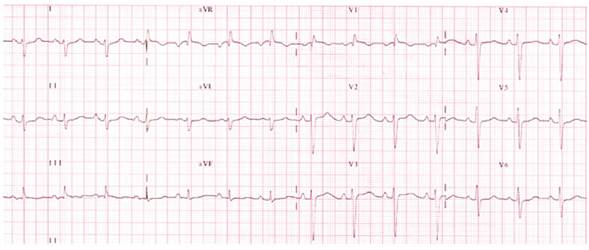
Radiografía de tórax evidenció derrame pleural bilateral pequeño, cefalización de flujo e imagen de edema pulmonar bilateral. Electrocardiograma en ritmo sinusal con frecuencia de 90 LPM, con trastorno de repolarización en derivaciones inferiores. Con la combinación de ventilación no invasiva y terapia diurética con furosemida endovenosa, la mejoría fue marcada. A las 6 horas de inico de manejo en UCI el paciente se encontraba con saturación por pulsioximetria de 90 % y PAO2 de 70 mmHg.
Se realizó TAC de tórax/AngioTAC que documentó edema pulmonar bilateral con derrame pleural bilateral y cisuritis. Descartó estenosis de las venas pulmonares y presencia de hallazgos compatibles con tromboembolismo. Ecocardiograma trans torácico reportó disfunción leve del ventrículo derecho y aumento de gradiente transtricuspídeo, así como aumento de la presión sistólica de la arteria pulmonar hasta 78 mm Hg (previamente de 38 mmHg en ECOTE previo a AVP).
TABLA 1 Complicaciones identificadas en relacion al procedimietno de aislamiento de venas pulmonares 6, 7, 8, 9, 10
| Tipo de complicacion | Definicion | Diagnostico | Manejo |
| Estenosis vena pulmonar | Reacción fibrotica por aplicación de radiofrecuencia en vena pulmonar, disminución del lúmen de la vena pulmonar. | TAC 3D/RMN | Angioplastia pulmonar |
| Injuria esofágica | Fístula atrio esofágica. Presenta sepsis severa, embolismo aéreo/séptico SNC, usualmente fatal. | TAC tórax / SNC / RMN, ECOTE | Dx rápido y cirugía temprana |
| Lesión nervio frénico | Ablación de Vena Pulmonar derecha, y traumática. | Fluoroscopia, clínica | Según síntomas, ventilación mecánica, ventilación no invasiva |
| Tromboembolismo | Embolia a SNC, embolia pulmonar, embolia renal | TAC SNC / RMN / angiografí | Según zona afectada, endovascular/ cateterismo |
| Complicaciones vasculares | Accesos venosos | Hematoma, fistula, pseudoaneurisma | Manejo médico, compresión intermitente ms inferiores |
| Injuria vagal peri esofágica | Lesion de nervio/plexo esofágico | Trastorno de motilidad esofágica/gástrica | Cine tac / endoscopia alta despues del 2 mes po avp |
| Radio exposición | Radiodermatitis | Lesión cutánea en tórax posterior | Manejo clínica heridas |
Se continuó con suplementación de oxígeno por 48 horas y se tituló terapia diurética. Al segundo día tomando en cuenta mejoría franca y resultado de muestras y cultivos negativas por gérmenes se suspendieron antibióticos. A 72 horas de su ingreso hospitalario el paciente se consideró para alta hospitalaria. Su balance hídrico al término de la segunda hospitalización de -6200 cc. Se revisó balance hídrico de hospitalización previa y era de +4820 cc. Se consideró insuficiencia respiratoria tipo 1 secundaria a edema pulmonar asociado a sobrecarga hídrica post AVP con terapia diurética insuficiente, con egreso hospitalario en condiciones de sobrecarga hídrica.
Alteración de coeficiente de atenuación en 4 cuadrante pulmonares, con acumulación de líquido en cisura, hallazgos sugestivos de edema pulmonar cardiogénica y menos probable en relación a hemorrágica alveolar. Se descarta tromboembolismo pulmonar y estenosis pulmonar post AVP.
Discusión
La fibrilación auricular es probablemente la arritmia cuyo procedimiento de ablación es el más frecuente en laboratorios electrofisiológicos en el mundo y su indicación está validada por la guías internacionales de las sociedades mundiales de electrofisiología1.
Cualquier revisión que contribuya a la identificación de potenciales complicaciones derivadas del manejo y su prevención es importante. La ablación de fibrilación auricular o aislamiento de venas pulmonares (AVP) es un procedimiento seguro, y se cuenta con la experticia adecuada tiene índices de efectividad aceptables. La tasa de complicaciones relacionadas al AVP según el estudio de Capato et al 2 es del 4.5% y definitivamente la prevención de complicaciones es mejor que su cura 3.
Las complicaciones definidas derivadas del procedimiento según revisión de J. Brugada 4y Raviele A, et al 5se aprecian en la tabla 1.
El síndrome de distrés respiratorio agudo (SRDA)12fue definido como el cociente entre presión parcial de oxígenoarterial (PaO2) y la fracción de oxígeno inspirada (FiO2)por debajo de 200 mmHg y presencia de infiltrados alveolares en la Radiografía de tórax. Puede tener causas pulmonares (injuria alveolar primaria) o extrapulmonares (secundarias). En el caso del paciente se consideró como diagnóstico edema pulmonar hidrostático secundario a sobrecarga hídrica en relación al manejo líquido durante el procedimiento de AVP.
El paciente implicado en este reporte presenta FEVI normal previo al procedimiento pero con disfunción diastólica tipo 1 y dilatación moderada de la aurícula izquierda. El manejo diurético es clave en el manejo de la sobrecarga hídrica que los pacientes en los que se utiliza catéteres irrigados y procedimientos bajo anestesia general con infusión de múltiples medicamentos. Natale et al 13 reportaron algunos casos aislados de pacientes con disfunción diastólica auricular izquierda, edema pulmonar, hipertensión pulmonar secundaria transitoria después de AVP. Ellos identificaron como factores de riesgo para este Síndrome cicatrización severa en aurícula izquierda, diámetros auriculares de más de 45 mm, Sd. Apnea e hipoventilación del sueño (SAHOS), diabetes mellitus (DM) y disfunción diastólica del ventrículo derecho (aumento de presiones en aurícula izquierda). Un segundo trabajo presentado por Powell et al14mostró que cerca del 8% de los pacientes desarrolla hipertensión pulmonar y disfunción diastólica de la aurícula izquierda luego de AVP. Consideramos por lo tanto mantener un balance hídrico cercano al neutro es fundamental en la prevención de aparición temprana o tarde de edema pulmonar post AVP. En nuestro caso el manejo diurético inicial fue insuficiente y se egresó al paciente con balance de más de 2000 cc positivo, y, tomando en cuenta las condiciones predisponentes del paciente (SAHO, Aurícula dilatada, disfunción diastólica) se facilitó la aparición de hipertensión pulmonar y sobrecarga hídrica con posterior desarrollo de edema pulmonar que llevó a distrés respiratorio tipo 2.
Sólo se encontró 1 reporte de Síndrome de distrés respiratorio en la revisión de bibliografía reportado por Novak y Segal11.
Conclusion
El AVP es una técnica segura, reproducible y con buenos resultados para el manejo de la fibrilación auricular refractaria a manejo médico (Indicación IIa). Las complicaciones post AVP pueden ser prevenidas y la sobrecarga hídrica es una de ellas. Un manejo diurético oportuno en caso de documentar balance positivo puede ser de utilidad para evitar desarrollo de edema pulmonar sobre todo en paciente con factores de riesgo para desarrollo de Síndrome de aurícula paralítica post AVP.
Responsabilidades eticas
Protección de personas y animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki. Confidencialidad de los datos. Los autores declaran que en este artículo no aparecen datos de pacientes. Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.