Caso clínico
Femenina de 58 años, quien presentó a la edad de 50 años evento cerebrovascular isquémico, cuyas secuelas han sido hemparesia derecha, el cual fue catalogado como criptogénico. En ese momento se le realizó un ecocardiograma que no documentaba defectos segmentarios, FE: 55%, disfunción diastólica tipo I, no crecimiento de cámaras. EKG: BRDHH con hemibloqueo anterior izquierdo (figura 1).
A la edad de 52 años, a través de la consulta externa se ingresa en el salón de cardiología, para estudios por cuadro de aproximadamente 3 meses de evolución de dolor torácico anginoso, a veces punzante, a veces opresivo, presentado tanto en esfuerzo como en reposo y que se catalogó como un angor estable clase canadiense (CCS) III. En un estudio de perfusión nuclear miocárdica con esfuerzo (MIBI) se documentó defecto mixto infero lateral, además de un control ecocardio gráfico que mostraba acinesia postero-inferior basal con fracción de eyección del 50%. Se realizó en dicha hospitalización una arteriografía coronaria que no documentó lesiones obstructivas. Se egresa con tratamiento convencional como si se tratara de una cardiopatía isquémica.
Un holter en consulta externa a los 6 meses de ese internamiento fue reportado con trigeminismo y cuadrigeminismo ventricular, con 7 135 extrasístoles ventriculares en 24 horas.
Al año siguiente a la edad de 53 años se le inició rosuvas tativa 40mg, siempre bajo el principio de asumir su patología como enfermedad coronaria de pequeño vaso.
Un nuevo holter 2 años posteriores al primer internamiento cardiaco reportó 14 200 extrasístoles ventriculares, con 2065 episodios de bigeminismo y 174 episodios de taquicardia ventricular no sostenida de al menos 5 latidos (Figura 2), se decide iniciar carvedilol 12,5 mg/Bid. Para entonces la paciente lo que refería era la sensación de palpitaciones y disnea de esfuerzos moderados.
En un segundo internamiento por cardiología, 5 años posteriores a la primera, se interna nuevamente por dolor torácico anginoso. Un nuevo ecocardiograma documenta acinesia extensa de todos los segmentos ínfero laterales con una fracción de eyección del 35%, por lo que se ingresa nuevamente para arteriografía coronaria, la cual describe ausencia de lesiones coronarias obstructivas significativas. Se egresa nuevamente con el diagnóstico de posible enfermedad arterial coronaria de pequeño vaso y cardiopatía isquémica.
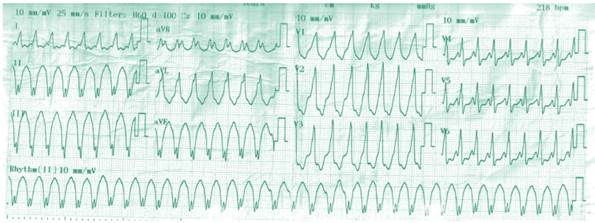
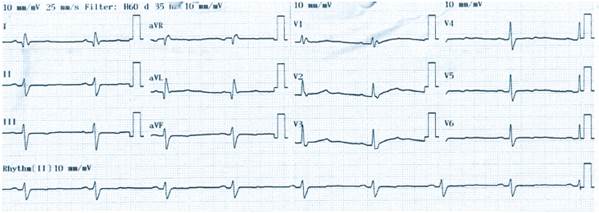
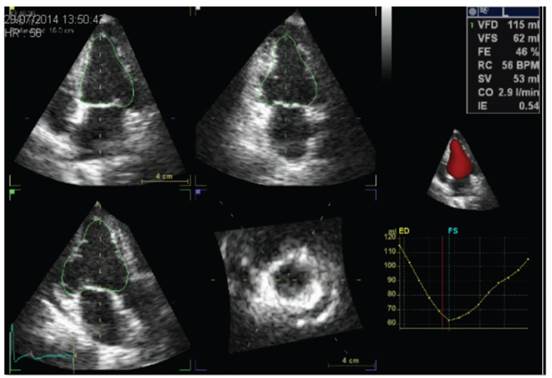
En un último internamiento a cardiología, a 6 años de que debutó con los síntomas cardiacos y a los 8 años de que presento el evento cerebro vascular, consulta por cuadro de 8 días de dolor torácico, palpitaciones, vómitos y disnea de mínimos esfuerzos según la clasificación de Nueva York III (NYHA III), que persistieron y empeoraron el día que decidió consultar. A su llegada a emergencias se documenta criodiaforética, inestable hemodinámicamente sin sensado de presión arterial, con frecuencia cardiaca en 170 lat/min y con un ritmo catalogado como una taquicardia ventricular sostenida (Figura 3), el cual se cardioverte eléctricamente con 200 J, y retorna a ritmo sinusal (Figura 4). En ese momento se le realiza un nuevo ecocardiograma que documenta acinesia y remodelado aneurismático de los segmentos basales inferior, inferolateral, anterior y lateral con hipocinesia leve de los segmentos medios de las mismas paredes y normocinesia de los segmentos restantes para una fracción de eyección del 40%, con una insuficiencia mitral moderada funcional Carpentier IIIb (Figura 5 y 6).
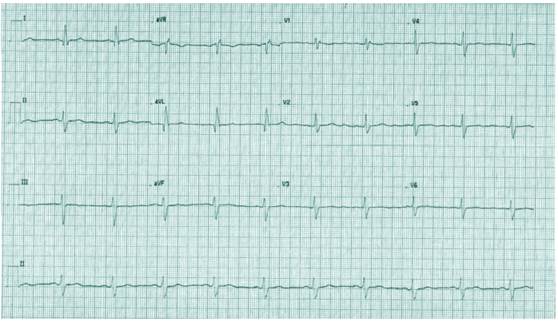
Figura 1 Electrocardiograma de base. Muestra un ritmo sinusal con un bloqueo de rama derecha del haz de his y un bloqueo de fascículo antero- superior izquierdo.
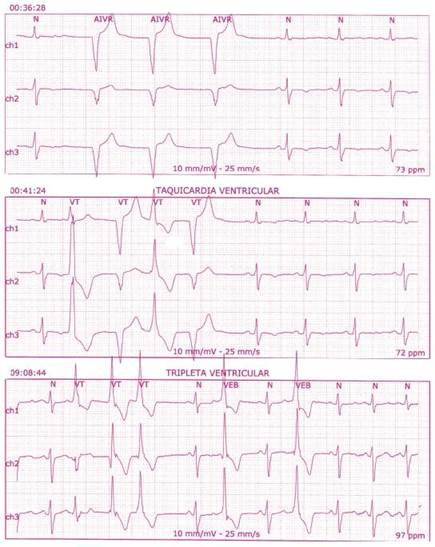
Figura 2 Holter de 24 horas muestra colgajo de taquicardia ventricular con extrasístoles ventriculares frecuentes de al menos tres focos diferentes.
En el cuadro 1 se anexan los resultados de los laboratorios del último internamiento. Ante la presencia de una paciente con coronarias angiográficamente normales y trastornos segmentarios no correspondientes a un lecho coronario, se tomaron serologías, en donde se documentó positivo por chagas por dos métodos diferentes (hemaglu tinación indirecta y ELISA), permitiendo la confirmación del diagnóstico de miocardiopatía chagásica.
Tres meses antes a este último internamiento, en la consulta externa se le había iniciado amiodarona a la paciente por sensación de palpitaciones y habérsele documentado en Holter la presencia de extrasístoles ventriculares frecuentes incluso con episodios de dupletas, hasta este punto en el contexto de una paciente con una cardiopatía estructural con coronarias normales en dos ocasiones.
Se decidió la colocación de desfibrilador automático im plantable (DAI), ya que no toleró dosis altas de B bloqueadores por hipotensión y bradicardia, y aún a pesar de amiodarona y B bloqueadores persistía con colgajos de taquicardia ventricular no sostenida que le generaban síntomas de bajo gasto.
Se le realizó colon por enema, ultrasonido de vías urinarias y esofagograma que fueron normales.
Actualmente 3 meses posteriores a la colocación del DAI paciente refiere sentirse bien, no ha vuelto a tener episodios de palpitaciones.
Cuadro 1 Laboratorios del último internamiento
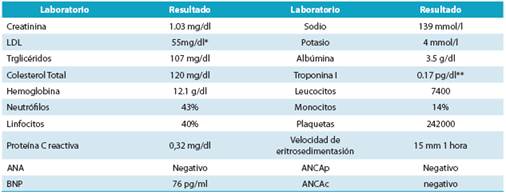
* Ya en tratamiento con Rosuvastatina.
** troponina discretamente elevada en tres ocasiones pero sin aumento significativo entre ellas ( 0.17 pg/dl- 0.2 pg/dl- 0.15 pg/dl).
Discusión
La enfermedad de Chagas, también conocida como Trypanosomiasis Americana, es una infección sistémica protozoaria causada por el flagelado Trypanosoma Cruzi, la cual tiene una alta asociación a situaciones económicas y sociales limítrofes a tal punto que es considerada por la Organización Mundial de la Salud como parte del grupo de la enfermedades tropicales por descuido. Aunque tradicionalmente se considera asociada a zonas rurales y subdesarrolladas de América Latina, la migración ha globalizada la enfermedad de Chagas. Se estima que cerca de 8-14 millones de personas tienen la presentación crónica de la patología.1
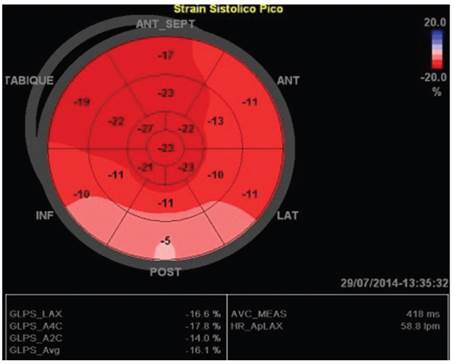
Figura 6. Ojo de Buey que evidencia el compromiso en la deformación de la fibra miocárdica (Strain longitudinal) de los segmentos basales y medios inferiores, ínfero-laterales, lateral y anterior, distribución no correspondiente a un territorio coronario específico.
Mortalidad y complicaciones asociadas
En el 2006, se considero que la Enfermedad de Chagas fue responsable de 12 500 muertes en Latino América. Las tasas de mortalidad en los pacientes con insuficiencia cardiaca sintomática por Chagas son tan altas como del 63% y 84% a los 5 y 10 años, respectivamente. Las principales causas de muerte en los pacientes con cardiomiopatía por Chagas se dividen como insuficiencia cardiaca refractaria en primer lu gar, seguido por muerte súbita y el evento cerebro-vascular en segundo y tercer lugar, respectivamente. 1 De hecho varios reportes de casos y estudios observacionales, han demostra do la presencia de un riesgo de desarrollar un evento-cerebro vascular con un Odds Ratio de hasta 2,1 en los pacientes que poseen Cardiomiopatía por Chagas.1-2 El mecanismo de dicha asociación no está del todo dilucidada aún, se consideran como posibles factores de riesgo el desarrollo de fibrilación auricular, la formación de aneurismas apicales, la formación de trombos murales y la disfunción sistólica del ventrículo izquierdo. Sin embargo, esta observación lo que pone en evidencia es la necesidad de futuros estudios, que logren definir aún mas dicha asociación, su relación en el desarrollo de eventos-cerebro vasculares isquémicos versus hemorrágicos, la significancia en el pronóstico de estos pacientes, y principalmente si se justificaría la implementación de alguna medida terapéutica preventiva en estos pacientes como lo es la anticoagulación. No olvidemos que en la paciente que describimos en este caso clíico, el primer contacto que tuvo con el centro hospitalario fue por un evento cerebro-vascular isquémico, pudiendo ser la primera manifestación de la En fermedad de Chagas, como ya se ha descrito en otros casos.3
Cardiomiopatía por chagas: clínica y fisiopatología
La cardiomiopatía es la manifestación crónica más frecuente de la infección por el Trypanosoma Cruzi, desarrollán dose únicamente en un 30% de los pacientes que se infectan con el parásito, aunque también pueden existir manifestaciones a nivel del tracto gastro-intestinal en un 10% de los infectados, y la gran mayoría (60-70%) cursan asintomáticos sin manifestaciones cardiacas ni gastrointestinales. Estas fase crónica se caracteriza por un infiltrado miocárdico mononu clear generando un espectro de manifestaciones que van desde la insuficiencia cardiaca, arritmias, bloqueo auriculo-ventricular, tromboembolismo, accidente cerebrovascular y muerte súbita, hasta el paciente asintomático. Un 10% de los pacientes infectados desarrollan una miocardiopatía cha gásica crónica letal, que se caracteriza por miocardiopatía dilatada con disfunción sistólica y diastólica, insuficiencia cardiaca y arritmias.
La enfermedad aguda por Chagas con frecuencia es inespecífica y subclínica, con presencia de miocarditis de forma uniforme, reportada por biopsia endomiocárdica aún en pacientes asintomáticos, lo cual evidentemente dificulta el diagnóstico temprano, 4-5 y de los cuales solo un tercio pro gresan a una fase crónica, momento en que la mayoría son diagnosticados de forma incidental.
Estudios clínicos en modelos murinos han demostra do una profunda alteración bioquímica a nivel intracelular que es la que conlleva a la cardiotoxicidad, documentán dose entre ellos: 1) incremento en la glicólisis con la consecuente acumulación de sorbitol, fructuosa y productos de glicosilación avanzada, 2) daño en la cadena de respiración mitocondrial, 3) acumulación de lípidos dentro del miocito y 4) producción de especies reactivas de oxígeno y de ácido úrico en respuesta a la hiperactividad de la enzima xantina oxidasa. Mecanismos que corresponden a las vías finales de la sobreexpresión de linfocitos TH1 y macrófagos a nivel del miocardio, con una secreción de citocinas (relación 2:1 de lin focitos CD8+/CD4+) proinflamatorias predominantemente INF gamma y TNF alfa,4 conduciendo a una marcada respuesta inmune de tipo celular, no obstante también se describe la presencia de una marcada respuesta humural mediada por la reacción cruzada generada ante la presencia de anticuerpos contra antígenos del parásito que se convierten en autoanticuerpos contra antígenos miocárdicos similares, tal como es el caso de los anticuerpos contra los antígenos p2B y B13 parasitarios que actúan como autoanticuerpos contra el receptor B1 adrenérgico y la miosina cardiaca respectivamente,6 generándose por ejemplo una asociación directa entre el desarrollo de la miocardiopatía crónica chagásica letal y la presencia en el 100% del anti-B13, presente únicamente en un 17% de los pacientes que no desarrollan miocardiopatía dilatada chagásica.6
Aunque llama la atención que sólo un 30% de quienes sufren una infección aguda por chagas llegan a desarrollar una fase crónica, se desconocen con exactitud cuáles son los mecanismos por los cuales un paciente es susceptible a la perpetuación del proceso inflamatorio. No obstante estudios en animales han determinado la presencia de polimorfismos sobre los HLA clase I y los HLA clase II, además de polimor fismos en el genoma del parásito, como eventuales factores que favorecerían al desarrollo de esta respuesta inflamatoria crónica y el desarrollo de autoanticuerpos contra el miocardio; entre ellos podría mencionarse la presencia del antígeno HLA clase II DQ-1 como factor que confiere suceptibilidad para la cronificación tras la infección hasta en 2 a 10 veces, mientras que la presencia del antígeno HLA clase II DQ-7 con fiere protección al desarrollo de la autoinmunidad tras la infección por el parásito.5
Predictores de mortalidad y riesgo de arritmias en miocardiopatía chagásica
La miocardiopatía chagásica se caracteriza por ser un grupo heterogéneo, aquel 30% que tras una infección aguda progresa a la fase crónica, se pueden clasificar en tres grupos: Grupo I. Caracterizados por no tener alteraciones electrocardiográficas, ecocardiográficas, ni clínicas, el diagnóstico se hace por medios serológicos o exámenes parasitológicos, pueden detectarse lesiones cardiacas subclínicas principalmente por medio de resonancia magnética a través de focos positivos al realce tardío de gadolinio. Grupo II. Caracteriza dos por alteraciones electrocardiográficas, pero sin alteraciones ecocardiográficas y con función sistólica conservada. Grupo III. Corresponderían a los que presentan alteraciones electrocardiográficas, miocardiopatía dilatada y disfunción sistólica tanto del ventrículo derecho como del ventrículo izquierdo. La distinción de cada uno de estos subgrupos tiene su importancia clínica, pues son los del grupo III los que se asocian a una mayor tasa de mortalidad, incluso al ser com paradas con otros tipos de miocardiopatías. 6-7-8
Las alteraciones electrocardiográficas son variadas y de hecho no existe un patrón específico de la afectación miocárdica por la Enfermedad de Chagas, aunque la literatura médica describe el bloqueo de rama derecha y el hemiblo queo antero superior izquierdo como las afectaciones más frecuentes, y las cuales por sí solas no se consideran un factor pronóstico de riesgo de muerte,9 sin embargo, constituye una herramienta útil, de bajo coste y globalmente disponible para el cribado de miocardiopatía crónica chagásica, dada su alta sensibilidad (83%), pero sobretodo, su alto valor predictivo negativo (96%), lo que permitiría limitar la realización de test de imágenes cardiacas sólo en aquellos pacientes que presenten alguna alteración electrocardiográfica,9 en el con texto de serologías positivas por el parásito.
Se han descrito varios trastornos segmentarios a nivel ecocardiográfico, pero con predominio de afectación de los segmentos apicales, septales inferiores e inferiores medioba sales y laterales basales.
Varios factores se han asociado como predictores de mortalidad, entre ellos la presencia de disfunción ventricular izquierda y derecha, la presencia de aneurisma apical, incremento del volumen atrial, presencia de extrasístoles ventriculares y algunos datos de gabinete como elevación de BNP por encima de 200 pg/dl y elevación de troponina, son catalogados como factores independientes de mortalidad en pacientes con miocardiopatía chagásica.8
Con respecto a los factores predictores de arritmias cardiacas, la presencia de aneurisma apical, la enfermedad arterial coronaria y la fracción de eyección reducida fueron las asociadas a episodios de arritmias ventriculares documenta das por holter o inducidas por estudios electrofiosológicos.9 Otro factor con un rol más modesto en la identificación de pacientes con miocardiopatía chagásica en riesgo de desarrollar arritmias ventriculares sería una duración mayor a 100ms del pico de la onda T al final de la misma (Tp-Te > 100ms).9
El Rassi score,10 es una escala que estratifica a los pacien tes con miocardiopatía crónica chagásica dentro de grupos de bajo, intermedio y alto riesgo de muerte por eventos arrítmicos, tras la combinación de 6 factores de riesgo : NYHA III o IV ( 5 puntos), cardiomegalia en la radiografía de tórax (5 puntos), Anormalidades globales o segmentarios de la con tractilidad por eco 2D (3 puntos), Taquicardia Ventricular no sostenida en holter de 24 horas (3 puntos), voltajes de QRS bajos en el electrocardiograma (2 puntos) y sexo masculino (2 puntos); siendo de 0-6 puntos un paciente de bajo riesgo con una tasa de mortalidad del 2% y del 10% a los 5 y 10 años res pectivamente, de 7-11 puntos de riesgo intermedio con una tasa de eventos mortales arrítmicos del 18% y 44% a los 5 y 10 años y de 12-20 puntos de alto riesgo de eventos con una tasa mortalidad del 63% y 84% a los 5 y 10 años, respectiva mente.10 No obstante, aún cuando se tienen claros cuales son los pacientes de alto riesgo de eventos arrítmicos mortales, no se ha definido si efectivamente el Desfibrilador Automáti co Implantable (DAI) es superior al tratamiento antiarrítmico como la amiodarona en la disminución de la mortalidad en estos pacientes, reportes de casos y estudios unicéntricos no aleatorizados,11 arrojan datos a favor del DAI, sin embargo, por tal razón en este momento se encuentra en proceso el estudio CHAGASICS Trial,12 que correspondería al primer estudio multicéntrico, aleatorizado y con un solo ciego, realizado principalmente en más de 60 centros brasileños, que busca definir si el DAI es mejor que la amiodarona en disminución de la mortalidad global como punto primario, en pacientes con miocardiopatía chagásica crónica con riesgo de interme dio a alto de mortalidad según la escala de Rassi.
La paciente que describimos en este caso clínico, correspondería a una paciente de alto riesgo de mortalidad según la escala de Rassi, y en quien aún a pesar de las dudas existentes con respecto a la terapia con DAI, se le ofreció la colocación del dispositivo sumado a una dosis de 200mg diarios de amiodarona, con lo cual en el poco seguimiento que se le ha dado hasta el momento (3 meses), la paciente refiere al menos un franco alivio sintomático si nuevos episodios arrítmicos.
Lastimosamente hasta el día de hoy no existe un tratamiento eficaz para los casos en que se logra determinar una infección aguda por Chagas, que demuestre una disminución en la tasa de progresión a la fase crónica, sin embargo, aquel 30% que progresa a cardiomiopatía chagásica crónica, y principalmente el 10% que desarrollan la miocardiopatía crónica chagásica letal con disfunción sistólica del ventrículo izquierdo, se ven beneficiados de la terapia con inhibidores de la en zima convertidora de angiotensina (IECAS) u antagonistas de los receptores de angiotensina II (ARA -II), así como de los an tagonistas de aldosterona y los B- bloqueadores, con impacto en la morbimortalidad y disminución en el remodelado como se ha demostrado en otros tipos de cardiomiopatías,13-20 por lo que su uso es indispensable en el manejo crónico de los mismos, independientemente de la tasa de riesgo de arritmias mencionado anteriormente.