Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Costarricense de Cardiología
Print version ISSN 1409-4142
Rev. costarric. cardiol vol.11 n.2 San José Dec. 2009
Anatomía básica cerebral para el cardiólogo intervencionista
Dr. Jonathan Poveda Fernández.
Servicio de Cardiología, Hospital San Juan de Dios. Av. Paseo Colón, San José Costa Rica. Tel: (506) 2257-6282 ext 2075; Fax: (506) 2522-1000 ext 2109; jpoveda@clinicabiblica.com
Resumen
El estudio angiográfico de los vasos supraaórticos, las arterias carótidas y la circulación cerebral, se realiza con mayor frecuencia en los labotatorios de hemodinamia de los servicios de cardiología, debido a que un número importante de pacientes presenta enfermedad vascular coronaria, asÍ como carotídea y del sistema nervioso central concomitante. Esta revisión, provee al cardiólogo invasivo, los conocimientos generales de la circulación carotídea y cerebral, asi como la correlación de los síntomas asociados a enfermedad isquémica cerebral, de acuerdo a los lechos vasculares afectados así como algunos principios técnicos básicos para una óptima valoración de estos territorios vasculares.
Abstract
Basic brain circulatory anatomy for the interventional cardiologist
Angiographic studies of the supraortic vessels, including the carotid arteries and the cerebral circulation, are usually performed in the cardiac catheterization laboratory of a division or department of cardiology or cardiovascular medicine. This is a result of efficiency and of the clinical status of many coronary artery patients who have concomitant cerebrovascular disease.This review, provides the interventional cardiologist with general information involving the carotid and cerebral artery circulations and correlates symptoms associated with cerebral ischemia according to the artery involved. Basic techniques for an optimal assessment of these vascular territories are discussed.
Key words: angiography, cerebral, coronary intervention.
Introducción
Los procedimientos intervencionistas endovasculares que involucran el territorio carotídeo y cerebral se han vuelto más comunes en los últimos tiempos y son realizados por igual por el especialista vascular periférico, el neurocirujano neurovascular y el cardiólogo intervencionista en nuestro medio. Es imperativo que aquellos médicos clínicos que realicen estos procedimientos, se familiarizen con el manejo de estos pacientes y tengan un conocimiento más detallado de la anatomía neurovascular y la metodología de manejo de éstos pacientes en el laboratorio de hemodinamia1,2. De ahí que este articulo pretenda proveer los conocimientos básicos de la anatomía cerebral vascular y sus variantes comunes, así como algunos principios técnicos utilizados en el laboratorio para su estudio.
Arco Aórtico
Normalmente el tronco braquiocefálico, la carótida común izquierda y la arteria subclavia izquierda se derivan de la superficie superior del arco aórtico. El origen común de el tronco braquiocefálico y la carótida común izquierda (arco bovino) ocurren ocasionalmente. También la carótida común izquierda puede nacer directamente del tronco braquiocefálico3. El origen directo desde el arco aórtico de la arteria vertebral izquierda y el origen separado de la subclavia derecha y la carótida común derecha desde el arco, son más bien infrecuentes. Por otro lado, la arteria subclavia derecha aberrante es la malformación más común del arco, con una frecuencia del 0.4-2%. En este caso, usualmente la subclavia derecha se convierte en la última rama que se desprende del arco aórtico. El arco aórtico derecho con la subclavia izquierda aberrante se describe solamente en 0.1 % de la población.
Sistema Carotídeo
Como se mencionó, la carótida común izquierda se deriva del arco aórtico, mientras que la carótida común derecha se deriva de la arteria innominada. Las variaciones más comunes incluyen el origen anómalo de la carótida común izquierda a partir de la innominada o la carótida común derecha, del arco aórtico. Usualmente no se derivan ramificaciones de las carótidas comunes antes de su bifurcación, aunque la arteria tiroidea superior y la arteria faríngea ascendente pueden derivarse de este vaso cuando la bifurcación ocurre a un nivel muy alto, usualmente mas allá del cuerpo de la tercera vértebra cervical4,5.
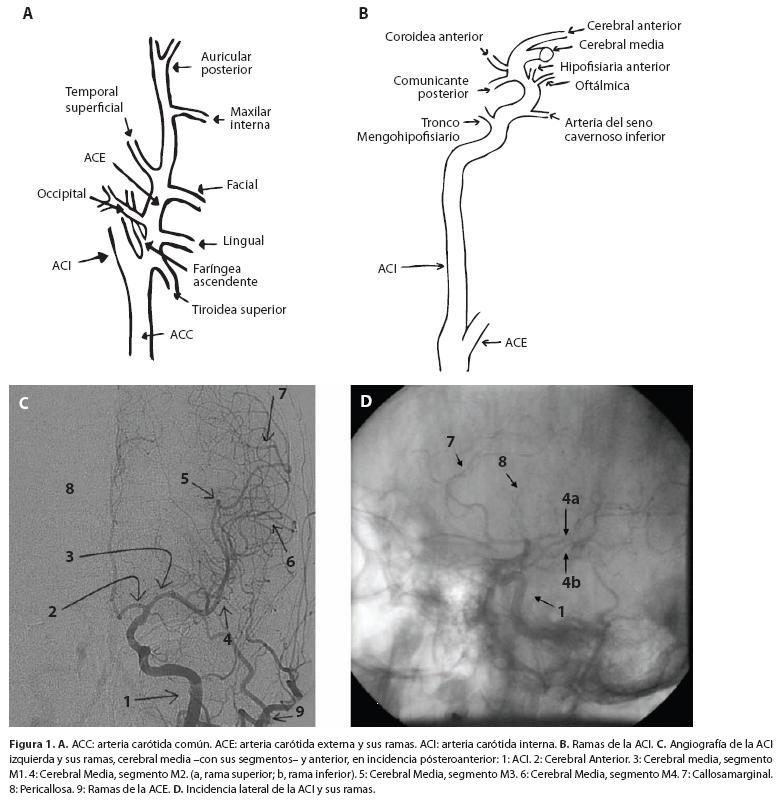
Arteria carótica externa
La arteria carótida externa tiene ocho ramas (Fig. 1, A), las cuales irrigan usualmente segmentos extracraneanos. Estas son: la tiroidea superior, la faríngea ascendente, la lingual, la facial, la occipital, la auricular posterior, la temporal superficial y la arteria maxilar. Varias de estas arterias suplen la duramadre de la superficie cerebral basal y lateral. Dichas ramas meníngeas suplen también la duramadre de la fosa posterior de manera compartida con ramas de la arteria occipital. La arteria maxilar interna provee el flujo a la duramadre de la fosa media y anterior. La carótida externa puede proveer un flujo intracraneano importante cuando existe una obstrucción severa de la arteria carótida interna ipsilateral, a través de la arteria oftálmica: la arteria óftalmica recibe flujo a través de colaterales de la carótida externa y el flujo reverso a través de ella, irriga la porción subaracnoidea proximal de la carótida interna. La arteria vertebral puede también comunicarse con el sistema carotídeo, a través de la faríngea ascendente y de ramas que se conectan con la arteria occipital, derivada de la carótida externa. Luego de una oclusión vertebral, la arteria occipital , derivada de la carótida externa. Luego de una oclusión vertebral, la arteria occipital puede proveer flujo distal a los segmentos terminales vertebrales, a través de comunicantes intramusculares.
Arteria carótida interna
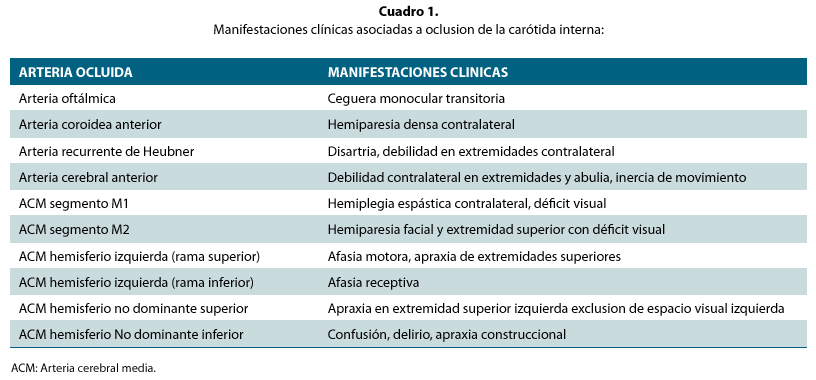
La arteria carótida interna provee flujo sanguíneo a los hemisferios cerebrales, el ojo, la cara y la nariz (Fig. 1, B-D). Se divide en cuatro segmentos: cervical, petroso, cavernoso y supraclinoideo. Usualmente, no presenta ramas en su segmento cervical o petroso. Las ramas cavernosas son el tronco meningohipofisiario y la arteria al seno cavernoso inferior. El tronco meningohipofisiario origina la arteria tentorial, la hipofisiaria inferior y la meníngea dorsal. El tronco inferolateral suple los vasos que irrigan los nervios craneales y la duramadre del seno cavernoso inferior y la del piso de la fosa media. Estas arterias son las se que comunican con la carótida externa o con sus homólogas contralaterales, en caso de obstrucción carotídea. El segmento supraclinoideo de la carótida interna origina la arteria oftálmica, la comunicante posterior y la arteria coroidea anterior. En la tabla 1 se muestran las manifestaciones clínicas, según la arteria obstruida.
Las ramas de la arteria oftálmica incluyen la central de la retina, la lacrimal, las etmoidales anteriores y posteriores y la supraorbitaria y troclear. La amaurosis fugaz es el síntoma relacionado a la isquemia de la arteria oftálmica. La arteria comunicante posterior, que nace de la carotida interna después de la hipofisiaria superior, se une a la arteria cerebral posterior para completar el segmento posterior del circulo de Willis. La comunicante posterior genera varias ramas perforantes, y suplen el tálamo, hipotálamo, subtálamo, la cápsula interna, el quiasma óptico, el tracto óptico y el tallo hipofisiario. La rama terminal de la carótida interna es la coroidea anterior, que suple el tracto óptico, el pedúnculo cerebral, el cuerpo geniculado lateral y el lóbulo temporal. El plexo de la coroidea anterior suple la capsula interna, el tálamo, el cuerpo geniculado lateral, el pedúnculo cerebral, y el tracto óptico. La oclusión de esta arteria, produce hemiparesia densa contralateral, que afecta la cara, el brazo y la pierna, pérdida sensorial contralateral y hemianopsia contralateral, en caso de estar comprometido el cuerpo geniculado. Distalmente, la carótida interna se bifurca para generar la arteria cerebral anterior y la arteria cerebral media.
Arteria cerebral anterior. Esta arteria se genera de la bifurcación de la carótida interna y se une a su homóloga contralateral a través de la comunicante anterior, completando el segmento anterior del círculo de Willis (Fig. 3, A). La oclusión de arteria cerebral anterior causa debilidad motora contralateral de la pierna y el hombro; usualmente se presenta déficit cortical, que involucra pérdida de localización táctil al estimulo bilateral. El segmento proximal de la cerebral anterior se denomina segmento A1; el segmento A2 comprende desde la comunicante anterior hasta el rostrum del cuerpo calloso. Perforantes de este segmento suplen el hipotálamo anterior, el septum pelúcido, la comisura anterior, los pilares del fórnix y el segmento anterior del cuerpo estriado. La arteria recurrente de Heubner nace de la porción proximal de A2 y suple la cara anterior del núcleo caudado, el tercio anterior del putamen y la porción externa del globus pallidus y el brazo anterior de la capsula interna. La oclusión de la arteria recurrente de Heubner puede causar debilidad de la extremidad contralateral acompañada de disartria, apatía y dificultad para iniciar los movimientos. La porción distal de la arteria cerebral anterior, denominada "arteria pericallosa" genera varias ramas corticales. La primera es la órbitofrontal, que suple el segmento medial del giro orbitario, el giro recto y el bulbo y tracto olfatorio. La rama pericallosa más larga, es la callosa marginal, que suple los dos tercios anteriores del hemisferio cerebral.
Arteria cerebral media. Esta se divide en cuatro segmentos: el esfenoidal o M1, el insular o M2, el opercular o M3 y el cortical o M4. (Fig. 1 C, D). El segmento M1 genera múltiples perforantes, denominadas "arterias lenticuloestriadas", que penetran la substancia perforada anterior para suplir la capsula interna, el cuerpo y la cabeza del núcleo caudado y la parte lateral del globos pallidus. En algunos pacientes, el segmento M1 genera ramas corticales tempranas hacia los lóbulos frontal y temporal. El infarto en la distribución de este segmento produce hemiplejia espástica contralateral, asociada a una alta mortalidad. El segmento M2 genera dos ramas mayores, la superior y la inferior, que suplen áreas frontales y temporales. El compromiso isquémico de estos segmentos genera hemiparesia que afecta de manera más importante la cara y el brazo que a la pierna; también puede generar alteraciones del campo visual. La oclusión proximal de M2 genera hemianopsia homónima contralateral, asociada a desviación de la mirada hacia el lado afectado. La obstrucción de la arteria M2 inferior, genera cuadrantopsia homónima superior contralateral. La afasia motora se debe a la lesión isquémica del opérculo frontal del hemisferio dominante, suplido por la rama superior de la cerebral media. La apraxia se debe usualmente al compromiso de la rama superior de M2. Si ocurre en el hemisferio dominante, el paciente tendrá apraxia en ambas extremidades superiores; si el evento ocurre en el hemisferio no dominante, el paciente presenta un profundo trastorno del espacio izquierdo, así como confusión y delirio. La oclusión de la rama inferior o posterior de la cerebral media produce afasia receptiva, si el giro temporal superior del hemisferio dominante está comprometido. El segmento M3 se origina de los segmentos inferior y superior de M2 y finaliza cuando los vasos distales llegan a la superficie de la cisura de Silvio. Es una rama que suple predominantemente la corteza cerebral. El segmento M4 suple los dos tercios laterales de los hemisferios cerebrales frontal, parietal, temporal y occipital, toda la superficie insular y opercular, la superficie orbital lateral del lóbulo frontal, el polo temporal y la superficie inferior lateral del lóbulo temporal. Las perforantes anteriores pueden originarse de la carótida interna, la coroidea anterior, la cerebral media o la cerebral anterior y suplen los cuernos frontales de los ventrículos laterales, el núcleo caudado, putamen, la capsula interna, el globus palidus y el tálamo.
Sistema Vértebro-Basilar
Arteria vertebral
La arteria vertebral se divide en cuatro segmentos: el inicial, el intervertebral, el horizontal, y el intracraneano (Fig. 2). Su segmento inicial no tiene ramas. Las ramas del segmento intervertebral son la meníngea, la muscular y las radiculares. Las meníngeas suplen la duramadre del foramen magno; las musculares, los músculos profundos del cuello y crean anastomosis hacia la occipital. Las radiculares entran al canal espinal y proveen colaterales hacia la espinal anterior y posterior, ramas del segmento horizontal. Este segmento provee también ramas meníngeas pequeñas, que suplen a la duramadre de la fosa posterior y se anastomosan con su vertebral homóloga y con ramas de la carótida externa. Las mencionadas ramas espinales proveen flujo hacia la médula oblongata (o bulbo raquídeo) y a la espina dorsal posterior. Las ramas del segmento intracraneano incluyen la espinal anterior y la ínferoposterior cerebelar.
Las arterias vertebrales pueden generarse de la aorta, la carótida común, la carótida externa, las intercostales, y las tiroideas inferiores. Usualmente, el diámetro es diferente la una de la otra. En ocasiones, las vertebrales pueden acabar como arteria cerebelosa posteroinferior y no contribuir con el flujo de la arteria basilar. El segmento distal de la vertebral intracraneana origina las arterias ventrales espinales, que originan la arteria espinal anterior. Esta suple las pirámides, el lemnisco medial, los haces interolivares, el núcleo hipotalámico así como los fascículos longitudinales posteriores y los dos tercios anteriores del cordón espinal. La arteria cerebelosa pósteroinferior, es la rama más larga de la arteria vertebral. Suple la cara lateral de la medula oblongata, el vermis inferior, el cuarto ventrículo y la cara inferior de los hemisferios cerebelosos. La oclusión vertebral unilateral genera síntomas variables y usualmente benignos; sin embargo la oclusión bilateral simultanea de la cerebelosa pósteroinferior lesiona la cara lateral de la médula oblongata y la superficie cerebelosa posteroinferior, generando el Síndrome de Wallemberg.
Arteria basilar
La arteria basilar genera varias ramas que suplen el tallo cerebral, el cerebelo, la corteza cerebral, que incluyen la cerebelar anteroinferior, la cerebelosa superior y la cerebral posterior (Fig. 2, B,C). Ramas perforantes de la basilar, suplen el puente y segmentos superiores del tallo cerebral. La arteria cerebelar anteroinferior tiene numerosas ramas penetrantes que van a los dos tercios inferiores del puente y el segmento superior de la médula oblongata; también suple la porción petrosa cerebelar , el surco pontomedular, la fosa supraolivar, los nervios glosofaríngeo y vago y segmentos inferiores de la porción petrosa cerebelar. La arteria cerebelar superior provee arterias perforantes que suplen el puente ventrolateral superior y los núcleos profundos cerebelares. Las ramas de la cerebral posterior suplen el tallo cerebral, los plexos coroideos y segmentos de los lóbulos occipital, parietal y temporal; estas ramas se categorizan en tres tipos: centrales, ventriculares y cerebrales. Las ramas centrales van al tálamo posterior y originan ramas perforantes tálamogeniculadas y pedunculares. Las ramas ventriculares son la coroidea medial posterior y la coroidea láteroposterior. Las ramas cerebrales de la cerebral posterior son la inferior temporal, la parietooccipital, la calcarina y las ramas esplénicas. Las ramas perforantes posteriores que se generan de la arteria basilar suplen el diencéfalo y el mesencéfalo. Dependiendo del número de sus vasos colaterales, la oclusión basilar puede generar varios síntomas. Las arterias cerebelosas pueden originar un sistema de colaterales leptomeningeas que pueden derivar en flujo colateral basilar; la carótida interna puede también generar colaterales a través de la comunicante posterior.
Polígono de Willis
El polígono de Willis está conformado por las dos carótidas internas, los dos segmentos de arteria cerebral anterior, las arterias comunicantes anteriores, posteriores y las arterias cerebrales posteriores (Fig. 3, A). Usualmente provee la comunicación entre la circulación posterior y la anterior, aunque esta conformación normal se observa en el 50% de los pacientes. Las variaciones más comunes son la hipoplasia de la comunicante posterior izquierda, ramas de la comunicante posterior paralelas a la coroidea anterior, la comunicante posterior izquierda originándose de la carótida interna izquierda y la ausencia de la arteria comunicante posterior derecha.
Además de la arteria comunicante posterior, existen otras anastomosis importantes entre la circulación anterior y la posterior, (Fig. 3, B), siendo las más importantes, la persistencia de la arteria trigeminal (que nace de la carótida interna y se una a la arteria basilar), la arteria hipoglósica primitiva y la arteria ótica (ambas nacen en la carótida interna y se unen a la basilar). Es infrecuente encontrar comunicaciones entre la arteria carótida y la vertebral; sin embargo, pueden verse a través de las arterias intersegmentarias proatlánticas y cervicales. La arteria proatlántica conecta ambas arterias a través del segmento horizontal de la arteria vertebral, mientras que la arteria intersegmentaria las conecta a través de los segmentos intervertebrales. La arteria occipital puede conectarse a la arteria vertebral a través de ramas intramusculares. Finalmente, la arteria carótida externa puede proveer un flujo importante a la carótida interna a través de la arteria oftálmica. En la tabla 2 se muestran las manifestaciones clínicas, según la arteria obstruida.
Técnica Angiográfica
El acceso por vía arteria femoral, se obtiene con un introductor corto de 6 French (F) para realizar, de ser posible, angiografía del arco aórtico; usualmente, se utiliza un catéter "pigtail" de 5 F, en proyección oblicua anterior izquierda (a 40° ó 50°), e inyecta 40 mL de medio de contraste al 60%, a una velocidad de 20 mL/s mediante inyector automático6. El extremo distal del catéter se coloca en la aorta ascendente, sobre la válvula aórtica, para obtener una adecuada mezcla del medio de contraste con la sangre, antes de progresar hacia el arco aórtico (Fig. 3, C). Debe vigilarse meticulosamente el riesgo de embolización: todo el equipo debe ser purgado de aire, no contener restos sanguíneos o medio de contraste, además de ser adecuadamente irrigado con solución con heparina sódica. Las maniobras a realizar deben ser finas y gentiles, para prevenir perforaciones vasculares y debe minimizarse la utilización de guías de intercambio; todas las herramientas endovasculares no deben permanecer en el lecho cerebrovascular más de lo necesario.
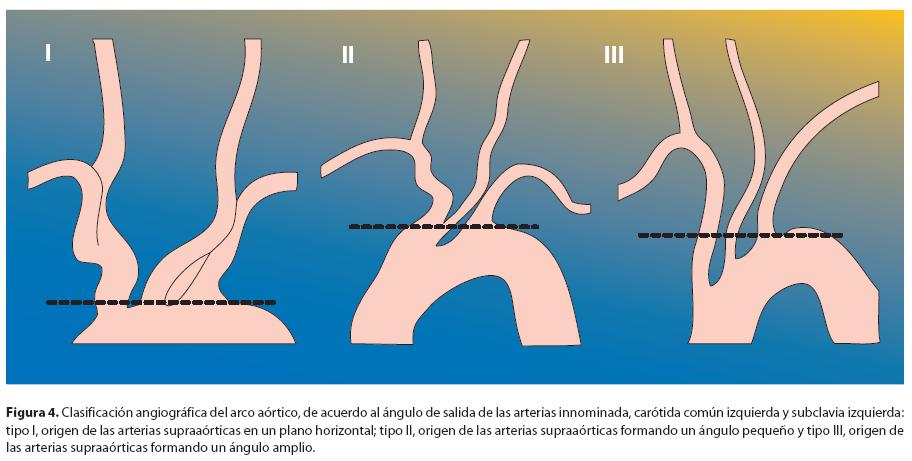
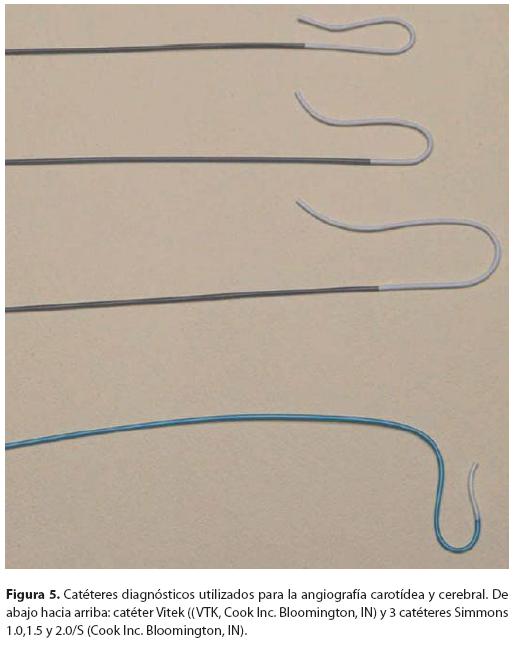
Utilizando sustracción digital, las imágenes permiten obtener información sobre el tipo de arco aórtico, la presencia de una variante anatómica, la presencia de enfermedad aterosclerótica o tortuosidad en el segmento proximal de los grandes vasos. Todos estos factores, influyen en la selección del catéter diagnóstico a utilizar, así como la estrategia a emplear. Desde un punto de vista angiográfico, el arco aórtico, se clasifica de acuerdo al ángulo de salida de los grandes vasos7, (Fig. 4); para todos los pacientes con arco aórtico tipo I y la mayoría de los de tipo II, el catéter JR4 es de primera elección. En pacientes con arco aórtico tipo III, generalmente se requerirá un catéter Vitek (VTK, Cook Inc. Bloomington, IN, Estados Unidos) o un catéter Simmons (Cook Inc. Bloomington, IN, Estaos Unidos), Fig. 5. La angiografía de la arteria carótida común izquierda y del bulbo, se realiza con el catéter en el origen de la arteria, aunque en algunas ocasiones es necesario desplazar el catéter sobre una guía hidrofílica tipo "glidewire" hasta su segmento medio. Para explorar la arteria carótida común derecha, primero debe desplazarse el catéter sobre una a guía hidrofílica a través de la arteria innominada hacia la carótida común derecha hasta su segmento medio. En la mayoría de los pacientes una vista ipsilateral oblicua a 30 ó 45° y una vista lateral de la carótida común, definen la anatomía de la bifurcación carotídea. Algunas vistas adicionales tales como la ánteroposterior, oblicua contralateral, o angulaciones craneales o caudales, se utilizan para definir una lesión de interés, especialmente cuando existe tortuosidad del árbol carotídeo. Las arterias carótida interna intracraneana y la cerebral media, se analizan mejor en incidencia ánteroposterior con ligera angulación craneal y en incidencia lateral; en ambas, debe incluirse la tabla interna del cráneo en el campo visual, para permitir la visualización de las estructuras venosas. Típicamente, mediante inyección rápida de 4-5 mL de contraste, se realiza angiografía con substracción digital para visualizar la fase venosa de la imagen. De ser posible, debe solicitársele al paciente permanecer quieto y sin respirar o tragar durante la inyección, ya que esto podría permitir que algunas lesiones pasen desapercibidas.
Luego de visualizar ambos árboles carotídeos, debe explorarse al menos una arteria vertebral, usualmente la izquierda dominante, para explorar la posibilidad de flujo colateral desde la comunicante anterior, comunicante posterior o las comunicante piales desde la circulación posterior a la cerebral media. La angiografía debe también excluir la presencia de aneurismas, malformaciones arteriovenosas cerebrales o tumores cerebrales vasculares. Para visualizar la arteria vertebral, es necesario primero cateterizar la arteria subclavia y obtener un angiograma no selectivo del segmento V1, en incidencia oblicua contralateral, para descartar la presencia de lesiones ostiales; luego se cateteriza este segmento y se realiza angiografía con substracción digital, con disparos suaves y más retardados que los utilizados para visualizar el árbol carotídeo. La vista oblicua ipsilateral, permite visualizar los segmentos V2 y V3 y las vistas lateral y ánteroposterior, permiten apreciar el segmento V4, la arteria basilar y la arteria cerebral posterior. Es necesario recordar que la arteria vertebral puede suplir ramas colaterales hacia la arteria espinal anterior, que parten medialmente desde el segmento cervical; por lo tanto, si se utiliza una guía hidrofílica para introducir el catéter en el segmento V1, esta debe ser dirigida lateralmente, para evitar oclusión o ruptura de estas colaterales con el consiguiente infarto espinal.
Conclusión
El cardiólogo intervencionista que realiza procedimientos angiográficos de la circulación cerebral, debe tener pleno conocimiento de la anatomía intra y extracraneal, así como de sus variaciones más comunes, para comprender mejor su patología y alcance clínico que se deriva de la enfermedad aterosclerótica de este territorio.
Agradecimento especial al Dr. Franz Chaves Sell, Jefe del Departamento de Neurología del Hospital Clinica Bíblica, Costa Rica, por la detallada revisión de este texto.
Referencias
1 Cho L, Mukherjee D. Basic cerebral anatomy for the carotid interventionalist. Cath and Card. Interv. 2006; 68: 104-111 [ Links ]
2. Rosenfield KM;SCAI/SVMB/SVS Writing Committee. Clinical competence statement on carotid stenting: Training and credentialingfor carotid stenting-Multispecialty consensus recommendations. Catheter Cardiovasc Interv 2005;64:1-11 / J Am Coll Cardiol 2004;44:941-957 [ Links ]
3. Renfro MB, Day AL, Rhoton AL. The extracranial and intracraneal vessels: Normal anatomy and variation. In: Batjer HH, editor. Cerebrovascular Disease. Philadelphia. Lippinocott-Raven; 1997. p 1-21. [ Links ]
4. Baum S, editor. Abram’s Angiography: Vascular and Interventional Radiology, 4th ed. Boston: Little Brown; 1997. [ Links ]
5. Osborn AG. Diagnostic Cerebral Angiography 2nd ed. Philadelphia. Lippincott, William and Wilkins; 1999. [ Links ]
6. Al-Mubarak N, Roubin GS, Iyer SS, Vitek JJ. Carotid artery stenting, 1st ed. Lippincott Williams and Wilkins; 2004. [ Links ]
7. Yadav JS, Casserly IP, Sachar R, Manual of Peripheral Vascular Intervention. 1st ed. Lippincott Williams and Wilkins; 2005. [ Links ]